Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Клинико-морфологическая картина, диагностика и лечение
инфекционного поражения эндокарда
Автореферат диссертации на соискание учёной степени доктора
медицинских наук
Николаевский Евгений Николаевич
14.00.06 – кардиология
14.00.44 – сердечно-сосудистая хирургия
На правах рукописи
Санкт - Петербург 2004
Работа выполнена в Военно-медицинской академии имени С.М. Кирова
Николаевский Е.Н. Клинико-морфологическая картина, диагностика и лечение
инфекционного поражения эндокарда: Автореф. … дис. доктора мед. наук: 14.00.06 –
кардиология, 14.00.44 – сердечно-сосудистая хирургия. – СПб.: ВМедА имени С.М.
Кирова, 2004. – 40 с.
Николаевский Евгений Николаевич – доктор медицинских наук, старший преподаватель
кафедры терапии Самарского военно-медицинского института Министерства Обороны РФ
(адрес организации: 443099, Самара, ул. Пионерская, д. 22; домашний адрес:
443111, Самара, ул. Ново-Вокзальная, д. 140, кв. 144), электронная почта:
nicolaev2@yandex.ru
Научные консультанты:
доктор медицинских наук, профессор С.Б. ШУСТОВ
Лауреат Государственной премии Российской Федерации,
доктор медицинских наук, профессор Г.Г. ХУБУЛАВА
Официальные оппоненты:
доктор медицинских наук, профессор А.С. СВИСТОВ
доктор медицинских наук, профессор А.М. ЖИРКОВ
доктор медицинских наук, профессор В.В. ГРИЦЕНКО
Ведущая организация:
Главный военный клинический госпиталь МО РФ им. академика Н.Н. Бурденко
Учёный секретарь диссертационного совета:
Доктор медицинских наук, профессор В.Н. Власенко
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы
Решение проблем диагностики и лечения инфекционного эндокардита в настоящее
время приобретает особую актуальность в связи с ростом заболеваемости в 3-4 раза
(Гуревич М.А., 2000; Тюрин В.П., 2003). С наибольшей частотой (до 86%) болезнь
развивается у трудоспособного населения в возрасте 20-50 лет (Татарченко И.П.,
Комаров В.Т., 2001).
Распространённость инфекционного эндокардита в различных странах неодинакова.
В США заболеваемость наибольшая и составляет 38-92,9 на 1 млн. населения, в
Канаде – 20-25 человек (Mayer D.V. et al., 1997). В странах Европы
заболеваемость выше в Швеции – 59 человек на 1 млн. населения, в Англии – 23-25,
во Франции – 18-23, в Германии и Италии – 16 (Jaffe W.M., 1999). В России
заболеваемость ИЭ достигает 46,3 человек на 1 млн. населения (Тюрина Т.В.,
1997).
Рост заболеваемости обусловлен широким распространением внутривенной
наркомании, кардиохирургических операций, инвазивных медицинских манипуляций и
исследований (длительные катетеризации вен, зондирование сердца, длительное
использование катетера Sven-Ganz, хронический гемодиализ и т.д.) (Шевченко Ю.Л.
и др., 2003).
В связи с этим появились особые клинические формы заболевания: ИЭ у
наркоманов (с преимущественным поражением правых камер сердца), ИЭ протеза
клапана, нозокомиальный инфекционный эндокардит, ИЭ у лиц с имплантированным
электрокардиостимулятором и лиц, находящихся на программном гемодиализе,
эндокардит у реципиентов трансплантированного органа (Мишаевский А.Л., 2001;
Мазуров В.И. и др., 2001).
На первое место в России выходит проблема наркомании, которая актуальна для
Вооружённых Сил (Путин В.В., 2000; Литвинцев С.В. и др., 2001). По данным
“Демографического ежегодника России” (2002) уровень заболеваемости наркоманией в
2002 году достиг 45,2-48,7 на 100 тысяч населения. По сравнению с 1990 годом
заболеваемость выросла в 16,5 раз за счёт “шприцевых” форм (Шевченко Ю.Л. и др.,
2001). Однако действительное соотношение лиц, обратившихся за медицинской
помощью и злоупотребляющих наркотиками, составляет 1:10 (Коэн Г. и др., 2000;
Яковлев В.А. и др., 2001). Осложнением внутривенного введения наркотических
веществ является инфекционный эндокардит. Заболеваемость ИЭ среди наркоманов
составляет 5-10% в год, что значительно превышает общепопуляционные показатели
(Дёмин А.А. и др., 2002).
Осложнением хирургического лечения врождённых и приобретенных пороков сердца
стал инфекционный эндокардит протеза клапана (Черепанин И.М., 1999). Риск
развития ИЭ в течение первого года после имплантации протеза составляет 2-4%, в
последующем – до 1% ежегодно (Тюрин В.П., 2002). Заболеваемость ИЭ среди лиц с
имплантированным искусственным клапаном составляет 3-11,4% (Maroni J.P. et al.,
1999). Общая летальность в этой группе пациентов остаётся довольно высокой и
варьирует от 23% до 80% (Цукерман Г.И. и др., 2000; Douglas J.L., 1999).
По данным C.C. Lamas (2001) увеличение заболеваемости ИЭ связано с ростом
нозокомиального эндокардита (14-17%) вследствие инфицирования внутривенных
катетеров (10,3-24%), катетеров ярёмной вены и лёгочной артерии – 8,1-8,5%,
катетеров Sven-Ganz – 18%, гемодиализных шунтов и фистул – 57-61% (Staszevski et
al., 1995). После имплантации электрокардиостимулятора ИЭ развивается у 0,5-1%
больных. Программный гемодиализ становится причиной развития болезни в 1,7-5,1%
случаев. Смертность в этой группе больных составляет 48% (Тюрин В.П., 2001). В
течение 2 лет после трансплантации печени и пересадки сердца инфекционный
эндокардит развивается у 1,7-6% реципиентов, смертность достигает 57% (Paterson
D.L. et аl., 1998).
Смертность при эндокардите во многом обусловлена возбудителями заболевания.
Основными возбудителями (75-80%) инфекционного эндокардита являются стафилококки
и стрептококки (Тюрин В.П., 1998; Chastre J., 1999). Смертность при ИЭ,
вызванном золотистым стафилококком, составляет 60-80% (Гуревич М.А., 2001).
Однако получить положительную гемокультуру удаётся у 45-50% с острым и у 15-20%
больных с подострым и затяжным течением болезни (Шевченко Ю.Л. и др., 2003).
Среди возбудителей эндокардита вырос удельный вес грамотрицательных бактерий
группы НАСЕК (4-21%) и грибов (до 4-7%), которые в подавляющем большинстве
случаев резистентны к антибактериальной терапии (Тазина С.Я. и др., 2000).
Смертность при грибковом эндокардите достигает 60-100%, а при инфекционном
эндокардите, вызванном грамотрицательной микрофлорой – 47% (Буткевич О.М. и др.,
2001).
При инфекционном эндокардите в патологический процесс вовлекаются
сердечно-сосудистая система, печень, селезёнка, лёгкие, почки, центральная и
периферическая нервная система. Это определяет полиморфизм клинической картины,
в результате чего срок установления диагноза варьирует от 3,8 до 12 месяцев (Тазина
С.Я., Гуревич М.А., 1999). У 40% лиц болезнь длительное время остаётся
нераспознанной или не диагностируется вовсе. Частота обнаружения впервые
выявленного ИЭ на операции и аутопсии варьирует от 13,3% до 25% (Шевченко Ю.Л.,
1999).
Для современного течения болезни свойственно развитие осложнений, которые
определяют ведущую органную патологию (Дробышева В.П., 2003; Wladica S., 2001).
Наиболее тяжёлыми являются эмболии, острая сердечная и полиорганная
недостаточность. Они ответственны за 60-75% летальных исходов в предоперационном
периоде (Тюрин В.П., 2003). Снижения смертности можно достигнуть в результате
проведения ранней диагностики и своевременного лечения. Это возможно в том
случае, если есть достоверные критерии диагноза, эффективные методы диагностики
и лечения.
В настоящее время не решён ряд важных проблем. Не достаточно исследованы
клинико-морфологическая картина современных вариантов течения и клинических форм
инфекционного эндокардита, особенности изменений органов при затяжном, подостром
и остром течении заболевания, инфекционном эндокардите у наркоманов и
эндокардите искусственных клапанов. Не в полной мере разработаны диагностические
критерии и критерии активности болезни. Недостаточно определены возможности
чреспищеводной эхокардиографии в ранней диагностике. Мало изучены эффективность
плазмафереза, внутрисосудистого лазерного и ультрафиолетового облучения крови в
комплексном лечении заболевания, не разработаны показания к применению.
Разноречивы данные отечественных и иностранных авторов о факторах риска и
прогнозе эмболических осложнений, острой сердечной и полиорганной
недостаточности.
Вышеуказанные обстоятельства вызвали необходимость изучения
клинико-морфологической картины инфекционного эндокардита, проведения анализа
результатов терапии, данных инструментально-лабораторных исследований для
разработки диагностических критериев, поиска важных направлений в диагностике и
лечении заболевания.
Цель исследования
Изучение клинико-морфологической картины современных клинических форм
и вариантов течения инфекционного эндокардита, разработка клинико-лабораторных и
инструментальных диагностических критериев, оценка эффективности
антибактериальной, синдромной терапии, экстракорпоральной гемокоррекции для
повышения результативности диагностики и лечения заболевания.
Задачи исследования
- Изучить клинико-морфологическую картину затяжного,
подострого, острого вариантов инфекционного эндокардита современного
течения, инфекционного эндокардита у наркоманов, инфекционного эндокардита
искусственного клапана.
- Изучить клинико-лабораторные, инструментальные диагностические признаки
болезни, показатели активности инфекционного эндокардита для повышения их
надёжности в диагностике.
- Разработать алгоритмы диагностики инфекционного эндокардита с
использованием клинических, инструментальных, лабораторных исследований.
- Изучить эффективность антибактериальной и синдромной терапии инфекционного
эндокардита современного течения.
- Исследовать эффективность, разработать показания к применению плазмафереза,
внутрисосудистого лазерного облучения крови, ультрафиолетового облучения крови
в комплексном лечении инфекционного эндокардита.
- Определить возможности прогноза острой сердечной и полиорганной
недостаточности, эмболий при инфекционном эндокардите.
Научная новизна исследования
Впервые проведена оценка информативности клинических, лабораторных и
инструментальных методов исследования в диагностике затяжного, подострого,
острого течения болезни, инфекционного эндокардита протеза клапана,
инфекционного эндокардита у наркоманов (с преимущественным поражением правых
камер сердца).
Изучены особенности морфологических изменений внутренних органов (сердце,
сосуды, лёгкие, печень, почки, головной мозг и др.) при затяжном, подостром и
остром течении заболевания, инфекционном эндокардите протеза клапана,
инфекционном эндокардите у наркоманов.
Впервые разработаны показания для лечебного плазмафереза, внутрисосудистого
лазерного облучения крови, ультрафиолетового облучения крови в комплексном
лечении инфекционного эндокардита, основанные на изучении иммунологических,
гемостазиологических, реологических нарушений у больных эндокардитом.
Выявлено корригирующее влияние экстракорпоральной гемокоррекции на
иммунологические, гемостазиологические, реологические нарушения у больных ИЭ.
Установлена ведущая роль цитокинов (ФНО-L, интерлейкина-1) в реализации
иммуностимулирующих эффектов лазерной фотомодификации крови, роль цитокинов в
реализации иммуномодулирующих эффектов квантовой и эфферентной гемокомпонентной
терапии.
На основании изучения и анализа данных клинического,
инструментально-лабораторных исследований разработаны диагностические критерии,
которые с вероятностью до 92% позволяют верифицировать заболевание. Изучение и
анализ клинического и лабораторных методов исследования позволил разработать
достоверные критерии активности инфекционного эндокардита.
Впервые оценены возможности ультразвукового исследования для выявления
кардиальных и внекардиальных признаков болезни. Разработаны “главные” и
“дополнительные” ультразвуковые критерии инфекционного эндокардита, позволяющие
с вероятностью до 95% верифицировать диагноз.
Предложены новые алгоритмы диагностики раннего и позднего инфекционного
эндокардита протеза клапана, основанные на комплексном использовании
клинических, лабораторных методов исследования и чреспищеводной эхокардиографии,
достигающей 98% информативности в диагностике заболевания.
Определены диагностические критерии развития острой сердечной и полиорганной
недостаточности, эмболий при инфекционном эндокардите, разработаны модели их
прогноза.
Основные положения, выносимые на защиту
1. При инфекционном эндокардите изменения органов происходят в результате
системного поражения, обусловленного повреждением эндотелия сосудов
высоковирулентными бактериями, токсинами. Клинико-морфологическая картина
заболевания обусловлена полиорганными изменениями, возникающими под воздействием
сепсиса, тромбоэмболий, иммунокомплексных реакций, сердечной недостаточности.
Наибольший вклад в формирование клинико-морфологической картины вносят гепатит
(91%), спленит (88%), миокардит (86%), нефрит (68%), инфаркты органов (65%),
дистрофия миокарда (64%), абсцессы (56%), перикардит (52%), пневмония (45%),
миокардитический кардиосклероз (41%), гипертрофия миокарда (37%),
гломерулонефрит (32%), плеврит (24%), “застойная” почка (23%), инфаркт-пневмония
(20%).
2. Клиническая картина заболевания определяется совокупностью
инфекционнотоксического синдрома (24%), синдрома сердечной недостаточности
(21%), ведущими осложнениями иммунокомплексного, септического, эмболического
генеза (16%), нарушением центральной гемодинамики (12%), спленомегалией (8%). В
зависимости от преобладания симптомов и сочетания синдромов формируются варианты
течения и клинические формы болезни, возникают осложнения.
3. “Главными” диагностическими критериями инфекционного эндокардита являются:
вегетации, выраженная регургитация, абсцессы сердца, “отрыв” протеза клапана,
положительная гемокультура из двух и более проб крови, аускультативная динамика
шумов сердца, повышение температуры тела свыше 380С. Применение
диагностических критериев позволяет с вероятностью до 92% (при положительной
гемокультуре) и 78% (при отрицательной гемокультуре) установить диагноз.
4. Клиническими критериями активности заболевания являются: функциональный
класс сердечной недостаточности, длительность формирования порока сердца,
динамика аускультативных шумов сердца, выраженность лихорадки, озноба,
потливости, снижения массы тела, септического поражения почек, суставного и
эмболического синдромов, спленомегалии. В состав лабораторных критериев входят
показатели полиорганной недостаточности. Дифференцированная оценка критериев
активности в динамике позволяет оценить эффективность лечения.
5. “Главными” ультразвуковыми критериями инфекционного эндокардита являются:
вегетации, абсцессы сердца, выраженная регургитация, признаки “отрыва” протеза
клапана. В состав “дополнительных” входят: выпот в полость перикарда, отрыв
хорд, перфорации и разрыв створок клапанов, тромбоз протеза клапана,
парапротезные фистулы, септическое поражение органов брюшной полости. Диагноз
достоверен при выявлении не менее 1 “главного” и 2 “дополнительных” или 2
“главных” критериев при характерной клинической картине. При выявлении не менее
3 “малых” или только 1 “главного” ультразвукового критерия для подтверждения
диагноза необходимы положительная гемокультура, оценка клинической картины в
динамике.
Практическая значимость и реализация данных исследования
Разработаны диагностические критерии, критерии активности инфекционного
эндокардита, которые позволяют с вероятностью до 92% установить диагноз, степень
активности заболевания.
Предложен алгоритм комплексной диагностики инфекционного эндокардита с
использованием клинических, лабораторных и инструментальных методов исследования
на догоспитальном и госпитальном этапах обследования. Разработана программа
ранней диагностики инфекционного эндокардита протеза клапана, основанная на
оценке клинико-лабораторных признаков, применении чреспищеводной эхокардиографии.
Разработаны показания для лечебного плазмафереза, внутрисосудистого
лазерного, ультрафиолетового облучения крови у больных инфекционным
эндокардитом. Предложена программа экстракорпоральной гемокоррекции, основанная
на применении лечебного плазмафереза, внутрисосудистого лазерного и
ультрафиолетового облучения крови, для лечения иммунологических,
гемостазиологических, реологических нарушений у больных инфекционным
эндокардитом, что уменьшает вероятность развития фатальных осложнений.
Предложены алгоритмы проведения эмпирической антибактериальной терапии
инфекционного эндокардита, основанные на анализе структуры возбудителей,
комплексной оценке клинической картины заболевания.
Результаты исследования внедрены в практическую деятельность
кардиологического центра Главного военного клинического госпиталя МО РФ имени
академика Н.Н. Бурденко (Москва), кардиологического центра 442 Окружного
военного клинического госпиталя имени З.П. Соловьёва (Санкт-Петербург), клиники
кафедры сердечно-сосудистой хирургии имени академика П.А. Куприянова, клиники
кафедры военно-морской и общей терапии, клиники кафедры общей терапии № 1,
клиники кафедры терапии усовершенствования врачей Военно-медицинской академии
(Санкт-Петербург), кардиологического отделения клиник кафедры терапии Самарского
военно-медицинского института (Самара), кардиологического отделения клиник
кафедры терапии Томского военно-медицинского института медицинского университета
(Томск), кардиологических отделений областных клинических больниц в Самаре,
Томске.
Материалы исследования внедрены в учебный процесс и лекционный курс кафедры
сердечно-сосудистой хирургии им. П.А. Куприянова, кафедры военно-морской и общей
терапии, клиники кафедры общей терапии № 1, кафедры терапии усовершенствования
врачей Военно-медицинской академии (Санкт-Петербург), кафедры терапии, кафедры
терапии усовершенствования врачей Томского военно-медицинского института
(Томск), кафедры терапии, кафедры терапии усовершенствования врачей Самарского
военно-медицинского института (Самара), кафедры внутренних болезней
педиатрического факультета, кафедры факультетской терапии лечебного факультета
Сибирского государственного медицинского университета (Томск).
Издано учебное пособие “Инфекционный эндокардит: патогенез, клиника,
диагностика, лечение и профилактика” (Томск, 2003), содержащее информацию о
патогенезе, классификации, клинике, особенностях современного течения болезни. В
издании приводятся рекомендации по диагностике, дифференциальному диагнозу,
профилактике и лечению заболевания, которые получены на основании собственных
исследований.
Апробация работы
Материалы диссертации изложены на II Съезде врачей Сибири (Томск, 1999),
Всероссийской научно-практической конференции “Инфекционный эндокардит:
современные методы диагностики и лечения” (Москва, 2001), III Всероссийской
конференции с международным участием “Инфекция в хирургии – проблемы современной
медицины” (Москва, 2002).
По итогам работы сделаны сообщения на I Региональной научно-практической
конференции “Эфферентная медицина на современном этапе: достижения, проблемы,
перспективы решения” (Томск, 2002), III научных чтениях, посвящённых памяти
академика РАМН Е.Н. Мешалкина (Новосибирск, 2002).
Основные результаты исследований сообщены на Всероссийской
научно-практической конференции “Терапевтическая помощь в экстремальных
ситуациях” (С-Петербург, 2003), Всероссийской конференции, посвящённой памяти
В.Ф. Войно-Ясенецкого “Актуальные вопросы гнойно-септической хирургии”
(Красноярск, 2003), VI Всероссийской научно-практической конференции “Актуальные
вопросы диагностики и лечения в многопрофильном стационаре” (С-Петербург, 2003),
Международной конференции “Хирургические инфекции: профилактика и лечение”
(Москва, 2003).
Публикации
По теме диссертации опубликовано 30 печатных работ. На основании полученных
результатов исследования подготовлена и издана монография “Клиника и диагностика
инфекционного эндокардита” (Томск, 1999), учебное пособие “Инфекционный
эндокардит: патогенез, клиника, диагностика, лечение и профилактика” (Томск,
2003).
Структура и объём работы
Диссертация состоит из введения, 8 глав, включающих обзор литературы,
характеристику исследуемого контингента и методов исследования, 5 глав
собственных исследований, заключения, выводов, практических рекомендаций, списка
литературы, 56 приложений. Работа изложена на 242 страницах машинописного
текста, содержит 78 таблиц, 30 рисунков. Библиография включает 482 литературных
источников.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Материал исследования
Материал исследований базируется на наблюдении 250 больных и анализе 148
архивных историй болезни за десять лет (1991-2001 гг). Возраст больных составил
36,3+8,18 года. Среди обследованных было 26,4% женщин и 73,6% мужчин
(таблица 1). Больные основной группы были разделены на 5 подгрупп. В 1 подгруппе
– 54 больных затяжным ИЭ, во 2 подгруппе – 50 больных подострым ИЭ, в 3
подгруппе – 47 больных острым ИЭ. Для изучения особенностей клиники ИЭ у
наркоманов, ИЭ протеза клапана проведен анализ клинической картины у 44 и 55
больных, которые вошли в состав 4 и 5 подгрупп соответственно.
Таблица 1. Возраст, пол больных, длительность заболевания и
лечения
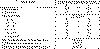
Примечание: абс. - абсолютное число больных, % - число больных в процентах, n
- число больных в группе.
Встречаемость вариантов течения и клинико-морфологических форм инфекционного
эндокардита у больных основной группы представлены в таблице 2.
Таблица 2. Варианты течения, клинико-морфологические формы
эндокардита
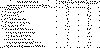
Выраженность СН определяли по классификации Нью-Йоркской
ассоциации кардиологов (1995), степень активности ИЭ – по классификации
Шевченко Ю.Л. (1995) (таблица 3).
Таблица 3. Активность инфекционного эндокардита,
функциональный класс сердечной недостаточности
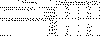
Локализация и частота поражения клапанов сердца инфекционным процессом у
исследуемого контингента была следующей: изолированное поражение АК у 92 (36,8%)
человек, ТК – у 42 (16,8%), МК – у 38 (15,2%), поражение АК и МК у 21 (8,4%), АК
и ТК у – 2 (0,8%) (табл. 4).
Таблица 4. Локализация и частота поражения клапанов сердца
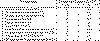
Регургитация 3, 4 степени на нативном АК, протезе АК отмечалась в 28,8% и
14,4% случаев соответственно, регургитация 3 степени на МК – в 14%, регургитация
3, 4 степени на ТК – в 12,4%, регургитация 2 степени на АК – в 11,2%. Достоверно
чаще определялись крупные (>10 мм), множественные, подвижные микробные вегетации
(49,6%) и крупные (>10 мм), единичные, подвижные микробные вегетации (20%) на
аортальном (36,8%) и трикуспидальном (17,6%) клапанах сердца, а также протезе АК
(14,4%) (таблица 5).
Таблица 5. Трансклапанная регургитация, характеристика
микробных вегетаций
В 48,9% случаев первичный ИЭ развивался после операций, медицинских
манипуляций и исследований: операций на сердце и других органах (7,5%),
катетеризации бедренной вены и артерии (6,8%), катетеризации подключичной вены
(6,8%), экстракции зубов (6%), тонзиллэктомии (4,5%), имплантации
электрокардиостимулятора (3,8%), урологических исследований (3,8%), частых
внутривенных инъекций (3,8%), наложения артериовенозного шунта при хроническом
гемодиализе (3%), зондирования сердца (2,3%), медицинского аборта (0,8%) и др.
Внутривенное введение наркотических веществ явилось причиной первичного ИЭ с
преимущественным поражением ТК в 33,1% случаев. Хронические очаги инфекции,
нтеркурентные инфекции, пневмония, инфекция мочевыводящих путей были причинами
формирования болезни в 20%, 6%, 3%, 0,7% случаев соответственно. В 12% случаев
выявлено сочетание нескольких причин (таблица 6).
Таблица 6. Причины развития первичного инфекционного
эндокардита
Диагноз инфекционного эндокардита основывался на диагностических критериях
D.T. Durac et al. (1994). По результатам гистологического исследования диагноз
подтверждён у 67% больных, по исследованию операционного материала – у 91%.
Положительная гемокультура выделена у 64% больных. Стафилококки высевались в 32%
случаев, стрептококки – в 13%, грамотрицательные бактерии – в 8%, смешанная
микрофлора – в 6,8%, грибы – в 2,4%, другие микроорганизмы – в 1,2% случаев.
Структура возбудителей представлена в таблице 7.
Таблица 7. Структура возбудителей инфекционного эндокардита
Больные основной группы предназначались для изучения клинической картины
заболевания, факторов риска острой сердечной и полиорганной недостаточности,
эмболий. Контрольную группу составили 43 больных в возрасте 36,6+1,96
лет. В её состав вошло 35% женщин и 65% мужчин. Структура исследуемых основной и
контрольной групп по своим параметрам, возрасту, полу, срокам существования
болезни и развития осложнений была однородна. В группе контроля положительная
гемокультура выделена в 61% случаев. Спектр выявленных микроорганизмов не
отличался от такового в основной группе. Это позволило использовать данную
группу для оценки факторов риска и точности прогноза осложнений.
Для анализа чувствительности и специфичности диагностических критериев
затяжного, подострого, острого инфекционного эндокардита использовались 2 группы
сравнения. В состав первой вошли больные ревматизмом (50 человек), второй –
больные сепсисом (50 человек). Эти группы больных по основным показателям не
отличались от больных ИЭ.
Всем больным проводилось лечение, включающее в себя антибактериальную и
синдромную терапию. Оно было направлено на купирование септического процесса,
компенсацию сердечной недостаточности, коррекцию осложнений. В каждом случае
терапия была индивидуальной с учётом выделенного возбудителя, тяжести состояния
больного, изменений в органах и системах, фазы развития и варианта течения
заболевания. Этиотропная антибактериальная химиотерапия проводилась с учётом
объёма лечения на предыдущих этапах. После получения результатов
бактериологических исследований крови применяли антибиотики с учётом
чувствительность микрофлоры.
Девяностосеми больным ИЭ наряду с медикаментозной терапией проведена
экстракорпоральная гемокоррекция: внутрисосудистое лазерное облучение крови,
ультрафиолетовое облучение крови, лечебный плазмаферез. В состав этой группы
вошло 29 больных затяжным ИЭ в активной стадии, 31 больной подострым ИЭ, 27
больных острым ИЭ. Контрольную группу составили 43 больных, которые получали
только традиционную терапию. Исследуемые группы не различались по частоте
встречаемости синдромов и симптомов, выраженности сердечной недостаточности,
степени активности заболевания, видовому составу бактерий, половым и возрастным
признакам. Эффективность экстракорпоральной гемокоррекции оценивали клинически,
по данным лабораторных и инструментальных исследований.
Время установления диагноза составило 2,0+0,21 месяца,
продолжительность заболевания – 5,43+0,35 месяцев. Длительность лечения в
основной группе не превышала 37+1,15 дней, в группе контроля – 35,8+1,72
дней. После консервативного лечения 140 (56%) пациентам по жизненным показаниям
проведена операция (реоперация) протезирования искусственного клапана. В
послеоперационный период у 31 (22%) больного развился ранний, у 24 (17%) –
поздний ИЭ протеза клапана. Летальный исход произошёл у 127 (51%) человек из
основной группы (у 16 из 1 подгруппы, у 21 из 2 подгруппы, у 36 из 3 подгруппы,
у 32 из 4 подгруппы, у 22 из 5 подгруппы), у 30 (72%) человек из контрольной.
Для изучения клинико-морфологической картины болезни рассмотрены 148
секционных наблюдений острого (31), подострого (28), затяжного (29)
инфекционного эндокардита, а также материалы секций 33 случаев ИЭ у наркоманов,
27 случаев ИЭ протеза клапана. Исследование охватило десятилетний период (с 1991
по 2001 гг.) и базировалось на сопоставлении историй болезни и протоколов
патологоанатомических вскрытий (таблица 8).
Таблица 8. Характеристика секционного материала
Таким образом, для изучения инфекционного эндокардита современного течения в
исследование вошло 250 больных и 148 секционных наблюдений за 10 лет (1991-2001
гг).
Методы исследования
Показатели сократительной способности сердца, центральной гемодинамики
изучали по данным эхокардиографии, которая проводилась на аппарате “ACUSON-128
XP/10” (США). Использовали В- и М-модальные режимы, спектральный,
постоянно-волновой и цветной допплер по стандартной методике. Чреспищеводную
ЭхоКГ выполняли на том же аппарате мультиплановым датчиком в стандартных
позициях. Использовали М- и В-модальные режимы, импульсный, постоянно-волновой,
цветной допплер, DTI-режим с кодированием движущихся тканей в определённый цвет
в зависимости от скорости их движения (DTI - vel.; DTI - асе.).
Рассчитывали следующие показатели: конечный систолический и диастолический
размер левого желудочка, толщину задней стенки в диастолу, конечный
систолический и диастолический объёмы, ударный объём, фракцию выброса ПЖ и ЛЖ,
фракцию укорочения, конечный систолический и диастолический индексы, массу
миокарда ЛЖ, индекс массы миокарда, индекс расслабления миокарда, сердечный
индекс, ударный индекс, минутный объём кровообращения, удельное периферическое
сопротивление и др. (Dodge H.T. et al., 1966; Беленков Ю.Н., 1986; Шиллер Н.,
Осипов Н.А., 1996; Сибалак Ш., 2002).
Изменения внутренних органов (печень, почки, селезёнка) исследовали на
аппарате “ACUSON-128 XP/10”(США) по стандартным методикам. Регистрацию
электрокардиограммы покоя осуществляли на электрокардиографе “BIOSET-8000”(ФРГ).
Изменения со стороны лёгких и сердца оценивали по результатам рентгенографии
органов грудной клетки в двух проекциях.
Биохимические показатели крови (общий билирубин, общий белок, альбумин,
глобулин, альбумин-глобулиновый индекс, креатинин, азот мочевины, АСТ, АЛТ,
щелочная фосфотаза и др.) определяли с использованием биохимических анализаторов
“SMA 12/60” фирмы “Technicon”(США), “Spectrum T-12” фирмы “Aввот” (США).
Диагностика основных гематологических синдромов включала в себя клинический
анализ крови, расчёт лейкоцитарного индекса интоксикации по методике
Кальф-Калифа Я.Я. (1941). Оценивали в динамике время рекальцификации плазмы (Bergerhof
H.D., Roka L., 1954), величину протромбинового индекса (Туголуков В.Н., 1953),
концентрацию общего фибриногена (Рутберг Г.А., 1961), фибринолитическую
активность (Котовщикова М.А., Кузник Б.И., 1962), толерантность плазмы к
гепарину (Капитаненко А.М., Дочкин И.И., 1988). Малоновый диальдегид в сыворотке
крови определяли методом M. Uchiyama, M. Мihara (1978).
Иммунный статус оценивали путем определения концентрации иммуноглобулинов M,
G, A (Mancini G. et al., 1965), циркулирующих иммунных комплексов (Гриневич
Ю.А., Алферова А.Н., 1981), количества Т- и В-лимфоцитов (CD3+, CD22+клеток),
Т-хелперов (СD4+клеток), Т-супрессоров (CD8+клеток), рецепторов интерлейкина-2
(СD25+) и Т-лимфоцитов (DR+) с помощью моноклональных антител серии НКО (“МБС”,
Москва) (Смирнов В.С. и др., 1993). Определяли индекс активности нейтрофилов в
базальных условиях и после стимуляции зимозаном (Меньшиков В.В., 1987).
Концентрацию фактора некроза опухоли, интерлейкина-1 в сыворотке крови
определяли иммуноферментным методом (“Протеиновый контур”, С-Петербург).
Cпособность клеток к продукции цитокинов изучали при стимуляции пирогеналом (Кетлинский
С.А., 1992). В лимфоцитах исследовали содержание продуктов деградации
нуклеопротеидов и активность супероксидисмутазы (Иванник Б.П. и др., 1986;
Дубинина Е.Е. и др., 1988). Из наиболее информативных гемореологических
показателей изучали вязкость цельной крови и плазмы с использованием
вискозиметра ВК-04. Индекс деформируемости эритроцитов, коэффициент вязкости
эритроцитов определяли по методу Фёдоровой З.Д. и др. (1989).
Патологоанатомический материал фиксировался в 10% нейтральном растворе
формалина, далее подвергался общепринятой воскопарафиновой проводке. Парафиновые
срезы окрашивались гематоксилиноэозином по Ван-Гизон (Лилли Т., 1969).
Для определения эффективности прогноза осложнений на основной и контрольной
группах применены критерии чувствительности и специфичности. Чувствительность
метода определялась по формуле (Ардашев В.Н., 1990):
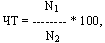
где: ЧТ – показатель чувствительности (%), N1 – число больных
правильно предсказанных, N2 – общее число больных. Специфичность
метода определялась по формуле (Ардашев В.Н., 1990):
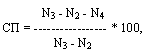
где: СП - показатель специфичности (%), N2 - число осложнений
рассматриваемого вида, N3 - общее число осложнений, N4 -
число ложноположительных решений для данного вида осложнений.
Математическая обработка цифровых данных исследования проводилась с
использованием персонального компьютера IBM PC/АТ-333ММХ по пакетам
статистических программ “Statistica-5”.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
1.1. Морфологическая картина инфекционного эндокардита современного течения
Морфологическая картина инфекционного эндокардита формировалась совокупностью
морфологических изменений органов. В 68% наблюдений обнаружена изолированная
недостаточность клапанов: аортального (30%), трикуспидального (22%), митрального
(14%). Сочетанное поражение аортального и митрального клапанов выявлено в 13%
случаев. Клинико-морфологическую картину заболевания обусловили гепатит (91%),
спленит (88%), миокардит (86%), нефрит (68%), инфаркты органов (65%), дистрофия
миокарда (64%), абсцессы (56%), перикардит (52%). Несколько реже
зарегистрированы пневмония (45%), миокардитический кардиосклероз (41%),
гипертрофия миокарда (37%), гломерулонефрит (32%), плеврит (24%). “Застойная”
почка (23%), инфаркт-пневмония (20%), эмпиема плевры (10%) выявлены значительно
реже.
Для затяжного ИЭ типично изолированное поражение клапанов (74%).
Аортальный клапан поражался достоверно чаще (58%) митрального (16%). Сочетанная
недостаточность аортального и митрального клапанов обнаружена в 25% наблюдений.
Первичный затяжной эндокардит развился после медицинских манипуляций и операций
(29%). Наиболее частыми причинами вторичного затяжного эндокардита (71%) были
ревматизм (45%) и атеросклероз (16%). Наибольший вклад в формирование
клинико-морфологической картины затяжного эндокардита внесли гепатит (87%),
спленит (77%), гипертрофия миокарда (87%), миокардит (84%), нефрит (77%),
инфаркты органов (58%). Несколько реже зарегистрированы миокардитический
кардиосклероз (52%), дистрофия миокарда (45%), “застойная” почка (42%).
Пневмония (29%), гломерулонефрит (29%), перикардит (19%), абсцессы (6,5%),
плеврит (6,5%), эмпиема плевры (3%) выявлены значительно реже.
При остром и подостром ИЭ характерно изолированное поражение клапанов (82%,
73%). Недостаточность аортального клапана обнаружена в 46% и 48% наблюдений
соответственно, митрального – в 36% и 24%. Сочетанное поражение МК и АК (18%,
24%), МК и ТК (3,4%) выявлено значительно реже. Морфологические изменения
формировались в результате распространённого эндоваскулита, множественных
тромбоэмболий, прогрессирующей сердечной недостаточности. Наибольший вклад в
клинико-морфологическую картину острого, подострого эндокардита внесли гепатит
(93%, 86%), спленит (100%, 93%), миокардит (82%, 93%), перикардит (76%, 50%),
дистрофия миокарда (55%, 71%), нефрит (43%, 86%), множественные инфаркты (79%,
68%), абсцессы (62%, 46%). Реже развивались пневмония (45%, 29%),
миокардитический кардиосклероз (38%, 46%), гипертрофия миокарда (21%, 46%),
гломерулонефрит (28%, 36%), плеврит (21%, 4%), “застойная” почка (17%, 39%).
Инфаркт-пневмония (10%, 4%), эмпиема плевры (14%, 4%) выявлены значительно реже.
При стафилококковом эндокардите некротизированные ткани часто подвергались
абсцедированию (74%).
Морфологические изменения органов при ИЭ у наркоманов соответствовали острому
и подострому течению заболевания, вызванного золотистым и эпидермальным
стафилококком. Специфично поражение интактного трикуспидального клапана (100%),
лёгких в виде инфаркт-пневмоний (64%) с формированием множественных абсцессов
(33%), которые наряду с септическим поражением печени (100%), селезёнки (94%),
почек (79%) определяли полисиндромность клинической картины. Значительный вклад
в формирование клинико-морфологической картины внесли миокардит (100%),
дистрофия миокарда (82%), нефрит и пневмония (79%), множественные абсцессы
(70%), инфаркты (61%), перикардит (61%). Несколько реже зарегистрированы плеврит
(42%), миокардитический кардиосклероз (33%). Эмпиема плевры (18%),
гломерулонефрит (21%), “застойная” почка (6%), гипертрофия миокарда (15%)
выявлены значительно реже.
При ИЭ искусственного клапана морфологические изменения соответствовали
острому и подострому течению болезни. Характерно поражение протеза клапана в
аортальной позиции (63%) с формированием параклапанных фистул (85%), отрывом
протеза (74%), развитием множественных абсцессов в фиброзном кольце (70%),
миокарде желудочков, межжелудочковой перегородке (22%), стенке аорты (7%).
Септическое поражение органов развивалось за непродолжительный период времени. В
формирование клинико-морфологической картины ИЭПК наибольший вклад внесли
множественные абсцессы (100%), гепатит (85%), спленит (74%), миокардит (67%),
дистрофия миокарда (67%), множественные инфаркты (59%), перикардит (56%), нефрит
(52%), гломерулонефрит (48%). Несколько реже выявлены миокардитический
кардиосклероз (37%), пневмония (41%), плеврит (44%). Гипертрофия миокарда (15%),
“застойная” почка (11%), инфаркт-пневмония (19%), эмпиема плевры (11%)
обнаружены значительно реже. Множественные септические очаги (93%) и инфаркты
(59%) обусловили тяжёлое течение заболевания, развитие острой сердечной и
полиорганной недостаточности, которые в 85% случаев явились причинами
смертельного исхода.
2.2. Клиническая картина инфекционного эндокардита современного течения
На первом этапе исследования использование факторного анализа позволило
изучить клиническую картину заболевания, выделить ведущие патологические
синдромы, определить значение каждого симптома и синдрома. На втором этапе
исследования выявлены особенности клинической картины различных вариантов
течения, особых клинических форм болезни (ИЭ у наркоманов, ИЭ протеза клапана).
Для клинической картины острого течения болезни характерны
выраженный инфекционнотоксический синдром, синдром сердечной недостаточности
(III-IV ФК по NYHA). Осложнения, нарушения в центральной гемодинамике дополняли
клиническую картину этого варианта болезни. Поражение сердца проявлялось
выраженным снижением сократительной способности ЛЖ, обусловленное развитием
миокардита и перикардита, значительным нарушением внутрисердечной гемодинамики
при формировании выраженной недостаточности АК и МК. Поражение эндокарда
заключалось в митральной, аортальной регургитации 2, 3 степени с локализацией
множественных, крупных, подвижных МВ на АК и МК, аортальной регургитацией 2
степени с локализацией МВ на АК, митральной регургитацией 2, 3 степени с
локализацией множественных, крупных, подвижных МВ на МК.
Среди изменений органов брюшной полости преобладали спленомегалия,
септические изменения селезёнки, печени, почек, их множественные эмболии,
инфаркты, абсцессы. В лабораторной картине наибольшее значение имели признаки
септического поражения печени и почек, воспаления, изменений в свёртывающей
системе крови. Положительная гемокультура острого эндокардита представлена
staphylococcus aureus, staphylococcus epidermidis, грамотрицательными
бактериями.
Подострое течение заболевания характеризовалось тем же сочетанием
синдромов, но в качестве ведущего выступал синдром сердечной недостаточности
(II-III ФК по NYHA) и лишь затем инфекционнотоксический синдром. Нарушение
центральной гемодинамики и осложнения дополняли клиническую картину болезни.
Изменения со стороны сердца заключались в гипертрофии ЛЖ, снижении показателей
систолической и диастолической функции ЛЖ. Поражение эндокарда проявлялось
аортальной регургитацией 3 степени с локализацией множественных, крупных,
подвижных МВ на АК, аортальной и митральной регургитацией 1, 2 степени с
множественными, мелкими, подвижными МВ, митральной и аортальной регургитацией 2,
3 степени с множественными, крупными, подвижными МВ на МК и АК. Для поражения
органов брюшной полости характерны септические изменения, сплено- и
гепатомегалия, множественные эмболии и инфаркты селезёнки, почек. Из данных
лабораторных исследований наиболее значительными были признаки иммунодефицита,
воспаления.
Затяжной вариант болезни характеризовался менее выраженными синдромами
сердечной недостаточности (I-II ФК по NYHA) и общей интоксикации, гипертрофией
миокарда и дилатацией ЛЖ, нарушением насосной функции ЛЖ. Поражение эндокарда
проявлялось митральной, аортальной регургитацией 2, 3 степени с множественными,
мелкими, подвижными МВ на АК, митральной регургитацией 2 степени с единичной,
крупной, подвижной МВ на МК, аортальной регургитацией 3 степени с
множественными, крупными, подвижными МВ на АК. Со стороны органов брюшной
полости чаще обнаруживали умеренное и незначительное увеличение печени и
селезёнки. Септическое поражение органов выявлено реже. Наиболее значимыми
лабораторными признаками заболевания были увеличение концентрации ЦИК, Ig A, M,
G, уменьшение лимфоцитов крови.
В клинической картине ИЭ у наркоманов доминировал
инфекционнотоксический синдром, который характеризовался лихорадкой до 39-420С,
потрясающими ознобами, артромиалгиями, обильным потоотделением, увеличением ЧСС
до 142, значительным снижение массы тела. Специфично отсутствие облегчения у
пациентов после снижения температуры и потоотделения. Выраженная интоксикация,
наблюдавшаяся у большинства пациентов (91%), вызвана неспособностью систем
организма справиться с увеличением концентрации токсинов.
По частоте встречаемости и значимости синдром поражения лёгких занимал второе
место (75%). Он проявлялся: выраженной одышкой в покое и при незначительной
физической нагрузке, приступами удушья, кашлем с мокротой, кровохарканьем,
жёстким и (или) ослабленным везикулярным дыханием, влажными хрипами в лёгких,
увеличением ЧДД до 32-36.
Синдром сердечной недостаточности (III-IV ФК по NYHA) развивался позднее чем
при поражении АК и МК, потому что изменения в центральной гемодинамике при
недостаточности ТК развивались значительно медленнее. Этот синдром
характеризовался увеличением печени, наличием выраженных отёков ног, асцита,
одышкой в покое, ортопное, наличием ослабленного везикулярного дыхания и влажных
хрипов, тяжестью в правом подреберье. Выраженная сердечная недостаточность
обусловлена лёгочной гипертензией (41%), инфекционнотоксическим миокардитом
(59%) и др. причинами.
В четвёртый клинический синдром вошли признаки, отражающие проявления
наркотической абстиненции, наиболее выраженной на 2-3 сутки пребывания пациентов
в клинике: повышенная раздражительность, боли во всём теле, бессонница, тремор
рук, кровотечение из носа, обильное потоотделение, повышение уровня
систолического АД, тахикардия, тошнота и рвота. Синдром гепатоспленомегалии
умеренно выражен.
При ИЭ у наркоманов (с преимущественным поражением правых камер сердца)
обнаружены выраженные изменения признаков, вошедших в эхокардиографические
синдромы нарушения сократительной способности миокарда и насосной функции
правого желудочка (33%), сердечной недостаточности по малому кругу (23%),
нарушения центральной гемодинамики (15%).
Зарегистрировано увеличение конечного систолического, диастолического объёмов
ПЖ, уменьшение фракции выброса ПЖ. Изменения насосной функции (уменьшение
ударного объёма ПЖ, МОК по малому кругу) были менее выражены. Нарушение
сократительной способности, снижение насосной функции ПЖ обусловлены развитием
миокардита, экссудативного перикардита (72-86%), дилатацией правых камер сердца,
изменением внутрисердечной гемодинамики при формировании выраженной
недостаточности трёхстворчатого клапана. Эхокардиографические признаки поражения
эндокарда представлены: трикуспидальной регургитацией 3 степени с локализацией
множественных, крупных, подвижных МВ на ТК (34%), трикуспидальной регургитацией
2 степени с локализацией крупных, множественных, подвижных МВ на ТК (24%),
трикуспидальной регургитацией 2 степени с локализацией мелких, множественных,
подвижных МВ на ТК (14%). Ультразвуковую картину изменений органов брюшной
полости сформировали признаки септического поражения печени, селезёнки, почек
(78%). Вклад признаков, вошедших в синдром поражения печени, превысил 34%. Чаще
регистрировались септические изменения, множественные эмболии с последующим
формированием инфарктов и абсцессов.
В состав электрокардиографических проявлений этой формы болезни вошли:
синусовая тахикардия (28%), нарушение проводимости (17%) и возбудимости сердца
(14%), неполная атриовентрикулярная блокада (12%). Рентгенологическая картина
органов грудной клетки представлена лёгочной инфильтрацией и деструкцией,
абсцедированием лёгких, выраженными застойными явлениями, увеличением правых
камер сердца (85%). Среди данных лабораторных исследований наиболее выразительны
признаки воспаления (24%), иммунодефицита (20%), поражения печени и почек (16%),
гипо - и диспротеинемия (8%). Положительная гемокультура представлена
staphylococcus aureus, staphylococcus epidermidis.
Анализ структуры осложнений ИЭ у наркоманов выявил преобладание абсцессов
(61%) с локализацией в лёгких (70%), сердце (22%), селезёнке (3,7%),
почках (3,7%). В структуре эмболий (57%) поражение лёгочной артерии обнаружено в
92% случаев. Зарегистрировано достоверное увеличение количества пневмоний (46%),
которые подвергались абсцедированию более чем в 2/3 случаев. Среди
поражений лёгких (79%) преобладали инфаркт-пневмонии (32%). Септический спленит
(36%), гепатит (27%), миокардит (32%), плеврит (23%), нефрит (25%) выявлены
менее чем у 40% больных. Острая сердечная и полиорганная недостаточность
зарегистрированы в 21% и 18% случаев соответственно. Для ИЭ у наркоманов
характерно частое развитие тромбоэмболии лёгочной артерии, которая в 25% случаев
была причиной смерти больных.
В клинической картине ИЭ протеза клапана выявлено несколько синдромов:
инфекционнотоксический, сердечной недостаточности, ведущих осложнений,
гепатоспленомегалии. Превалировал инфекционнотоксический синдром, который
проявлялся повышением температуры тела до 39,5-410С с потрясающими
ознобами, артромиалгиями, гектической и фебрильной лихорадкой, обильным
потоотделением, увеличением ЧСС до 158, снижением массы тела.
По частоте встречаемости и значимости синдром сердечной недостаточности
(III-IV ФК по NYHA) занимал второе место. Он проявлялся одышкой в покое,
ортопное, увеличением печени, наличием асцита, выраженных отёков на ногах,
ослаблением везикулярного дыхания, влажными хрипами в лёгких, тяжестью в правом
подреберье.
В состав третьего синдрома вошли признаки ведущих осложнений (острая
сердечная и полиорганная недостаточность, эмболии, инфаркты органов, гепатит,
спленит, миокардит, перикардит): частые приступы удушья, кровохарканье,
увеличение ЧДД и ЧСС, ортопное, ослабленное везикулярное дыхание, выявляемое при
аускультации лёгких и др.
Нарушения в центральной гемодинамике представлены симптомами,
характеризующими динамику изменений сердечно-сосудистой системы при формировании
парапротезных фистул (80-92%), отрыве протезов АК (66%), МК (18%), МК и ТК (7%),
АК и МК (3,6%), ТК (3,6%). В его состав вошли: снижение уровня систолического,
диастолического, среднего гемодинамического АД, выраженные отёки ног, увеличение
размеров печени. Синдром гепатоспленомегалии занял пятую позицию.
Ранний ИЭПК развивался спустя 0,9+0,1 месяца после операции на сердце,
характеризовался выраженными клиническими признаками. В
большинстве случаев лихорадка сопровождалось ознобом, который завершался
обильным потоотделением. При активном расспросе все больные предъявляли жалобы
на одышку, приступы удушья, боли в области сердца, сердцебиение, перебои в
работе сердца, артромиалгии, отсутствие аппетита. При осмотре выявлены бледность
и желтушность кожи, иктеричность склер, признаки аутоиммунного васкулита
(петехии, геморрагическая сыпь, симптом Лукина), симптомы декомпенсации
сердечной недостаточности (выраженная общая слабость, одышка в покое, отёки
нижних конечностей, асцит и др.).
У всех больных ранним ИЭПК зарегистрировано тяжёлое (42%), крайне тяжёлое
состояние (58%). При объективном обследовании более чем у 2/3 больных
выслушивались новые аускультативные шумы сердца, происходило изменение ранее
существовавших. Для лиц с протезами АК характерно появление диастолического шума
параклапанной недостаточности. У пациентов с протезами МК, ТК часто выслушивался
систолический шум параклапанной недостаточности. Значительно реже определялся
шум, вызванный обструкцией протеза клапана тромботическими массами, крупными МВ.
Характерными клиническими признаками раннего ИЭПК были метастатические
абсцессы в сердце, печени, селезёнке, почках, лёгких и головном мозге (100%),
спленомегалия (68%), эмболии артерий конечностей, почек, лёгких, головного мозга
(39%).
Поздний ИЭПК развивался спустя 2,7+0,2 месяца после операции на
сердце. Клиническое течение имело подострый характер, что затрудняло
своевременную диагностику. Симптомы сепсиса были мало выражены у 50% больных. В
5 (21%) случаях наблюдалось безлихорадочное течение, в 10 (42%) – повышение
температуры тела до субфебрильных цифр. У остальных больных (38%) определялся
подъём температуры в виде “свечи”, сопровождающийся потрясающим ознобом,
проливным потом. Менее выраженными, чем при раннем ИЭПК были одышка,
сердцебиение, общая слабость, артромиалгии.
Проявления иммуновоспалительных реакций в виде системного васкулита (21%),
спленомегалии (67%), гломерулонефрита (42%) по сравнению с ранним ИЭПК выявлены
чаще. Однако, артериальные эмболии (25%) и абсцессы органов (50%) встречались
реже. Появление аускультативных шумов сердца, изменение их характеристик
обнаружено у 15 (63%) больных. Виды дисфункций искусственного клапана (парапротезные
фистулы, тромбозы, микробные вегетации и др.), их аускультативные характеристики
соответствовали таковым при раннем ИЭПК.
В этой группе определены выраженные изменения эхокардиографических синдромов
сердечной недостаточности (35%), нарушения сократительной способности и насосной
функции ЛЖ (26%), нарушения центральной гемодинамики (17%), гипертрофии и
дилатации ЛЖ (10%). Зарегистрированы максимальные изменения в показателях
сократительной способности ЛЖ (увеличение КСО, КДО, уменьшение фракции выброса и
фракции укорочения). Нарушение насосной функции ЛЖ (уменьшение ударного объёма,
МОК по большому кругу) было менее выражено и компенсировалось увеличением ЧСС.
Эхокардиографические признаки поражения эндокарда характеризовались
параклапанной регургитацией на протезе АК с локализацией множественных, крупных,
подвижных МВ (25%), парапротезными фистулами с тромбозом и отрывом
искусственного АК (21%), параклапанной регургитацией на искусственном МК с
локализацией множественных, мелких, подвижных МВ (15%), парапротезными
фистулами, тромбозом и отрывом искусственного МК (12%), параклапанной
регургитацией на протезе МК с локализацией крупной, единичной, подвижной МВ
(8%).
Ультразвуковую картину изменений органов брюшной полости сформировали
признаки септического поражения селезёнки (32%), печени (26%), почек (18%). При
раннем ИЭПК превалировали множественные тромбоэмболии (86%) с формированием
инфарктов и абсцессов. При позднем ИЭПК эмболии развивались значительно реже
(32%). При электрокардиографии зарегистрированы нарушения проводимости (30%) и
возбудимости сердца (22%), ишемия и ишемическое повреждение миокарда (16%),
неполная блокада левой и правой ножек пучка Гиса (9%), синусовая тахикардия
(7%).
Рентгенологическая картина изменений органов грудной клетки представлена
застойными явлениями в лёгких, признаками отрыва протеза клапана, лёгочной
инфильтрацией, увеличением левых и правых камер сердца (78%). Из данных
лабораторных исследований наиболее выражены признаки воспаления (21%),
иммунодефицита (14%), поражения печени и почек (12%), нарушения в свёртывающей
системе крови (10%). Гемокультура представлена staphylococcus epidermidis,
staphylococcus aureus, стрептококками, грамотрицательными бактериями (18%).
2.3. Диагностические критерии инфекционного эндокардита, критерии активности
инфекционного эндокардита
На третьем этапе исследования проведен анализ показателей чувствительности и
специфичности более 270 клинико-лабораторных, инструментальных признаков
инфекционного эндокардита. По величине показателей чувствительности,
специфичности отобраны 4 главных и 11 дополнительных диагностических критериев
заболевания (таблица 9).
Таблица 9. Диагностические критерии инфекционного
эндокардита

Главными диагностическими критериями ИЭ являются микробные вегетации,
выраженная регургитация на клапанах, парапротезных фистулах, абсцесс сердца,
“отрыв” протеза клапана, положительная гемокультура, лихорадка свыше 380С,
аускультативная динамика шумов сердца. Ознобы, снижение массы тела, обильные
поты, артромиалгии, петехии, симптом Лукина, симптом Ослера, сплено - и
гепатомегалия, анемия, выпот в полость перикарда, ускорение СОЭ, “септическая”
почка, лейкоцитоз, лимфопения, отрыв хорд, перфорации и разрыв створок клапанов
вошли в состав дополнительных признаков. Применение разработанных
диагностических критериев позволило с точностью до 92% (при положительной
гемокультуре) и 78% (при отрицательной гемокультуре) установить диагноз.
Разработаны клинические и лабораторные критерии активности ИЭ, которые
использовались для оценки эффективности лечения (таблица 10, 11).
Таблица 10. Клинические критерии активности инфекционного
эндокардита

Примечание: + + + – значительное, + + – выраженное, + – умеренное, + -
– непостоянно.
Таблица 11. Лабораторные критерии активности инфекционного
эндокардита
Примечание: + + + - значительное, + + - выраженное, + - умеренное увеличение
концентрации.
Высокая (III степень) активность характеризовалась III-IV ФК сердечной
недостаточности, быстрой динамикой аускультативных шумов сердца, быстрым
формированием пороков, лихорадкой до 39-410С, обильными потами,
ознобами, суставным синдромом, частыми эмболиями, значительным снижением массы
тела, гепатоспленомегалией, частым поражением почек.
Отмечались гиперлейкоцитоз (свыше 16*109/л) или лимфопения,
выраженная гипохромная анемия (гемоглобин менее 80 г/л, эритроцитов менее 3*1012/л),
уменьшение количества тромбоцитов (менее 100*103/л), ускорение СОЭ
(свыше 40 мм/час), увеличение ЛИИ (более 6 усл. ед.), значительное увеличение
ЦИК (более 140 опт. ед.), иммуноглобулинов А, M, G, АСТ (свыше 100 ммоль/л), АЛТ
(свыше 100 ммоль/л), креатинина (более 2 мг/%), глобулина (более 60%),
уменьшение концентрации общего белка (менее 60 г/л), альбумина (менее 40%).
Регистрировалось снижение показателя протромбинового индекса (менее 60%),
увеличение концентрации фибриногена (свыше 7 г/л).
Для умеренной (II степень) активности свойственны II ФК сердечной
недостаточности, медленная динамика аускультативных шумов сердца,
продолжительное формирование пороков, лихорадка до 38-390С.
Характерны выраженное снижение массы тела, увеличение размеров печени и
селезёнки.
Отмечались лейкоцитоз (9-16*109/л) или лимфопения, гипохромная
анемия (гемоглобин 80-100 г/л, эритроциты 3-3,7*1012/л), уменьшение
количества тромбоцитов (100-180*103/л), ускорение СОЭ (20-40 мм/час),
выраженное увеличение показателя ЛИИ (2-6 усл. ед.), концентрации ЦИК (90-140
опт. ед.), иммуноглобулинов А, M, G. При биохимическом исследовании крови
регистрировалось увеличение концентрации АСТ (50-100 ммоль/л), АЛТ (40-100 ммоль/л),
креатинина (1-2 мг/%), глобулина (40-60%), уменьшение концентрации общего белка
(60-80 г/л), альбумина (40-60%). Снижены показатели протромбинового индекса
(60%-90%), увеличена концентрация фибриногена (4-7 г/л).
Минимальная (I степень) активность характеризовалась субфебрильной лихорадкой
(до 380С), I ФК сердечной недостаточности, очень медленной динамикой
шумов сердца, медленным формированием порока. Потливость, ознобы, суставной
синдром непостоянны. Могут отсутствовать эмболии, увеличение печени и селезёнки,
признаки поражения почек. В анализах крови: лейкоцитоз (менее 9*109/л),
умеренная гипохромная анемия (гемоглобин более 100 г/л, эритроцитов более 3,7*1012/л),
незначительное уменьшение количества тромбоцитов (не менее 180*103/л),
ускорение СОЭ (менее 20 мм/час), умеренное увеличение показателя ЛИИ (менее 2
усл. ед.), концентрации ЦИК (менее 90 опт. ед.), иммуноглобулинов А, M, G.
Регистрировалось незначительное увеличение концентрации АСТ (менее 50 ммоль/л),
АЛТ (менее 40 ммоль/л), креатинина (менее 1 мг/%), общего белка (более 80 г/л),
альбумина (более 60%), глобулина (менее 40%). Повышен показатель протромбинового
индекса (более 90%), снижена концентрация фибриногена (менее 4 г/л).
2.4. Результаты ультразвуковой диагностики
По данным исследования разработаны диагностические ультразвуковые критерии
инфекционного эндокардита естественного и искусственного клапанов, которые по
показателям чувствительности и специфичности расклассифицированы на главные и
дополнительные (таблица 12).
К главным диагностическим ультразвуковым критериям отнесены вегетации,
выраженная регургитация. В состав дополнительных вошли: абсцессы сердца,
септическое поражение органов, отрыв хорд, перфорации и разрыв створок клапанов,
выпот в полость перикарда.
Таблица 12. Ультразвуковые диагностические критерии ИЭ
естественных клапанов

Диагноз ИЭЕК достоверен при выявлении не менее 1 главного и 2 дополнительных,
2 главных критериев при наличии характерной клинической картины: аускультативная
динамика шумов сердца, лихорадка, ознобы, снижение массы тела, обильные поты,
артромиалгии, петехии, сопровождающиеся увеличением ЛИИ, ускорением СОЭ,
гипохромной анемией, лейкоцитозом со сдвигом влево или выраженной лимфопенией.
Чувствительность и специфичность диагностических признаков для определения ИЭЕК
составили 77% и 93% соответственно.
В состав главных диагностических ультразвуковых критериев ИЭ протеза клапана
вошли: вегетации, располагающиеся на искусственном клапане или параклапанно,
абсцесс сердца и признаки “отрыва” протеза. К дополнительным критериям отнесены:
парапротезные фистулы, регургитация на парапротезных фистулах, тромбоз протеза
клапана, выпот в полость перикарда, септическое поражение внутренних органов
(таблица 13).
Таблица 13. Ультразвуковые диагностические критерии
ИЭ протеза клапана
Диагноз ИЭПК достоверен при выявлении не менее 1 главного и 2 дополнительных
критериев, 2 главных критериев при наличии характерной клинической картины. При
определении 1 главного или не менее 3 дополнительных признаков для верификации
болезни проводили динамическое наблюдение за сердцем с использованием
чреспищеводной ЭхоКГ, анализировали клиническую картину и результаты
бактериологического исследования крови, операционного материала.
Чувствительность и специфичность ЭхоКГ для верификации ИЭ протеза клапана
составили 85% и 94% соответственно. Чреспищеводная ЭхоКГ оказалась наиболее
чувствительной (95%) и специфичной (100%) методикой диагностики кардиальных
признаков болезни. УЗИ внутренних органов было чувствительным (88%) и
специфичным (94%) методом диагностики экстракардиальных признаков инфекционного
эндокардита.
Ультразвуковые признаки эндокардита по показателям чувствительности и
специфичности расклассифицированы на главные и дополнительные диагностические
критерии. К главным ультразвуковым критериям отнесены: вегетации (100%, 100%),
признаки “отрыва” протеза клапана (100%, 100%), выраженная регургитация (74%,
100%), абсцессы сердца (72%, 100%). В состав дополнительных вошли: септическое
поражение органов брюшной полости (86%, 91%), выпот в полость перикарда (71%,
77%), тромбоз протеза клапана (22%, 72%), парапротезные фистулы (20%, 69%),
отрыв хорд, перфорации, разрыв створок клапанов (51%, 59%).
При апробации чувствительность и специфичность разработанных диагностических
критериев составили 93% и 98% при выявлении не менее 1 главного и 2
дополнительных ультразвуковых критериев, 2-3 главных при наличии характерной
клинической картины. Диагноз ИЭ наиболее вероятен при обнаружении не менее 3
дополнительных критериев или 1 главного ультразвукового критерия. В таких
случаях для подтверждения диагноза необходимо получение положительной
гемокультуры из трёх и более проб крови, оценка клинической картины в динамике.
2.5. Алгоритмы диагностики
На основании данных проведенного исследования разработаны алгоритмы
диагностики инфекционного эндокардита. Алгоритмы включают сбор жалоб и анамнеза,
проведение физикального обследования, изучение клинической картины, исследование
клинических и биохимических анализов крови, показателей иммунитета. Из данных
лабораторного обследования наиболее информативны бактериологическое исследование
крови и операционного материала, определение количества эритроцитов,
гемоглобина, лейкоцитов, лимфоцитов крови, подсчёт лейкоцитарного индекса
интоксикации. Исследование иммунитета включало оценку концентрации ЦИК и
иммуноглобулинов крови. Из биохимических показателей важны АСТ, АЛТ, креатинин,
белок крови и его фракции.
При амбулаторном обследовании (поступлении в стационар) в случае подозрения
на ИЭ, выявляли клинико-лабораторные признаки болезни: аускультативные шумы
сердца, длительное повышение температуры тела, лихорадку, ознобы, обильные поты,
артромиалгии, снижение массы тела, петехии, увеличение ЛИИ, ускорение СОЭ,
гипохромную анемию, лейкоцитоз (лимфопению). По показаниям проводили ЭхоКГ, УЗИ
печени, почек, селезёнки.
Во время стационарного обследования осуществляли динамический контроль за
показателями температуры тела, АД, ЧСС, ЧДД, массы тела, диурезом. При
физикальном обследовании больных оценивали в динамике шумы сердца,
аускультативную картину лёгких, признаки активности инфекционного эндокардита,
выраженности сердечной недостаточности. Для выявления кардиальных ультразвуковых
признаков наиболее эффективны полипозиционная ТТЭхоКГ, дуплексное и триплексное
сканирование с использованием комбинаций В-режима с постоянно-волновым,
импульсно-волновым, цветным допплером, В-режима с DTI. При отрицательных
результатах ТТЭхоКГ проводили чреспищеводную ЭхоКГ с частотой, определяемой
изменением клинической картины заболевания.
Особенностью диагностики ИЭ протеза клапана в послеоперационном периоде
является разделение больных на две группы по наличию инфекционных осложнений. В
группе больных без инфекционных осложнений проводили клиническое наблюдение и
обследование, сходное с таковыми при стационарном лечении. Во второй группе
проводили трёхкратное бактериологическое исследование крови, ЭхоКГ-мониторинг с
использованием ТТЭхоКГ и ЧПЭхоКГ (с интервалом в 1-3 дня) для раннего выявления
кардиальных ультразвуковых признаков ИЭПК.
Наиболее информативно триплексное сканирование: комбинация В- и М-режимов с
цветным допплером, комбинация В-режима с импульсно-волновым и постоянно-волновым
допплером. Эти режимы применяли для выявления парапротезных фистул, оценки
выраженности регургитации на искусственном клапане. При проведении ЭхоКГ
оценивали функционирование протеза клапана, трансклапанный кровоток,
сократительную способность и насосную функцию левого желудочка сердца. В ходе
УЗИ селезёнки, печени, почек регистрировали экстракардиальные признаки болезни.
С учётом изменений в клинической картине проводили рентгенологическое
исследование органов грудной клетки, электрокардиографию. Осуществляли
мониторинг показателей центральной гемодинамики, метаболизма.
2.6. Осложнения, причины летальных исходов
У большинства пациентов развились осложнения (82%), которые нередко были
множественными (45-58%). Частыми осложнениями ИЭ были спленит и гепатит (73%,
62%), эмболии (68%), инфекционнотоксический миокардит (58%), нефрит (57%).
Перикардит (49%), абсцессы и инфаркты органов (46%, 41%), пневмония (30%),
плеврит (23%), острая сердечная и полиорганная недостаточность (17%, 16%)
зарегистрированы у менее 50% больных. Анализ осложнений в исследуемых группах
выявил определённые закономерности их развития, которые соответствовали варианту
течения, клинической форме заболевания.
Летальный исход зарегистрирован у 127 (51%) больных. Наиболее частыми
причинами смерти были острая сердечная (29%) и полиорганная недостаточность
(28%), эмболии в головной мозг, коронарные артерии, лёгочную артерию (25%). Их
суммарный вклад в структуру причин летальных исходов составил более 81%.
Септический шок (8%), острая почечная недостаточность (5,5%), абсцедирующая
пневмония (5,5%) были фатальными достоверно реже (19%). Эмболический инфаркт
миокарда явился причиной смерти 4 (3%) больных инфекционным эндокардитом.
Актуальность лечения и профилактики данных осложнений вызвала необходимость
изучения возможности их прогноза.
2.7. Прогноз фатальных осложнений
Для разработки моделей прогноза фатальных осложнений отобраны признаки по
степени информативности, достоверности. С целью адекватного прогноза
руководствовались общепринятыми этапами статистической обработки данных
клинических и инструментально-лабораторных исследований. Из методов многомерной
статистики использовали регрессионный анализ. Модель прогноза острой сердечной
недостаточности имеет вид:
ОСН = 6,5 - 0,1*Х 1 - 1,2*Х 2 - 0,2*Х 3 -
0,04*Х 4 - 0,01*Х 5 ,
где: ОСН - показатель прогноза острой сердечной недостаточности (усл. ед.),
6,5 - константный показатель,
Х 1 - продолжительность неэффективного лечения (дни),
Х 2 - функциональный класс сердечной недостаточности по NYHA (1,
2, 3, 4),
Х 3 - показатель лейкоцитарного индекса интоксикации (усл. ед.),
Х 4 - удельное периферическое сопротивление (усл. ед.),
Х 5 - масса миокарда левого желудочка сердца (г).
Модель прогноза полиорганной недостаточности имеет вид:
ПOН = 20 - 0,1*Х 1 - 0,5*Х 2 - 0,8*Х 3 -
0,8*Х 4 - 0,3*Х 5 - 0,03*Х 6 + 0,1*Х 7
+ 2*Х 8 ,
где: ПOН - показатель прогноза полиорганной недостаточности (усл. ед.),
20 - константный показатель,
Х 1 - продолжительность неэффективного лечения (дни),
Х 2 - температура тела (0С),
Х 3 - функциональный класс сердечной недостаточности по NYHA (1,
2, 3, 4),
Х 4 - показатель лейкоцитарного индекса интоксикации (усл. ед.),
Х 5 - концентрация общего билирубина в крови (мг/%),
Х 6 - концентрация азота мочевины в крови (мг/%),
Х 7 - концентрация иммуноглобулина G в крови (г/л),
Х 8 - концентрация белка в моче (г/л).
Модель прогноза эмболий имеет вид:
ЭО = 3,5 - 0,9*Х 1 - 0,2*Х 2 - 0,9*Х 3 - 2*Х
4 - 1,9*Х 5 + 1,3*Х 6 + 2*Х 7 ,
где: ЭО - показатель прогноза эмболических осложнений (усл. ед.),
3,5 - константный показатель,
Х 1 - функциональный класс сердечной недостаточности по NYHA (1,
2, 3, 4),
Х 2 - показатель лейкоцитарного индекса интоксикации (усл. ед.),
Х 3 - локализация микробных вегетаций на митральном, аортальном
клапане
(нет-0, есть-1),
Х 4 - локализация микробных вегетаций на трикуспидальном клапане
(нет - 0, есть - 1),
Х 5 - крупные (более 10 мм), множественные, подвижные микробные
вегетации
(нет - 0, есть - 1),
Х 6 - митральная, аортальная регургитация 3 степени (нет - 0, есть
- 1),
Х 7 - трикуспидальная регургитация 3 степени (нет - 0, есть - 1).
Разработанные модели прогноза позволили выявить больных с развитием
фатальных осложнений по величине рассчитываемого показателя прогноза. При
апробации точность прогноза по ОСН составила 95%, по ПОН и ЭО – 87% и 89%
соответственно. Наибольшая специфичность достигнута при прогнозе ОСН (97%),
несколько меньше для ПОН и ЭО (93%, 94%). В целом чувствительность и
специфичность прогноза фатальных осложнений ИЭ достигли 93% и 97%
соответственно. Из вышеуказанных моделей прогноза наибольшей точностью обладала
модель прогноза ОСН.
2.8. Комбинированное лечение инфекционного эндокардита
Лечебная программа включала антибактериальную и синдромную терапию,
экстракорпоральную гемокоррекцию (плазмаферез, ультрафиолетовое облучение крови,
внутрисосудистое лазерное облучение крови), проведение операции по показаниям. В
каждом случае лечение было индивидуальным. Учитывали вид возбудителя, тяжесть
состояния больного, фазу развития и вариант течения заболевания, объём лечебных
мероприятий на предыдущих этапах.
2.8.1. Результаты антибактериальной терапии
Основой предоперационного лечения ИЭ является антибактериальная терапия. При
лечении использовали бактерицидные антибиотики в максимальных суточных дозах.
Предварительно устанавливали чувствительность выделенного возбудителя к
антибиотикам. Определяли минимальную бактерицидную, минимальную подавляющую
концентрации антибиотиков. Продолжительность АБТ до получения выраженного
клинического эффекта при стрептококковом ИЭ составила 4+0,12 недели, при
стафилококковом и грамотрицательном – 6+0,1 и 8+0,14 недель
соответственно.
При АБТ стрептококкового ИЭ использовали гентамицин (2-2,5 мг/кг через 6 ч),
ванкомицин (40 мг/кг/сут и более). Негемолитические стрептококки в 50% случаев
были резистентны к пенициллинам и аминогликозидам. Применение сочетания этих
препаратов позволяло преодолеть вторичную резистентность бактерий к АБ в 62%
случаев. При выделении стрептококка с минимальной подавляющей концентрацией 5
мкг/мл и менее, применяли ванкомицин (в/в 1000 мг через 12 ч). В случае
отсутствия эффекта использовали цефалоспорины 1, 2, 3 поколения (цефалотин,
цефазолин, цефотаксим, цефтриаксон), имипенем (в/м 500-750 мг через 12 ч).
Золотистый стафилококк и коагулазонегативные стафилококки в 68% случаев были
резистентны к пенициллину, но обладали чувствительностью к
пенициллиназоустойчивым полусинтетическим пенициллинам (76%). При выделении
эпидермального и золотистого стафилококков, резистентных к полусинтетическим
пенициллинам, применяли ванкомицин (в/в 500 мг через 6 ч; в/в 1000 мг через 12
ч) в виде монотерапии или в сочетании с аминогликозидами (гентамицин 60-80 мг
2-3 раза в день; амикацин 5 мг/кг каждые 8 ч). Сочетанное использование
ванкомицина (500 мг через 6 ч) с гентамицином (60-80 мг 2-3 раза в день)
вызывало более выраженный клинический эффект из-за синергизма действия
антибиотиков. Для лечения ИЭ, вызванным метициллинрезистентным штаммом staph.
aureus, использовали ванкомицин (в/в 1 г через 12 ч) с положительным эффектом в
88% случаев. В группе больных стафилокковым ИЭ достигнуты положительные
результаты в 78% случаев.
Резистентность энтерококков к цефалоспоринам, полусинтетическим пенициллинам,
макролидам выявлена в 32% случаев. Однако большинство штаммов энтерококков (Е.
Faecalis, Е. Faecium) сохраняло чувствительность к гентамицину (63%) и
ванкомицину (83%). Поэтому АБТ начинали с внутривенного введения ампициллина (до
20 г/сут) и гентамицина (240-300 мг/сут). При отсутствии эффекта в течение 3-5
дней внутривенно вводили ванкомицин (0,5 г 4 раза в день) с гентамицином (80 мг
3 раза в день) в течение 4-5 недель с положительным клиническим эффектом у 75%
больных.
В лечении ИЭ, вызванного грамотрицательными бактериями, наиболее эффективно
сочетанное применение цефалоспоринов 1-3 поколения (в/в цефалотин – 8 г/сут, в/в
цефазолин – 8 г/сут, в/в цефотаксим - 8 г/сут, в/в цефтриаксон - 6 г/сут) с
гентамицином (5-6 мг/кг/сут) в течение 6 недель. Применение вышеуказанных
антибиотиков позволило в 81% случаев добиться клинико-бактериологической
ремиссии заболевания.
Для лечения грибкового эндокардита использовали амфотерицин В (до 1
мг/кг/сутки) в сочетании с флуцитозином (150 мг/кг/сут) или флуконазолом
(200-400 мг/кг/сут). При грибковом эндокардите АБТ в 84-88% случаев
неэффективна.
До получения результатов бактериологического исследования крови, при
отрицательной гемокультуре проводили эмпирическую антибактериальную терапию. Её
содержание определяли по тяжести состояния пациентов, варианту клинического
течения заболевания. Учитывали изменение основных клинических,
лабораторно-инструментальных признаков. Эффективность эмпирической АБТ оценивали
по динамике клинико-лабораторных критериев активности ИЭ. Продолжительность
эмпирической АБТ до выраженного клинического эффекта, нормализации лабораторных
показателей активности составила 4-8 недель.
При остром ИЭ эмпирическую антибактериальную терапию начинали с применения
2-3 антибиотиков из группы цефалоспоринов 1-3 поколения (цефалотин - 6-8 г/сут,
цефазолин - 6-8 г/сут, цефотаксим - 6-8 г/сут, цефтриаксон - 4 г/сут) и
антибиотиков резерва (имипенем - 4 г/сут, карбапенем - 3 г/сут, ванкомицин - 2-4
г/сут, ципрофлоксацин - до 4-5 г/сут). Лечение проводили 6-8 недель с
достижением выраженного клинического эффекта у 50 больных (74,6%).
При подостром течении эндокардита эмпирическую АБТ проводили двумя
антибиотиками синергидного действия: ампициллином (12-16 г/сут) с гентамицином
(1 мг/кг веса), ванкомицином (2-4 г/сут) с гентамицином (1 мг/кг веса) в течение
4-6 недель. В случае отсутствия положительного эффекта в течение 3-5 дней
назначали 2-3 антибиотика из группы цефалоспоринов 1-3 поколения (цефалотин -
6-8 г/сут, цефазолин - 6-8 г/сут, цефотаксим - 6-8 г/сут, цефтриаксон - 4 г/сут),
антибиотиков резерва (имипенем - 4 г/сут, карбапенем - 3 г/сут, ванкомицин - 2-4
г/сут). Лечение продолжали в течение 6-8 недель. Достигнут выраженный
клинический эффект у 38 больных (88%).
У больных затяжным ИЭ лечение начинали с сочетанного применения двух
антибиотиков: ампициллина (12-14 г/сут) с гентамицином (1 мг/кг веса),
бензилпенициллина (18-20 г/сут) с гентамицином (1 мг/кг массы в сут) в течение 4
недель. При отсутствии положительной динамики через 3-5 дней назначали
цефтриаксон (2-4 г/сут), цефотаксим (4-6 г/сут) на протяжении 4-6 недель.
Клинико-бактериологическая ремиссия ИЭ достигнута в 96% случаев.
При эффективной антибактериальной терапии зарегистрированы уменьшение или
полное исчезновение признаков инфекционнотоксического синдрома (100%),
достоверное снижение клинико-лабораторных показателей активности ИЭ
(96%). Получены отрицательные результаты повторных бактериологических
исследований крови (94%). В 84% случаев уменьшилось количество септических и
эмболических осложнений.
2.8.2. Результаты синдромной терапии
Использовано лечение, представляющее строго детерминированную
последовательность купирования ведущих синдромов (инфекционнотоксического,
сердечной недостаточности, ведущих осложнений), проводимое под контролем
клинико-лабораторных показателей в динамике. Лечение ведущих синдромов затяжного
ИЭ не представляло затруднений. Однако, при остром и подостром ИЭ требовалась
оптимизация терапии для обеспечения максимального лечебного эффекта, сведения
к минимуму возможности развития осложнений.
Для лечения инфекционнотоксического синдрома использовали
детоксикационную терапию. Вводили растворы (физиологический раствор, 5% и 10%
раствор глюкозы, электролиты и др.) и мочегонные в таком количестве, чтобы
суточный диурез превышал объём введенной жидкости на 200-400 мл. Жаропонижающие
средства (ацетилсалициловая кислота, анальгин с димедролом) назначали при
температуре тела свыше 380С. Использовали средние терапевтические
дозы медикаментозных препаратов, при остром и подостром ИЭ с выраженными
проявлениями синдрома – максимальные. Признаками эффективного лечения являлись:
снижение температуры но нормальных величин, ликвидация озноба, уменьшение
потливости, слабости, недомогания, нормализация лабораторных показателей
активности ИЭ (таблица 11).
При терапии сердечной недостаточности использовали комплексный подход,
воздействовали на несколько патофизиологических механизмов. Проводили инотропную
стимуляцию миокарда, снижали пост- и преднагрузку на сердце, воздействовали на
воспаление и аутоиммунные процессы в миокарде. Для достижения этих целей
назначали сердечные гликозиды и преднизолон (80-120 мг/сутки, парентерально),
для стабилизации клеточной мембраны и коррекции аутоиммунного поражения
миокардиоцитов. В случае усиления электрической нестабильности миокарда,
нарастания симптомов СН использовали медикаментозные препараты с положительным
инотропным действием (дофамин, допамин). Для разгрузки сердца применяли
диуретики (петлевые, тиазидные), периферические вазодилататоры (нитраты,
гидралазин), ингибиторы ангиотензинпревращающего фермента (эналаприл, каптоприл).
У больных с I-II ФК СН по NYHA наибольший эффект в лечении достигнут от
комбинированного применения тиазидных диуретиков и ингибиторов АПФ. Схема
лечения СН III ФК включала 1-2 диуретика, ингибитор ангиотензинпревращающего
фермента, периферический вазодилататор. В лечении СН IV ФК использовали петлевой
и тиазидный диуретики, ингибитор АПФ. При недостаточном эффекте осуществляли
инотропную стимуляцию миокарда дофамином (допамином). При значительном снижении
ФВ ЛЖ применяли неотон. Однако консервативное лечение терминальной СН в
большинстве наблюдений малоэффективно.
Мочегонные средства назначали индивидуально, под контролем концентрации
калия, магния, натрия в плазме крови. При I-II ФК СН по NYHA использовали
тиазидные диуретики (гидрохлортиазид, индапамид), при III-IV ФК – комбинацию
петлевых (фуросемид, лазикс) и тиазидных (гидрохлортиазид). Подбирали такую дозу
препарата (ов), которая позволяла достичь адекватного диуреза. В то же время
вводили антикоагулянты для профилактики ДВС-синдрома. При эффективной терапии
уменьшались признаки застоя по малому и большому кругу кровообращения,
ликвидировались симптомы СН.
Лечение осложнений ИЭ заключалось в проведении комплексной
медикаментозной терапии ОСН, тромбоэмболий, диcсеменированного внутрисосудистого
свёртывания крови, иммунокомплексного поражения органов. Неотложная терапия ОСН
включала применение дофамина (допамина), салуретиков (фуросемид, лазикс),
преднизолона (90-140 мг), эуфиллина, дроперидола, ингаляций увлажнённого
кислорода через маску. Госпитальная смертность составила 52%. При лечении
иммунокомплексного поражения органов использовали неспецифические
противовоспалительные препараты, глюкокортикоиды с положительным эффектом у 72%
больных.
Показателями положительного эффекта синдромной терапии являются:
уменьшение или полная ликвидация признаков инфекционнотоксического
синдрома, СН, положительная динамика при осложнениях, снижение активности
острофазовых реакций, нормализация клинико-лабораторных показателей активности
ИЭ (таблицы 10, 11). Синдромная терапия ИЭ – комплексное лечение ведущих
патологических синдромов. Лечебное воздействие медикаментозных препаратов
направлено на купирование инфекционного процесса, иммунокомплексных реакций,
компенсацию СН, коррекцию нарушений в системе гемостаза.
2.8.3. Эффективность экстракорпоральной гемокоррекции
У 36 больных острым, подострым ИЭ (в септической фазе) проведен плазмаферез
на аппарате “ПФ-0,5” с интервалом в 1-2 дня. В течение 1-1,5 ч в режиме
непрерывного фракционирования проводили эксфузию 1000+120 мл плазмы.
Проведение 4-6 сеансов ПФ больным острым и подострым ИЭ с выраженным
инфекционно-токсическим синдромом, способствовало снижению его выраженности и
улучшению общего состояния больных. Использование ПФ позволило достичь
положительных результатов в антибактериальной терапии, купировать инфекционный
процесс в результате снижения вторичной резистентности бактерий к антибиотикам.
После 4-6 сеансов ПФ происходило значительное уменьшение концентрации ЦИК,
иммуноглобулинов, фактора некроза опухоли, количества лейкоцитов, Т-супрессоров.
Увеличивалось количество Т-лимфоцитов, Т-хелперов, повышалась активность
натуральных киллеров, происходила нормализация хелперно-супрессорного
соотношения по сравнению с группой контроля.
После ПФ уменьшилась концентрация общего билирубина, креатинина, азота
мочевины, глобулинов крови. Показатели трансаминаз достигли нормальных величин.
В 2,3 раза снизился показатель лейкоцитарного индекса интоксикации.
Использование ПФ оказывало положительное воздействие на сократительную и
насосную функцию сердца (увеличивалась фракция выброса ЛЖ, ударный объём,
ударный индекс) в результате удаления из организма бактерий, токсинов, ЦИК,
иммуноглобулинов, обладающих выраженным кардиотоксическим действием. Проведение
4-6 сеансов ПФ достоверно сократило сроки лечения, уменьшило количество иммунных
осложнений у больных подострым и острым ИЭ по сравнению с группой контроля.
Курс ВЛОК на аппарате “Изольда-1М”, состоящий из 4-6 сеансов с интервалом в
1-2 дня, выполнен 32 больным затяжным, подострым ИЭ. Использование ВЛОК оказало
нормализующее влияние на структурные и хронометрические показатели гемостаза.
Снижалась активность тромбообразования, уменьшилась концентрация фибриногена.
Произошла отчётливая коррекция реологических свойств крови, изменился индекс
деформируемости и коэффициент вязкости эритроцитов. После ВЛОК зарегистрировано
достоверное увеличение Т-лимфоцитов, уменьшение Т-супрессоров, нормализация
хелперно-супрессорного соотношения по сравнению с пациентами группы контроля.
После курса лазерного облучения увеличилось количество CD25-клеток, уменьшилась
концентрация фактора некроза опухоли, ЦИК, иммуноглобулинов А, М, G в крови,
стали менее выраженными лейкоцитоз, лимфопения. Количество септических
осложнений уменьшилось на 19%, тромбогеморрагических - на 18%, нарушений ритма и
проводимости сердца - на 14%. При исследовании иммунитета выявлен рост пула
Т-клеток, тенденция к увеличению Т-хелперов, повышение дифференцировочного
индекса CD4/CD8 по сравнению с аналогичными показателями группы контроля в такие
же сроки наблюдения.
У 29 больных ИЭ, получавших УФОК, достигнут выраженный клинический эффект:
достоверно снизилась длительность лихорадочного периода, уменьшилась
выраженность проявлений инфекционно-токсического синдрома (понизилась
температура тела, уменьшились озноб, потливость, ЧСС, ЧДД, размеры селезёнки и
др.). При оценке степени активности ИЭ в динамике происходили изменения
признаков, которые характеризовали его снижение. Выздоровление наступало на 6+0,5 дней
раньше чем в группе контроля. Продолжительность антибактериальной терапии
сократилась на 5-6 дней.
Выраженный клинический эффект достигнут у больных затяжным, подострым ИЭ с
синдромом висцеральных иммунокомплексных поражений. После проведения 3-4 сеансов
УФОК элиминировались ЦИК, увеличивалась концентрация гемоглобина, уменьшалось
количество лейкоцитов, лимфоциты достигали нормальных величин. Зарегистрировано
увеличение Т-лимфоцитов (CD3+клетки), тенденция к увеличению В-лимфоцитов
(CD22+клетки). После курса УФОК уменьшились признаки иммунокомплексных поражений
органов. Происходила положительная динамика клинических и лабораторных признаков
активности ИЭ. Достоверно сократились сроки лечения, купирования
иммунокомплексных осложнений. Однако у больных острым ИЭ не получено выраженного
клинического эффекта.
После УФОК увеличивалась спонтанная продукция ФНО-L и ИЛ-1, достоверно
увеличивалось количество Т-лимфоцитов и Т-хелперов. Увеличение экспрессии
Т-клеточных рецепторов (DR+клетки) обусловлено прямым действием
ультрафиолетового облучения на мембрану лимфоцитов, изменением продукции
иммуномодуляторов. Основной иммунорегуляторный эффект УФОК обусловлен продукцией
клетками крови эндогенных иммуномедиаторов (ИЛ-1, ФНО-L).
2.8.4.
Показания к хирургическому лечению
Лечение инфекционного эндокардита невозможно без хирургического
вмешательства. На практике важно определить тот момент, когда терапия исчерпала
свои возможности и её продолжение может привести к снижению функциональных
резервов больного. Основной тенденцией в хирургическом лечении ИЭ является
раннее проведение операции при минимальных внутрисердечных разрушениях, до
развития тяжёлых осложнений. Цель операции – устранение интракардиального очага
сепсиса, восстановление адекватной внутрисердечной гемодинамики, профилактика
осложнений.
Показаниями для хирургического лечения являются: формирование выраженной
недостаточности аортального клапана или нескольких клапанов; сепсис,
некупируемый антибактериальной терапией в течение 3-4 недель; нарастание
сердечной недостаточности до III-IV функционального класса по NYHA; высокий риск
развития или рецидив тяжёлых эмболических осложнений, острой сердечной и
полиорганной недосточности; билатеральное поражение сердца инфекционным
процессом; абсцессы сердца; эндокардит, вызванный высоковирулентной микрофлорой;
сочетание двух и более показаний. Снижение сократительной способности миокарда
(фракция выброса левого желудочка менее 40%), полиорганная недостаточность с
тяжёлыми и необратимыми изменениями органов являются противопоказаниями для
хирургического лечения.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ ИССЛЕДОВАНИЯ
Данные исследований свидетельствуют о патоморфозе инфекционного эндокардита.
Он обусловлен изменением микробиологического профиля с преобладанием
стафилококков, грамотрицательных бактерий и грибов, снижением удельного веса
стрептококков, развитием иммунодефицита, нерациональным использованием
антибиотиков. В последнее десятилетие увеличилось количество первичного
эндокардита в результате эпидемии внутривенной наркомании, нозокомиальных
причин, несостоятельности иммунитета и др. Чаще встречаются новые клинические
формы: инфекционный эндокардит у наркоманов (с преимущественным поражением
правых камер сердца), инфекционный эндокардит протеза клапана.
В последнее десятилетие клиническая картина инфекционного эндокардита
определялась морфологическими изменениями органов, которые формировались под
воздействием сепсиса, тромбоэмболий, иммунокомплексных реакций, хронической
сердечной недостаточности. При различных вариантах течения и клинических формах
болезни структура морфологических изменений претерпевала изменения.
Преобладал первичный инфекционный эндокардит (53%) с изолированной
недостаточностью одного клапана (67%): аортального (30%), трикуспидального
(22%), митрального (14%). Основными морфологическими изменениями были гепатит
(91%), спленит (88%), миокардит (86%), нефрит (68%), инфаркты (65%), дистрофия
миокарда (64%), абсцессы (56%), перикардит (52%), пневмония (45%),
миокардитический кардиосклероз (41%), гипертрофия миокарда (37%),
гломерулонефрит (32%), плеврит (24%), “застойная” почка (23%), инфаркт-пневмония
(20%), эмпиема плевры (10%).
Клиническая картина эндокардита, отражённая в факторном анализе признаков
всех обследованных больных отражала обобщённые клинические проявления
заболевания. Первый синдром представлен клиническими проявлениями сепсиса (24%).
Во второй синдром вошли клинические признаки сердечной недостаточности (21%).
Синдром ведущих осложнений представлен гепато - и спленомегалией,
периферическими отёками, асцитом, снижением массы тела, примесью крови в
мокроте, одышкой, петехиями, кардиалгией, артромиалгией (16%). Эти признаки
явились начальными проявлениями острой сердечной и полиорганной недостаточности,
эмболических осложнений. Четвёртое и пятое место заняли синдромы нарушения
центральной гемодинамики (12%), гепатоспленомегалии (8%). Следовательно,
проявления сепсиса, сердечной недостаточности, септических и эмболических
осложнений определяют клинику инфекционного эндокардита современного течения.
В состав электрокардиографических проявлений вошли синусовая тахикардия
(29%), нарушение проводимости сердца (21%), экстрасистолия (19%), неполная
атриовентрикулярная блокада (16%). Изменения центральной гемодинамики и
сократительной способности миокарда представлены признаками сердечной
недостаточности (42%), снижением систолической функции ЛЖ (25%), гипертрофией
миокарда ЛЖ (17%).
В эхокардиографическую картину поражения эндокарда наибольший вклад внесли:
аортальная регургитация 3 степени с локализацией МВ на АК (16%), митральльная
регургитация 3 степени с локализацией МВ на МК (13%), множественные, крупные,
подвижные МВ на МК и АК (12%), трикуспидальная регургитация 3 степени с
локализацией МВ на ТК (11%), митральная и аортальная регургитация 1, 2 степени с
локализацией МВ на МК, АК (10%).
Ультразвуковую картину брюшной полости сформировали признаки септического
поражения печени (33%), селезёнки (28%), почек (17%). По данным
рентгенологического исследования выявлены увеличение правых и левых камер сердца
(26%), лёгочная инфильтрация и деструкция (21%), выраженные застойные явления в
лёгких (19%), лёгочная инфильтрация, деструкция и абсцедирование (10%). Из
данных лабораторных исследований наиболее выражены признаки воспаления (23%),
иммунодефицита (14%), поражения почек (7%), гипо- и диспротеинемия (66%),
нарушения в свёртывающей системе (5%), острофазовые реакции (10%), мочевой
синдром (5%). Положительная гемокультура представлена стафилококками,
стрептококками, грамотрицательными бактериями, смешанной микрофлорой (19%).
Анализ данных исследований выявил взаимосвязи между лабораторными и
инструментальными признаками при разных вариантах течения инфекционного
эндокардита. У больных затяжным ИЭ эхокардиографическая картина представлена
тремя синдромами: сердечной недостаточности (36%), гипертрофии миокарда и
дилатации ЛЖ (24%), снижения насосной функции ЛЖ (17%). Их суммарный вклад
достиг 77%.
Из эхокардиографических признаков поражения эндокарда наиболее выражены
первые четыре: митральная, аортальная регургитация 2, 3 степени с
множественными, мелкими, подвижными МВ на АК (22%), митральная регургитация 2
степени с единичной, крупной, подвижной МВ на МК (17%), аортальная регургитация
3 степени с множественными, крупными, подвижными МВ на АК (13%), аортальная
регургитация 2 степени с множественными, мелкими, подвижными МВ на МК и АК
(11%). Их общий вклад превысил 72%.
Ультразвуковую картину брюшной полости сформировали признаки септического
поражения печени (34%), селезёнки (27%), почек (19%) с суммарным вкладом 9%. В
состав электрокардиографических проявлений вошли синусовая тахикардия (27%),
экстрасистолия и неполная атриовентрикулярная блокада (22%), нарушение
проводимости сердца (18%). Рентгенологическая картина представлена увеличением
правых и левых камер сердца, выраженными застойными явлениями в лёгких,
увеличением левых камер сердца (74%). Из данных лабораторных исследований
наиболее выражены показатели иммунодефицита (19%) и воспаления (13%), гипо- и
диспротеинемия (9%), острофазовые реакции (6%) с общим вкладом 59%.
Положительная гемокультура представлена streptococcus viridans, streptococcus
bettagemoliticuse, смешанной микрофлорой (11%).
В группе подострого ИЭ эхокардиографические признаки нарушения
центральной гемодинамики, сократительной способности миокарда не претерпели
кардинальных изменений. Но их числовые значения более выражены по сравнению с
предыдущей группой. Весовой вклад сердечной недостаточности и гипертрофии ЛЖ,
нарушения насосной функции ЛЖ составил 441% и 33% соответственно. Снижение
диастолической функции ЛЖ (11%) проявлялось уменьшением индекса расслабления
миокарда. Суммарный вклад этих синдромов достиг 89%. Эхокардиографические
признаки поражения эндокарда представлены: аортальной регургитацией 3 степени с
локализацией множественных, крупных, подвижных МВ на АК (21%), аортальной,
митральной регургитацией 1, 2 степени с множественными, мелкими, подвижными МВ
(18%), митральной и аортальной регургитацией 2, 3 степени с множественными,
крупными, подвижными МВ на МК и АК (12%), аортальной регургитацией 1, 2 степени
с локализацией МВ на АК (9%), локализацией множественных, мелких, подвижных МВ
на МК (6%). Ультразвуковую картину брюшной полости сформировали признаки
септического поражения селезёнки (32%), печени (29%), почек (16%). Чаще выявляли
сплено - и гепатомегалию, множественные эмболии и инфаркты селезёнки, почек.
В состав электрокардиографических проявлений вошли экстрасистолия и
пароксизмальная мерцательная аритмия (24%), нарушение проводимости (21%),
синусовая тахикардия и неполная блокада левой ножки пучка Гиса (14,81%),
неполная атриовентрикулярная блокада (13%) с суммарным вкладом 73%.
Рентгенологическая картина представлена лёгочной инфильтрацией, деструкцией,
увеличением правых и левых камер сердца, выраженными застойными явлениями в
лёгких (83%). Из показателей лабораторных исследований выражены признаки
воспаления (23%), иммунодефицита (16%), поражения почек (9%), изменений в
свёртывающей системе крови (7%), острофазовые реакции (12%), гипо- и
диспротеинемия (7%). Положительная гемокультура представлена staphylococcus
aureus и staphylococcus epidermidis (13%). Общий весовой вклад превысил 86%.
В группе острого ИЭ зарегистрированы достоверное уменьшение фракции выброса и
фракции укорочения ЛЖ, обусловленные развитием инфекционнотоксического
миокардита, экссудативного перикардита, нарушением внутрисердечной гемодинамики
при выраженной недостаточности АК и МК (36%). Синдромы сердечной недостаточности
(24%), нарушения центральной гемодинамики (17%) по своим весовым вкладам
занимали вторую и третью позицию. Выявлено значительное увеличение массы
миокарда и толщины задней стенки ЛЖ, увеличение конечного систолического и
диастолического размеров ЛЖ (11%). Их суммарный вклад превысил 88%. Для
эхокардиографических признаков поражения эндокарда характерны: митральная,
аортальная регургитация 2, 3 степени с локализацией множественных, крупных,
подвижных МВ на АК и МК (30%), аортальная регургитация 2 степени с локализацией
МВ на АК (22%), митральная регургитация 2, 3 степени с локализацией
множественных, крупных, подвижных МВ на МК (17%), митральная, аортальная
регургитация 1 степени с локализацией МВ на МК и АК (12%). Их общий весовой
вклад достиг 82%. Ультразвуковую картину изменений органов брюшной полости
сформировали признаки эмболий, инфарктов и абсцессов селезёнки, печени, почек
(83%). Весовой вклад септического поражения селезёнки превысил 35%.
В состав электрокардиографических проявлений вошли: синусовая тахикардия
(34%), неполная блокада левой ножки пучка Гиса и экстрасистолия (29%), неполная
атриовентрикулярная блокада (20%) с суммарным вкладом 82%. Рентгенологическая
картина представлена застойными явлениями в лёгких, лёгочной инфильтрацией,
увеличением правых и левых камер сердца, увеличением левых камер сердца (90%).
Из данных лабораторных исследований наибольшее значение имели признаки поражения
печени и почек (24%), воспаления (17%), изменений в свёртывающей системе крови
(11%), гипо - и диспротеинемия (10%), иммунодефицит (7%). Положительная
гемокультура представлена staphylococcus aureus, staphylococcus epidermidis,
грамотрицательными бактериями (20%). Суммарный весовой вклад синдромов превысил
89%. Обращает на себя внимание тот факт, что значения показателей лабораторных и
инструментальных исследований претерпевали изменения, которые связаны с
увеличением степени активности инфекционного эндокардита, выраженности
хронической сердечной недостаточности.
В состав комбинированного лечения ИЭ входят антибактериальная, синдромная
терапия, экстракорпоральная гемокоррекция, проведение операции по показаниям.
Антибактериальная терапия направлена на борьбу с возбудителями. Синдромная
терапия позволяет компенсировать сердечную недостаточность, снизить активность
инфекционного процесса, иммунокомплексных реакций, провести коррекцию нарушений
в системе гемостаза.
Экстракорпоральная гемокоррекция обладает выраженным детоксикационным,
иммуностимулирующим, кардиотропным, гемореологическим действием. Проведение
плазмафереза, ультрафиолетового и внутрисосудистого лазерного облучения крови
способствует коррекции и предупреждению развития септических, иммунокомплексных,
тромботических, геморрагических осложнений. Данные исследований указывают на то,
что экстракорпоральная гемокоррекция является важным дополнительным методом
лечения.
В настоящее время инфекционный эндокардит в значительной степени становится
хирургической проблемой. Тем не менее, для её решения необходима интеграция
усилий врачей разных специальностей. Основой успешного лечения является
своевременная диагностика, эффективная предоперационная терапия, ранняя
операция. Однако, в каждом конкретном случае необходим индивидуальный подход,
основанный на взвешенной оценке тяжести состояния больного, эффективности
проводимого консервативного лечения, вероятности развития фатальных осложнений.
Выводы
1. Современное течение инфекционного эндокардита характеризуется
преобладанием первичных форм заболевания у мужчин трудоспособного возраста,
изолированным (52%) и сочетанным (8%) поражением аортального и митрального
клапанов, изменением структуры возбудителей за счёт повышения удельного веса
стафилококков, грамотрицательных бактерий, грибов. При разных вариантах течения,
клинических формах заболевания видовой состав микрофлоры изменяется.
2. При затяжном варианте течения инфекционного эндокардита положительная
гемокультура представлена стрептококками (78%), смешанной микрофлорой (22%), при
подостром - стафилококками (61%), стрептококками (17%), смешанной микрофлорой и
грамотрицательными бактериями (8,7%, 8,7%), при остром – стафилококками (62%),
грамотрицательными бактериями (16%), смешанной микрофлорой (10%), грибами
(3,2%), при инфекционном эндокардите у наркоманов - стафилококками (78%),
смешанной микрофлорой (9,4%), грамотрицательными бактериями (6%), при
инфекционном эндокардите протезов клапанов - стафилококками (45%),
стрептококками (14%), грамотрицательными бактериями (22%), грибами (8%).
3. Клинико-морфологическая картина заболевания складывается из признаков
полиорганной патологии, формирующихся в результате септического эндоваскулита,
множественных эмболий, иммунокомплексных реакций, недостаточности
кровообращения. В формирование клинико-морфологической картины наибольший вклад
вносит сочетанное изменение органов, обусловленное системным поражением сосудов.
4. Клиническая картина инфекционного эндокардита является отражением
сочетания ведущих синдромов: инфекционнотоксического (24%), сердечной
недостаточности (21%), ведущих осложнений (16%), нарушения центральной
гемодинамики (12%), спленомегалии (8%). У наркоманов: инфекционнотоксического
(25%), лёгочных осложнений эмболического генеза (19%), сердечной недостаточности
(17%), наркотической абстиненции (15%), спленомегалии (13%). Инфекционного
эндокардита искусственного клапана: инфекционнотоксического (25%), сердечной
недостаточности (21%), ведущих осложнений (17%), нарушения центральной
гемодинамики (12%), гепатоспленомегалии (9%).
5. Главными диагностическими критериями заболевания являются: вегетации,
выраженная регургитация, абсцессы сердца, “отрыв” протеза клапана, положительная
гемокультура из 2 и более проб крови, повышение температуры тела свыше 380С,
аускультативная динамика шумов сердца. Диагностика основывается на оценке
совокупности клинико-лабораторных, инструментальных признаков с вероятностью до
92%.
6. Степень активности инфекционного эндокардита характеризуется
клинико-лабораторными признаками. В состав клинических признаков входят:
выраженность сердечной недостаточности, длительность формирования порока,
аускультативная динамика шумов сердца, выраженность лихорадки, озноба,
потливости, снижения массы тела, септического поражения почек, суставного и
эмболического синдромов, увеличение размеров печени, селезёнки. К лабораторным
признакам следует отнести: количество гемоглобина, эритроцитов, тромбоцитов,
лейкоцитов, лимфоцитов, концентрацию циркулирующих иммунных комплексов,
иммуноглобулинов, АЛТ, АСТ, креатинина, белков, фибриногена крови, скорость
оседания эритроцитов, лейкоцитарный индекс интоксикации, протромбиновый индекс.
7. Прогноз фатальных осложнений (с вероятностью до 87%) обусловлен
выраженностью сердечной недостаточности, величиной показателя лейкоцитарного
индекса интоксикации, продолжительностью неэффективного лечения, значительным
изменением уровня удельного периферического сопротивления, увеличенной массой
миокарда левого желудочка, повышенным содержанием общего билирубина, азота
мочевины и иммуноглобулина G в крови, белка в моче, локализацией, размером,
количеством и степенью подвижности вегетаций в сочетании с выраженностью
регургитации на аортальном, митральном, трикуспидальном клапанах.
8. При лечении инфекционного эндокардита с неустановленным возбудителем
рационально применять цефалоспорины 1-3 поколения и антибиотики резерва. При
подозрении на стафилококковый ИЭ необходимо использовать цефалоспорины 1-3
поколения и антибиотики резерва. При наиболее вероятном энтерококковом
эндокардите необходимо назначать два антибиотика синергидного действия (ампициллин
и гентамицин, ванкомицин и гентамицин). Продолжительность эмпирической
антибактериальной терапии составляет 4-6 недель. Признаками её эффективности
являются уменьшение выраженности клинических признаков, нормализация
лабораторных показателей активности эндокардита.
9. Проведение плазмафереза показано больным острым, подострым инфекционным
эндокардитом при выраженном синдроме эндогенной интоксикации, иммунодефиците,
вторичной резистентности бактерий к антибиотикам. Ультрафиолетовое и
внутрисосудистое лазерное облучение крови необходимо больным подострым и
затяжным эндокардитом средней степени тяжести, синдроме висцеральных
иммунокомплексных поражений. Экстракорпоральная гемокоррекция противопоказана
при полиорганной недостаточности.
10. Показаниями для проведения хирургического лечения являются: формирование
выраженной недостаточности аортального клапана или нескольких клапанов; сепсис,
некупируемый антибактериальной терапией в течение 3-4 недель; нарастание
сердечной недостаточности до III-IV функционального класса по NYHA; высокий риск
развития или рецидив тяжёлых эмболических осложнений, острой сердечной и
полиорганной недосточности; билатеральное поражение сердца инфекционным
процессом; абсцессы сердца; эндокардит, вызванный высоковирулентной микрофлорой;
сочетание двух и более показаний. Снижение сократительной способности миокарда
(фракция выброса левого желудочка менее 40%), полиорганная недостаточность с
тяжёлыми и необратимыми изменениями органов являются противопоказаниями для
хирургического лечения.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. При подозрении на инфекционный эндокардит у больных с лихорадкой неясного
генеза, выраженными ознобами, обильными потами, аускультативными шумами сердца,
необходимо выполнить не менее 3 посевов крови на стерильность (до начала
антибактериальной терапии) и провести ультразвуковое исследование сердца,
селезёнки, печени, почек.
2. Для больных с подозрением на инфекционный эндокардит ультразвуковое
исследование является скрининговым методом обследования. В ходе динамического
наблюдения использовать трансторакальную эхокардиографию с интервалом в
несколько дней. Обращать особое внимание на выявление ведущих кардиальных и
внекардиальных признаков заболевания. При развитии инфекционного эндокардита
протеза клапана проводить чреспищеводную эхокардиографию с интервалом в 1-3 дня.
3. Стандартное ультразвуковое исследование больных инфекционным эндокардитом
включает визуализацию клапанов и камер сердца в разных режимах (дуплексное,
триплексное сканирование с использованием комбинаций М- и/или В-режима с
постоянно-волновым, импульсно-волновым, цветным допплером, DTI). Для выявления
признаков септического поражения печени, селезёнки, почек использовать
ультразвуковое исследование в динамике. Ультразвуковой мониторинг при остром
течении заболевания осуществлять через 1-2 дня, при подостром (без признаков
полиорганной недостаточности) - через 3-4 дня, при затяжном - через 8-10 дней.
4. Антибактериальную терапию стрептококкового инфекционного эндокардита
необходимо проводить ампициллином (12-14 г/сут) с гентамицином (1 мг/кг веса) в
течение 3-4 недель. В случае отсутствия эффекта надо назначать антибиотики из
группы цефалоспоринов (цефтриаксон - 2-4 г/сут, цефотаксим - 4-6 г/сут) в
течение 4-6 недель до выраженного клинического эффекта и нормализации
лабораторных показателей активности заболевания.
5. Лечение инфекционного эндокардита, вызванного грамотрицательными
бактериями, целесообразно проводить 2-3 антибиотиками синергидного действия:
ампициллином (12-16 г/сут) с гентамицином (1 мг/кг массы тела) или ванкомицином
(2-4 г/сут) с гентамицином (1 мг/кг веса) в течение 4-6 недель до выраженного
клинического эффекта, нормализации лабораторных показателей активности
инфекционного эндокардита.
6. В антибактериальной терапии стафилококкового инфекционного эндокардита
рационально использовать цефалоспорины 1-3 поколения (цефалотин – 6-8 г/сут,
цефазолин – 6-8 г/сут, цефотаксим - 6-8 г/сут, цефтриаксон – 4 г/сут) с
антибиотиками резерва (имипенем - 4 г/сут, карбапенем - 3 г/сут, ванкомицин –
2-4 г/сут). Лечение проводить 4-6 недель до выраженного клинического эффекта,
нормализации лабораторных показателей активности заболевания.
7. Эффективность лечения целесообразно оценивать в динамике по
функциональному классу сердечной недостаточности, времени формирования
недостаточности клапанов, изменению характеристик аускультативных шумов сердца,
размерам печени и селезёнки, выраженности лихорадки, озноба, потливости,
эмболического синдрома, по изменению количества гемоглобина, эритроцитов,
лейкоцитов, лимфоцитов, тромбоцитов, концентрации ЦИК, иммуноглобулинов, АЛТ,
АСТ, общего белка, альбуминов, глобулинов, фибриногена, креатинина в крови, по
изменению показателей лейкоцитарного индекса интоксикации.
8. Прогноз острой сердечной и полиорганной недостаточности, эмболий
необходимо определять по продолжительности неэффективного лечения,
функциональному классу сердечной недостаточности, показателю лейкоцитарного
индекса интоксикации, уровню удельного периферического сопротивления, массе
миокарда левого желудочка, концентрации общего билирубина, азота мочевины и
иммуноглобулина G в крови, содержанию белка в моче, локализации, размеру,
количеству, подвижности вегетаций, степени регургитации.
9. Больным острым, подострым инфекционным эндокардитом с выраженным
инфекционнотоксическим синдромом, синдромом эндогенной интоксикации, при
развитии резистентности патогенных бактерий к антибиотикам необходимо проводить
4-6 сеансов плазмафереза с интервалом в 1-2 дня. Противопоказаниями являются
сердечная недостаточность IV функционального класса, полиорганная
недостаточность. Для оценки эффекта от плазмафереза использовать мониторинг
концентрации ЦИК, иммуноглобулинов, ФНО-L, AСТ, АЛТ, креатинина, белка и его
фракций в крови.
10. Больным затяжным, подострым инфекционным эндокардитом средней степени
тяжести на фоне синдрома иммунокомплексных висцеральных поражений целесообразно
проводить 3-4 сеанса ультрафиолетового облучения крови через 1-2 дня.
Противопоказаниями являются острое течение заболевания, выраженный
инфекционнотоксический синдром, сердечная недостаточность III-IV функционального
классов, полиорганная недостаточность. Для оценки эффекта от УФОК определять в
динамике концентрацию ЦИК, ФНО-L, ИЛ-1 в крови.
11. Больным острым, подострым инфекционным эндокардитом средней степени
тяжести на фоне синдрома вторичного иммунодефицита, диссеминированного
внутрисосудистого свёртывания 1-2 стадий, сердечной недостаточности II-III
функционального классов необходимо проводить 3-4 сеанса внутрисосудистого
лазерного облучения крови с интервалом в 2-3 дня. Противопоказаниями являются
синдром диссеминированного внутрисосудистого свёртывания 3-4 стадий, сердечная
недостаточность IV функционального класса, полиорганная недостаточность. Для
контроля результативности фотомодификации крови оценивать в динамике
концентрацию фибриногена крови, показатели деформируемости и вязкости
эритроцитов.
12. Хирургическое лечение противопоказано при снижении сократительной
способности миокарда (фракция выброса левого желудочка менее 40%), полиорганной
недостаточности с тяжёлыми и необратимыми изменениями органов. Показаниями для
хирургического лечения являются: формирование выраженной недостаточности
аортального клапана или нескольких клапанов; сепсис, некупируемый
антибактериальной терапией в течение 3-4 недель; нарастание сердечной
недостаточности до III-IV функционального класса по NYHA; высокий риск развития
или рецидив тяжёлых эмболических осложнений, острой сердечной и полиорганной
недосточности; билатеральное поражение сердца инфекционным процессом; абсцессы
сердца; эндокардит, вызванный высоковирулентной микрофлорой; сочетание двух и
более показаний.
Список работ, опубликованных по теме диссертации
1. Клиника и диагностика инфекционного эндокардита (Монография) Под ред.
проф. С.Б. Шустова, Г.Г. Хубулавы, Б.Б. Удальцова. - Томск: Изд. ТУСУР. - 1999.
- С. 110. Личный вклад автора в выполненную работу - 70%.
2. Инфекционный эндокардит: патогенез, клиника, диагностика, лечение,
профилактика (Учебное пособие). Под ред. проф. С.Б. Шустова, Г.Г. Хубулавы, Б.Б.
Удальцова. - Томск: Изд. ТУСУР. - 2003. - С. 94. Личный вклад автора в
выполненную работу - 70%.
3. Современный инфекционный эндокардит: особенности развития и течения // Сиб.
мед. журнал. - 2002. - № 3. - С. 78-85. (соавтор: М.В. Солдатенко). Личный вклад
автора в выполненную работу - 80%.
4. Этиология современного инфекционного эндокардита // Сб. материалов
Всероссийской науч.-практ. конф. “Инфекционный эндокардит: современные методы
диагностики и лечения”. - Москва, ГВКГ им. Н.Н. Бурденко. - 2001. - С. 5-7.
(соавторы: С.Б. Шустов, Б.Б. Удальцов). Личный вклад в выполненную работу - 60%.
5. Прогноз эмболических осложнений при инфекционном эндокардите // Там же. -
Москва, 2001. - С. 22-25. (соавторы: С.Б. Шустов, Б.Б. Удальцов, Г.Г. Хубулава).
Личный вклад автора в выполненную работу - 80%.
6. Возможности эхокардиографии в диагностике инфекционного эндокардита
естественного клапана // Там же. - Москва, 2001. - С. 46-48. (соавторы: М.В.
Солдатенко, Р.О. Гайсаев, М.В. Тупицын, С.Л. Окунев). Личный вклад в выполненную
работу - 80%.
7. Ультразвуковая диагностика инфекционного эндокардита протеза клапана //
Сб. трудов III Всероссийской науч. конф. с межд. участием “Инфекция в хирургии –
проблемы современной медицины”. - Москва, 2002. - С. 104-105. (соавторы: С.Б.
Шустов, Б.Б. Удальцов, Г.Г. Хубулава, М.В. Солдатенко). Личный вклад автора в
выполненную работу - 70%.
8. Диагностические критерии инфекционного эндокардита протеза клапана // Там
же. - Москва, 2002. - С. 105-106. (соавторы: С.Б. Шустов, Б.Б. Удальцов, Г.Г.
Хубулава). Личный вклад автора в выполненную работу - 70%.
9. Видовой состав и структура возбудителей инфекционного эндокардита протеза
клапана // Там же. - Москва, 2002. - С. 106-107. (соавторы: С.Б. Шустов, Б.Б.
Удальцов, Г.Г. Хубулава). Личный вклад автора в выполненную работу - 70%.
10. Клиническое наблюдение эффективности плазмафереза в лечении инфекционного
эндокардита // Сб. материалов VII Сибирской науч.-практ. конф. с межд. участием
“Актуальные вопросы консервативной и инвазивной кардиологии”. - Красноярск,
2002. - С. 132-133. Личный вклад автора в выполненную работу - 70%.
11. Ультразвуковые диагностические признаки инфекционного эндокардита
искусственного клапана // Там же. - Красноярск, 2002. - С. 134-135. Личный вклад
автора в выполненную работу - 80%.
12. Осложнения инфекционного эндокардита // Сб. материалов Всероссийской
научн.-практ. конф. “Терапевтическая помощь в экстремальных ситуациях”. - СПб.,
2003. - С. 320. (соавторы: С.Б. Шустов, Б.Б. Удальцов, Г.Г. Хубулава, А.Н.
Коваленко). Личный вклад автора в выполненную работу - 70%.
13. Неотложная терапия острой сердечной недостаточности у больных
инфекционным эндокардитом // Там же. - СПб., 2003. - С. 334-335. (соавторы: С.Б.
Шустов, Б.Б. Удальцов, Г.Г. Хубулава, А.Н. Коваленко). Личный вклад автора в
выполненную работу - 70%.
14. Причины смерти больных инфекционным эндокардитом // Там же. - СПб., 2003.
- С. 313-314. (соавторы: С.Б. Шустов, Б.Б. Удальцов, Г.Г. Хубулава, А.Н.
Коваленко). Личный вклад автора в выполненную работу - 80%.
15. Септические осложнения инфекционного эндокардита протеза клапана // Сб.
материалов Всероссийской конф. “Актуальные вопросы гнойно-септической хирургии”.
- Красноярск, 2003. - С. 111-112. (соавторы: С.Б. Шустов, Б.Б. Удальцов, Г.Г.
Хубулава). Личный вклад автора в выполненную работу - 70%.
16. Возможности диагностики септических осложнений инфекционного эндокардита
протеза клапана // Там же. - Красноярск, 2003. - С. 45-46 . (соавторы: С.Б.
Шустов, Б.Б. Удальцов, Г.Г. Хубулава). Личный вклад автора в выполненную работу
- 70%.
17. Особенности этиологии и клинической картины инфекционного эндокардита с
преимущественным поражением правых камер сердца // Сб. трудов Всероссийской науч.
конф. “Актуальные проблемы хирургии сердца и сосудов”. - СПб.: ВМедА, 2003. - С.
209-211. (соавтор: Г.Г. Хубулава). Личный вклад автора в выполненную работу -
70%.
18. Возможности ультразвуковой диагностики инфекционного эндокардита с
преимущественным поражением правых камер сердца // Там же. - СПб.: ВМедА, 2003.
- С. 208-209. (соавтор: Г.Г. Хубулава). Личный вклад автора в выполненную работу
- 70%.
19. Анализ осложнений инфекционного эндокардита за 10 лет // Там же. - СПб.:
ВМедА, 2003. - С. 253-254. (соавтор: С.Б. Шустов). Личный вклад автора в
выполненную работу - 70%.
20. Возможности ультразвуковой диагностики поражения печени, почек, селезёнки
при инфекционном эндокардите современного течения // Там же. - СПб.: ВМедА,
2003. - С. 255-256. (соавтор: С.Б. Шустов). Личный вклад в выполненную работу -
70%.
21. Анализ причин летальных исходов больных инфекционным эндокардитом за 10
лет // Там же. - СПб.: ВМедА, 2003. - С. 196-197. (соавтор: Б.Б. Удальцов).
Личный вклад автора в выполненную работу - 70%.
22. Особенности этиологии и клинической картины инфекционного эндокардита
искусственного клапана // Там же. - СПб.: ВМедА, 2003. - С. 198-199. (соавтор:
Б.Б. Удальцов). Личный вклад автора в выполненную работу - 70%.
23. Ультразвуковые диагностические критерии инфекционного эндокардита
нативного клапана // Сб. материалов VI Всероссийской науч.-практ. конф.
“Актуальные вопросы диагностики и лечения в многопрофильном стационаре”. - СПб.,
2003. - С. 372-373. (соавторы: С.Б. Шустов, Б.Б. Удальцов, Г.Г. Хубулава, А.Н.
Коваленко). Личный вклад автора в выполненную работу - 70%.
24. Антибактериальная терапия инфекционного эндокардита // Там же. - СПб.,
2003. - С. 303-304. (соавторы: С.Б. Шустов, Б.Б. Удальцов, Г.Г. Хубулава, А.Н.
Коваленко). Личный вклад автора в выполненную работу - 70%.
25. Сравнительная оценка причин смерти при инфекционном эндокардите
естественного и искусственного клапанов // Там же. - СПб., 2003. - С. 298-299.
(соавторы: С.Б. Шустов, Б.Б. Удальцов, Г.Г. Хубулава, А.Н. Коваленко). Личный
вклад автора в выполненную работу - 70%.
26. Значение ультразвукового исследования в диагностике инфекционного
эндокардита протеза клапана // Сб. трудов Международной научн. конф.
“Хирургические инфекции: профилактика и лечение”. - Москва, 2003. - С. 342-343.
(соавторы: С.Б. Шустов, Б.Б. Удальцов, Г.Г. Хубулава). Личный вклад в
выполненную работу - 70%.
27. Возбудители инфекционного эндокардита протеза клапана современного
течения // Там же. - Москва, 2003. - С. 64-65. (соавторы: С.Б. Шустов, Б.Б.
Удальцов, Г.Г. Хубулава). Личный вклад автора в выполненную
работу - 70%.
28. Организация диагностики инфекционного эндокардита в поликлинике // Сб.
материалов Всероссийской научн. конф. “Актуальные вопросы эпидемиологии
сердечно-сосудистых заболеваний и организации кардиологической помощи”. -
Кемерово, 2003. - С. 25-26. Личный вклад автора в выполненную работу - 70%.
29. Организация диагностики инфекционного эндокардита в стационаре // Там же.
– Кемерово, 2003. - С. 97-98. Личный вклад автора в выполненную работу - 70%.
30. Изменение надпочечников при инфекционном эндокардите // Сб. материалов
Всероссийской науч. конф. “Клиническая эндокринология – достижения,
перспективы”. - СПб., 2003. - С. 56. (соавторы: С.Б. Шустов, Б.Б. Удальцов).
Личный вклад автора в выполненную работу - 80%.
Список сокращений
| АБТ |
- антибактериальная терапия |
| АПФ |
- ангиотензинпревращающий фермент |
| АЛТ |
- аланинаминотрасфераза |
| АСТ |
- аспартатаминотрасфераза |
| АК |
- аортальный клапан |
| АД |
- артериальное давление |
| ВЛОК |
- внутрисосудистое лазерное
облучение крови |
| DTI |
- тканевое допплеровское
сканирование |
| ИД |
- импульсный допплер |
| ИЭ |
- инфекционный эндокардит |
| ИЭЕК |
- инфекционный эндокардит
естественных клапанов |
| ИЭПК |
- инфекционный эндокардит протеза
клапана |
| КДО |
- конечно-диастолический объём |
| КСО |
- конечно-систолический объём |
| ЛЖ |
- левый желудочек |
| ЛИИ |
- лейкоцитарный индекс
интоксикации |
| МВ |
- микробные вегетации |
| МОК |
- минутный объём кровообращения |
| МК |
- митральный клапан |
| NYHA |
- Нью-Йоркская ассоциация
кардиологов |
| ОСН |
- острая сердечная
недостаточность |
| ПВ |
- постоянно-волновой допплер |
| ПОН |
- полиорганная недостаточность |
| ПЖ |
- правый желудочек |
| ПФ |
- плазмаферез |
| СН |
- сердечная недостаточность |
| СОЭ |
- скорость оседания эритроцитов |
| ЧПЭхоКГ |
- чреспищеводная эхокардиография |
| ЧСС |
- частота сердечных сокращений |
| ТТЭхоКГ |
- трансторакальная
эхокардиография |
| ТК |
- трёхстворчатый клапан |
| ТЭЛА |
- тромбоэмболия лёгочной артерии |
| УЗИ |
- ультразвуковое исследование |
| УФОК |
- ультрафиолетовое облучение
крови |
| ФК |
- функциональный класс |
| ЦД |
- цветной допплер |
| ЦИК |
- циркулирующие иммунные
комплексы |
| ЭхоКГ |
- эхокардиография |

