Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Организация желудочного пищеварения
Г.Ф. Коротько
ФГУ Российский центр функциональной хирургической гастроэнтерологии Росздрава
Одним из замечательных свойств пищеварительного тракта, его высокой
функциональной надежности являются выраженные компенсаторные возможности из-за
дублированности дигестивной функции на протяжении пищеварительного канала,
возможности широкого варьирования времени пребывания пищевого содержимого в его
отделах и полифункциональности органов пищеварительной системы.
Принцип полифункциональности органа ярко представлен деятельностью желудка.
Это прежде всего сложно организованные моторная и секреторная функции,
реализуемые соответственно трехслойными пластами унитарных гладких мышц стенки
органа и его морфофункционально различающимся по отделам желудка железистым
аппаратом слизистой оболочки. При этом фундальная и антральная части органа
существенно различаются в пищеварительных и непищеварительных функциональных
отправлениях. Различия секреции желез большой и малой кривизны, передней и
задней стенок фундальной части, кардиального и антрального отделов органа
[6,8,9,11,22-24] объясняются тем, что желудок не является химическим реактором
идеального перемешивания [11], имеет сложную принципиально различающуюся
гидродинамику пищевого фундального и антрального желудочного содержимого, его
порционной эвакуации в двенадцатиперстную кишку (ДПК) с элементами
физиологической регургитации дуоденального химуса [5,13,17-19,21,25,27,28,30]. К
этому следует добавить и функциональную полипотентность желудочного секрета,
компоненты которого имеют разное назначение в пищеварительных и
непищеварительных функциях желудка.
Итак, пищеварительные функции кардиального и фундального отделов желудка
заключаются в депонировании принятой пищи, ее мацерации, денатурации белков,
растворении нутриентов, их ферментативном гидролизе; антрального и пилорического
отделов - в частичной нейтрализации перешедшего в них фундального содержимого,
перетирании его, частичной регургитации содержимого в фундус, порционной
эвакуации антрального содержимого в ДПК с физиологической регургитацией ее
химуса в антрум, выраженность которой зависит от свойств антродуо-денального
пищевого содержимого. Трансформации нутриентов желудочного содержимого имеют
большое значение для деятельности тонкокишечного пищеварительного конвейера.
Во-первых, начальная деградация полимеров в желудке повышает их атакуемость
панкреатическими и кишечными гидролазами; во-вторых, кислое содержимое желудка и
находящиеся в нем продукты начального гидролиза пищевых белков выполняют важную
регуляторную роль как стимуляторы (и ингибиторы) секреции желудочных и
поджелудочной желез, эвакуации антрального содержимого в ДПК, скорости транзита
по ней химуса [2,13,14].
Секреция желудочных желез регуляторно реализуется в три фазы [10,27-29]. В
первой сложнорефлекторной фазе происходят пусковые стимулирующие влияния акта
еды и пищи с дистантных и контактных рецепторов на железы желудка посредством
эфферентов блуждающих нервов и их нейротрансмиттеров. В стимуляции секреции
желудочных желез в первой фазе принимает участие и гастриновый механизм-рилизинг
гастрина из антральных G-клеток, который производится вагусными
нейротрансмиттерами - пептидом и ацетилхолином [28]. Названные механизмы
стимулируют секрецию главных клеток-продуцентов пепсиногенов и обкладочных
клеток-продуцентов хлористоводородной кислоты, на первую фазу секреции
приходится около 30-40% общего объема постпрандиального секрета, что зависит от
возбудимости пищевого центра, легко тормозится и в большой мере определяет
возбудимость секреторных (и моторных) эффекторов в их последующей деятельности
во второй и третьей фазах.
Вторая фаза - желудочная, на нее приходится около 50% объема
постпрандиального секрета, обеспечивается рефлекторными (в основном вагусными) и
гуморальными (в основном гастриновым и гистаминовым) механизмами, инициируемыми
с механо- и хеморецепторов фундальной и антральной частей желудка. В роли
стимуляторов последних выступают полипептиды, некоторые аминокислоты и ионы
водорода, действующие на рецепторы сенсорных нейронов, секреторных и моторных
клеток-мишеней, ECL, G- и D-клетки-продуценты гистамина, гастрина и
соматостатина соответственно непосредственно или опосредованно [28,29]. Вагусные
эфференты в зависимости от параметров импульсации нейронов меняют соотношение в
составе желудочного секрета пепсиногенов и соляной кислоты (НСl) [7]. В
сопряжении их секреции существенную роль играет фундо-фундальный рефлекс в ответ
на раздражение рецепторов слизистой оболочки НСl [26]. В саморегуляции ее
секреции велико значение торможения рилизинга гастрина G-клетками низкими
значениями рН, когда секреция НСl уменьшается из-за избыточно высокой
кислотности антрального содержимого. Таким образом, во второй фазе секреции есть
стимулирующий и тормозной компоненты управления секреторным аппаратом желудка.
Третья фаза - кишечная, составляет около 10% постпрандиального объема сока.
Имеет корригирующее значение в зависимости от свойств дуоденального химуса, в
том числе от его рН - при высокой кислотности усиливается высвобождение
S-клетками секретина, который тормозит секрецию НСl; холецистокинин, наоборот,
стимулирует главные и обкладочные клетки желудочных желез, увеличивая секрецию
пепсиногенов и НСl.
Примечательным свойством желудочного секрета является наличие в нем
нескольких изопепсинов, образующихся из нескольких (8-10) изопепсиногенов,
синтезируемых главными клетками желудочных желез. Изопепсины различаются
субстратной специфичностью и оптимумами рН протеолитической активности. Это
объясняется тем, что интрагастральный протеолиз осуществляется пепсинами при
разной кислотности пищевого желудочного содержимого и определяется разным
напряжением секреции желудочных желез и буферных свойств данного содержимого, а
также характерной для желудка топографией интрагастрального протеолиза. Нами в
свое время в сложных опытах на собаках [11] было показано, что пищевое
содержимое желудка в зависимости от его удаленности от поверхности слизистой
оболочки в теле желудка имеет разный рН: не превышает 3,0-4,0, в центральной
части примукозной зоны рН содержимого около 2,0. При дистальном перемещении
перистальтической волной примукозного содержимого оно замещается из более
удаленной зоны, где протеолиз проходил при более высоком значении рН и была
повышена атакуемость пищевых белков действием на них изопепсинов типа
гастриксина и самого пепсина. Это ускоряло протеолиз в примукозном слое
содержимого. В антральной части желудка содержимое активно перемешивается и
протеолиз продолжается в широком диапазоне рН, для чего необходим и гастриксин с
его максимальной активностью при рН 3,0-3,5. Это объясняет синтез антральными и
пилорическими железами его предшественника - пепсиногена 2 [11,28,29]. Описанные
прежние наши эксперименты с учетом интрагастрального протеолиза во времени и
пространстве, при его моделировании in vitro и проверке в оригинальной
математической модели [11] были дискретными. В ФГУ РЦФХГ И.И. Щербина и А. О.
Демина, применив созданную ими ультразвуковую методику, подтвердили в
наблюдениях на здоровых добровольцах описанную гидродинамику пищевого
содержимого желудка. Не учитывать ее в современных представлениях организации
перемещения желудочного содержимого в угоду прежним постулатам, основанным на
наблюдениях динамики непищевого содержимого желудка, означает отход от
фактической организации желудочного пищеварения.
Таблица 1. Соотношение секреции гастриксина и пепсина
| Фракция желудочного секрета |
Здоровые добровольцы |
Больные ЯБ ДПК |
| до лечения |
после медикаментозного лечения |
после хирургического лечения |
| Натощаковая |
0,74 |
0,74 |
1,11* |
1,18* |
| Базальная |
0,76 |
0,61 |
1,04* |
1,34* |
| Стимулированная (гистамин): |
. |
. |
. |
. |
| первая порция |
0,93 |
0,63 |
1,47* |
0,99* |
| вторая порция |
0,63 |
0,83 |
0,95 |
1,18* |
| третья порция |
0,61 |
0,75 |
0,91* |
1,28* |
| четвертая порция |
0,72 |
0,75 |
0,87 |
0,82 |
Примечание. Выделенные показатели отличаются от таковых у здоровых; *
- от таковых у больных до антисекреторной терапии.
Показано [3,4,11], что изоферментный спектр желудочного сока человека
различается в норме в зависимости от вида тестового завтрака и существенно
изменяется при язвенной болезни (ЯБ) ДПК.
В развитие новых экспериментальных данных о регуляторном сопряжении кислото-
и ферментовыделительной деятельности желудочных желез [26] такая сопряженнсть
изучена у здоровых добровольцев при нормальном кислотовыделении; у больных ЯБ
ДПК с характерным для данного заболевания повышенным кислотовыделением;
медикаментозно (с применением блокаторов протонной помпы - эзомепразол и Н2-рецепторов
париетальных клеток - фамотидин) и хирургически (селективная проксимальная
ваготомия - СПВ) сниженным кислотовыделением. Результаты этой работы подтвердили
тесную связь кислото- и ферментовыделения желудочных желез в норме и при
названной патологии, т.е. два типа секреции главных и обкладочных клеток
сопряжены при нормальном, повышенном и пониженном кислотовыделении [15]. Такие
результаты, видимо, лежат в основе непопулярности определения с диагностической
целью желудочного ферментовыделения и общепринятости
мониторинга кислотовыделения, особенно методом интрагастральной рН-метрии.
Представлялось теоретически и клинически важным исследовать зависимость
изоферментного спектра желудочного секрета и дебитов изопепсинов от
кислотовыделительной деятельности секреторного аппарата желудка. Анализ
полученного клинического материала показал, что в норме, при ЯБ ДПК, при ее
медикаментозном и хирургическом лечении кислото- и ферментовыделение находится в
прямой зависимости. Новым фактом явилась установленная нами сопряженность с
кислотовыделением соотношения секреции изопепсиногенов, образующих пепсин и
гастриксин. Это соотношение нами описывается в виде коэффициента: гастриксин/пепсин.
Характер трансформаций данного коэффициента представлен в табл. 1.
Как видно из представленных данных, у здоровых людей активность пепсина в
желудочном соке существенно выше, чем активность гастриксина. У больных ЯБ ДПК в
базальном желудочном секрете и первой порции секрета после стимуляции желез
гистамином коэффициент гастриксин/пепсин снижается, т.е. в гиперацидном
состоянии в секрете относительно возрастает доля пепсина, что следует
расценивать как адаптивную трансформацию секреции изоферментов главными клетками
желудочных желез.
Подавление желудочной секреции у больных не только снизило кислото- и
ферментовыделение желудочных желез, но и трансформировало соотношение в секрете
двух гидролаз: активность гастриксина в соке стала выше, чем пепсина, по
сравнению и со здоровыми, и с больными ЯБ ДПК до их лечения, т.е. в условиях
пониженного кислотовыделения увеличилась секреция пепсиногена, образующего
гастриксин - фермент с оптимумом протеолиза при невысокой кислотности
желудочного сока. Еще более выраженное подавление желудочной секреции в
результате СПВ в еще большей мере повысило коэффициент гастриксин/пепсин
(особенно при базальной секреции, которая по своему механизму является
стимулированной раздражением механорецепторов желудка).
Таблица 2. Корреляция параметров секреции желудочных желез здоровых и
больных осложненной ЯБ ДПК
| Коррелируемые пары параметров
секреции |
Здоровые добровольцы (n=10) |
Больные ЯБ ДПК |
| до антисекреторной терапии (n=25) |
после антисекреторной терапии (n=25) |
после СПВ (n=20) |
| рН-пепсин |
-0,16 |
-0,26 |
-0,10 |
-0,44 |
| рН-гастриксин |
-0,66 |
-0,26 |
-0,23 |
-0,20 |
| Пепсин-гастриксин |
0,52 |
0,13 |
0,55 |
0,27 |
| Кислотность-пепсин |
0,38 |
0,30 |
0,15 |
0,35 |
| Ксилотность-гастриксин |
0,73 |
0,25 |
0,13 |
0.54 |
| Дебит HCl-дебит пепсина |
0,59 |
0,58 |
0,45 |
0,56 |
| Дебит HCl-дебит гастриксина |
0,66 |
0,14 |
0,43 |
0,65 |
| Дебит HCl-пепсин |
0,36 |
0,31 |
0,01 |
0,43 |
| Дебит HCl-гастриксин |
0,60 |
0,16 |
0,03 |
0,38 |
Примечание. Выделены статистически значимые коэффициенты корреляции.
Это подтверждает регуляторную сопряженность кислотовыделения с
преимущественным возбуждением секреции разных изопепсиногенов, образующих при
активации гастриксин или пепсин.
Результаты корреляционного анализа показали, что у клинически здоровых лиц
при нормальном кислотовыделении желудочных желез секреция пепсина и гастриксина
связана прямой зависимостью со средним по величине коэффициентом корреляции
(0,52, табл. 2). Показательно, что с кислотовыделением (по рН сока, кислотности
и дебиту НСl) в более выраженной зависимости находится секреция гастриксина (по
его активности в соке и дебиту), чем секреция пепсина, т.е. в норме с
кислотовыделением регуляторно в разной мере сопряжена секреция разных
изопепсиногенов, которая имеет, следовательно, не только генерализованные, но и
селективные механизмы управления в зависимости от кислотовыделения и
интрагастральной кислотности содержимого. Это принципиальное заключение требует
дальнейшей экспериментальной разработки и конкретизации механизмов реализации.
У больных осложненной ЯБ ДПК, имевших возросшую кислотовыделительную
деятельность желудочных желез, связь секреции пепсина и гастриксина нарушена (r
= 0,13), как и выраженная у здоровых людей зависимость секреции гастриксина от
кислотовыделения, тогда как связь с ним секреции пепсина сохранена.
Следовательно, контур регуляции секреции пепсина в зависимости от
кислотовыделения продуктивно функционирует в диапазоне средних (нормальных) и
низких (состояния гиперацидности) значений интрагастрального рН. При
гиперацидных состояниях он становится более актуальным, чем контур регуляции
секреции гастриксина.
Подавление кислотовыделения при антисекреторной терапии блокаторами протонной
помпы и Н2-рецепторов париетальных клеток снижало ферментовыделение
желудочных желез [15], восстанавливало прямую связь секреции пепсина и
гастриксина (r = 0,55), в неполной мере - дебитов гастриксина и НСl (r = 0,43).
Антисекреторная терапия путем СПВ вызвала в отдаленные послеоперационные сроки
восстановление положительных связей кислотовыделения с секрецией гастриксина и
пепсина не только по дебиту последнего, но и активности двух изопепсинов в
желудочном соке. Такие результаты свидетельствуют о перифирическом механизме
сопряжения с кислотовыделением не только суммарного ферментовыделения, но и
изоферментного спектра желудочного секрета. Есть основание рассматривать это
явление как компенсаторный механизм, адаптирующий желудочную секрецию к
гидролизу пищевых белков в желудке при низкой кислотности его содержимого в
условиях гипосекреции и гипацидного состояния. М.А. Плешкова наблюдала больных
ЯБ ДПК, у которых после курса антисекреторной терапии, приведшего к снижению
кислото- и ферментовыделительной деятельности секреторного аппарата желудка, не
произошло описанного выше перераспределения ферментативных активностей
желудочного сока - не повышалась доля в нем гастриксина. Есть основание считать,
что в данном случае глубокий патологический процесс поразил тонкие регуляторные
механизмы компенсаторного сопряжения ферментовыделения с кислотовыделительной
деятельностью желудочных желез.
При полиферментной организации пищеварительного конвейера желудочно-кишечного
тракта, наличии в составе панкреатического секрета зимогенов, образующих
несколько эндо- и экзопептидаз, реализующих свое гидролитическое действие в
полостном тонкокишечном пищеварении, актуально образование железами желудка
нескольких изопепсиногенов, реализующих после их активации протеолиз в широком
диапазоне рН. Видимо, актуально, если существуют механизмы варьирования спектра
желудочных протеиназ, сопряжение их секреции с кислотовыделительной
деятельностью желудка и в норме, и при кислотозависимой патологии.
Секреция нескольких изопепсиногенов железами желудка необходима для
обеспечения протеолиза в широком диапазоне рН, реально существующего в полости
желудка и являющегося одним из параметров саморегуляции секреции посредством
гастринового механизма [8,28,29]. Как было сказано выше, рН пищевого содержимого
желудка зависит от напряжения секреции желез желудка, в основном от пула их
париетальных клеток, от буферных свойств содержимого желудка, прежде всего его
белкового компонента; причем с гидролизом белков их буферность снижается, и этот
эффект находится в прямой зависимости от количества гидролизованных белков и
глубины интрагастрального протеолиза [11]. Кислотность желудочного содержимого
зависит и от времени пребывания пищи в желудке, от удаленности содержимого от
сецернирующей слизистой оболочки, где рН наиболее низок и откуда секрет
диффундирует вглубь пищевого содержимого желудка, где рН выше. Здесь начальный
гидролиз белков идет посредством гастриксина, в результате чего атакуемость
полипептидов повышается и это ускоряет их гидролиз в примукозной зоне
содержимого, которое перистальтической волной перемещается в сторону антрума и
замещается центральнее расположенным пищевым желудочным содержимым. Это и
составляет сущность внутрижелудочного дигестивного конвейера [11,14], в
реализации которого важна специфическая моторика фундальной части желудка,
реализуемая только в желудке представленными трехслойными гладкомышечными
пластами, приближенными к циркулярному, продольному и косому их направлению, в
стенке органа [2,30]. Это позволяет, не перемешивая фундальное содержимое
желудка, "слизывать" поверхностный его слой все более углубляющимися от кардии к
антруму перистальтическими волнами, которые заполняют антрум фундальным
содержимым. Именно здесь происходит перетирание содержимого желудка, его
перемешивание, введение в состав этой гомогенизируемой массы слабощелочного
секрета пилорических желез с изопепсинами типа гастриксина, продолжающими
протеолиз при более высоком рН (3,0-3,5), чем в примукозной зоне фундальной
части желудка (рН 1,5-2,0). Следовательно, интрагастральная дигестия пищевых
белков в фундальной и антральной частях желудка совершается по конвейерному
принципу в широком диапазоне кислых значений рН несколькими пепсинами, секреция
которых во вторую фазу в разных соотношениях изопепсиногенов корригируется
фундофундальным периферическим рефлексом с "кислотных" хеморецепторов слизистой
оболочки желудка. Это сопрягает кислото- и селективное ферментовыделение
желудочных желез. Напомню, что в центральной зоне пищевого содержимого желудка,
куда еще не диффундировал кислый желудочный секрет, инактивирующий слюнную
осмилазу, происходит под ее гидролитическим действием переваривание
полисахаридов в проглоченном пищевом комке. В целом же из желудка в ДПК
эвакуируется содержимое предварительно подвергнутой механической и химической
(ферментной) переработке принятой пищи для последующего обогащения этого
гомогенного содержимого панкреатическим и кишечным секретами и желчью, т.е.
приготовления адекватного по составу и свойствам дуоденального химуса,
нутритивные компоненты которого будут затем подвергнуты полостному перевариванию
в основном химическом реакторе пищеварительного тракта - тонкой кишке.
В числе многих параметров, по которым корригируется скорость эвакуации
пищевого желудочного содержимого в ДПК [5], должны быть названы параметры
дигестивно трансформированного эвакуируемого из него в ДПК содержимого.
Первые порции желудочного содержимого, перешедшего в ДПК, вызывают
дуоденогастральный (энтерогастральный) тормозной рефлекс [2]. Он имеет
универсальный характер - вызывается механическим и химическим раздражением
практически всех пищевых веществ, что доказано большим числом экспериментальных
исследований [2,11,27,28,30]. Начальная задержка эвакуации пищевого желудочного
содержимого, следовательно, обусловлена не только (и не столько) закрытием
пилорического сфинктера, но и снижением моторо-эвакуаторной активности желудка и
ДПК. Разная скорость эвакуаторного процесса в большой степени зависит от свойств
дуоденального содержимого. При прочих равных условиях с наибольшей скоростью
желудок покидает углеводная, медленней - белковая и еще медленней - жирная пища
[5,11,12].
В лаборатории И.П. Павлова [17,25] было показано, что при эвакуации жиров
нормальным процессом является регургитация дуоденального содержимого в
антральную часть желудка. Образуется общая "полость", в которой в достаточно
активной согласованной моторике осуществляется смешивание антрального и
дуоденального содержимого. Результаты сонографических исследований нашего центра
(И.И. Щербина, А.О. Демина) показали, что это происходит на протяжении всего
эвакуаторного процесса, несколько активнее в его начале, чем в конце. В большой
мере именно по этой причине эвакуация из желудка жирной пищи совершается
медленнее, чем белковой и углеводной. Регургитация при эвакуации из желудка
белкового тестового завтрака наблюдается в меньшей мере и практически не
отмечается при эвакуации углеводного завтрака (манной каши).
Задержка эвакуации под влиянием жира и регургитация жирной пищи в антрум
сопровождаются торможением секреции фундальных желез желудка. Это способствует
сохранению активности панкреатических ферментов, эффективности эмульгирования
жиров и последующему пищеварению в полости тонкой кишки [2,11]. Низкая секреция
желудочных желез была обнаружена и описана в лаборатории И.П. Павлова [19].
Несмотря на такие подкрепляющие результаты исследований лабораторий И.П.
Павлова [19] и Е.С. Лондона [18] наши наблюдения, следует сказать о
противоречивости суждений о механизмах реализации эвакуаторного процесса [5].
Немаловажной причиной такой противоречивости являются различия методических
приемов исследования эвакуации содержимого желудка в ДПК. В экспериментах на
животных с фистулой учитывается убыль в желудке введенных в него растворов
различных веществ [11]. При этом периодическое извлечение для измерения и
обратное введение через фистулу остатка растворов в желудок изменяют скорость
эвакуации. С этой же целью получение растворов из запилорической фистулы [5]
изменяет эвакуаторный процесс в еще большей мере. Исследования эвакуации из
желудка бариевой взвеси показали, что "избавление" желудка от инородного
содержимого принципиально отличается от динамики эвакуации растворов питательных
веществ. Адекватный метод количественного учета скорости и динамики эвакуации
должен характеризовать таковые в отношении пищевого содержимого желудка в
естественных условиях, т.е. после перорального приема тестового завтрака и без
нанесения дополнительных раздражений (например, введенным в пищеварительный
тракт зондом). Таким требованиям отвечают методы динамической сцинтиграфии и
сонографии, с помощью которых учитывается время полувыведения из желудка
принятого раствора стандартного пищевого продукта [1,14,16,20,30]. Известно, что
скорость его эвакуации имеет существенные индивидуальные различия, поэтому важно
учитывать и дифференцированность эвакуаторного процесса, определяя время
полуэвакуации из желудка растворов разных нутриентов.
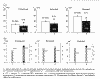
Нами разработан метод сонографического учета скорости и дифференцированности
эвакуации из желудка манной каши (углеводный завтрак), ее же с добавлением
яичного белка (белковый завтрак) или с добавлением сливочного масла (жировой
завтрак). Метод в последующей модификации предусматривает также сонографический
учет моторной активности антральной части желудка (частоты и силы сокращений,
площадь поперечного сечения антрума в период его систолы и диастолы). На метод
получен патент [12] и модифицированный вариант метода недавно описан [14].
Время полуэвакуации из желудка трех видов используемых нами растворов у
клинически здоровых испытуемых статистически достоверно различается (<0,001),
имея не очень большую вариабельность (CV%). Каждый из эвакуируемых растворов
имеет характерные особенности антральной моторики (см. рисунок). На рисунке
следует обратить внимание на особенность антральной моторики при эвакуации из
желудка жирового завтрака - неполные, слабые и редкие систолы. Принципиально,
что антральная часть желудка выполняет не только эвакуаторную роль, но и до того
готовит "шихту" из локально приготовленных ее предшественников, образованных на
разных секреторных полях фундальной части желудка.
Регургитация дуоденального содержимого в антрум усложняет состав его
содержимого. Именно оно поступает в ДПК и из нее под регуляторным контролем
переводится в основной химический реактор - тонкую кишку. Следовательно, в
разной мере выраженная дуоденоантральная регургитация, не дошедшая по размерам,
длительности и регулярности (в том числе и натощаковой) до патологического
дуоденогастрального рефлюкса, должна рассматриваться как нормальный
физиологический процесс.
Тема данной статьи потребовала показа того, что прием с пробными завтраками
панкреатина (креон 10 000) ускоряет их эвакуацию из желудка. К этому добавлю,
что экзосекреторная недостаточность поджелудочной железы при хроническом
панкреатите замедляет эвакуацию из желудка углеводного и белкового завтраков, но
ускоряет эвакуацию жирового завтрака. Самое характерное то, что при ряде
гастроэнтерологических заболеваний (ЯБ, хронический панкреатит, гастрит,
желчнокаменная болезнь, дуоденит, гепатит) не только в разной мере изменяется
скорость эвакуации, но и нарушается ее дифференцированность [14]. Такие
результаты подтверждают полученные нами ранее экспериментальные данные [11] о
том, что среди многих параметров, по которым регуляторно сенсорами желудка и ДПК
контролируется скорость эвакуации из желудка его пищевого содержимого,
немаловажное значение имеет гидролизованность нутриентов и потенциальная
возможность последующего их эффективного гидролиза. Поэтому эмульгированные жиры
из желудка эвакуируются быстрее неэмульгированных, растворы белков эвакуируется
быстрее, если к ним добавлены протеиназы. Данный нетрадиционный системный аспект
рассмотрения эвакуаторной деятельности гаст-родуоденального комплекса, имеющий
теоретический и прикладной интерес, требует дальнейших целенаправленных
методически строго выверенных исследований.
Заключение
Итак, во-первых, роль желудка в пищеварительном конвейере дигестивная. Она
заключается в активном депонировании принятой пищи, что выражается в гидролизе
полисахаридов осамилазой слюны в проглоченных пищевых комках в центральной зоне
пищевого содержимого желудка; гидролизе пищевых белков эндопептидазами секрета
желудочных желез по конвейерному принципу при разных рН от центра содержимого
желудка к его примукозному слою и от кардии к антральной части. Это объясняет
актуальность секреции желудочными железами нескольких изопепсиногенов, из
которых образуются несколько изопепсинов с разными каталитическими свойствами, и
регуляторную сопряженность кислото- и ферментовыделительной деятельности желез
желудка. В реализации данного внутрижелудочного конвейера огромную роль играет
сложноорганизованная моторика желудка, объясняя необходимость трех мышечных
слоев органа и сфинктерных мультипараметрически регулируемых структур.
Среди параметров, по которым регулируется эвакуация пищевого желудочного
содержимого, немаловажной является реализованность в желудке механической,
физико-химической и химической переработки пищи, включая деградацию полимеров
нутриентов и совершенство завершения приготовления в ДПК "шихты" для основного
химического реактора - тонкой кишки. В числе этих параметров: гомогенность
дуоденального химуса, его рН, начальная гидролизованность пищевых белков и
полисахаридов, эмульгированность липидов, ферментирован -ность химуса
панкреатическими энзимами с максимально возможным соответствием количества
ферментов и их нутритивных субстратов. Данные параметры в большой мере
определяют дуоденальную коррекцию скорости и дифференцированного
эвакуаторного процесса.
Во-вторых, роль желудка в пищеварительном конвейере регуляторная.
Кислотовыделение в зависимости от его соотнесенности с буферными и иными
свойствами пищевого содержимого желудка определяет скорость его
гастродуоденальной эвакуации и транзита дуоденального химуса, напряжение
панкреатической секреции и холереза посредством секретинового механизма.
Начальный гидролиз белков желудочными эндопептидазами, антродуоденальная
моторика и задержка химуса обеспечивают секрецию панкреатичесих ферментов и
холекинез посредством рефлекторного и холецистокининового механизмов. Это в свою
очередь является непременным условием эффективного полостного пищеварения в
тонкой кишке.
Конечно, непищеварительные функции желудка также вносят свой вклад в
эффективную реализацию деятельности желудочно-кишечного тракта как ключевого
компонента трофосистемы организма человека.
Литература
1. Аблязов А.А., Коротько Г.Ф. Способ диагностики
нарушений эвакуаторной функции желудка. А.С. № 1653740. Приоритет от 08.02.91.
2. Богач П.Г. Двигательная деятельность желудка и механизмы ее регуляции //
Физиология пищеварения: Руководство по физиологии. Л.: Наука, 1974. С. 277-310.
3. Гинодман Л.М., Нестерова А.П., Орехович В.Н. и др. Хроматографическое
исследование желудочного сока при хронических гастритах и язвенной болезни //
Вопр. мед. химии. 1965. Т. 10. №6. С. 604-610.
4. Гинодман Л.М., Соловьева Т.А. Определение пепсина и гаст-риксина в
желудочном соке человека // Вопр. мед. химии. 1965. Т.П. №2. С. 87-89.
5. Гройсман С Д. Характеристика пищеварительного процесса в желудке.
Эвакуация его содержимого // Физиология пищеварения: Руководство по физиологии.
Л.: Наука, 1974. С. 310-319.
6. Давыдов Г.М. Секреторные поля желудка и их взаимосвязи. Архангельск:
Облполиграфиздат, 1950.
7. Золотарев В.А., Хропычева Р.П., Поленов С.А. Селективное управление
желудочной секрецией кислоты пепсиногена и бикарбонатов разными популяциями
С-волокон блуждающего нерва // Бюл. экспер. биол. 2002. Т. 133. № 3. С. 249-253.
8. Климов П.К., Барашкова Г.М. Физиология желудка. Механизмы регуляции. Л.:
Наука, 1991.
9. Коротько Г.Ф. К методике исследования секреторной
деятельности задней стенки желудка // Сборник науч. трудов. Ташкент: Медгиз
УзССР, 1962. Т. 3. С. 128-132.
10. Коротько Г.Ф. Выделение ферментов железами желудка
(очерки). Ташкент: Медицина, 1971.
11. Коротько Г.Ф. Желудочное пищеварение, его
функциональная организация и роль в пищеварительном конвейере. Ташкент:
Медицина, 1980.
12. Коротько Г.Ф., Касян Г.Г., Ковалевская О.В. Способ
определения функционального состояния гастродуоденального комплекса. Патент на
изобретение № 2167609. Приоритет от 03.09.99. Опубликовано 27.05.01. БИ № 15.
13. Коротько Г.Ф. Конвейерный принцип организации
пищеварения // Вестн. интенсив, тер. 2004. № 5. С. 6-9.
14. Коротько Г.Ф. Секреция поджелудочной железы. 2-е
доп. изд. Краснодар: Изд-во КГМУ, 2005.
15. Коротько Г.Ф., Плешкова М.А. Адекватность
характеристики ферментовыделительной деятельности желудочных желез // Вестн.
интенсив, тер. 2005. № 5. С. 249-253.
16. Лемешко З.А., Пиманов С.И. Ультразвуковое исследование желудка //
Клиническое руководство по ультразвуковой диагностике / Под ред. В.В. Митькова.
М.: Видар, 1997. Т. 4. С. 9-39.
17. Линтварев С.И. О роли жиров в переходе содержимого
желудка в кишки. СПб., 1901.
18. Лондон Е.С. Физиология и патология пищеварения:
(Руководство для врачей и студентов, лекции). М.; Петроград, 1924.
19. Павлов Н.И. Поли. собр. соч. М.; Л.: Изд-во АН
СССР. 1951. Т. 2, кн. 2.
20. Пиманов С.И., Сатрапинский В.Ю., Гордеев В.Ф.
Ультразвуковая диагностика моторно-эвакуаторных нарушений желудка // Сов. мед.
1996. № 2. С. 5-8.
21. Саенко В.Ф., Бабенков Г.А., Гройсман С.Д. Внутриподжелудочный кровоток и
векторно-эндокринная регуляция секреторной функции желудочно-кишечного тракта.
Хирургические аспекты // Кубанск. науч. мед. вестн. 1994. № 2-4 (3-5). С. 10-12.
22. Соловьев А.В. Характер нервно-гуморальных влияний на секреторную функцию
различных полей желудка // 13-е совещание по физиол.
проблемам, посвящ. памяти И.П. Разенкова. М.: Изд-во АН СССР, 1948.
23. Соловьев А.В. Новые данные о секреторной функции желудка и поджелудочной
железы. М.; Л.: Наука, 1959.
24. Уголев A.M. Изолированный желудочек на передней стенке // Бюл. экспер.
биол. 1957. Т. 44. № 7.
25. Эдельман И.У. Движения желудка и переход
содержимого из желудка в кишки. СПб., 1906.
26. Blandizzi С, Colucci R., Carignani D. et al. Positive Modulation of
Pepsinogen Secretion by Gastric Acidity After Vagal Cholinergic Stimulation //
Amer. J. Physiol. 1997. V. 283(3). P. 1043-1050.
27. Davenport H.W. Physiology of the Digestive Tract. 3-rd. Ed. Year Book
Medical Publishers Incorporated. Chicago, 1971.
28. Gastroitestinal physiology / Ed. L.R. Johnson. St. Louis; London: Mosby,
1999. 6-th Ed.
29. Modlin I.M. Acid related diseases. Biology and treatment.
Schnetztor-Verlag GmbH B-Konstanz, 1998.
30. Schuster M.M., Crowell M.D., Koch K.L.
Gastrointestinal motility in Health and Disease. London: ВС Decker Inc. Hamilton,
2002. 2-nd Ed.
Вестник хирургической гастроэнтерологии. 2006 № 1, с.
17-25.
Статья опубликована на сайте
http://www.gastroscan.ru

