Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Метаболический синдром (МС) представляет собой комплекс
взаимосвязанных нарушений углеводного и жирового обмена, механизмов регуляции
артериального давления и функций эндотелия, формирующихся на фоне
нейроэндокринной дисфункции, в условиях пониженной чувствительности тканей к
инсулину — инсулинорезистентности (ИР). Считается, что все компоненты МС
генетически обусловлены, а объединяющей основой данных проявлений является
первичная ИР и сопутствующая ей системная гиперинсулинемия (ГИ), природа
возникновения которых гетерогенна.
Подробное изучение отдельных звеньев МС началось еще в 20-е
годы прошлого века. Г. Ф. Ланг обратил внимание на «тесную взаимосвязь между
артериальной гипертензией (АГ), ожирением, нарушением липидного и углеводного
обмена и подагрой». Е. Kylin в 1923 году описал синдром «гипертензии —
гипергликемии — гиперурикемии». В 1947 году J. Vague описал два типа
распределения жировой ткани и отметил частое сочетание андроидного типа с
инсулиннезависимым сахарным диабетом (СД II), ишемической болезнью сердца
(ИБС) и подагрой [1, 2]. J. Camus в 1966 году ввел понятие «метаболического
трисиндрома», включавшего в себя СД II, подагру и гиперлипидемию [3]. В 1967
году Avogaro P., Crepaldi G. описали сочетание метаболических нарушений при
ожирении как «полиметаболический синдром» [4]. В 1988 году G. Reaven описал
первичную ИР с последующей компенсаторной ГИ, нарушение толерантности к
глюкозе (НТГ), дислипопротеинемию и АГ, объединив их в «метаболический синдром
Х» [5, 6]. В 1991 P. Bjorntorp указывает на основополагающую роль
абдоминально-висцерального ожирения в развитии «цивилизационного синдрома» или
«гормонально-метаболического синдрома» [2, 7].
В настоящее время в симптомокомплекс МС включены: ИР и ГИ,
абдоминально-висцеральное ожирение, первичная АГ, НТГ или СД II, дислипидемия
атерогенной направленности, гиперурикемия (ГУ) и подагра, нарушения гемостаза
предтромботического характера, микроальбуминурия (МАУ), ранний атеросклероз
или ИБС.
Постоянное развитие и совершенствование методов и принципов
научного исследования МС помогает объяснить природу возникновения и общий
характер его проявлений, но, с другой стороны, это приводит к неизбежному
увеличению количества компонентов, включаемых в состав МС и затрудняющих его
диагностику. Наиболее удачное решение данной проблемы предложили эксперты
Международной федерации по диабету (IDF), которые разработали четкие и
достаточно простые в применении критерии диагностики МС у взрослых (2005 год)
и детей и подростков (2007 год) [8–10].
Исходя из концепции экспертов IDF об основополагающей роли
абдоминально-висцерального ожирения в диагностике МС, нам показалось
интересным провести многоплановое исследование среди московской популяции
детей и подростков, имеющих единый критерий отбора — ожирение, для
установления характера и частоты обменных нарушений, свойственных МС.
Материалы и методы
Исследования проводились на базе Морозовской детской городской
клинической больницы. Критерием отбора пациентов являлось ожирение. Степень
ожирения определялась по проценту избытка массы в сравнении с долженствующей с
использованием центильных таблиц для детей: I — 10–25%, II — 26–49%, III —
50–99%, IV — ≥ 100%. У детей старшего школьного возраста учитывался индекс
Кетле (индекс массы тела (ИМТ), кг/м2): 18,5–24,5 (нормальная масса тела);
25–29,9 (избыточная масса тела); 30–34,9 (соответствует I степени ожирения);
35–39,9 (соответствует II степени); ≥ 40 (соответствует III степени). Для
детей младшего и среднего школьного возраста использовались данные пограничных
значений ИМТ, предложенных Katmarzyk P. T. [11]. Было обследовано 116 детей
(87 мальчиков и 29 девочек) с ожирением I–IV степени в возрасте от 6 до 17 лет
(рис. 1).
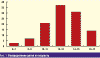
Всем детям проводилось комплексное обследование, включающее:
-
изучение анамнеза ребенка, членов семьи и ближайших родственников (с
уточнением наличия проявлений и осложнений ИБС, АГ, ожирения, нарушений
обмена углеводов, липидов и пуриновых оснований);
-
антропометрию (измерение роста и массы тела, окружности талии). Оценка
окружности талии (ОТ) проводилась по сводной таблице данных пограничных
величин для детей (Katmarzyk P. T.), с учетом рекомендаций IDF от 2007
года (≥ 90 перцентиля, либо > 80 см у девочек и > 94 см у мальчиков в
возрасте 16 лет и старше) [10, 11];
-
регулярное измерение артериального давления (АД в мм рт. ст.) при помощи
тонометра и манжеты по методике Короткова на двух руках в течение 1,5
недель и его оценка с применением центильных таблиц для детей разного
возраста, пола и роста (не должно превышать 95-го перцентиля) и учетом
рекомендаций IDF от 2007 года (≥ 130/85 мм рт. ст.) [10];
-
изучение липидного, углеводного спектров и обмена пуриновых оснований. Для
определения нарушений в липидном спектре крови использовались следующие
значения: по общему холестерину (ОХС) > 5,2 ммоль/л, по триглицеридам (ТГ)
> 1,7 ммоль/л, по холестерину липопротеидов низкой плотности (ХС ЛПНП) >
2,85 ммоль/л, по холестерину липопротеидов высокой плотности (ХС ЛПВП) <
1,03 ммоль/л для детей младше 16 лет и < 1,03 ммоль/л у мальчиков и < 1,29
ммоль/л у девочек в возрасте 16 лет и старше. Углеводный обмен
исследовался при помощи: определения толерантности к глюкозе (методом
перорального стандартного глюкозотолерантного теста (СГТТ), при котором
уровень глюкозы капиллярной крови не должен превышать 7,8 ммоль/л в
контроле через 2 часа после нагрузки), в динамике исследовался уровень
глюкозы капиллярной крови (при норме менее 5,6 ммоль/л натощак) с
использованием глюкометра Accu-Chek®Active. Обмен пуриновых
оснований оценивался по уровню мочевой кислоты (МК) в сыворотке крови. За
пограничное значение МК был взят показатель 0,48 ммоль/л;
-
электрокардиограмма (ЭКГ), эхокардиография (ЭХО-КГ).
Результаты и их обсуждение
Анализ анамнестических данных показал, что у 80% детей
развитие ожирения отмечалось как закономерный процесс, обусловленный
определенными пищевыми привычками в семье, при этом у 65% дополнительным
фактором риска являлась гиподинамия. Средний возраст начала значительной
прибавки массы тела (по 7 ± 1,5 кг в год) приходится на 10,5 ± 2,25 года.
Только у 17 детей (14 мальчиков и 3 девочек) родители указывали на то, что
избыточная прибавка массы тела явилась результатом чрезмерного потребления
пищи, при этом у 85% (99 человек: 73 и 26) такой закономерности не
наблюдалось. По полученным данным, чаще всего встречались дети с ожирением II
и III степени (рис. 2).
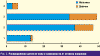
Более 2/3 пациентов (69%) имели превышение по значению ОТ (56
мальчиков (64%) и 24 девочки (82%)), являющемуся патогномоничным признаком
абдоминального ожирения.
Повышение АД зафиксировано у 73 детей, при этом у 50 человек
(38/12) отмечено эпизодическое повышение АД, связанное с эмоциональными и/или
физическими нагрузками, а у 23 детей (17/6) — стойкое. Более того, среди детей
со стойким повышением АД в 40% случаев (7/3) имелось поражение
органов-мишеней. Самым частым из ранних поражений являлась ангиопатия сетчатки
в виде суженных и извитых артерий и расширенных вен глазного дна (у 8 детей).
У двух детей выявлялись симптомы гипертрофии миокарда левого желудочка (по
данным ЭКГ, подтвержденным ЭХО-КГ,— увеличение массы миокарда левого желудочка
(МЛЖ) более чем 120 г/м2, толщина межжелудочковой перегородки (МЖП)
и задней стенки левого желудочка (ЗСЛЖ) более 95 перцентиля) как проявления
вовлеченности сердечной мышцы в патологический процесс.
Известно, что в первую очередь при ожирении страдает липидный
обмен. Так, по нашим данным нарушения обмена липидов были выявлены у 56
человек (48,3%): повышение уровня ОХС — у 34 детей (29,3%) до 6,4 ммоль/л
преимущественно за счет увеличения ХС ЛПНП (до 3,64 ± 0,11 ммоль/л).
Повышенная концентрация ТГ определялась у 26 детей (22,4%) до 3,27 ммоль/л.
Снижение уровня ХС ЛПВП до 0,79 ± 0,12 ммоль/л было выявлено у 35 детей
(30,2%). Кроме того, у 11 мальчиков было зафиксировано сочетание повышенных
концентраций ТГ и ОХ, а у 15 детей (12,9%) (10 мальчиков/5 девочек) — высокого
содержания ТГ и сниженного ХС ЛПВП.
Достаточно частым спутником ожирения является и гипергликемия
как проявление нарушения обмена углеводов. По нашим сведениям гипергликемия
имела место у 26 (22,4%) детей в возрасте от 10 до 16 лет: 20 (23%, по пробе
СГТТ 9,36 ± 1,09 ммоль/л, p < 0,05) и 6 (20,7%, от 8,0 до 9,0 ммоль/л), в том
числе у 18 человек — впервые выявленная (69%) и 5 — СД II (19%).
Нарушений обмена МК среди девочек не встречалось, но они
зарегистрированы у 22 мальчиков (18,9% всех мальчиков) в виде ГУ (0,53 ± 0,024
ммоль/л, p < 0,05) в возрасте от 11 до 16 лет.
Особый интерес представлял анализ сочетания
клинико-биохимических синдромов. Сочетание нарушений липидного обмена и
гипергликемии отмечено у 15 детей (12,9%): 11 (12,6%) и 4 (13,8%) в возрасте
от 9 до 16 лет. Сочетание ГУ и нарушения обмена липидов выявлено у 5 мальчиков
(5,74%); у 9 мальчиков (10,3%) — сочетание ГУ и гипергликемии (возраст детей
12–17 лет). Наличие трех-четырех компонентов в различных комбинациях обменных
и регуляционных нарушений определено у 20 детей (17,2%). У одного ребенка
(мальчик 14 лет с IV степенью ожирения) был обнаружен полный вариант МС.
Таким образом, в детском и подростковом возрасте при наличии
абдоминального ожирения часто встречаются сопутствующие нарушения обмена
липидов (48,3%), углеводов (22,4%), пуриновых оснований (19%) и регуляции АД
(43,1% — эпизодические, 19,8% — стойкие нарушения), характерные для МС.
Результаты анамнестического анализа говорят о схожести клинической картины
основных патологических проявлений среди детей и их ближайших родственников
(более чем в 66,6% случаев), что позволяет предположить, что на процесс
формирования и клиническую выраженность перечисленных признаков у детей с
ожирением значительное влияние оказывают генетические факторы, лежащие в
основе наследственной предрасположенности, заранее определяющей общие черты и
особенности будущих признаков. Их выявление поможет объяснить наличие или
отсутствие ожидаемых проявлений заболевания, а также заблаговременно
сформировать группу риска развития МС и определить возможность и эффективность
немедикаментозной и фармакотерапии.
Детям, входящим в группу риска развития МС, как и уже имеющим
основные признаки синдрома, показана комплексная терапия, объем и методы
которой подбираются строго индивидуально и зависят от выраженности и формы
заболевания, во многом определяемым генотипом ребенка.
Основной целью профилактики и лечения является предотвращение
или снижение общего риска развития и прогрессирования сердечно-сосудистой
заболеваемости, характерной для МС. В детском и подростковом возрасте на
первый план выходит профилактика формирования и развития составляющих МС. На
любом этапе развития заболевания важны мероприятия, направленные на
формирование здорового образа жизни, борьбу с избыточной массой тела,
перееданием и несбалансированным питанием, оптимизацию двигательного режима,
отказ от вредных привычек.
Наиболее эффективным методом воздействия практически на все
компоненты МС является борьба с избыточной массой тела. Снижение массы тела на
10–15% от исходной способствует повышению чувствительности к инсулину,
улучшает показатели углеводного и липидного обмена, снижает системную ГИ и АД.
Данные эффекты достигаются путем рационального питания в сочетании с
индивидуально подобранной физической нагрузкой. При неудовлетворительном
результате возможно сочетание с медикаментозной терапией. Успешно применяется
орлистат (Ксеникал*) — ингибитор панкреатической и кишечной липазы,
стабилизирующий массу тела, улучшающий показатели липидного и углеводного
обмена, назначается нами с 12 лет по 120 мг 3 раза в день. При
диагностированной гипергликемии на фоне ИР препаратом выбора является
метформин (Сиофор, Глюкофаж) — бигуанид, повышающий чувствительность тканей к
инсулину, способствующий стабилизации и снижению массы тела и оказывающий
гипотензивный эффект, назначаются нами с 10–12 лет по 500–1000 мг 1 раз в день
[1, 12–14].
При выраженной дислипидемии детям и подросткам назначаются
гиполипидемические препараты. При смешанной и изолированной
гиперхолестиринемии применяют эссенциальные фосфолипиды, анионообменные смолы,
антиоксиданты (Элькар, Кудесан), пробукол, статины (разрешены с 12 лет). При
гипертриглицеридемии — препараты, содержащие омега-3-полиненасыщенные жирные
кислоты (Омакор*) и фибраты (разрешены с 12 лет) [1, 12, 13, 15]. Кроме того,
неплохие результаты по нормализации липидного спектра были получены на фоне
применения про- и пребиотиков, таких как Бифиформ® Малыш
(содержащий лакто- и бифидобактерии) и Дюфалак® (содержащий
лактулозу), что объясняется непосредственным участием нормальной микрофлоры в
процессах регуляции обмена липидов. Определенный интерес для оптимизации
обменных процессов и сохранения нормальной функции печени имеет использование
такого препарата, как Хофитол, применение которого сопровождается умеренным
липидснижающим, вазодилятирущим, гепатопротекторным эффектами.
В лечении пациентов, страдающих АГ, связанной с МС, важен
подбор препаратов, не ухудшающих показатели углеводного и липидного обмена.
Хорошо себя зарекомендовали ингибиторы АПФ (Капотен*, Ренитек), которые, кроме
гипотензивного эффекта, обладают протективным нефро- и кардиоваскулярным
эффектом, снижают ИР и назначаются нами с 10–12 лет по 5–10 мг 1 раз в день
[1, 12–15]. Перспективны в этом плане и агонисты I1-имидазолиновых
рецепторов (моксонидин (Физиотенз*)), снижающие системное сосудистое
сопротивление и АД, оказывающие нефро- и кардиопротективное действие [12, 14].
Препаратами выбора, как у детей, так и у взрослых, остаются: диуретики (индапамид
(Арифон*) — по 1,5 мг/сут, Верошпирон), селективные бета1-адреноблокаторы
(Корвитол, Небилет, бисопролол), антагонисты кальция (верапамил/нифедипин)
[12, 14, 15].

