Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Адеметионин в лечении хронических заболеваний печени с
холестазом
О. Н. Минушкин, доктор медицинских наук, профессор
ФГУ Учебно-научного медицинского центра Управления делами Президента РФ, Москва
Печень представляет собой центральный орган химического
гомеостаза, где создается единый обменный и энергетический пул для метаболизма
жиров и углеводов, кроме того, печень участвует в синтезе некоторых ферментов,
витаминов, принимает непосредственное участие в водном, минеральном и пигментном
обмене; чрезвычайно важное значение имеет детоксицирующая функция печени.
Круг патологических состояний печени очень велик, и большинство
этих изменений могут сопровождаться нарушением любой из перечисленных функций
печени или многими с тем или иным преобладанием.
Образование желчи является одной из важнейших функций печени.
Любые нарушения синтеза, секреции или тока желчи, приводящие к биохимическим,
патофизиологическим, патолого-анатомическим изменениям, сопровождающимся теми
или иными клиническими проявлениями, обозначаются термином «холестаз», который
классифицируют на 2 группы: внутрипеченочный и внепеченочный. Внепеченочный
холестаз обусловлен механическим препятствием в протоковой системе, а
внутрипеченочный— нарушением функции гепатоцита или нарушением тока желчи в
межклеточном пространстве. В свою очередь внутрипеченочный холестаз
классифицируют на две подгруппы: печеночно-канальцевый (внутридольковый) и
протоковый (междольковый). Различные типы холестаза в значительной степени
перекрываются между собой. Накопление желчных кислот внутри клеток печени может
в конечном итоге вести к их гибели, т.е. возникает порочный круг, в котором
внутрипеченочный холестаз, вызванный различными типами повреждений печени, в
свою очередь усугубляет эти нарушения [1].
Гептрал (адеметионин)— S-аденозил-L-метионин— аминокислота,
которая синтезируется в организме и участвует в ферментативном переаминировании
и пересульфировании, синтезе иактивации гормонов, нейромедиаторов, нуклеиновых
кислот, фосфолипидов. Отдавая метильную группу при переметилировании и
пересульфировании, адеметионин способствует образованию глутатиона— основного
клеточного антиокислителя, обезвреживающего воздействие ряда экзо- иэндотоксинов.
В медицинской практике используется в двух формах: инъекционной,
состоящей из 1 флакона с лиофилизированной солью адеметионина и 1 ампулы
растворителя, который делает вводимую среду нейтральной (рН 7,5±1). Форма
Гептрала для перорального применения представляет собой белые таблетки в
энтеросолюбильной оболочке, нерастворимой в кислой среде желудка. Адеметионин
является универсальным соединением, участвующим в трех важных метаболических
реакциях: трансметилировании, транссульфировании и аминопропилировании (синтез
полиаминов), где служит либо донором групп, либо модулятором ферментов. Активная
роль адеметионина в этих реакциях обусловлена наличием положительного заряда на
атоме серы, благодаря чему происходит разрыв сероуглеродных связей.
Независимо от патогенеза внутрипеченочного холестаза,
адеметионин играет важную роль как в развитии, так и в предотвращении
внутрипеченочного холестаза. Адеметионин является донором метильной группы,
участвуя в реакциях трансметилирования (это биосинтез фосфолипидов, которые
являются основными строительными блоками клеточной мембраны). Количество
фосфолипидов определяет «текучесть» клеточной мембраны. Показано, что
«текучесть» клеточной мембраны является важнейшим фактором, влияющим на
связанные с мембраной ферментативные процессы. Структура и состав мембран
гепатоцитов являются ключевым звеном в регуляции наиболее важных метаболических
путей, участвующих в выработке желчи (Chawla et al., 1990).
Снижение «текучести» мембраны ведет к уменьшению активности Na/K-АТФазного
насоса и нарушению натрийзависимых синтранспортных систем (имеющих прямое
отношение к транспорту желчных кислот). Адеметионин способен предотвращать
подобные изменения.
Вторым положительным аспектом влияния адеметионина является его
участие в поддержании на достаточном уровне глутатиона— серосодержащего пептида,
имеющего отношение к защите печеночной клетки от токсического повреждения
свободными радикалами. Наконец, участвуя в реакциях сульфатирования, адеметионин
играет важную роль в детоксикации ряда метаболитов, таких как токсичные желчные
кислоты, переводя их в сульфаты, которые не оказывают повреждающего действия на
клетку. Предыдущие два эффекта имеют прямое отношение к защите печени от
токсического эффекта этанола, который реализуется через ацетальдегид. Эти
эффекты предотвращаются адеметионином, посредством поддержания митохондриального
транспорта глутатиона.
Клиническое изучение эффективности Гептрала у больных,
страдающих заболеваниями печени с внутрипеченочным холестазом, было начато в
90-е годы. Так, Frezza et al., 1990 провели лечение адеметионином 220 больных с
патологией печени, доказанной биопсией. Необходимым условием лечения было, по
крайней мере, двукратное повышение общего и конъюгированного билирубина и
щелочной фосфатазы в сыворотке крови. Больные получали либо 1600мг препарата
внутрь, либо плацебо. Продолжительность лечения составила 15 дней. При этом была
доказана эффективность Гептрала как в отношении клинических проявлений, так
илабораторных показателей холестаза (по сравнению с плацебо). В 1992 году
Manzillo и соавт. у 420 больных провели лечение в 2 этапа (первый— 800мг в день
внутривенно 2 недели, затем— 1600 мг в день или плацебо в течение 8 недель). Они
подтвердили еще больший эффект при увеличении продолжительности лечения (он
составил 68%). Таким образом, было показано, что у больных с хроническими
заболеваниями печени более продолжительное лечение сопряжено с дальнейшим
улучшением биохимических показателей печени. В дальнейшем была подтверждена
эффективность адеметионина у женщин с внутрипеченочным холестазом при
беременности (Frezza M., Terpin, 1992), у больных с депрессией (Rozenbaum,
1990), у больных с хроническим панкреатитом— для того, чтобы ингибировать
активность свободных радикалов (Bilton et al.,1994); при остром панкреатите (Braganza
et al., 1995)— для снижения окислительного стресса. Рассматриваются и другие
возможности использования Гептрала (профилактика поражений печени при
парентеральном питании, при гипоксических состояниях, при операциях
трансплантации печени). Оценка эффективности Гептрала у разных групп больных
(алкогольное поражение, вирусное, в стадии цирроза печени, в дистрофической
стадии с печеночно-клеточной недостаточностью). Рассматривались различные дозы
препарата, разные пути введения, разная продолжительность лечения (500 мг, 800
мг, 1600 мг). Все исследования сравнивали с плацебо, и эффект Гептрала составлял
60% и выше, пероральный прием усиливал эффект парентерального введения
(продолжительность лечения составляла от 2 недель до месяца и более (Lieber
C.S.,1999; Di Perri T. et al., 1999; Mato J.M., 1999)). Переносимость Гептрала
оценивалась всеми исследователями как хорошая. Побочные эффекты в виде
кратковременной бессонницы, тошноты, потливости, легкого флебита при двойном
слепом исследовании отмечены у очень небольшого количества больных и не
отличались от группы плацебо.
Учитывая вышеизложенное, мы также оценили эффективность
применения Гептрала у 60 больных с хроническими заболеваниями печени и синдромом
холестаза.
Характеристика больных:
-
первичный билиарный цирроз— 8 больных;
-
алкогольный гепатит— 22 больных;
-
хронический гепатит С— 20 больных;
-
хронический гепатит В— 4 больных;
-
хронический вирусный гепатит встадии цирроза печени— 4 больных;
-
первичный склерозирующий холангит— 2 больных.
Мужчин было 38, женщин 22; возраст от 30 до 65 лет (средний
возраст 43,4±1,7 года); средняя продолжительность заболевания 5,7±3 года
(минимально— 3 года, максимально — 12 лет). Больные с алкогольным поражением
печени длительное время (от 15 до 17 лет) употребляли алкоголь с частотой от 2
до 7 раз в неделю; ежедневно доза алкоголя в пересчете на этанол составляла от
60 до 200 мл. Критериями включения в эту группу служили: диффузный характер
поражения печени, «алкогольный» анамнез, системность поражения, отсутствие
маркеров вирусов гепатита В и С.
Методы исследования:
-
клиническая оценка (желтуха, кожный зуд, астенический синдром, гепатомегалия,
спленомегалия, асцит);
-
биохимический мониторинг (АлАТ, АсАТ, билирубин, холестерин, гамма-ГТП, ЩФ,
белок и белковые фракции, креатинин— исходно и по окончании курса лечения);
-
ультразвуковой мониторинг и оценка денситометрических показателей, размеров
печени и селезенки, диаметра селезеночной вены, измерения «столба затухания»
с отключением автоматического усиления сигнала по глубине;
-
маркеры вирусов гепатита В и С (анти-HCV; HbsAg; HbeAg; HBcAg; HCV-РНК;
HBV-ДНК);
-
рутинные лабораторные исследования (общий анализ крови, мочи);
-
больным циррозом печени проводили эзофагогастродуоденоскопию с оценкой
степени варикозно-расширенных вен пищевода и «коронарных» вен желудка.
Лечение
Гептрал назначался в дозе 800 мг внутривенно, медленно — в
течение 14 дней с последующим переходом на пероральный прием в дозе 1600 мг в
сутки (разделенных на 2 приема) — на протяжении 14 дней.
У 10 больных с недостаточным эффектом терапии (сохраняющийся
холестаз и кожный зуд) — принимали решение о продолжении лечения Гептралом в
суточной дозе 3200 мг (по 1600 мг×2 приема) — на протяжении 2 недель.
Цель использования дозы 3200 мг заключалась в оценке лечебного
эффекта и переносимости дозы.
Клинические проявления заболевания в зависимости от
нозологической формы и их динамика под влиянием терапии Гептралом представлены в
таблице (в числителе представлены исходные данные, в знаменателе — эффективность
терапии).
10 больных с сохраняющимся кожным зудом, желтухой, астенией
продолжили лечение Гептралом в суточной дозе 3200 мг (по1600 мг×2 раза в день)
еще 2 недели. При этом были купированы клинические синдромы и продолжено
улучшение лабораторных показателей.
Из представленной таблицы видно, что клинический эффект Гептрала
за 4 недели лечения отмечен у большей части больных (полное купирование от 50 до
100%), прежде всего у больных с алкогольным поражением (по всем клиническим и
лабораторным показателям). Астенический синдром начал уменьшаться к 5–7 дню
лечения, кожный зуд начал уменьшаться к концу второй недели, при этом важно
отметить, что его динамика была заметной даже при сохранении лабораторного
синдрома холестаза. У большей части больных зафиксирована положительная динамика
размеров печени (особенно при алкогольном поражении). Асцит был зарегистрирован
у 6 больных (у 4 с циррозом печени и у 2 с обострением алкогольного гепатита).
Разрешения асцита удалось добиться у всех больных — у 4 с
циррозом печени потребовалось введение в комплекс лечения Верошпирона и
мочегонных.
У 10 больных заметной динамики лабораторных признаков холестаза
отмечено не было, а клинические синдромы только уменьшились в интенсивности. У
этой группы больных доза Гептрала была повышена до 3200 мг/сутки еще на
протяжении 14 дней (по 1600 мг ´ 2 раза в день).
Практически у всех больных это лечение сопровождалось дальнейшим
улучшением или нормализацией клинических проявлений и положительной динамикой
лабораторных показателей (особенно билирубина, который на исходных дозах
положительной динамики не показал).
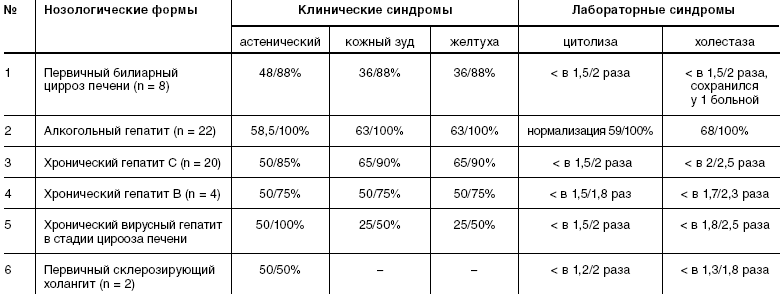
Результаты лечения (динамика основных клинических и лабораторных
синдромов)
Побочных эффектов у больных, получавших Гептрал в дозе 3200 мг в
сутки, отмечено не было, переносимость препарата была хорошей.
Общее заключение:
-
Гептрал является эффективным препаратом в лечении больных, страдающих
хроническими воспалительными заболеваниями печени с холестазом.
-
Эффект зависит от использованной дозы и продолжительности лечения.
-
Доза Гептрала 3200 мг/сутки в течение 2 недель лечения, как показал наш
клинический опыт, возможно, является альтернативой рекомендуемому
4-недельному двухфазному курсу.
-
Препарат максимально эффективен при алкогольном поражении печени.
-
Переносимость обеих форм препарата хорошая, побочных эффектов не
наблюдалось.
Литература
-
Подымова С. Д. Внутрипеченочный холестаз: патогенез и лечение с современных
позиций // Consillium Medicum, приложение № 2 (гастроэнтерология). 2004. С.
3–6.
- Chawla R. K., Bonkovsky H. L., J. T. Biochemestrry and pharmacology of
S-adenosyl-L- metheonine and rationale for its use in liver disease // Drugs.,
1990. 40 (suppl. 3): 98–110. 3.
Frezza M., Surrenti C., Manzillo G. et al. Oral S-adenosylmetheonine in the
symptovatic of intrahepatic cholestasis // Gastroenterology. 1990. 99:
211–215.
- Manzillo G., Piccinino F., Surrenti C et al. Multicentre double — blind
placebo — controlled study of intravenous and oral S-adenosyl-L-metheonine (SAMe)
in cholestatic patients with lover disease // Drug Invest. 1992. 4 (suppl. 4):
90–100. 5.
Frezzza M., Terpin M. The use of S-adenosyl-L-metheonine in the treatment of
cholestatic disorders. A meta — analisis of clinical trials // Drug Invest.
1992. 4 (suppl. 4): 101–108.
- Rosenbaum J. F., Fava M., Falk W. E. et al. The antidepressant potential
or oral S — adenosyl — L — metheonine // Acta Psychiatr. Scand. 1990. 81:
432–436. 7.
Bilton D., Schofield D., Schofield D., Mei G. et al. Placebo — controlled
trials of antioxidant therapy including S-adenosylmetheonine in patients with
recurrent nongallstone pancreatitis // Drug Invest. 1994. 8: 10–20.
- Braganza J. M., Scott P., Bilton D. et al. Evidence for early oxidative
stress in acute pancreatitis// Int.J. Pancreatol. 1995.17: 69–81. 9. Lieber C.
S. Role of S-adenosyl-L-metheonine in the treatment of liver disease // J.
Hepatology. 1999. 30: 1155–1159б.
- Fiorelli G. S-adenosylmetheonine in the treatment of intrahepatic
cholestasis of chronic liver disease: A field trial. current Therapeutic
Research, vol. 60, 6: 335–348. 11.
Di Perri T., Sacco T., Festi D. Ademethionine in the treatment of chronic
hepatic disease. A multicenter study // Gastroenerology Internationale. 1999.
Vol. 12, 2: 62–68.
-
Mato J. M., Camara J., de Paz J. F. et al. S-Ademethionine in alcoholic
liver cirrosis: a randomized, placebo — controlled, double — blind,
multicenter clinical trial // J. Hepatology. 1999. 30: 1081–1089.
Статья опубликована в журнале
Лечащий Врач

