Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Рецидивы воспалительного процесса в мочевыводящих путях,
возникающие в послеоперационном периоде, сводят на нет результаты сложнейших
реконструктивных операций, требуют изменения тактики ведения пациентов и
дополнительных затрат для лечения и реабилитации больных [5, 8]. Значимая роль
в патогенезе хронического обструктивного пиелонефрита отводится транслокации
микрофлоры кишечника в мочевые пути и возникновению инфекционного процесса.
Факторами риска транслокации потенциально-патогенных бактерий
в мочевыделительную систему являются нарушение иммунного статуса и применение
массивной антибактериальной терапии [4]. Следует отметить, что нормальная
микрофлора желудочно-кишечного тракта (ЖКТ) отвечает за ряд жизненно важных
функций в организме: участвует в ферментативном расщеплении пищи, всасывании
железа, кальция, различных витаминов, обмене желчных пигментов, регуляции
кишечной перистальтики, а также в выработке антител и созревании
макрофагально-гистиоцитарной системы [9, 10, 11]. Кроме того, несмотря на
весьма богатый диапазон современных представителей антибактериальных
препаратов, все чаще выявляются штаммы возбудителей микробно-воспалительного
процесса в мочевыводящих путях, обладающие полирезистентностью к антибиотикам,
что затрудняет лечение хронического обструктивного пиелонефрита у детей. В
связи с этим постоянно проводится активный поиск новых подходов в лечении и
профилактике обострения данной патологии. Очевидно, что нормализация
микробиоценоза ЖКТ является перспективным направлением в профилактике
периоперационных осложнений воспалительного генеза на фоне обструкции
мочевыводящих путей.
В клинике хирургии детского возраста Саратовского
государственного медицинского университета апробировано применение
биологически активной добавки (БАД) Бифидум № 791 БАГ с целью снижения частоты
и тяжести обострения хронического обструктивного пиелонефрита у детей в
послеоперационном периоде. Микробиологической основой препарата является
консорциум, состоящий из наиболее эффективных штаммов бифидобактерий (Bifidobacterium
bifidum 791/БАГ, Bifidobacterium bifidum 8-3 и Bifidobacterium longum ДВА-13,
принадлежащих к роду Bifidobacterium, семейству Actinomycetaceae). Бифидум №
791 БАГ выпускается в первичной, жидкой форме, и его штаммы бифидобактерий
находятся в физиологически активном состоянии, имеют высокую адгезивную
способность и кислотоустойчивость, обладают повышенными антагонистическими
свойствами и колонизационной резистентностью в отношении многих
микроорганизмов.
Бифидум № 791 БАГ является наиболее приемлемым средством для
лечения дисбактериоза кишечника, поскольку прошел клинические испытания,
безвреден, обладает высокой активностью в отношении восстановления
нормобиоценоза кишечника, не вызывает нежелательных реакций при использовании
его в соответствии с разработанной инструкцией.
Материалы и методы исследования
В основу исследования положен анализ лечения 40 детей с
обструктивными уропатиями (гидронефрозом, пузырно-мочеточниковым рефлюксом,
мегауретером). Все больные были разделены на две группы: 1 группа —
исследования с включением в комплексное лечение БАД Бифидум № 791 БАГ, 2
группа — сравнения со стандартной терапией.
В группу исследования вошли 20 детей (мальчиков — 13, девочек
— 7) с обструктивными уропатиями (пузырно-мочеточниковым рефлюксом — 10,
гидронефрозом — 8, мегауретером — 2), в возрасте от 3 до 15 лет (средний
возраст больных 8,6 ± 5,2 года). На участие в исследовании получено
информированное согласие родителей. После проведения стандартного
урологического обследования за день до оперативного лечения в комплекс
лечебных мероприятий вводился БАД Бифидум № 791 БАГ per os, 2–3 раза в день за
30–40 мин до еды, запивая молоком, кисломолочными продуктами или водой в
возрастной дозировке (детям от 1 года до семи лет — 2–3 мл на 1 прием,
взрослым и детям старше семи лет применять 3–5 мл на 1 прием). Курс лечения
составлял 14 дней.
Группу сравнения составили 20 детей (мальчиков — 9, девочек —
11) с аналогичной патологией (пузырно-мочеточниковым рефлюксом — 8,
гидронефрозом — 9, мегауретером — 3), той же возрастной категории (8,1 + 4,6),
но без применения Бифидум № 791 БАГ.
В обеих группах больных до оперативного лечения обструктивной
уропатии была проведена оценка исходного состояния больного, включавшая в
себя: клинические данные (общее состояние, жалобы, термометрию и т. д.), общий
анализ крови на автоматическом гематологическом анализаторе Sysmex XT-1800 i с
расчетом лейкоцитарных индексов клеточной реактивности: индекса ядерного
сдвига (ИЯС), лейкоцитарного индекса интоксикации (ЛИИ), лимфоцитарного
индекса (ЛИ), индекса иммунологической реактивности (ИИР); протеинограмму с
определением уровня общего белка и его фракций, общий анализ мочи и анализ
мочи по Нечипоренко. Затем динамика исследуемых показателей была исследована в
обеих группах на 3–5 и 14–15 сутки после оперативной коррекции обструктивного
синдрома мочевыводящих путей.
Статистический анализ результатов обследования и лечения
пациентов проведен с использованием пакета прикладных программ Statistica 6.0
for Windows.
Результаты и их обсуждение
Пациенты обеих групп до исследования находились в состоянии
ремиссии по течению обструктивного пиелонефрита; показатели состава
периферической крови, лейкоцитарные индексы клеточной реактивности, белкового
спектра сыворотки крови, общего анализа мочи и анализа мочи по Нечипоренко не
выходили за пределы возрастной нормы. Таким образом, исходное состояние
пациентов группы исследования и группы сравнения достоверных отличий не имело.
Далее нами был проведен внутригрупповой и сравнительный анализ
изменения исследуемых показателей. Полученные результаты исследования
приведены в табл. 1, 2, 3, 4 и на рис.
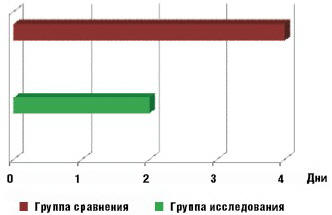
Рис. Длительность лихорадки у больных с обструктивными
уропатиями в послеоперационном периоде
В группе исследования на фоне включения в комплекс лечения
Бифидум № 791 БАГ на 3–5 сутки после операции обнаружены следующие изменения:
-
в ОАК отмечалось увеличение количества сегментоядерных нейтрофилов и
снижение уровня лимфоцитов по сравнению с исходными показателями (p <
0,05) (табл. 1);
-
повышение ЛИИ и снижение ЛИ и ИИР (p < 0,05) (табл. 2);
-
выраженных изменений белкового состава сыворотки крови не выявлено (табл.
3);
-
в ОАМ и анализе мочи по Нечипоренко на 3–5 сутки после операции выявлены:
гематурия, лейкоцитурия, протеинурия и цилиндрурия (p < 0,05) (табл. 4).
На 14–15 сутки после операции указанные изменения возвращались
к исходному уровню. Продолжительность лихорадки составила 1,7 ± 1,3 дня
(рис.). Изменения характера стула в послеоперационном периоде отмечались у 3
пациентов (15%).
Динамика показателей периферической крови и лейкоцитарных
индексов клеточной реактивности у детей с обструктивными уропатиями в
периоперационном периоде
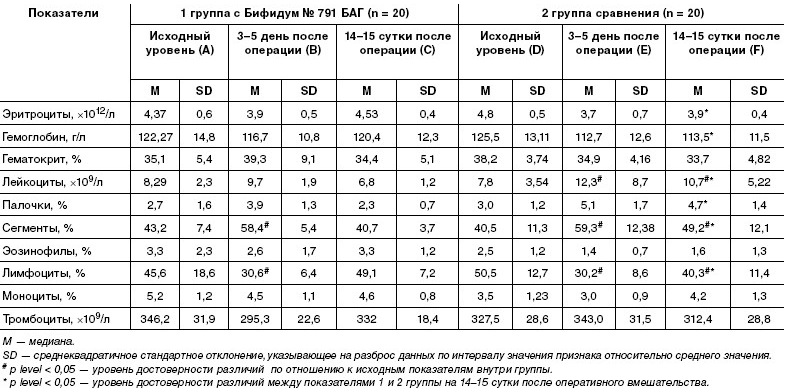
Изменение лейкоцитарных индексов клеточной реактивности у
детей с обструктивными уропатиями
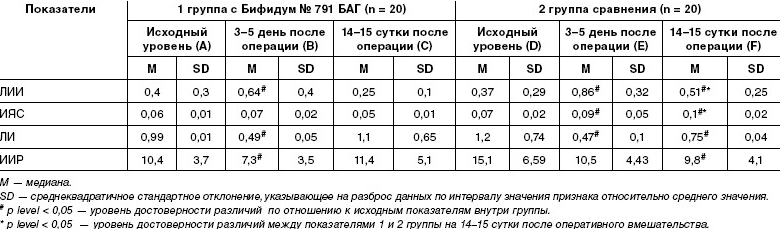
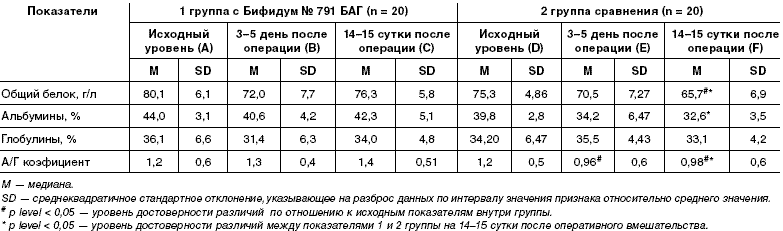
Показатели белкового спектра крови в обследованных
группах детей в периоперационном периоде
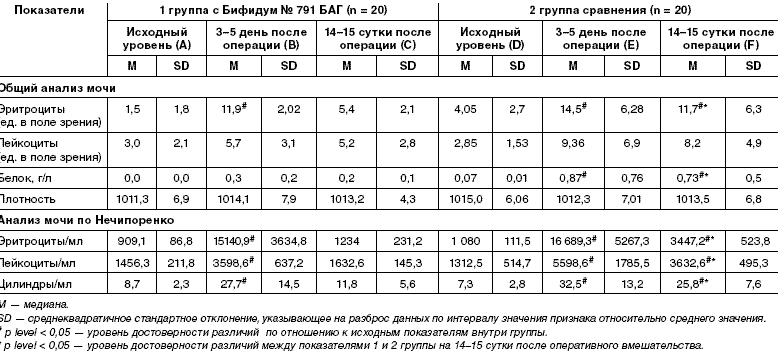
Изменения показателей мочи в периоперационном периоде у
детей с обструктивными уропатиями
В группе сравнения на 3–5 сутки после операции выявлены
следующие изменения:
-
в ОАК имел место лейкоцитоз, увеличение сегментоядерных нейтрофилов,
снижение количества лимфоцитов (p < 0,05) (табл. 1);
-
отмечалось повышение ЛИИ, ИЯС, снижение ЛИ, ИИР (p < 0,05) (табл. 2);
-
в биохимическом анализе получено снижение общего белка крови и
альбумино-глобулинового коэффициента (p < 0,05) (табл. 3);
-
в ОАМ и анализе мочи по Нечипоренко отмечалось увеличение количества
эритроцитов, лейкоцитов, цилиндров, повышение содержания белка в моче (p <
0,05) (табл. 4).
Выявленные изменения сохранялись и на 14–15 день после
операции. Продолжительность лихорадки в этой группе больных составляла 2,75 ±
2,25 дня (рис.). Расстройства стула, связанные с развитием дисбиоценоза на
фоне массивной антибактериальной терапии в послеоперационном периоде,
отмечались у 7 пациентов (35%).
Следует отметить, что клинически послеоперационный период у
больных обеих групп протекал гладко, выраженного обострения воспалительного
процесса в мочевыводящих путях не наблюдалось, осложнений, потребовавших
дополнительных оперативных вмешательств и изменения тактики ведения пациента,
не регистрировалось. Однако детальный анализ исследуемых показателей позволил
выявить ряд достоверных различий на 14–15 сутки после оперативного лечения:
-
в группе сравнения в ОАК отмечалась более выраженная анемия, лейкоцитоз со
сдвигом влево (p < 0,05) (табл. 1);
-
в группе сравнения ЛИИ и ИЯС оставался выше, чем у пациентов группы
исследования с применением Бифидум № 791 БАГ (p < 0,05) (табл. 2);
-
в группе сравнения наблюдалась диспротеинемия со снижением
альбумино-глобулинового коэффициента (p < 0,05) (табл. 3);
-
в группе сравнения в ОАМ определялись более выраженные гематурия, скрытая
лейкоцитурия, протеинурия, цилиндрурия (p < 0,05) (табл. 4);
-
в группе сравнения период лихорадки был более длительным (p < 0,05)
(рис.);
-
в группе сравнения более часто (у 35% больных) отмечалось изменение
характера стула в послеоперационном периоде, связанное с дисбиоценозом
кишечника.
Таким образом, при применении БАД Бифидум № 791 БАГ течение
послеоперационного периода было более гладким, отмечались более быстрая
регрессия анемии и лейкоцитоза, лейкоцитарных индексов клеточной реактивности.
Санация мочи и восстановление температурного гомеостаза происходили в более
краткие сроки. По всей видимости, поддержание нормального микробиоценоза ЖКТ с
помощью БАД Бифидум № 791 БАГ позволило добиться быстрой локализации и
купирования воспалительного процесса в мочевыводящих путях, способствовало
полноценной реабилитации детей с обструктивными уропатиями в послеоперационном
периоде.
Полученные результаты, на наш взгляд, позволяют рекомендовать
включение БАД Бифидум № 791 БАГ в комплекс лечения хронического обструктивного
пиелонефрита у детей в периоперационном периоде
Литература
-
Леванов А. В. Феномен бактериальной транслокации условно
патогенных микроорганизмов из желудочно-кишечного тракта // Антибиотики и
химиотерапия. 2001. Т. 46, № 5. С. 28–31.
-
Лоран О.Б.,Синякова Л.А. Воспалительные заболевания
органов мочевой системы.Актуальные вопросы:Учебное пособие для
врачей.М.:ООО«Медицинское информационное агентство»,2008.88 с
-
Яцык С. П., Сенцова Т. Б., Фомини Д. К., С. М. Шарков.
Патогенез хронического обструктивного пиелонефрита у детей и подростков.
М.: ООО«Медицинское информационное агентство»,2007. 176 с.
-
Bird A. R., Brown I. L., Topping D. L. Starches, resistant
starches, the gut microfloraand human health // Curr. Issues. Intest.
Microbiol. 2002. Vol. 1, P. 25–37.
-
Fric P. Probiotics in gastroenterolodgy/ P.Fric // J.
Gastroenterol. 2002. Vol. 40, № 3. P. 197–201.
-
Zboril V. Physiology of microflora in the digestive tract/
V. Zboril // Vnitr. Lek. 2002. Vol. 48, № 1. P. 17–21.

