Краткий обзор клинических исследований иммуногенности и
безопасности гриппозной вакцины
М. К. Ерофеева*, доктор медицинских наук
И. Ю. Никаноров*
С. М. Харит**, доктор медицинских наук, профессор
В. В. Романенко***, кандидат медицинских наук
* НИИ гриппа Северо-Западного отделения РАМН, Санкт-Петербург
** НИИ детских инфекций ФМБА, Санкт-Петербург
*** ФГУ «Центр гигиены и эпидемиологии в Свердловской области», Екатеринбург
Всемирная система мониторинга циркуляции вирусов, новые
технологии выделения и очистки отдельных протективных субъединиц и использование
новых субстратов для выращивания вакцинных вирусов позволяют производить
эффективные и безопасные препараты в необходимых объемах. Отечественные
современные высокотехнологичные инактивированные гриппозные вакцины можно
рассматривать как наглядный пример реализации накопленных знаний в сочетании с
применением инновационных технологий.
Вакцина Гриппол® Нео — одна из современных отечественных вакцин
последнего поколения семейства «Гриппол®» — представляет собой
усовершенствованный аналог препаратов Гриппол® и Гриппол® плюс, применяемых для
массовой вакцинопрофилактики россиян в рамках национального проекта «Здоровье».
Гриппол® Нео сконструирован с применением комбинации двух инновационных
технологий: вакцина включает безопасный водорастворимый адъювант Полиоксидоний®
и антигены, выделенные из штаммов вируса гриппа, выращенных на культуре клеток
линии MDCK — Madine Darby Canine Kidney. Так же, как и в других вакцинах
семейства «Гриппол®», содержание вирусных антигенов в Грипполе® Нео втрое меньше
по сравнению с существующими зарубежными вакцинными препаратами. Как и вакцина
Гриппол® плюс, Гриппол® Нео не содержит консерванта и производится на
современном фармацевтическом предприятии в соответствии с международными
требованиями GMP, в готовой к применению упаковке — шприц-дозе [1]. Важно
отметить, что Гриппол® Нео стала первой российской гриппозной вакциной, не
противопоказанной людям с аллергией на белок куриного яйца ввиду того, что
куриные эмбрионы полностью исключены из технологического процесса.
Доклиническая оценка вакцины Гриппол® Нео проводилась
несколькими аккредитованными организациями согласно утвержденным протоколам. В
различных моделях было показано, что в дозах, многократно превышающих
человеческую, вакцина не оказывает токсического, пирогенного, аллергизирующего
действия как на взрослых, так и на неполовозрелых и новорожденных животных,
безопасна для иммунной системы как в короткие, так и в отдаленные сроки после
вакцинации. Результаты доклинических исследований позволили рекомендовать ее к
проведению клинических исследований.
Цель данной статьи — ознакомить читателей с результатами
клинических исследований вакцины Гриппол® Нео.
Оценка безопасности вакцины Гриппол® Нео у взрослых
добровольцев
Клиническое рандомизированное сравнительное двойное слепое
контролируемое исследование в параллельных группах (Фаза I), проводимое с целью
оценки безопасности, включало 60 здоровых добровольцев обоего пола в возрасте
18–54 лет [2]. Все участники, отобранные в соответствии с критериями
включения/исключения, были случайным образом распределены в три группы по 20
человек. Течение поствакцинального процесса, регистрацию и классификацию реакций
осуществляли в соответствии с утвержденным протоколом и с учетом требований
национальных регулятивных документов и рекомендаций [3–5]. Оценка реактогенности
показала, что из симптомов нарушения общего состояния в основном регистрировали
слабость (у 3,1% вакцинированных); из местных реакций у 4,0% вакцинированных
регистрировали боль в месте инъекции при физической нагрузке или надавливании.
В целом на основании анализа результатов наблюдений сделано
заключение о том, что обе дозировки вакцины, полученной с применением клеточной
технологии, безвредны и слабо реактогенны. Не зарегистрировано сильных
поствакцинальных реакций и серьезных нежелательных явлений. Полученные
результаты стали основанием рекомендовать вакцину Гриппол® Нео для проведения
исследований на расширенном контингенте вакцинируемых [6]. Задачей клинического
исследования Фазы II явилась оценка реактогенности, безопасности, иммуногенной
активности двух доз вакцины Гриппол® Нео (5 + 5 + 5) мкг ГА и (10 + 10 + 10) мкг
на расширенном контингенте добровольцев в сравнении с референс-препаратом —
вакциной Гриппол®. Работа проведена в период с декабря 2008 года по февраль 2009
года на базе кафедры инфекционных болезней и эпидемиологии ГОУ ВПО СПбГМУ им.
академика И. П. Павлова и НИИ детских инфекций Росздрава. Рандомизированное
двойное слепое контролируемое исследование в параллельных группах включало 300
здоровых добровольцев обоих полов в возрасте 18–54 лет. В соответствии с
протоколом было сформировано три группы по 100 человек: две группы участников
были вакцинированы Грипполом® Нео, одна группа — вакциной сравнения. В
поствакцинальном периоде (5 дней наблюдения после вакцинации) оценивали
реактогенность препарата по частоте местных и общих реакций. В течение трех
месяцев после вакцинации проводился мониторинг интеркуррентной заболеваемости.
В табл. 1 представлено общее число вакцинированных по группам с
местными и общими реакциями на прививку.

Местные реакции выражались в форме боли при надавливании,
гиперемии, уплотнения и зуда в месте инъекции. Все регистрируемые реакции были
слабой степени выраженности и проходили в течение двух дней. Среди общих реакций
преобладали недомогание, ринит; в единичных случаях зарегистрированы
субфебрильная температура, боль в горле, кашель, увеличение регионарных
лимфоузлов. Продолжительность выявленных реакций, как правило, не превышала
одного-двух дней. По результатам трехмесячного мониторинга число случаев
соматической, инфекционной и аллергической заболеваемости привитых по группам
составило 6, 6 и 5 человек [7].
Таким образом, на основании анализа результатов исследований
было установлено, что препарат Гриппол® Нео безвреден для вакцинации людей. Не
выявлено сильных поствакцинальных или неожиданных реакций, серьезных
нежелательных явлений. Вакцина рекомендована для проведения клинических
исследований по расширению контингентов с включением детей 3–17 лет.
Безопасность вакцины Гриппол® Нео при вакцинации детей
3–17 лет
В эпидемическом сезоне 2009–2010 гг. в период с октября по
апрель на базе НИИ детских инфекций ФМБА, НИИ гриппа РАМН и ФГУ «Центр гигиены и
эпидемиологии в Свердловской области» проведено рандомизированное, двойное,
слепое, контролируемое сравнительное исследование, включившее 180 детей в
возрасте от 3 до 17 лет.
Для вакцинации детей использовали инактивированную субъединичную
адъювантную вакцину Гриппол® Нео, в одной вакцинирующей дозе (0,5 мл) содержащую
по 5 мкг очищенных протективных антигенов (гемагглютинин и нейраминидаза),
выделенных из вируса гриппа типа А и В, выращенного в культуре клеток МDCK,
связанных с водорастворимым иммуноадъювантом Полиоксидоний®. Исследования
проведены в соответствии с протоколом, утвержденным компетентными регулятивными
органами и согласованным с Комитетом МИБП и ФГУН ГИСК им. Л. А. Тарасевича.
После получения информированного согласия от самих участников или их родителей
дети были рандомизированно распределены в две группы, по 90 человек в каждой:
первую группу вакцинировали Грипполом® плюс, вторую Грипполом® Нео. Вакцинацию
проводили в три этапа. На первом этапе иммунизировали детей старшей возрастной
группы (12–17 лет). После оценки реактогенности вакцины у детей старшего
возраста была проведена иммунизация следующей возрастной группы (7–11 лет),
далее — в аналогичном режиме — вакцинировали детей младшей возрастной группы
(3–6 лет). После введения вакцины привитые в течение 30 минут находились под
наблюдением врача, ответственного за проведение вакцинации, и в течение 5 дней
под амбулаторным наблюдением медицинского персонала.
Оценку реактогенности проводили в поствакцинальном периоде с
нулевого по пятый дни исследования, анализируя жалобы на недомогание, лихорадку
и любые другие симптомы как проявление системных реакций, а также боль в месте
инъекции, появление гиперемии и отека как симптомы местных реакций. Далее
оценивали состояние пациентов в течение трех недель после прививки.
Дополнительно в течение трех месяцев после вакцинации были собраны данные обо
всех случаях инфекционных, соматических и аллергических заболеваний.
Местные вакцинальные реакции расценивали как слабые, если отек и
гиперемия в месте введения вакцины не превышали 25 мм в диаметре, средние при
диаметре 25–50 мм и сильные при диаметре более 50 мм. В качестве местной
вакцинальной реакции регистрировали также болезненность по субъективным
ощущениям слабой степени, средней и выраженную. Из местных реакций у одного
ребенка регистрировали боль в месте инъекции при надавливании.
В табл. 2 представлены данные по количеству местных и общих
реакций у привитых.

При анализе общих реакций всего было зарегистрировано жалоб на
нарушение общего характера в группе привитых вакциной Гриппол® Нео в 4,4% и
Гриппол® плюс в 5,6% случаев соответственно. Регистрируемые общие реакции
включали единичные случаи субъективных жалоб на недомогание, головную боль; все
они отмечены у детей старшего возраста (два ребенка в группе 7–11 лет, один
ребенок в группе 12–17 лет). В младшей группе у одного вакцинированного отмечена
кратковременная температурная реакция (37,2 °C), не повлиявшая на общее
состояние. Все наблюдаемые системные реакции были легкими, не вызывали нарушения
самочувствия и проходили самостоятельно в течение нескольких часов после
вакцинации. Было отмечено, что оба препарата малореактогенны, хорошо переносятся
детьми: местные реакции практически отсутствовали, общие реакции,
зарегистрированные у незначительного числа детей, относятся к нормальным
реакциям слабой степени выраженности.
Таким образом, 94,4% привитых вакцинацию переносили
бессимптомно. Полученные результаты свидетельствуют о высоком профиле
безопасности и хорошей переносимости вакцины [8].
Мониторинг заболеваемости вакцинированных в течение трех месяцев
после прививки выявил по два случая заболевания легкими формами ОРВИ в каждой
группе.
На основании проведенных исследований были внесены изменения в
инструкцию по применению вакцины Гриппол® Нео: вакцина рекомендована для
вакцинации детей с трех лет и взрослых без ограничения возраста.
Иммуногенность вакцины Гриппол® Нео
Оценку иммуногенности проводили у тех же контингентов для двух
дозировок гриппозной субъединичной адъювантной вакцины Гриппол® Нео — по 5 и по
10 мкг гемагглютинина (ГА) каждого из трех рекомендованных штаммов.
Парные сыворотки, взятые до и спустя 21 день после иммунизации,
анализировали в методе реакции торможения гемагглютинации (РТГА) в соответствии
с описанием МУ 3.3.21758–03.
Уровень сероконверсий (процент лиц с четырехкратным увеличением
титра антител после вакцинации) для трех вакцинных штаммов А/H1N1, A/H3N2 и В
варьировал в диапазоне от 77,4% до 92,6%; уровень серопротекций (процент людей с
защитными титрами антител после вакцинации) составил от 93% до 97%, кратность
прироста титров антител — 7,5 до 18,5 соответственно. Результаты оценки
иммуногенности двух доз вакцины Гриппол® Нео у исходно серонегативных взрослых
представлены в табл. 3.
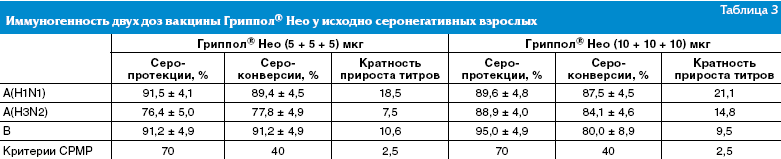
Из таблицы видно, что две дозы вакцины (по 5 и по 10 мкг ГА
каждого из актуальных штаммов) достоверно не отличаются. В качестве конечной
дозировки была выбрана доза (5 + 5 + 5) мкг ГА каждого штамма.
Таким образом, Гриппол® Нео обладает хорошей иммуногенностью и
удовлетворяет всем трем критериям, сформулированным Европейским комитетом для
гриппозных вакцин [9].
Заключение
Неоднократно показано, что сезонная вакцинопрофилактика гриппа
является надежным средством, не только обеспечивающим защиту от гриппа, но и
способствующим повышению резистентности организма к другим вирусным ОРВИ. Именно
результаты независимых исследований, показавшие высокую профилактическую
эффективность иммунизации, стали основанием для включения прививки от гриппа в
Национальный календарь профилактических прививок. А необходимость ежегодной
вакцинации, в свою очередь, стала стимулом для создания ареактогенных вакцин,
обладающих высочайшим профилем безопасности.
При производстве вакцины Гриппол® Нео использованы наиболее
передовые технологии в области создания гриппозных вакцин: втрое сниженное
содержание антигенов, отсутствие в составе вакцины консервантов и антибиотиков,
отсутствие белков куриного яйца, включение безопасного иммуноадъюванта
Полиоксидоний®; атравматическая игла для безболезненной инъекции. Вакцина
Гриппол® Нео позволяет исключить единственное абсолютное противопоказание к
вакцинации против гриппа — аллергию на белок куриного яйца. Хочется отметить,
что в России ситуация с гриппозными вакцинами полностью обеспечивает возможности
для своевременного проведения вакцинации в рамках Национального календаря
профилактических прививок и Национальной программы «Здоровье».
Литература
-
Некрасов А. В., Пучкова Н. Г. Стратегия совершенствования и методы оценки
гриппозных вакцин. Гриппол® плюс — современная защита от гриппа // РМЖ.
2008, № 23 (16): 1–4.
-
Войцеховская Е. М., Вакин В. С., Васильева А. А., Кузнецова Е. В. и др.
Иммуногенность новой гриппозной вакцины // Лечащий Врач. 2009, № 10: 77–79.
-
Локоткина Е. А., Харит С. М., Черняева Т. В., Брусов Н. К. Поствакцинальные
осложнения (клиника, диагностика, лечение, профилактика). Пособие для врача.
Под ред. Ивановой В. В. СПб, 2004, 79 с.
-
Методы определения показателей качества иммунобиологических препаратов для
профилактики и диагностики гриппа: Методические указания МУ
3.3.2.1758–03.2003.
-
Озерецковский Н. А., Федорова А. М. и др. Иммунопрофилактика-2007. Под ред.
Таточенко В. К. М., 2007, 192 с.
-
Отчет «Клинические испытания вакцины гриппозной инактивированной
субъединичной адъювантной Гриппол® ТС (I фаза). НИИ гриппа, С.-Пб, 2007.
-
Некрасов А. В., Пучкова Н. Г., Харит С. М., Черняева Т. В. и др. Вакцина
Гриппол® Нео:Результаты клинических исследований безопасности и
реактогенности (фаза II) // Эпидемиология и вакцинопрофилактика. 2009, № 5
(48): 54–60.
-
Харит С. М., Ерофеева М. К., Никаноров Н. Ю. и др. Безопасность вакцинации
детей в возрасте 3–7 лет субъединичной адъювантной гриппозной вакциной,
содержащей антигены вируса гриппа, выращенного на стерильной культуре клеток
MDCK // Вопросы современной педиатрии. 2010, август, № 4.
-
CPMP/EWP/1045/01. Concept paper on the revision of the CPMP/BWP Note for
Guidance on Harmonization of Requirements for Influenza Vaccines CPMP/BWP/214/96.
Статья опубликована в журнале
Лечащий Врач