Сравнительная характеристика диагностики и лечения
гельминтно-протозойных инвазий у детей на современном этапе
В. А. Александрова, доктор медицинских наук, профессор
В. Е. Одинцева
СПб МАПО, Санкт-Петербург
Паразитарные заболевания и в XXI веке остаются одним из самых
частых видов патологии и представляют собой медико-социальную проблему. К
настоящему времени из 1415 известных возбудителей заболеваний человека 353
возбудителя вызывают протозойные заболевания и гельминтозы. Экспертная оценка
ВОЗ свидетельствует, что более 4,5 млрд человек в мире поражено возбудителями
этой группы болезней [1]. Из них 2 млрд человек инфицированы Ascaris
lumbricoides [2]. Ежегодно в мире аскаридозом заражаются около 650 млн человек,
энтеробиозом — 460 млн [3]. По оценкам специалистов, ежегодно число заболевающих
паразитарными болезнями в России превышает 20 млн человек и имеет тенденцию к
увеличению [4]. По мнению ряда авторов, в последнее время под воздействием
различных факторов происходит изменение картины паразитарных заболеваний,
проявляющееся в неспецифичности проявлений глистно-протозойных инвазий у детей
[5], в бессимптомном течении паразитарных заболеваний [6, 7, 8], в формировании
у паразитов клеточных структур, способных изменять иммунный ответ хозяина на
присутствие в организме паразита [9, 10, 11]. Особенностью большинства
паразитарных болезней является хроническое течение, не сопровождающееся
развитием острых симптомов.
Из числа протозойных инвазий наиболее массовой является лямблиоз.
До сих пор проблемой является разработка эффективных лечебных мероприятий в
отношении хронически рецидивирующего лямблиоза у детей. Устойчивость к
противопаразитарным препаратам может быть обусловлена антигенными различиями
видов лямблий с разной восприимчивостью к разным противопаразитарным препаратам
[12, 13]. Наиболее массовыми гельминтозами в России являются нематодозы,
возбудителями которых служат круглые гельминты: острицы, аскариды и др. [14].
Одной из актуальных задач в борьбе с паразитарными инвазиями на сегодняшний день
является разработка эффективных, безопасных, недорогих методов лечения
гельминтно-протозойной инвазии у детей. Лечение паразитарных инвазий эффективно
при проведении комплексного подхода под контролем исследования кала, т. к. целью
лечения является эрадикация паразита из кишечника [15, 16, 17]. Однако
применение медикаментов широкого спектра действия не обеспечивает полного
излечения при однократном курсе терапии и у ряда больных вызывает побочные
эффекты аллергического, диспепсического и неврологического характера.
Учитывая сложности в диагностике паразитарных инвазий у детей,
актуальной является проблема поиска новых, чувствительных, экономически
эффективных и доступных методов диагностики. Полимеразная цепная реакция [ПЦР]
[18, 19] нашла широкую область применения в паразитологии, ДНК-технологии имеют
большое значение во многих областях паразитологии включая идентификацию и
систематизацию паразитов, анализ генетической структуры, генной организации,
изучение лекарственной устойчивости [20, 21, 22]). Метод ПЦР позволяет прямо
обнаружить инфекционный агент или генетическую мутацию в любой биологической
среде организма (слюна, мокрота, кровь, моча, кал).
Современные взгляды зарубежных и отечественных ученых на
взаимоотношения паразит–хозяин с позиции колебательных и волновых процессов,
присущих всем живым организмам, позволили разработать новый подход к диагностике
различных заболеваний, в том числе и паразитарных. Одним из таких методов
является вегетативный резонансный тест (ВРТ), позволяющий определить наличие
паразитов в организме человека на разных стадиях развития: яйца, личинки,
взрослых особей. Маркерами для диагностики являются резонансные электромагнитные
частоты, характеризующие индивидуальный спектр электромагнитного излучения
паразитов [23, 24]. Метод является гигиеническим, неинвазивным, безболезненным,
что особенно важно для детей. ВРТ официально разрешен и рекомендован к
медицинскому применению Министерством здравоохранения Российской Федерации
(Методические рекомендации № 98/232, 99/96, 2000/74) [25].
Цель нашего исследования — совершенствование диагностики и
лечения паразитозов у детей на современном этапе.
Материалы и методы исследования
В основу работы положены результаты обследования 540 детей в
возрасте от 2 месяцев до 17 лет с различными гастродуоденальными заболеваниями:
хроническим гастродуоденитом (53,5%), функциональным расстройством желудка
(8,2%), дискинезиями желчевыводящих путей (30%). Среди сопутствующих заболеваний
были диагностированы: аномалии желчного пузыря (4,8%), аллергические заболевания
(10%), последствия перинатальной патологии ЦНС (7,7%), хронический иерсиниоз
(1,8%), заболевания ЛОР-органов (1,8%).
Для постановки диагноза использовался тщательный сбор анамнеза,
анализ жалоб, объективный осмотр, проведение необходимых лабораторных и
инструментальных исследований (копроовоскопический метод диагностики,
исследование кала с консервантом Барроуза, ПЦР-диагностика кала,
вегетативно-резонансное тестирование).
Вегетативно-резонансное тестирование проводилось на
аппаратно-программном комплексе (АПК) «Имедис-Фолль». АПК «Имедис-Фолль»
включает следующие взаимосвязанные и взаимодополняющие системы: диагностическая
система (ДС), электронный медикаментозный селектор (ЭМС), система биорезонансной
терапии (БРТ), система мультирезонансной терапии. Показания и противопоказания
для обследования предусмотрены Методическими рекомендациями «Электропунктурный
вегетативный резонансный тест» (Министерство здравоохранения РФ, методические
рекомендации № 99/96).
Результаты исследования и их обсуждение
По возрасту дети были распределены на четыре группы: группа I —
дети от 2 месяцев до 3 лет, группа II — от 3 до 7 лет, группа III — от 7 до 12
лет, группа IV — от 12 до 17 лет. Кроме того, в зависимости от наличия или
отсутствия подтвержденной гельминтно-протозойной инвазии каждая группа была
разделена на две подгруппы: А — без паразитарной инвазии, В — с подтвержденной
паразитарной инвазией.
Среди обследованных детей преобладали жалобы на отрыжку,
тошноту, рвоту, снижение аппетита, боли в животе в околопупочной области,
неустойчивый стул (табл. 1).

Жалобы на отрыжку и тошноту достоверно (р < 0,05) чаще всего
предъявляли дети III возрастной группы (7–12 лет). Жалобы на снижение аппетита,
боли в околопупочной области и бруксизм достоверно (р < 0,05) чаще беспокоили
детей II группы (3–7 лет), а неустойчивый стул достоверно (р < 0,05) чаще
наблюдался у детей от 2 месяцев до 3 лет.
Кроме того, имелись отличия в характере предъявляемых жалоб в
зависимости от наличия или отсутствия паразитарной инвазии. Такой симптом, как
тошнота, достоверно (р < 0,05) чаще встречался у детей от 3 до 7 лет и у детей
от 7 до 12 лет, имеющих гельминтно-протозойную инвазию, по сравнению с детьми
тех же возрастных групп без паразитарной инвазии. Жалобы на снижение аппетита
предъявил 291 ребенок, данный симптом встречался с одинаковой частотой у детей,
имеющих паразитарную инвазию и без нее. Боли в околопупочной области достоверно
(р < 0,05) чаще беспокоили детей третьей возрастной группы (7–12 лет) (41
ребенок (56,16%)), инвазированных паразитами, по сравнению с детьми той же
группы без паразитарной инвазии (табл. 2).

Обследованные дети с подтвержденной паразитарной инвазией имели
три вида моноинвазий (лямблиоз, аскаридоз, энтеробиоз) и четыре вида сочетанной
глистно-протозойной инвазии (лямблиоз/энтеробиоз, лямблиоз/аскаридоз,
аскаридоз/энтеробиоз, лямблиоз/аскаридоз/энтеробиоз). Характеристика жалоб и
объективного осмотра детей в зависимости от вида паразитарной инвазии
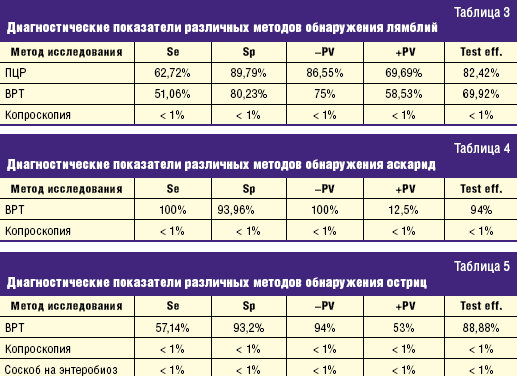
представлена в табл. 3. Как видно из таблицы, лишь головная боль и болезненность
в околопупочной области при объективном осмотре достоверно (р < 0,05) чаще
встречались у детей с сочетанной паразитарной инвазией лямблиоз/аскаридоз/энтеробиоз,
по сравнению с другими видами инвазий. Кроме того, нарушение сна достоверно (р <
0,05) чаще отмечалось у детей с моноинвазией аскаридами, а боли в околопупочной
области достоверно (р < 0,05) чаще встречались у детей с сочетанной гельминтной
инвазией аскаридоз/энтеробиоз, по сравнению с другими видами глистно-протозойной
инвазии. Различия между группами паразитарных инвазий в преобладании тех или
иных диспептических жалоб не достигали уровня значимости.
В нашем исследовании мы изучали диагностическую значимость
различных методов диагностики гельминтно-протозойной инвазии у детей.
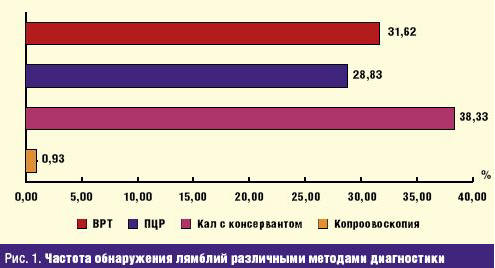
При диагностике лямблиоза при копроовоскопии 540 мазков цисты
лямблий были обнаружены менее чем в 1% случаев. При исследовании кала на цисты
лямблий с консервантом Барроуза лямблиоз диагностирован у 38,33% обследованных
детей. Методом ПЦР кала лямблии были обнаружены у 28,83% обследованных детей.
Методом ВРТ обследованы 136 детей, лямблии обнаружены у 31,62% детей (рис. 1).
Наиболее ценным диагностическим методом при исследовании на
лямблиоз оказался метод исследования кала с консервантом Барроуза, данный метод
был принят нами в качестве стандарта. Диагностические характеристики других
методов диагностики определяли относительно стандарта с помощью четырехпольной
таблицы. Для оценки эффективности диагностических тестов рассчитывали следующие
показатели: чувствительность (Se), специфичность (Sp), точность (test eff.),
прогностическая ценность отрицательного результата теста (–PV), прогностическая
ценность положительного результата теста (+PV).
Как известно, от значений чувствительности и специфичности
зависит прогностическая ценность (посттестовая вероятность) положительного и
отрицательного результатов теста. Чем чувствительнее тест, тем выше
прогностическая ценность его отрицательного результата (т. е. возрастает
уверенность врача в том, что отрицательные результаты теста отвергают наличие
заболевания). Чем специфичнее тест, тем выше прогностическая ценность его
положительного результата (то есть врач может с большей уверенностью считать,
что положительные результаты теста подтверждают предполагаемый диагноз).
Как видно из табл. 3, методы ПЦР и ВРТ обладают хорошими
диагностическими показателями и высокими показателями точности теста (для ПЦР —
82,42%, для ВРТ — 69,92%). Копроскопический метод диагностики характеризовался
чрезвычайно низкими диагностическими показателями (все показатели менее 1%), что
ставит под сомнение целесообразность его использования для диагностики лямблиоза
у детей.
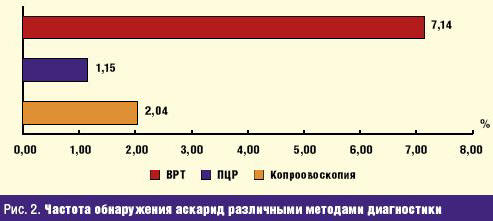
При диагностике аскаридоза мы исследовали кал на яйца глист
микроскопическим методом у 540 детей, аскариды обнаружены в 2,04% исследований.
Методом ПЦР кала обследовано 434 ребенка, аскариды обнаружены у 1,15% детей, а
методом ВРТ обследовано 135 детей, аскариды обнаружены у 7,14% детей (рис. 2).
В качестве стандарта в диагностике аскаридоза в нашем
исследовании использовали ПЦР-диагностику кала.
Как известно, не существует абсолютно чувствительных и абсолютно
специфичных тестов. Стопроцентные показатели получены, вероятно, из-за того, что
в исследовании принимало участие относительно небольшое количество
инфицированных аскаридами пациентов (табл. 4). Вероятно, с этим связаны и низкие
показатели прогностической ценности положительного результата теста (12,5%). Тем
не менее, полученные нами данные позволяют сделать вывод о высокой
информативности ВРТ-диагностики аскаридоза у детей (чувствительность теста —
100%, специфичность — 93,96%). При оценке диагностических показателей
копроскопического метода диагностики все показатели оказались менее 1%, что не
позволяет рекомендовать копроскопический метод для диагностики аскаридоза у
детей.
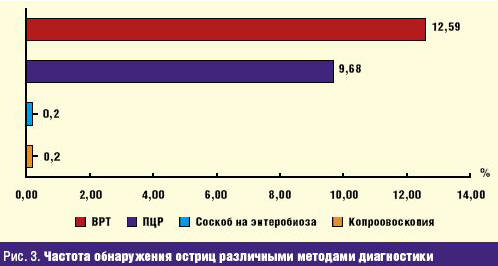
При диагностике энтеробиоза проводились однократные соскобы у
540 детей, острицы диагностированы у 0,2% детей. При исследовании кала на яйца
глист у всех обследованных детей, острицы были обнаружены также у 0,2% детей.
При проведении ПЦР-диагностики кала у 434 пациентов, острицы обнаружены у 9,68%
детей, при вегетативно-резонансном тестировании (обследовано 135 детей) — у
12,59% (рис. 3).
В нашем исследовании стандартом в диагностике энтеробиоза
являлась ПЦР-диагностика кала.
Как видно из табл. 5, копроскопический метод диагностики
энтеробиоза и однократные соскобы на энтеробиоз не имеют диагностической
значимости в диагностике энтеробиоза у детей. Вместе с тем метод ВРТ обладает
высокой специфичностью (93,2%) и точностью теста (88,88%) в диагностике
энтеробиоза.
При лечении лямблиоза процент успешной эрадикации паразита при
использовании метронидазола (20 мг/кг/сут в 3 приема 10 дней) составил 58%,
макмирора (15 мг/кг/сут в 2 приема 10 дней) — 53%, албендазола (200 мг/сут в 2
приема 7 дней) — 50%, фуразолидона (10 мг/кг/сут в 3 приема 10 дней) — 20%.
При лечении хронически рецидивирующего лямблиоза у 143 детей
были назначены биорезонансные препараты (Танаксол с Пара-уолнат-плас или
инверсионный нозод лямблий — предварительно протестированные гомеопатические
препараты) с положительным эффектом. Эрадикация простейших при использовании
Танаксола с Пара-уолнат-плас оказалась успешной в 47,5% случаев. При лечении
хронически рецидивирующего лямблиоза инверсионным нозодом лямблий эффективность
терапии была еще выше и составила 71,95% (различия между эффективностью данных
методов лечения были достоверными (p < 0,01%)).
При лечении аскаридоза — у 4 детей применялся Вермокс (мебендазол)
(для детей от 2 до 10 лет 0,05 г/сут в 3 приема, детям старше 10 лет — 0,1 г в
сутки в 3 приема во время еды. Курс лечения 3 дня), у 1 ребенка — Пирантел (12,5
мг/кг однократно), при лечении энтеробиоза 22 ребенка получали Вермокс, 20 детей
— Пирантел. Данные препараты оказались эффективными у всех детей с нематодозами.
Пациенты с сочетанной паразитарной инвазией получали терапию препаратом Немозол
(альбендазол) в случае сочетанной гельминтно-протозойной инвазии (лямблиоз/аскаридоз,
лямблиоз/энтеробиоз) в дозе 15 мг/кг/сут в 1 прием 10 дней; при сочетанной
инвазии аскаридоз/энтеробиоз Немозол назначался в дозе 400 мг внутрь однократно.
Выводы
-
Для детей с паразитарной инвазией наиболее характерными клиническими
проявлениями являются жалобы на тошноту и боли в околопупочной области.
Головная боль и болезненность в околопупочной области достоверно более
характерны для детей с сочетанной паразитарной инвазией лямблиоз/аскаридоз/энтеробиоз.
Нарушение сна достоверно чаще отмечается у детей с моноинвазией аскаридозом,
а боли в околопупочной области — у детей с сочетанной гельминтной инвазией
аскаридоз/энтеробиоз.
-
Число эозинофилов в периферической крови у обследованных детей во всех
возрастных группах было в пределах нормы и существенно не отличалось у детей
с подтвержденной гельминтно-протозойной инвазией и у детей без паразитарной
инвазии.
-
Метод копроовоскопии без использования консерванта для диагностики лямблиоза
малоинформативен, что не позволяет использовать его в широкой практике.
Наиболее информативными в диагностике лямблиоза оказались метод исследования
кала с консервантом Барроуза и метод ВРТ. При исследовании кала на цисты
лямблий с консервантом Барроуза лямблиоз диагностирован у 38,33%
обследованных детей, методом ВРТ лямблии обнаружены у 31,62% детей.
-
ВРТ является неинвазивным, высокоинформативным, удобным и недорогим методом
диагностики гельминтно-протозойной инвазии у детей. В диагностике
энтеробиоза и аскаридоза метод ВРТ имел высокую диагностическую значимость
наряду с методом ПЦР.
-
Стандартное медикаментозное лечение лямблиоза было эффективным лишь у 20–58%
детей. При лечении хронически рецидивирующего лямблиоза у 143 детей
максимальной эффективностью обладал инверсионный нозод лямблий (71,95%).
-
Лечение аскаридоза и энтеробиоза препаратами Пирантел и Вермокс оказалось
эффективным у всех детей.
Литература
-
Поляков В. Е., Лысенко А. Я. Гельминтозы у детей и подростков. М.: Медицина.
2003. С. 14–29.
-
Savioli L., Gabrielli A. F., Ramsan M. et al. Soil-transmitted helminths and
haemoglobin status among Afghan children in World Food Programme assisted
schools // J. Helminthol. 2005. Vol. 79 (4). P. 381–384.
-
Chan M. S. The global burden of intestinal nematode infections — fifty years
on // Parasitol. Today 1997. Vol. 13 (11). P. 438–443.
-
Онищенко Г. Г. О мерах по усилению профилактики паразитарных болезней в
России // Медицинская паразитология. 2003. № 3. С. 3–7.
-
Озерецовская Н. Н., Зальнова Н. С., Тумольская Н. И. Клиника и лечение
гельминтозов. М.: Медицина.1985. 183 с.
-
Horowicz M., Korman S., Shapiro M. et al. Asymptomatic Giardiasis in
children // Pediatr. Inf. Dis. 1989. Vol. 87. P. 733–779.
-
Morrow A. L., Reves R. R., West M. S. et al. Protection against infection
with Giardia lamblia by breast-feeding in a cohort of Mexican infants // J.
Pediatr. 1992. Vol. 121. P. 363–370.
-
Pickering L. K., Engelkirk P. G. Giardia lamblia // Pediatr. Clin. Nort. Am.
1988. Vol. 35. P. 565–577.
-
Kulakova L., Singer S. M., Conrad J., Nach T. E. Epigenetic mechanisms are
involved in the control of Giardia lamblia antigenic variation // Mol.
Microbiol. 2006. Vol. 61 (6). 1533–1542.
-
Nash T. E. Antigenic variation in Giardia lamblia and the host’s immune
response // Philos. Trans. R. Soc. London Ser. B. 1997. Vol. 352. P.
1369–1375.
-
Sun C. H., McCaffery J. M., Reiner D. S., Gillin F. D. Mining the Giardia
lamblia genome for new cyst wall proteins // J. Biol. Chem. 2003. Vol. 278
(24). P. 21701–21708.
-
Carnaby S., Ketelaris P. H., Neem A., Farthing M. J. G. Genotypic
heterogeneity within Giardia lamblia isolates demonstrated by M13 DNA
fingerprinting // Infect. Immun. 1994. Vol. 62. P. 1875–1880.
-
Majewska A. C., Kasprzak W., De Jonckheere J. F., Kaczmarek E. Heterogeneity
in the sensitivity of stocks and clones of Giardia to metronidazole and
ornidazole // Trans. R. Soc. Trop. Med. Hyg. 1991. Vol. 85. P. 67–69.
-
Тимченко В. Н., Леванович В. В., Абдукаева Н. С., Васильев В. В., Михайлов
И. Б. Паразитарные инвазии в практике детского врача. СПб. ЭЛБИ 2005. С.
60–68.
-
Запруднов А. М. Лекарственные средства в детской гастроэнтерологии. М.:
Медицина, 1997. 164 с.
-
Озерецовская Н. Н. Современные проблемы терапии гельминтозов // Мед.
паразитология. 1975. 33. С. 271–276.
-
Lohiya G. S., Tan-Figueroa L. et al. Epidemiology and control of
enterobiasis in a developmental center // West. J. Med. 2000. Vol. 172 (5).
P. 305–308.
-
Saiki R. K., Scharf S., Faloona F., Mullis K. B. et al. Enzymatic
amplification of beta-globin genomic sequences and restriction site analysis
for diagnosis of sickle cell anemia // Science. 1985. Vol. 230 (4732). P.
1350–1354.
-
Mullis K., Faloona F., Scharf S. et al. Specific enzymatic amplification of
DNA in vitro: the polymerase chain reaction // Cold. Spring. Harb. Symp.
Quant. Biol. 1986. Vol. 51. P. 263–273.
-
Zhu X., Chilton N. B., Jacobs D. E. et al. Characterisation of Ascaris from
human and pig hosts by nuclear ribosomal DNA sequences // Int. J. Parasitol.
1999. Vol. 29 (3). P. 469–478.
-
Gasser R. B., Rossi L., Zhu X. Identification of Nematodirus species (Nematoda:
Molineidae) from wild ruminants in Italy using ribosomal DNA markers // Int.
J. Parasitol. 1999. Vol. 29 (11). P. 1809–1817.
-
Zhang L., Gasser R. B., Zhu X., McManus D. P. Screening for different
genotypes of Echinococcus granulosus within China and Argentina by
single-strand conformation polymorphism (SSCP) analysis // Trans. R. Soc.
Trop. Med. Hyg. 1999. Vol. 93 (3). P. 329–334.
-
Готовский Ю. В., Косарева Л. Б., Фролова Л. А. Резонансно-частотная
диагностика и терапия грибков, вирусов, бактерий, простейших, гельминтов.
Метод. реком. М.: «Имедис», 2000. 70 с.
-
Готовский Ю. В., Перов Ю. Ф. Особенности биологического действия физических
факторов малых и сверхмалых интенсивностей и доз. М.: «Имедис», 2000. 192 с.
-
Электропунктурный вегетативный резонансный тест. Под ред. А. М. Василенко,
Ю. В. Готовскиго, Е. Е. Мейзерова, Н. А. Королевой, В. С. Каторгина. Метод.
реком. № 99/96. М.: МЗ РФ, ИПЦ ТМГФ, 2000. 27 с.
Статья опубликована в журнале
Лечащий Врач