
7.2. ПАТОГЕНЕЗ
Образование тромба в области разрыва или эрозии атеросклеротической бляшки
является решающим событием в общей последовательности формирования ОКС. Процесс
образования тромба претерпевает несколько стадий. Обнажение субэндокардиальных
структур в области атеросклеротической бляшки (коллагена, фактора Виллебранда,
фибронектина, ламинина) способствует усиленной адгезии и агрегации тромбоцитов с
образованием на поверхности поврежденной эрозированной атеросклеротической
бляшки “белого” тромбоцитарного тромба.
Основными факторами, определяющими процесс агрегации кровяных пластинок
являются: тромбоксан А2 (активация метаболизма арахидоновой кислоты в
тромбоцитах); тромбин; АДФ; серотонин; гликопротеиновые Iа, Ib рецепторы
тромбоцитов, обеспечивающие адгезию и первоначальную агрегацию кровяных
пластинок; гликопротеиновые IIb/IIIа рецепторы тромбоцитов, взаимодействие
которых с фибриногеном на заключительном этапе агрегации тромбоцитов приводит к
формированию относительно плотного тромбоцитарного тромба.
Коагуляционный гемостаз обеспечивает плотную закупорку поврежденных сосудов
так называемым “красным” тромбом, состоящим из сети волокон фибрина с
захваченными ею клетками крови (таблица 28).
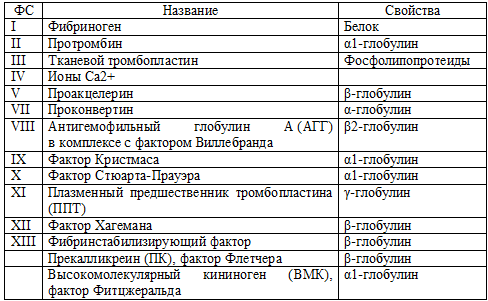
Таблица 28. Факторы свертывания крови (ФС)
Процесс свертывания крови, протекающий с участием специфических факторов
свертывания, разделяют на две основные фазы: 1. Фаза активации -
многоступенчатый этап свертывания, завершающийся активизацией протромбина
(фактор II) с превращением его в активный фермент тромбин (фактор IIа). 2. Фаза
коагуляции - конечный этап свертывания, в результате которого под влиянием
тромбина фибриноген (фактор I) превращается в фибрин.
Центральным звеном сложных химических превращений фаза активации является
образование “активатора протромбина”, который представляет собой ферментный
комплекс, состоящий из активизированных факторов свертывания Ха, Va, ионов Са2+
и фосфолипопротеинов. Источником могут быть: фосфолипопротеины, высвобождающиеся
при повреждении тканей эндотелия сосудов или соединительной ткани (тканевой
тромбопластин - фактор III); фосфолипопротеины мембран тромбоцитов, выходящие в
плазму при их разрушении (тромбоцитарный фактор 3). Формирование ключевого
ферментного комплекса этой фазы - “активатора протромбина” - происходит двумя
путями, в соответствие с которыми различают две системы свертывания.
В течение фазы коагуляции происходит образование фибрина из его
предшественника фибриногена. Процесс этот протекает в два этапа. На первом из
них фибриноген расщепляется тромбином на четыре растворимых мономера фибрина (по
два пептида А и В), у каждого из которых имеется по 4 свободные связи. На втором
этапе мономеры соединяются друг с другом, формируя полимеры, из которых строятся
волокна фибрина. Процесс необратимой полимеризации фибрина происходит с участием
фибриностабилизирующего фактора XIII в присутствии ионов Са2+.
На этой стадии трехмерная сеть волокон фибрина, которая содержит эритроциты,
тромбоциты и другие клетки крови, все еще относительно рыхлая. Свою
окончательную форму она принимает после ретракции сгустка, возникающей при
активном сокращении волокон фибрина и выдавливании сыворотки. Благодаря
ретракции сгустка он становится более плотным и стягивает края раны. Нередко в
клинической практике наблюдаются исключения из этого правила. У 1/4 больных
нетрансмуральным ИМ без зубца Q при ангиографии выявляется полная окклюзия КА, а
перфузия миокарда, относящегося к бассейну окклюзированной КА, осуществляется
через хорошо развитые коллатерали. Пристеночный тромбоз, формирование которого
сопровождается выраженным и длительным спазмом КА, может привести к развитию
трансмурального ИМ с зубцом Q, если коллатеpали не выражены.
|