Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Структурно-функциональное состояние миокарда у
больных артериальной гипертензией,
ассоциированной с гастроэзофагеальной
рефлюксной болезнью
Хлынова О.В., д.м.н., проф. кафедры
госпитальной терапии № 1, ГОУ ВПО Пермская
государственная медицинская академия им. Е.А.
Вагнера Росздрава, г. Пермь
Туев А.В., д.м.н., проф., зав.
кафедрой госпитальной терапии № 1 ГОУ ВПО
Пермская государственная медицинская академия
им. Е.А. Вагнера Росздрава, г. Пермь
Кокаровцева Л.В., к.м.н.,
врач-кардиолог МУЗ ГКБ № 4, г. Пермь
Китаева Е.А., аспирант кафедры
госпитальной терапии № 1 ГОУ ВПО Пермская
государственная медицинская академия им. Е.А.
Вагнера Росздрава, г. Пермь
Резюме
Цель исследования: изучить
структурно-функционального состояния миокарда
у больных артериальной гипертензией (АГ) в
сочетании с гастроэзофагеальной рефлюксной
болезнью (ГЭРБ). Материалы и методы. При
использовании анкетирования, клинических
методов обследования и эхокардиографии
обследовано 120 пациентов, среди которых у 30
человек была диагностирована АГ без
сопутствующей патологии, у 30 – изолировано
протекающая ГЭРБ, а у 60 пациентов –
наблюдалось сочетанное течение АГ и ГЭРБ.
Результаты. Изучены показатели,
характеризующие как состояние центральной
гемодинамики, так и структурно-функциональные
параметры миокарда у лиц с изолированным
течением АГ, ГЭРБ и при их сочетании.
Заключение. В результате сравнительного
анализа выделены особенности ремоделирования
миокарда в зависимости от стадии, степени АГ и
категории сердечно-сосудистого риска. Ключевые
слова: артериальная гипертензия,
гастроэзофагеальная рефлюксная болезнь,
ремоделирование миокарда
Введение
Наряду с такими общеизвестными сочетаниями
заболеваний как ишемическая болезнь сердца
(ИБС) и сахарный диабет, артериальная
гипертензия (АГ) и ИБС, АГ и ожирение,
желчнокаменная болезнь и диафрагмальная грыжа,
эрозивное поражение гастродуоденальной зоны (ГДЗ)
и хронические неспецифические бронхолёгочные
заболевания [1, 2 ,3], всё чаще появляются
указания на кажущиеся более редкими
комбинации, например, язвенная болезнь (ЯБ) и
ИБС, хронический гастродуоденит и дислипидемия,
сахарный диабет, бронхиальная астма и ЯБ [4,
5], и, наконец, кислотозависимые заболевания
ГДЗ и АГ [6]. Последнее сочетание в силу
различий вегетативной регуляции долго
считалось случайным и редко встречающимся.
Возможность коморбидности
гастроэзофагеальной рефлюксной болезни (ГЭРБ)
с заболеваниями сердечнососудистой системы (ССС)
чаще рассматривалась как маска
псевдокоронарного или бронхообструктивного
синдромов, а также как причина пароксизмальных
нарушений ритма сердца [7, 8, 9, 10, 11].
Сосуществование данных патологий многие
исследователи доказали, базируясь на
разъяснении основных патогенетических и
патофизиологических механизмов в их развитии
[8, 11]. Более того, опубликовано достаточное
количество клинических и экспериментальных
работ, посвященных изучению ассоциации ГЭРБ и
ИБС [6, 12, 13]. Однако, вопрос об
особенностях сочетанного течения ГЭРБ и АГ,
как наиболее распространённого заболевания
сердечно-сосудистой системы, остается
неизученным.
У этой категории больных противоречивы и
неоднозначны данные о характере особенности
вегетативной регуляции сосудистого тонуса, нет
единого мнения об особенностях суточного
профиля артериального давления (АД) и
центральной гемодинамики [13, 14]. Практически
неизученными остаются вопросы
структурно-функционального ремоделирования
миокарда при сочетании АГ и ГЭРБ, неизвестны
роль и место АГ и ГЭРБ в его формировании.
Изложенные выше позиции предопределили
актуальность настоящего исследования и
послужили основанием для определения его цели.
Целью данного исследования явилось изучение
структурно-функционального состояния миокарда
у больных АГ в сочетании с ГЭРБ.
Материалы и методы
Для проведения работы был использован
простой открытый параллельный дизайн (одна
группа наблюдения и две группы сравнения). В
исследование были включены 120 больных: 38
мужчин (31,7%) и 82 женщины (68,3%) в возрасте
от 20 до 73 лет (средний возраст 49,63 ± 11,39
лет). Из них у 30 человек была диагностирована
АГ без сопутствующей патологии, у 30 –
изолировано протекающая ГЭРБ. У 60 пациентов –
наблюдалось сочетанное течение АГ и ГЭРБ.
Группы сравнения были сопоставимы по полу,
стажу АГ и ГЭРБ, а также по основным факторам
риска изучаемых заболеваний.
При подборе пациентов определились
следующие критерии включения: возраст пациента
от 18 лет; соответствие диагностическим
критериям каждой нозологической формы:
эссенциальная АГ I или II стадии, степень АГ
1-3, риск 1-4 и/или ГЭРБ; возможность отмены
ранее назначенной терапии на срок до 72 часов.
Обследование проводилось на основе
информированного добровольного согласия
больных.
Критериями исключения из исследования
являлись: несоответствие критериям включения;
симптоматический характер АГ; ИБС; наличие
искусственного водителя ритма сердца;
некоронарогенные формы поражения миокарда;
пороки сердца любой этиологии; хроническая
сердечная недостаточность III и IV
функциональных классов по NYHA; указание на
острое расстройство мозгового кровообращения в
анамнезе; беременность и период лактации;
признаки развития острого или обострения
хронического инфекционного или паразитарного
заболевания; злокачественные новообразования;
патология эндокринных желез, а также наличие
бронхообструктивных заболеваний и
верифицированной патологии системы пищеварения
(за исключением ГЭРБ).
Клиническое обследование больных включало
опрос и осмотр по традиционной схеме с
детализацией жалоб кардиологического и
гастроэнтерологического характера, а также
сведений, указывающих на факторы риска
развития АГ и ГЭРБ.
Диагноз АГ верифицировался при клиническом
обследовании и исключении вторичных форм АГ по
общепринятой схеме (Арабидзе Г.Г. и соавт.,
1999).
Исследование функционального состояния
миокарда, его структурно-геометрических
показателей проводилось при помощи
эхокардиографии (ЭХОКГ) по стандартным
методикам в одномерном, двухмерном и
допплеровском режимах на эхокардиографах ALOKA
4000, Vivid-3 с использованием многоплановых
датчиков (частота ультразвука 2,5 МГц) в
стандартных позициях. В дополнение к
общепринятым показателям рассчитывали:
величину массы миокарда левого желудочка (ММ
ЛЖ) по формуле R.B.Devereux и A.Reichek
(1977); индекс ММ ЛЖ (ИММ ЛЖ) как отношение ММ
ЛЖ / ППТ, где ППТ– площадь поверхности тела,
определяемая по формуле D.Dubois (1975). За
нормальные значения ИММ ЛЖ согласно
рекомендациям Европейского общества по АГ и
Европейского общества кардиологов (2003)
принимались значения менее 125 г/м2 для мужчин
и менее 110 г/м2 для женщин. Также
рассчитывали относительную толщину стенок ЛЖ (ОТС
ЛЖ) в диастолу, за повышение данного
показателя принимались значения 0,45 и более.
На основе показателей ОТС ЛЖ и ИММ ЛЖ
оценивалась геометрическая модель ЛЖ в
соответствии с классификацией A.Ganau et al.
(1992).
Кроме перечисленных параметров, при
проведении ЭХОКГ изучались показатели
центральной гемодинамики (ударный объем (УО,
мл), минутный объем кровообращения (МОК,
л/мин), сердечный индекс (СИ, л/ (мин×м2)),
общее периферическое сосудистое сопротивление
(ОПСС, дин×с/см5). На основании величины СИ
проводилась оценка типов центральной
гемодинамики.
Для верификации диагноза ГЭРБ проводилась
фиброэзофагогастродуоденоскопия («Olympus GIF
F», Япония) с прицельной биопсией слизистой
оболочки пищевода. Согласно Лос-Анжелесской
классификации (1997) выделяли эндоскопически
позитивную (ЭПРБ) и эндоскопически негативную
(ЭНРБ) формы заболевания. Степень тяжести
эзофагита оценивали в соответствии с
классификацией по Savary-Miller (1977) в
модификации Ивашкина В.Т., Трухманова А.С.
(2000). При эндоскопически негативном варианте
ГЭРБ дополнительно проводилась рентгеноскопия
пищевода и желудка с барием в положении
Тренделенбурга и /или 24-х часовая pH-метрия
(аппарат "Гастроскан-ЭКГ", Россия,
"Исток-система").
Степень ожирения оценивалась по значению
показателя ИМТ. Тип ожирения определяли
измерением окружности талии (см) и вычислением
отношения окружности талии (см) к окружности
бедер (см) – ОТ/ОБ.
Статистический анализ материала проведен
при помощи программы STATISTICA 6.0. Для
изучения характера распределения признаков был
применен критерий Жака-Бера. В связи с тем,
что распределение подавляющего большинства
признаков оказалось отличным от нормального,
применялись непараметрические статистические
критерии, а для описания данных использовались
медиана и интерквантильный размах (25-й и 75-й
процентили) в виде Me (25; 75). Для
установления различия между выборками
применялись U-критерий Манна-Уитни и φ*-
угловое преобразование Фишера. Корреляционный
анализ проводился с использованием
коэффициента ранговой корреляции rs Спирмена.
Нулевая гипотеза отвергалась при значении
уровня статистической значимости p < 0,05.
Результаты и их обсуждение
Пациенты с сочетанием АГ и ГЭРБ имели свои
клинико-анамнестические особенности (табл. 1).
Так данную категорию больных представляли
лица, по своим средним значениям, более
старшие (54 лет (47-60)), чем в группах с
изолированным течением заболеваний. Несмотря
на отсутствие различий по стадиям АГ, само
течение гипертонии в группе с данной
ассоциацией отличалось доминированием 2
степени АГ и большим сердечно-сосудистым
риском (p<0,05). Также группа наблюдения, по
сравнению с изолированной АГ,
характеризовалась большей частотой
встречаемости курения и ожирения, несмотря на
отсутствие значимых различий в средней
величине ИМТ. В сравнении с группой
изолированной ГЭРБ у лиц с ассоциацией
заболеваний в 2 раза реже наблюдалось наличие
грыжи пищеводного отверстия диафрагмы (ГПОД),
но при этом в 2,5-3 раза чаще отмечалось
поражение пищевода в виде 1-2 стадии
рефлюкс-эзофагита.
Таблица 1.
Характеристика пациентов, включенных в
исследование
| Показатели |
АГ, N=30
|
ГЭРБ,
N=30 |
АГ+ГЭРК, N=60 |
|
Пол:
Женский |
22 (73,3
%) |
19(63,3%)
|
41 {68,3
%) |
Мужской
|
8 (26,7
%) |
11 (36,7
%) |
19(31,7%)
|
|
Возраст,
годы |
49
(43-54,8) |
46,5
(38,3-55,5) |
54
(47-60) |
|
Стаж АГ,
лет |
2(1-14,3)
|
- |
8(2,8-15)
|
|
Стадии АГ:
I стадия |
15(50%)
|
|
28 (46,7
%) |
II стадия
|
15(50%)
|
|
32 (53,3
%) |
|
Степени АГ:
I степень |
0 |
|
2 (3,33
%) |
2 степень
|
6 (20 %)*
|
|
24 (40
%)* |
3 степень
|
24 (80
%)* |
|
34 (56,7
%)* |
|
Категория
риска: 2 степень |
6 (20 %)*
|
|
22 (36,7
%)* |
3 степень
|
5(16,7%)
|
|
7(11,7%)
|
4 степень
|
19(63,3%)
|
|
31
(51,7%) |
|
Стаж ГЭРБ
|
|
3 (2-4)
|
4 (2-5,8)
|
|
Наличие
грыжи ПОД |
|
11/36,7%&
|
11 (18,3
%)& |
|
Стадии
рефлюкс-эзофагита:
1 стадия
|
|
4 / 13,3%
|
14(23%)
|
2 стадия
|
|
5/16,7%
|
10(16,7%)
|
3 стадия
|
|
6 / 20%
|
5 (8,3 %)
|
4 стадия
|
|
1 / 3,3%
|
1(1,7%)
|
|
Индекс
массы тела, кг/м2 |
27,9(24,6-30,3) |
25,3(21,5-29,4) |
28,7
(26,8-32) |
|
Нормальная
масса тела |
10(33,3%)* |
14/(46,7%)&& |
8(13,3%)*&& |
|
Избыточная
масса тела |
12(40%)
|
10(33,3%)
|
28 (46,7
%) |
|
Ожирение 1
степени |
4(13,3%)*
|
4(13,3
%)& |
21
(35%)*& |
|
Ожирение 2
степени |
4(13,3%)*
|
1 (3,3 %)
|
2 (3,3
%)* |
|
Ожирение 3
степени |
0 |
0 |
1(1,7%)
|
|
Недостаточная масса тела |
0 |
1 (3,3 %)
|
0 |
|
Курящие
пациенты (общее количество в группе)
|
4(13,3%)
|
5(16,7%)
|
11
(18,3%) |
#,& различия статистически значимы, p <
0.05 && различия статистически значимы, p <
0.01
Таблица 2.
Результаты структурно-функционального
состояния миокарда в группах наблюдения и
сравнения
| Показатели |
АГ, N=30
|
ГЭРБ,
N-30 |
АГ+ГЭРБ, N-60 |
|
КДР ЛЖ, мм
|
46 (45; 48)* |
45 (44; 47) |
48 (46; 50)* |
| КДО ЛЖ, мл |
97,3(92,5; 107,5)* |
92,5 (87,7; 102,4) |
107,5(97,3; 118,2)* |
| ПЖ, мм |
20(19; 22)** |
21 (20; 22) |
22 (20; 23)** |
| тзс: лж, мм |
10(10; И)* |
9,5 (9; 10) |
10.5(10; 11)* |
| ТМЖП, мм |
10(10; 11)** |
10(9; 10) |
10,5(10; 11)** |
| ММ ЛЖ, г |
189,6(172,1; 203,9)** |
170,6(145,7; 191,2) |
215,8(191,2;244,6)** |
| ИММ ЛЖ, г/м2 |
109,7(94,9; 118)* |
98,2(83,6; 102,4) |
115,2(101,6; 129,3)* |
| ФВ, % |
59 (55,1; 64) |
59,5 (55,6; 65,7) |
59 (55,6; 65,2) |
* различия статистически значимы, p < 0.05;
** различия статистически значимы, p < 0.01
Примечание: ЛЖ - левый желудочек; КДР ЛЖ -
конечный диастолический размер ЛЖ; КДО ЛЖ -
конечный диастолический объем ЛЖ; ПЖ – правый
желудочек; ТЗС ЛЖ - толщина задней стенки
левого желудочка в диастолу; ТМЖП - толщина
межжелудочковой перегородки в диастолу; ММ ЛЖ
- масса миокарда ЛЖ; ИММ ЛЖ - индекс массы
миокарда ЛЖ; ФВ – фракция выброса.
По данным эхокардиографии для
ассоциированного течения АГ и ГЭРБ были
характерны большие значения объемных
характеристик обоих желудочков, а также
показателей, характеризующих гипертрофию
миокарда ЛЖ (табл.2).
При анализе параметров
структурнофункционального состояния миокарда в
зависимости от стадии АГ, степени АГ и
категории риска сердечнососудистых событий
были выявлены определенные закономерности.
Даже у пациентов I стадии АГ в группе
сочетанной патологии при отсутствии
гипертрофии миокарда ЛЖ как таковой,
значительно чаще выявляется концентрическое
ремоделирование ЛЖ и статистически значимо
более «толстый» миокард ЛЖ. У пациентов же II
стадии группы сочетанной патологии
присоединяется увеличение размеров и правого
желудочка, которое не зависит от степени АГ. У
пациентов подгруппы АГ в сочетании с ГЭРБ и 4
категорией риска сердечно-сосудистых событий
были выявлены более значимые сдвиги
морфо-функциональных параметров миокарда, чем
в целом по группе АГ+ГЭРБ, что заключается не
только в повышении таких параметров как
конечный диастолический размер (КДР) и
конечный диастолический объем (КДО) ЛЖ,
толщина задней стенки (ТЗС) ЛЖ, толщина
межжелудочковой перегородки (ТМЖП), ММ ЛЖ, ИММ
ЛЖ, но и в статистически значимом увеличении
размеров конечного систолического размера (КСР)
и конечного систолического объема (КСО) ЛЖ.
Это свидетельствует о том, что увеличение
данных параметров не зависит от степени АГ и
стадии АГ, а является результатом повышения
суммарного сердечно-сосудистого риска в группе
сочетанной патологии.
Характер ремоделирования ЛЖ в группах был
представлен всеми 4 типами, причем даже при
изолированно протекающей ГЭРБ у 1/3 больных
выявлено концентрическое ремоделирование ЛЖ (КР
ЛЖ), а в группе сочетанной патологии несколько
чаще регистрировалась эксцентрическая
гипертрофия ЛЖ (ЭГ ЛЖ) (рис. 1).

Рис. 1. Типы ремоделирования миокарда
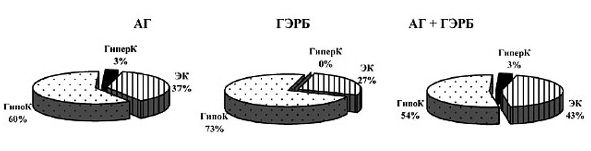
Рис. 2. Частота встречаемости различных
типов гемодинамики в группах
Анализ параметров центральной гемодинамики
показал значимое увеличение УО 63,1мл (56,4;
72,7) при со-четанной патологии против 59,1 мл
(53,2; 63,8) (p<0,05) при АГ и ОПСС в группе
изолированно протекающей АГ: 1876 дин×с/см5
(1723; 2188) (p<0,05) против 1683 дин×с/см5
(1446; 1962) (p<0,05) при сочетанной
патологии. При этом значения МОК и СИ в этих
группах существенно не отличались. Во всех
изучаемых группах преобладали пациенты с
гипокинетическим типом гемодинамики (рис.2).
Выводы
1. При ассоциированном течении АГ и ГЭРБ
имеют место особенности
структурно-функционального ре-моделирования
сердца в сравнении с изолированной АГ.
Так, у пациентов с данной синтропией
регистрируется статистически значимая большая
степень гипертрофии миокарда ЛЖ, вне
зависимости от стадии АГ и степени повышения
уровня АД, но являющаяся отражением
повышенного суммарного сердечно-сосудистого
риска. Более того, особенностью является
примерно равная выяв-ляемость всех типов
ремоделирования сердца.
2. По состоянию центральной гемодинамики
пациенты с сочетанной патологией не имеют
статистически значимых отличий от категории
лиц с изолированными АГ и ГЭРБ. Однако была
выявлена тенденция к преимущественному
формированию гипокинетического типа
гемоциркуляции (54%), частота которого
увеличивается в зависимости от стадии АГ и
степени сердечнососудистого риска.
Литература:
1. Гриневич В.Б., Мелкумов С.П., Успенский
Ю.П. Факторы осложнения язвенной болезни
перфорацией Рос журн гастроэнтерол., гепатол.,
колопроктол. — 1995.— №3. — С. 69.
2. Зонис Б.Я., Волкова Н.И., Соколов О.Ю.
Влияние эднита на активность ренин -
ангиогензин - альдостероновой системы и
функцию почек у больных артериальными
гипертониями в сочетании с сахарным диабетом.
Терапевтический архив.— 2000.— Т. 72, №2.— С.
53-55.
3. Кобалава Ж.Д. Артериальная гипертония и
ожирение: случайная ассоциация или
причинно-следственная связь? Клиническая
фармакология и терапия — 2000. — Т. 9, №3 . —
С. 35-38.
4. Ивкова И.А. Диагностика и лечение
язвенной болезни желудка, сочетанной с другими
заболеваниями: автореф. дис.... канд. мед.
наук. — Иваново.— 2001.— С. 24
5. Крылов А.А. Язвенная болезнь в сочетании
с другой патологией. Клинические проявления,
течение, терапия. Терапевтический архив. —
1992.— №2.— С. 121-124
6. Кузьмина А.Ю.Состояние
сердечно-сосудистой системы при патологии
верхнего отдела желудочно-кишечного тракта.
Лечащий врач—2004. — № 4.— C. 108-112.
7. Арутюнов А.Г., Бурков С.Г., Щерба Е.Л.
Механизмы взаимосвязи гастроэзофагеальной
рефлюксной болезни и бронхиальной астмы и
тактика ведения больных. Клинические
перспективы гастроэнтерологии, гепатологии -
2004. — №2. — С. 5-9.
8. Бурков С.Г., Алексеева E.П., Юренев Г.Л.
Гастроэзофагеальная рефлюксная болезнь и
бронхиальная астма. Атмосфера. Пульмонология и
аллергология — 2005. — №4 . — С. 30-33.
9. Славкина Е.А. Клинико-диапгостическое
значение гастроэзофагеального рефлюкса и
струкутрных изменений пищевода и желудка при
бронхиальной астме: автореф. Дисс. канд. мед.
наук— Саратов, 2004.— 27с
10. Bradley L.A., Richter J.E., Puffiam
T.J. et al. The relationship between stress
and symptoms of gastroesophageal reflux: the
influence of physiological factors. Am J.
Gastroenterol — 1993. — Vol 88. P. 11—19.
11. Vaezi M.T. Atypical Manifestations of
Gastroesophageal Reflux Disease. Medscape
General Medicine— 2005.— Vol 7, № 4, P. 25.
12. Haffner P. A, Valdez R. A et al
Prospective analysis of the insulin-resistance
syndrome (Syndrome X). Diabetes — 1992. Vol
41. — P. 715—722.
13. Mathus-Vliegen E.М., Tygat G.N.
Gastro-oesophageal reflux in obese subjects:
influence of overweight, weight loss and
chronic gastric balloon distension Scand J.
Gastroenterol — 2002. — Vol. 37, № 11. — P.
1246-1252.
14 Locke G.R., Talley N.J., Fett S.T. et al
Risk factors associated with symptoms of
gastroesophageal reflux Am. J.Med— 1999. —
Vol.106. — P. 642-649.
Статья опубликована на сайте
http://www.gastroscan.ru

