Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Значение Th17-пути дифференцировки лимфоцитов в патогенезе
ювенильного идиопатического артрита
И. З. Турцевич*
Г. А. Новик*, доктор медицинских наук, профессор
Н. М. Калинина**, доктор медицинских наук, профессор
Н. В. Бычкова**, кандидат биологических наук
Н. И. Давыдова**, кандидат биологических наук
* ГБОУ ВПО СПбГМПУ МЗ РФ, Санкт-Петербург
** ФГБУ ВЦЭРМ им. А. М. Никифорова МЧС России, Москва
Одним из наиболее частых и самых инвалидизирующих ревматических заболеваний,
встречающихся в детском возрасте, является ювенильный идиопатический артрит (ЮИА),
в структуру которого входят все формы артрита, которые начинаются до возраста 16
лет, длительностью 6 недель и более, при исключении другой патологии суставов
[1–3].
ЮИА является по своей природе аутоиммунным заболеванием, патогенез которого
глубоко уходит своими корнями в нарушение регуляции механизмов, посредством
которых Т-клетки способны различать «свое» от «чужеродного» [1, 4–6]. Антигенная
стимуляция наивных Т-клеток в присутствии специфических цитокинов, продуцируемых
клетками первичной иммунной системы, индуцируют активацию, экспансию и
дифференцировку в различные эффекторные Т-клетки [7–10].
Ранее считалось, что в патогенезе большинства аутоиммунных заболеваний, таких
как ревматоидный артрит, рассеянный склероз, сахарный диабет 1-го типа, а также
воспалительные заболевания кишечника, играют Th1-клетки и их цитокиновый
профиль, так как интерферон гамма (ИФН-γ) и ИЛ-12 обнаруживались в высоких
концентрациях в местах воспаления. При этом введение моноклональных антител к
ИФН-γ и ИЛ-12 приводило лишь к усугублению течения заболевания, что навело
исследователей на мысль, что существует, по крайней мере, еще один тип клеток,
который способен индуцировать и поддерживать развитие аутоиммунных заболеваний
[8, 11].
Открытие Th17-клеток в 2005 г. Harrington, Langrish, Park и соавт. расширило
знание о патогенезе многих воспалительных и инфекционных заболеваний. На
протяжении нескольких лет после их открытия не было единого мнения относительно
дифференцировки этих клеток. Результаты изучения функционального значения
Th17-клеток у мышей и человека выявили существенные различия. Если у мышей для
процесса дифференцировки Th17-клеток требуются ИЛ-6 и трансформирующий фактор
роста β (TGFβ), то у человека — ИЛ-6 и ИЛ-1β, без необходимости воздействия на
этот процесс TGFβ. Acosta-Rodrigues и соавт. (2007), исследовав процесс
дифференцировки Th17-клеток в образцах крови человека in vitro,
выявили, что активированные моноциты и циркулирующие дендритные клетки,
продуцирующие большое количество ИЛ-1β и ИЛ-6, достаточны для дифференцировки
Th17-клеток. При добавлении антител, нейтрализующих эти цитокины,
дифференцировка Th17-клеток блокировалась. Также была исследована функция TGFβ в
дифференцировке Th-клеток. Было обнаружено, что TGFβ блокировал дифференцировку
трех основных линий эффекторных Тh-клеток (Th1, Th2 и Th17) у человека, в
отличие от мышиной модели [12, 13].
В последнее время проводится большое количество исследований, посвященных
изучению роли семейства цитокинов ИЛ-17, а именно ИЛ-17A, который впервые был
идентифицирован в 1993 г. P. Rouvier и соавт., задолго до открытия
непосредственно Th17-клеток, и первоначально назывался CTLA-8 (cytotoxic T
lymphocyte associated antigen 8). ИЛ-17А продуцируется преимущественно
активированными CD4+ Т-клетками памяти и γδ-Т-лимфоцитами. Семейство
цитокинов ИЛ-17 включает в себя 6 членов — ИЛ-17А, ИЛ-17В, ИЛ-17С, ИЛ-17D,
ИЛ-17Е (или ИЛ-25) и ИЛ-17F. При этом ИЛ-17А высокогомологичен с ИЛ-17F и
является наиболее изученным цитокином этого семейства. Различные члены семейства
ИЛ-17, вероятно, играют разнообразную биологическую роль, однако Th17-клетки
продуцируют лишь 2 представителя этого семейства — ИЛ-17А и ИЛ-17F. Все члены
семейства цитокина ИЛ-17 имеют одинаковую структуру белка со значительными
расхождениями последовательности на N-концах. ИЛ-17А является гомодимерным
гликопротеином, состоящим из 155 аминокислот, и на 55% гомологичен ИЛ-17F, ген,
кодирующий ИЛ-17А, локализован на хромосоме 2q31 [14–16].
P. Rouvier и соавт. (1993), исследовав ИЛ-17А, обнаружили, что основной его
функцией является активация и усиление дифференцировки нейтрофилов (гранулопоэз)
из клеток-предшественников в костном мозге человека. Гиперэкспрессия ИЛ-17А
приводит к массивной нейтрофилии в периферической крови и повышению
предшественников нейтрофилов в селезенке. Эта функция ИЛ-17А зависит от
достаточной экспрессии гранулоцитарного колониестимулирующего фактора (G-CSF) и
трансмембранной формы SCF (stem cell factor). Гранулопоэтический ответ является
важным в контроле иммунной защиты против внеклеточных патогенов, включая
бактерии и грибы [14–19].
Новые данные подтвердили ранее полученные результаты относительно ИЛ-17А как
о цитокине, продуцируемом Т-клетками. После многочисленных экспериментов стало
очевидно, что Th17-клетки и их цитокины ассоциированы с различными аутоиммунными
и воспалительными заболеваниями, такими как ревматоидный артрит, ЮИА, системная
красная волчанка, рассеянный склероз, псориаз, воспалительные заболевания
кишечника, аллергия (гиперчувствительность замедленного типа — контактный
дерматит) и неатопическая астма [19, 20].
ИЛ-17А охарактеризован как цитокин-индуцирующий цитокин, проявляя свои
провоспалительные и гемопоэтические функции за счет способности к стимуляции и
высвобождению вторичных цитокинов и хемокинов, оказывая свои биологические
свойства на различных типах клеток. К тому же ИЛ-17А и ИЛ-17F могут
секретироваться как в виде гомодимера, так и в виде гетеродимера. ИЛ-17А/F-гетеродимер
биологически более эффективен, чем ИЛ-17F, но менее эффективен в индукции
хемокинов, по сравнению с гомодимером ИЛ-17А [14, 16, 18, 21].
ИЛ-17A в значительных количествах присутствует в воспаленном синовиуме и в
небольших количествах в периферической крови пациентов с РА. K. Nistala и соавт.
(2008) обнаружили высокий уровень Th17-клеток и ИЛ-17А в суставах детей с ЮИА, в
частности, при прогрессирующем олигоартикулярном варианте заболевания. При этом
Тh17-клетки были равномерно распределены в популяции Т-хелперов (CD4+)
и Т-клеток-памяти (CD45+RO) [22].
ИЛ-17А индуцирует экспрессию RANKL (Receptor activator of nuclear factor
kappa-B ligand — мембранный белок, цитокин) синовиальными фибробластами и
остеобластами, приводя к секреции остеокластогенных факторов, таких как ФНО-α и
ИЛ-1 β. Эта Th17-опосредованная индукция остеокластогенеза может представлять
важный клеточный механизм в патогенезе костно-хрящевой деструкции при
аутоиммунном артрите [23, 24].
Несмотря на значительный прогресс в лечении ЮИА генно-инженерными
биологическими препаратами (ГИБП), в частности антагонистами ФНО-α, ИЛ-1β или
ИЛ-6, до 30% пациентов не достигают клинико-медикаментозной ремиссии. Вероятно,
в патогенезе заболевания этих пациентов превалирующую роль играют Th17-клетки и
их ключевые цитокины ИЛ-17А и ИЛ-17F. Испытания моноклональных антител к ИЛ-17А/F
при таких аутоиммунных заболеваниях, как псориаз, ревматоидный артрит, болезнь
Бехтерева, показывают многообещающие результаты, основными из которых являются
полное блокирование симптомов и стойкая ремиссия. Основываясь на этих данных,
вероятно, следующим шагом станет введение этих препаратов в реестр по лечению
больных ЮИА [15, 25, 26].
Два моноклональных антитела, напрямую захватывающие и нейтрализующие ИЛ-17А,
протестированы в клинических испытаниях на человеке: Secukinumab (AIN457) —
полностью человеческое моноклональное антитело, и Ixekizumab (LY2439821) —
гуманизированное моноклональное антитело. Другие препараты, специфические для
ИЛ-17А, находятся в ранних клинических испытаниях, такие как SCH-900117 и RG4934
[15, 27–29].
Роль Th17-клеток и ИЛ-17А в развитии ЮИА не до конца изучена. Так, остается
неясным влияние Th17-клеток на течение и исход заболевания у детей при различных
вариантах течения ЮИА. Также остается непонятным, способны ли современные ГИБП,
применяемые у детей, ингибировать дифференцировку Th17-клеток из наивных
Тh-клеток.
Таким образом, исследование Th17-пути и его влияние на течение заболевания в
группе детей с ЮИА представляется наиболее перспективным исследованием, носит
практический интерес, связанный с тактикой ведения и лечения детей с ЮИА.
Целью данного исследования было установить особенности Th17-пути
дифференцировки лимфоцитов у детей с различными вариантами ЮИА как механизма,
определяющего характер клинического течения и исхода заболевания.
Материалы и методы исследования
Количественное определение лимфоцитов и их субпопуляций в условиях in
vitro осуществлялось методом непрямой иммунофлюоресценции с помощью
проточной цитометрии с использованием моноклональных антител к их поверхностным
антигенам (СD). Таким образом, всем пациентам с ЮИА и группе сравнения было
проведено иммунологическое исследование, включавшее определение общего
количества CD4+ (мономерный трансмембранный гликопротеин,
экспрессирующийся на Т-хелперах) клеток, определение дифференцировочного
антигена CD45 с изоформами RА, которая является маркером наивных Тh-клеток (CD4+CD45+RO-RA+),
и RO, которая экспрессируется на Тh-клетках памяти (CD4+CD45+RO+RA-),
и «переходную» форму Тh-клеток, несущую обе изоформы — дубль-позитивные
Тh-клетки (CD4+CD45+RO+RA+). Для
определения уровня Th17-клеток был измерен мембранный хемокиновый рецептор CCR6
(CD196), который является маркером этих клеток и характеризует их
субпопуляционный состав — наивных Th17-клеток (CCR6+RA) и Th17-клеток
памяти (CCR6+RO).
Забор венозной крови осуществлялся из локтевой вены в объеме 3 мл в
стерильные пробирки, содержащие антикоагулянт К2ЭДТА (Vacuette, Germany).
Образцы крови хранились при комнатной температуре в течение не более 2 часов до
начала исследования. В 500 мкл крови добавляли поочередно моноклональные
антитела к поверхностным антигенам CD4+ клеток CD4-PC5, наивных
Тh-клеток CD45RА-FITC, Тh-клеток памяти CD45RO-ECD (все реактивы Beckman coulter,
Immunotech, Франция) и моноклональные антитела к мембранному хемокиновому
рецептору CCR6, специфического для Th17-клеток (PE conjugated anti-human CD196,
Clon: R6H1, eBioscience, San Diego, CA, USA), создавая, таким образом, 4-цветную
метку. В дальнейшем образцы были смешаны на шейкере в течение 1–2 секунд и
инкубировались при комнатной температуре 10 минут. После чего добавляли 1 мл
лизирующего раствора Versalyse (Beckman coulter, Франция) для лизирования
эритроцитов с последующим перемешиванием на шейкере в течение 1–2 секунд и
инкубацией при комнатной температуре (18–25 °C) в течение 30 минут. Далее
окрашенный материал подвергался исследованию на проточном цитометре (Beckman
coulter NAVIOS). Все реагенты были использованы согласно инструкции
фирмы-производителя. Результаты выражали в процентах.
Количественное определение цитокинов ИЛ-1β, ИЛ-6, ИЛ-17 и ФНО-α
Количественное определение цитокинов ИЛ-1β, ИЛ-6, ИЛ-17 и ФНО-α в сыворотке
крови больных ЮИА и группы сравнения определяли с помощью иммуноферментного
анализа (ИФА-ELISA) с применением набора реагентов для ИЛ-1 β, ИЛ-6 и ФНО-α
фирмы ЗАО «Вектор-Бест» (г. Новосибирск), для ИЛ-17A — eBioscience (San Diego,
CA, США).
Всем пациентам было проведено рентгенологическое и ультразвуковое
исследование костно-суставной системы. Части пациентам проведена ультразвуковая
денситометрия. Преимуществом данного исследования является полное отсутствие
лучевой нагрузки на пациента, в отличие от рентгеновской денситометрии.
Результаты интерпретировались согласно общепринятым значениям Т (или Z) индекса:
от 0 до –1,5 — нормальная плотность костной ткани: от –1,5 до –2,5 — остеопения;
ниже –2,5 — остеопороз.
Статистическая обработка результатов исследования
Статистическая обработка результатов исследования осуществлялась с
использованием пакетов SPSS IBM версия 21.0 и Statistica 10. Для сравнения
выборок данных использовался анализ таблиц сопряженности, где оценивались
критерий Пирсона Хи-квадрат (χ) для анализа номинальных переменных, заданных
таблицами сопряженных признаков типа N × M. Двусторонний критерий Фишера
использовался для таблиц 2 × 2. Непараметрический U-критерий Манна–Уитни (Mann–Whitney
U Test) использовался для сравнения медиан двух выборок, если распределение хотя
бы одной из них существенно отличалось от нормального. Зависимость средних
значений Th-популяций и их субпопуляций, наивных Th17-клеток (CCR6+RA+),
Th17-клеток памяти (CCR6+RO+), а также ИЛ-1β, ИЛ-6, ИЛ-17
и ФНО-α от порядковых значений определялась с помощью построения трех порядковых
регрессий с определением значения χ2. Для анализа факторов риска
персистирования симптомов ЮИА применялась логистическая регрессия с построением
дерева решений и ROC-кривой.
Результаты исследования
В исследование было включено 108 детей с различными вариантами ЮИА в возрасте
от 2 до 18 лет (средний возраст 10,5 ± 3,8 года), которые полностью
соответствовали критериям ILAR (International League of Associations for
Rheumatology)(Durban, Edmonton, 2001, second revision 2004). В зависимости от
варианта течения все дети были разделены на 4 группы: дети с олигоартритом — 32
пациента (29,6%); дети с полиартритом, серонегативным по ревматоидному фактору
(РФ) — 30 пациентов (27,8%); группа с энтезитассоциированным артритом (ЭАС) — 33
ребенка (30,6%) с HLA-B27+ ювенильным анкилозирующим спондилоартритом (ЮАС);
группа с системным вариантом течения ЮИА составила 13 детей (12%).
В зависимости от эффективности проводимой терапии дети были разделены на две
подгруппы: дети с «активной» болезнью и дети с «неактивной» болезнью. «Активная»
болезнь определялась как наличие одного или более суставов с признаками
воспаления, болезненности и ограничения функций на фоне проводимого лечения.
«Неактивная» болезнь определялась как отсутствие всех клинико-лабораторных
признаков суставного воспаления и увеита в течение минимум 1 года на фоне
базисной терапии, совпадающих с нулевой активностью визуально-аналоговой шкалы
(ВАШ) (рис. 1).
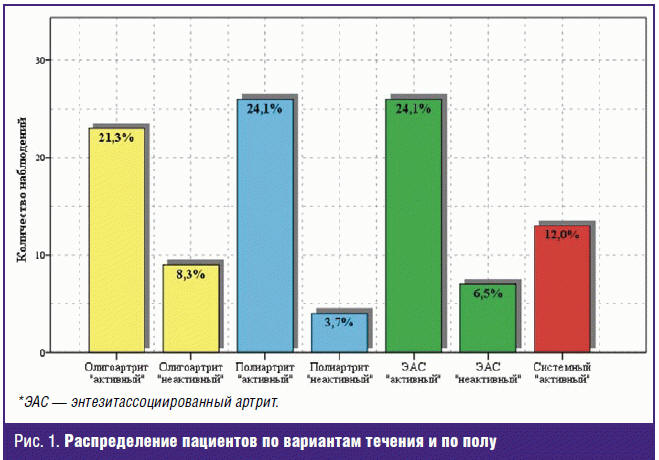
Группу сравнения составили 18 условно-здоровых детей с неотягощенной
наследственностью по аутоиммунным заболеваниям.
Для оценки активности заболевания и эффективности терапии применялись шкалы
ACRpedi и JADAS71 CRP, специально разработанные для использования в
педиатрической ревматологической практике.
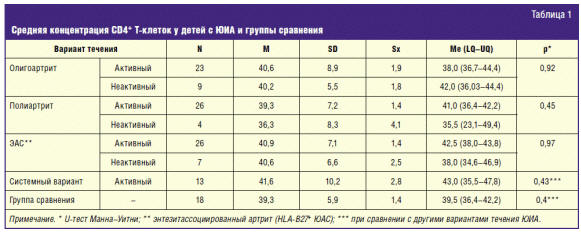
Сравнительная оценка общей популяции CD4+ Т-клеток не выявила
различий между пациентами с ЮИА и группой сравнения (р = 0,4), уровень этих
клеток был в пределах допустимых значений. В группе детей с «активной» и
«неактивной» болезнью статистически значимых различий уровня общей популяции CD4+
Т-клеток не выявлено (р > 0,05) (табл. 1).
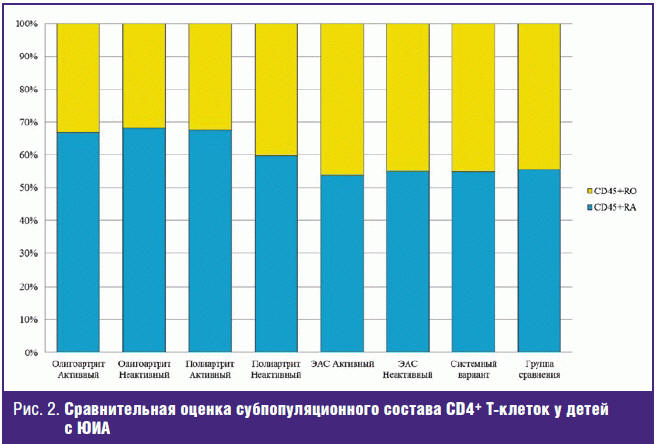
Наиболее высокий уровень наивных Тh-клеток (CD45+RA) и наиболее
низкий уровень Тh-клеток памяти (CD45+RO) наблюдался у детей с олиго-
и полиартритом (р = 0,022, р = 0,005 соответственно) как в «активной», так и
«неактивной» болезни. При энтезитассоциированном и системном варианте ЮИА
статистически значимых различий выявлено не было (р > 0,05) (рис. 2).
Уровень дубль-позитивных Тh-клеток (CD45+RO+RA+)
в периферической крови не отличался у детей с различными вариантами течения ЮИА
как при «активной», так и «неактивной» болезни (р > 0,05).
Сравнительная оценка уровня маркера Th17-клеток на наивных Тh-клетках (CCR6+RA)
не выявила статистически значимых отличий между детьми с ЮИА и группой сравнения
(р > 0,05).
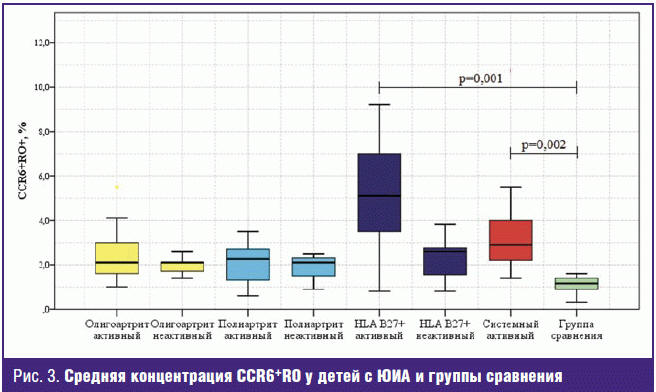
Статистически значимые отличия отмечались в уровне Th17-клеток памяти (CCR6+RO)
при всех вариантах течения ЮИА в сопоставлении с группой сравнения (р = 0,001).
Наиболее высокий уровень этих клеток в периферической крови был обнаружен у
детей с «активным» HLA-B27-ассоциированным артритом (р = 0,001) и системным
вариантом артрита (р = 0,002) (рис. 3).
Статистически значимых гендерных различий в уровне Th17-клеток памяти у детей
с различными вариантами ЮИА не было выявлено (р > 0,05).
ИЛ-1β, ИЛ-6, ИЛ-17А и ФНО-α были измерены в сыворотке крови у 90 пациентов
основной группы и 15 детей группы сравнения.
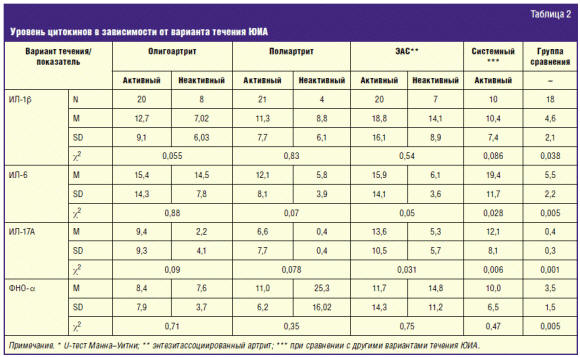
Уровень ИЛ-1β в сыворотке крови у детей с ЮИА как в «активной», так и
«неактивной» болезни статистически достоверно был выше, чем в группе сравнения (р
= 0,038). Особенно высокий уровень ИЛ-1β отмечался у больных с активным
HLA-B27-ассциированным артритом (р = 0,007). Статистически значимых различий
уровня ИЛ-1β между «активным» и «неактивным» артритом при всех вариантах течения
ЮИА не отмечалось (р > 0,05) (табл. 2).
При оценке гендерных различий была выявлена статистическая достоверность в
группе с «активным» энтезитассоциированным артритом. Так, уровень ИЛ-1β в
сыворотке крови у мальчиков с «активным» энтезит-ассоциированным артритом
значительно превышал уровень данного цитокина у девочек (22,9 ± 8,4 пг/мл и 11,4
± 6,9 пг/мл соответственно, при р < 0,05).
Уровень ИЛ-6 в сыворотке крови у детей с ЮИА был статистически достоверно
выше, чем в группе сравнения (р = 0,005). Наиболее высокий уровень ИЛ-6
отмечался у пациентов с системным вариантом артрита (р = 0,028) и в группе детей
с энтезитассоциированным артритом (р = 0,048) табл. 2).
Сравнительная оценка уровня ИЛ-17А в сыворотке крови выявила статистически
значимые различия между детьми с ЮИА и группой сравнения (р = 0,001). Наиболее
высокий уровень ИЛ-17А отмечался у детей с «активным» энтезитассоциированным
артритом (р = 0,001) и системным вариантом течения ЮИА (р = 0,006) (табл. 2).
Уровень ФНОα в сыворотке крови был достоверное выше у детей с ЮИА, при
сопоставлении с группой сравнения (р = 0,005). Статистически значимых
межгрупповых и внутригрупповых различий у детей с ЮИА обнаружено не было (р >
0,05) (табл. 2).
Сравнительная оценка общего количества CD4+ Т-клеток и их
субпопуляций в периферической крови выявила положительную корреляцию между общей
популяцией Т-хелперов с наивными Тh-клетками (CD45+RA) (коэффициент
Пирсона = 0,32, р = 0,008) и отрицательную корреляцию с Тh-клетками памяти (CD45+RO)
(коэффициент Пирсона = –0,25, р = 0,026). Уровень CD45+RO негативно
коррелировал с уровнем CD45+RA (коэффициент Пирсона = –0,85, p =
0,001), а уровень CD45+RA отрицательно коррелировал с
дубль-позитивными Тh-клетками (CD45+RO+RA+)
(коэффициент Пирсона = –0,517, р = 0,001).
С помощью метода линейной корреляции и построением уравнения множественной
регрессии была оценена степень влияния Th17-клеток и исследуемых
провоспалительных цитокинов на основные клинико-лабораторные показатели, где р <
0,05 считался статистически достоверным.
Как у мальчиков, так и у девочек выявлена положительная корреляция
Th17-клеток памяти (CCR6+RO) с общим уровнем Th-клеток памяти (R2 =
0,178, p = 0,03), отрицательная корреляция с наивными Th-клетками (R2 = 0,285, p
= 0,0001). При дальнейшей оценке была выявлена сильная положительная корреляция
ИЛ-1β с ИЛ-6 (R2 = 0,324, р = 0,001) и ИЛ-1β с ФНОα (R2 = 0,229, р = 0,001).
Оценка показателей относительного риска «активного» артрита и
клинико-медикаментозной ремиссии у детей с ЮИА в зависимости от уровня
Th17-клеток и основных цитокинов в периферической крови показала, что
совокупность лишь 2 исследуемых факторов имеет достоверное диагностическое
значение. Таким образом, было обнаружено, что при значении ИЛ-17А в сыворотке
крови выше 1,04 пг/мл риск рецидива заболевания повышается на 91,5% (OR = 2,755,
95% ДИ = 0,884–8,588, р = 0,04), в сочетании с повышением CCR6+RО в
периферической крови выше 3,2% риск повышается на 95,2% (OR = 3,030, 95% ДИ =
0,867–10,590, р = 0,003).
При оценке влияния исследуемых параметров на рентгенологические показатели
было обнаружено, что совокупность уровня ИЛ-17А выше 1,04 пг/мл и ИЛ-6 выше 10,1
пг/мл в сыворотке крови повышает риск развития остеопороза до 77,5% (OR = 2,902,
95% ДИ = 0,584–14,421, р = 0,008), а при значении ИЛ-6 в сыворотке крови менее
10,1 пг/мл риск развития остеопороза резко понижается — 27,5% (OR = 0,394, 95%
ДИ = 0,097–1,598, р = 0,037).
Заключение
Проведенный анализ позволяет использовать определение уровня Th17-клеток в
периферической крови и ИЛ-17А в сыворотке крови детей с ЮИА в качестве маркеров
высокого риска развития перехода из «неактивной» болезни в «активную».
Определение уровня ИЛ-6 и ИЛ-17А в сыворотке крови позволяет выявить группу
больных с ЮИА с высоким риском развития костно-суставной деструкции и
неблагоприятным вариантом течения заболевания.
Литература
- Алексеева Е. И. Ювенильный артрит: возможности медикаментозного и
немедикаментозного лечения на современном этапе // Лечащий Врач. 2011. № 8. С.
84–89.
- Баранов А. А., Алексеева Е. И. Детская ревматология. Атлас. М.:
Союз педиатров России, 2009. 248 с.
- Новик Г. А., Аббакумова Л. Н., Летенкова Н. М., Слизовский Н. В.,
Слизовская Н. Н. Ювенильные артриты — опыт диагностики и лечения //
Лечащий Врач. 2008. № 4. С. 23–27.
- Cassidy J., Petty R. et al. Textbook of pediatric rheumatology, 6
th Revised edition. Elsevier — Health Sciences Division, 2010. 800 c.
- Prelog M., Schwarzenbrunner N., Sailer-Hock M., Kern H., Klein-Franke
A., Ausserlechner M. J., Koppelstaetter C. et. al. Premature aging of the
immune system in children with juvenile idiopathic arthritis // Arthritis and
Rheumatism. 2008. Vol. 58. P. 2153–2162.
- Smith H. S., Smith A. R., Seidner P. Painful Rheumatoid Arthritis
// Pain Physician. 2011. Vol. 14. № 5. P. E427-E458.
- Калинина Н. М., Кетлинский С. А., Оковитый С. В. Заболевания
иммунной системы. Диагностика и фармакотерапия. М.: Эксмо, 2008. 496 с.
- Кетлинский С. А. Th17 — новая линия дифференцировки Т-хелперов:
обзор данных // Цитокины и воспаление. 2009. Т. 8. № 2. С. 24–39.
- Mossmann T. R., Kobie J. J., Lee F. E., Quataert S. A. T helper
cytokine patterns: defined subsets, random expression, and external modulation
// Immunology Research. 2009. Vol. 45. № 3. P. 173–184.
- Nakae S., Iwakura Y., Suto H., Galli S. J. Phenotypic differences
between Th1 and Th2 cells and negative regulation of Th1 cell differentiation
by ИЛ-17 // Journal of leukocyte biology. 2007. Vol. 81. P. 1258–1268.
- Annunziato F., Romagnani S. Heterogeneity of human effector CD4+
T cells // Arthritis Research & Therapy. 2009. Vol. 11, № 257 (doi:10.
1186/ar2843).
- Acosta-Rodriguez E. V., Napolitani G., Lanzavecchia A., Sallusto F.
Interleukins 1 β and 6 but not transforming growth factor — β are essential
for the differentiation оf interleukin 17 — producing human T helper cells //
Nature immunology. 2007. Vol. 8. № 9. Р. 942–949.
- Korn T., Bettelli E., Oukka M., Kuchroo V. K. IL-17 and Th17
Cells // Annual Review of Immunology. 2009. Vol. 27. P. 485–517.
- Jiang S. TH17 in health and disease. Springer-Verlag New York Inc.
2011. 552 с.
- Moissec P., Kolls J. K. Targeting IL-17 and Th17 cells in chronic
inflammation // Nature reviews. 2012. Vol. 11. P. 763–776.
- Gaffen S. L. Recent advances in the IL-17 cytokine family //
Current Opinion in Immunology. 2011. Vol. 23. № 5. P. 613–619.
- Pryhuber K. G., Murray K. J., Donnelly P. et al. Polymorphism in
the LMP2 gene influences disease susceptibility and severity in HLA-B27
associated juvenile rheumatoid arthritis // Journal of Rheumatology. 1996. Vol.
23. P. 747–752.
- Schwarzenberger P., La Russa V., Miller A., Ye P., Kolls J. K.
IL-17 stimulates granulopoesis in mice: use of an alternate, novel gene
therapy-derived method for in vivo evaluation of cytokines // Journal of
Immunology. 1998. Vol. 161. № 11. P. 6383–6389.
- Waite J., Skokos D. Th17 response and inflammatory autoimmune
diseases // International journal of
inflammation. 2012. Vol. 2012. P. 232–242.
- Eleftheriou D., Isenberg D. A., Wedderburn L. R., Ioannou Y. The
coming of age of adolescent rheumatology // Nature Review of Rheumatology.
2014. Vol. 10. P. 187–193.
- Lee Y. K., Turner H., Maynard C. L., Oliver J. R. et al. Late
developmental plasticity in the T helper 17 lineage // Immunity. 2009. Vol.
30. P. 92–107.
- Nistala K., Moncriefe H., Newton K. R., Wedderburn L. R.
Interleukin-17-Producing T cells are enriched in the joints of children with
arthritis, but have a reciprocal relationship to regulatory T cell number //
Journal of arthritis and Rheumatism. 2008. Vol. 58. № 3. P. 875–887
- Liu C., Walter T. S., Huang P., Zhang S., Zhu X., Wu Y., Wedderburn
L. R., Tang P. Structural and functional insights of RANKL-RANK
interaction and signaling // Journal of Immunology. 2010. Vol. 184. № 12. P.
6910–6919.
- Lubberts E., Marije I., Koenders E., Oppers-Walgreen B., van den
Bersselaar L. et al. Blocking of Interleukin-17 during Reactivation of
Experimental Arthritis Prevents Joint Inflammation and Bone Erosion by
Decreasing RANKL and Interleukin-1 // American Journal of Pathology. 2005. Vol.
167. № 1. P. 141–149.
- Corrado A., Neve A., Maruotti N., Cantatore F. P. Bone Effects of
Biologic Drugs in Rheumatoid Arthritis // Clinical and Developmental
Immunology. Vol. 201. P. 105–112.
- Sarkar S., Tesmer L. A., Endres J. L. et al. Interleukin-17 as a
molecular target in immune-mediated arthritis // Journal of Arthritis and
Rheumatism. 2007. Vol. 56. № 1. P. 89–100.
- Genovese M. C., van den Bosch F., Roberson S. A., Bojin S., Biagini I.
M., Ryan P. et al. LY2439821, a humanized anti-interleukin-17 monoclonal
antibody, in the treatment of patients with rheumatoid arthritis: a phase I
randomized, double-blind, placebo-controlled, proof-of-concept study //
Arthritis and Rheumatism. 2010. Vol. 62. P. 929–939.
- Hueber W., Patel D. D., Dryja T., Wright A. M., Koroleva I., Bruin G.
et al. Effects of AIN457, a fully human antibody to interleukin-17 A, on
psoriasis, rheumatoid arthritis, and uveitis // Science Translational Medicine.
2010. Vol. 2. № 52. P. 52–72.
- Leonardi C., Matheson R., Zachariae C., Cameron G., Li L. et al.
Anti-IL-17 monoclonal antibody ixekizumab in chronic plaque psoriasis // New
England Journal of Medicine. 2012. Vol. 366. P. 1190–1199.
Статья опубликована в журнале
Лечащий Врач

