
Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Роль серотониновых рецепторов в моторно-эвакуаторной функции
желудочно-кишечного тракта
Е. Ю. Плотникова, доктор медицинских наук, профессор
О. А. Краснов, доктор медицинских наук, профессор
ГБОУ ВПО КемГМА МЗ РФ, Кемерово
Основными классами рецепторов, участвующих в регуляции моторно-эвакуаторной
функции желудочно-кишечного тракта (ЖКТ), являются холинергические,
адренергические, допаминергические, серотониновые, мотилиновые и
холецистокининовые. Препараты, применяемые при депрессивных и тревожных
расстройствах, панических атаках и других вегетативных дисфункциях, действуют на
те же рецепторы, которые отвечают за моторно-эвакуаторную функцию
желудочно-кишечной трубки. Регулирование деятельности гладкой мускулатуры и
подвижности кишечника происходит на нескольких уровнях. Гормоны и нейротрансмиттеры являются доминирующими компонентами, которые прямо или
косвенно воздействуют на гладкомышечные клетки. Постпрандиальный эндокринный
ответ включает в себя выработку инсулина, нейротензина, холецистокинина (ХХК),
гастрина, глюкагоноподобных пептидов (ГПП-1 и ГПП-2), глюкозозависимый
инсулинотропный полипептид (ГИП, ранее известный как желудочный ингибиторный
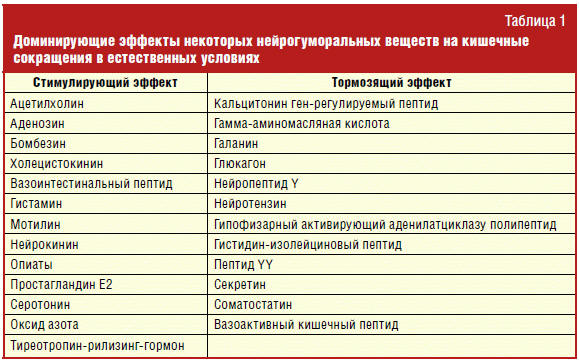
пептид) [1], данные об эффектах нейромедиаторов и гормонов представлены в табл.
1. Например, ХХК выделяется в проксимальных отделах тонкой кишки и
непосредственно влияет на сокращение мышечных клеток желчного пузыря и
нейромедиированную релаксацию мышц клеток сфинктера Одди, которая опосредуется
через ГИП нервно-мышечные соединения.
В настоящей статье особое внимание уделено серотонинергическим рецепторам,
которые являются одними из важных регуляторов кишечной перистальтики. Серотонин,
или 5-гидрокситриптамин (5-HT), — моноаминовый нейромедиатор, который является
главным посредником в физиологии психологического состояния и настроения
человека, а также одним из регуляторов функции сосудов и желудочно-кишечной
моторики. 5-HT, как известно, представлен в тромбоцитах, ЖКТ и центральной
нервной системе человека и животных [2–5]. Серотонин вырабатывается в организме
человека из поступившей с пищей аминокислоты триптофана — так как именно она
нужна для непосредственного синтеза серотонина в синапсах; второй путь выработки
серотонина связан с поступлением глюкозы с углеводной пищей, которая стимулирует
выброс инсулина в кровь, далее происходит катаболизм белка в тканях, что также
приводит к повышению уровня триптофана в крови.
На основе биохимических и фармакологических критериев 5-HT-рецепторы
подразделяются на семь основных подтипов, пять из которых находятся в кишечных
нейронах, энтерохромаффинных (ЭХ) клетках и в гладкой мускулатуре ЖКТ — это
5-HT1, 5-HT2, 5-HT3, 5-НТ4 и 5-HT7
[6, 7]. Около 80% от общего количества 5-НТ-рецепторов находятся в ЭХ-клетках
кишечника, где они принимают участие в кишечной перистальтике через несколько
подтипов 5-HT-рецепторов [8, 9]. За исключением 5-HT3-рецепторов,
лиганда закрытого ионного канала, все 5-HT-рецепторы связываются с рецепторами
G-белка, которые активируют внутриклеточные реакции второго каскада, стимулируя
возбуждающие или тормозные реакции в ЖКТ [10]. Серотонин обладает хорошо
изученным воздействием на кишечную моторику, секрецию и сенситивность через
центральные и периферические нейромедиаторные пути, что делает его ключевым
фармакологическим средством, применяемым в лечении моторных нарушений ЖКТ [11].
Серотонин высвобождается из ЭХ-клеток в ответ на химическое или механическое
раздражение слизистой оболочки [12] или в ответ при экспериментальных моделях
стресса [13]. Серотонин синтезируется и хранится не только в ЭХ-клетках (90%),
но и в нейронах кишечника (10%). Как говорилось выше, 5-HT выделяется в кровь
после приема пищи и в ответ на изменения давления в кишечной стенке, а также при
воздействии вредных раздражителей [13], а затем поступает в просвет кишечника и
далее в его стенки из базолатерального депо ЭХ-клеток [14]. 5-HT стимулирует
круговые и продольные мышцы желудка, двенадцатиперстной кишки и тощей кишки
[15]. Важно стратегическое расположение ЭХ-клеток в непосредственной близости от
сенсорных нервных окончаний слизистой оболочки кишечника, интерганглионарных
нейронов и синапсов двигательных возбуждающих и тормозных нейронов. Серотонин
увеличивает сокращение амплитуды мышц желудка, двенадцатиперстной кишки, тощей
кишки и подвздошной кишки [16]. В тонкой кишке 5-HT стимулируют круговые
сокращения мышц в течение первой манометрической фазы, вызываемые сокращения
распространяются, становятся более частыми и активируют быстрые моторные
комплексы [17]. В толстой кишке серотонин стимулирует подвижность на протяжении
всей длины, вызывая фазовые сокращения, но не гигантские двигательные комплексы
[18]. Кишечные гладкомышечные ритмические колебания определяются спонтанной
активностью интерстициальных клеток Кахаля, которые работают как
кардиостимулятор для клеток в ЖКТ [19–22]. Кишечная нервная система (КНС)
состоит из полуавтономных эффекторных систем, которые связаны с центральной
вегетативной системой. При освобождении серотонина из энтерохромаффинных клеток
происходит инициация вагусных рефлексов — перистальтических, выделительных,
сосудорасширяющих, ноцицептивных. Парасимпатический и симпатический отделы
вегетативной нервной системы образуют КНС через афферентные и эфферентные связи.
Текущие двунаправленные отношения рефлекторной дуги «мозг–кишка» с участием 5-HT
оказывают существенное влияние на эффекторные системы. Нарушенная
5-HT-трансмиссия может привести к возникновению как кишечных, так и внекишечных
проявлений синдрома раздраженного кишечника (СРК) [23].
Степень участия в функциональной перистальтической активности ЖКТ различных
5-HT подразделяется следующим образом — 5-HT3 — 65%, 5-НТ4
— 85% и 5-HT7 — 40%. В сочетании антагонисты этих рецепторов,
приведенные в парах, способны уменьшить перистальтическую активность кишечника
примерно на 16% (5-HT3 + 5-HT4), на 70% (5-HT3 + 5-HT7)
и на 87% (5-HT4 + 5-HT7), а одновременное введение всех
трех антагонистов неизбежно блокирует всю перистальтическую активности. Таким
образом, 5-HT-рецепторы играют ключевую роль в модуляции кишечной перистальтики
с одновременной блокадой трех рецепторов и подавляют перистальтическую
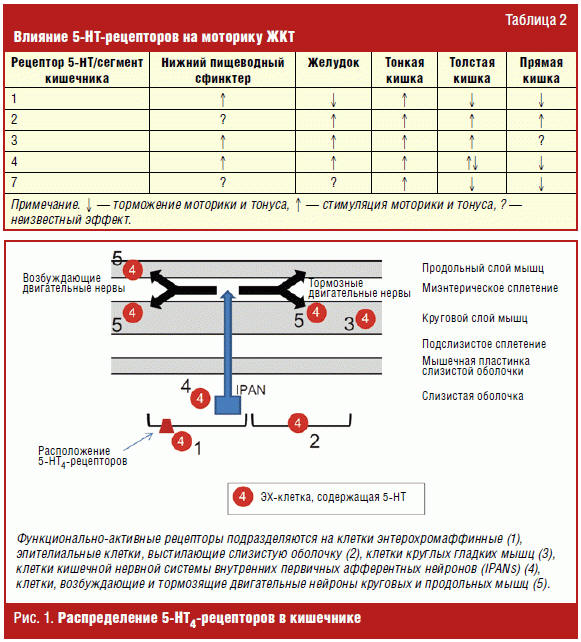
активность. Среди 5-HT-рецепторов ЖКТ подтип 5-HT4 наиболее
функционально важен для перистальтики, а 5-HT3- и 5-HT7-рецепторы
играют несколько менее активную роль в этом процессе, что отражено в табл. 2 и
на рис. 1 [24].
5-HT4-агонисты были доступны с введением в клиническую практику
метоклопрамида в 1964 г. Этот препарат является антагонистом дофаминовых D2-
и 5-HT3-рецепторов, а также агонистом 5-HT4-рецепторов и
до сих пор широко используется во всем мира. Его успех привел к разработке
альтернативных молекул, которые не влияют на D2-рецепторы, устраняя
тем самым такие неблагоприятные события, как акатизия и экстрапирамидные
двигательные расстройства.
Серотониновые рецепторы, в частности, 5-HT3 и 5-НТ4,
участвуют в сенсорных и рефлекторных реакциях на раздражители при
гастроинтестинальных расстройствах, обусловливая такие проявления, как рвота,
запор или диарея, нарушения пищевого поведения, боли в животе, измененные
сенсомоторные рефлексы [25]. Было высказано предположение, что селективные
ингибиторы обратного захвата серотонина (СИОЗС) могут влиять на функцию 5-HT3-рецепторов,
а также могут улучшить симптоматику СРК и сопутствующей депрессии у пациентов.
Согласно ряду исследований и обзоров [26–29], трициклические антидепрессанты (амитриптилин,
Мелипрамин), антидепрессанты ряда СИОЗС, такие как флуоксетин, пароксетин,
циталопрам, кломипрамин, литоксетин, тразодон, и ряда селективных ингибиторов
обратного захвата серотонина и норадреналина (СИОЗСиН) (дулоксетин) улучшают
симптомы СРК. Долгосрочные побочные эффекты данной терапии являются общими для
лечения антидепрессантами и связаны с антихолинергическим, серотонинергическим,
седативным, антигистаминым и альфа-адренергическим эффектами. Эти эффекты
необходимо учитывать при выборе подхода к лечению, поскольку описанные выше
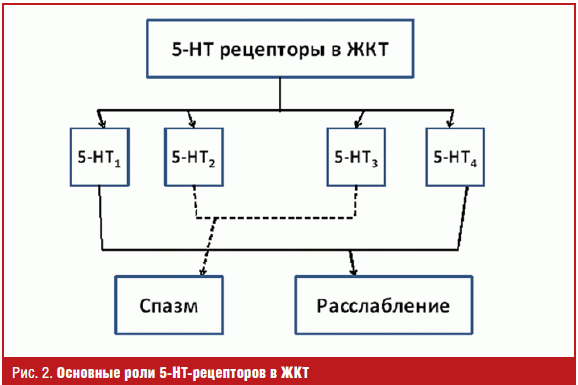
препараты влияют на моторику кишечника, функция кишечника пациента также должна
учитываться при выборе серотонинергических препаратов (рис. 2) [30].
Как указывалось ранее, 5-HT1-, 5-HT3- и 5-НТ4-подтипы
рецепторов играют важную роль в двигательных, чувствительных и секреторных
функциях ЖКТ. Препараты, непосредственно влияющие на 5-HT-рецепторы, в отличие
от трициклических антидепрессантов и СИОЗС, модулируют 5-гидрокситриптамин
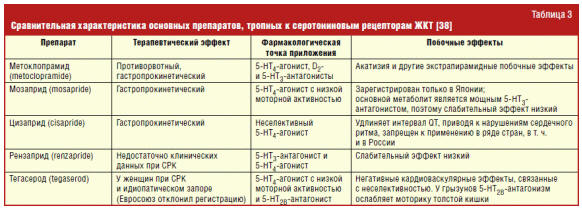
(5-HT) путем связывания с 5-HT-рецепторами, их характеристики отражены в табл.
3. Кишечные функции 5-HT-рецепторов связаны с гладкими мышцами, увеличением
количества дефекаций, а также со снижением кишечного транзитного времени [31,
32]. Блокада 5-НТ3-рецепторов, в частности противорвотными средствами
типа ондансетрона, приводит к запорам [33]. В течение последнего десятилетия
были разработаны и испытаны блокаторы 5-НТ3-рецепторов — алосетрон и
силансетрон при СРК-Д (СРК с диареей). Недавний систематический обзор и
метаанализ 11 рандомизированных контролируемых исследований (РКИ) сравнения этих
двух 5-НТ3-антагонистов с плацебо выявили положительный эффект
препаратов [34]. Тем не менее, ряд редких побочных эффектов, включая ишемический
колит и тяжелые запоры, привел к тому, что производство алосетрона и
исследования по силансетрону были приостановлены [35]. Алосетрон сегодня
доступен только по строгим показаниям (в США) для пациенток с тяжелым
резистентным СРК с диареей, которые не ответили на первую или вторую линии
терапии.
5-HT4-агонисты доказали свой терапевтический потенциал для лечения
больных с нарушениями моторики ЖКТ. Препараты, у которых отсутствует
селективность к 5-HT4-рецепторам, имеют ограниченный клинический
успех в гастроэнтерологической практике. Например, наряду со сродством к 5-HT4-рецепторам,
такие препараты, как цизаприд и тегасерод, имеют заметное сродство и к другим
рецепторам, каналам или белкам-трансмиттерам. Неблагоприятные кардиоваскулярные
события, наблюдаемые при применении этих средств, связаны с их неселективностью
и перекрестными эффектами. Систематический обзор и метаанализ показали, что
тегасерод превосходит плацебо при лечении запоров, в том числе и при СРК.
Большинство исследований, относящихся к тегасероду, проводились с участием
женщин, и в результате препарат первоначально был одобрен для лечения СРК-З (СРК
с запором) только у женщин. Тем не менее, маркетинг тегасерода был также
приостановлен, когда стали сообщаться данные о возможном росте
сердечно-сосудистых и цереброваскулярных событий на фоне приема препарата [6].
Важным событием в клинической фармакологии стало открытие селективного
лиганда (лиганд, от лат. ligare — связывать, атом, ион или молекула, связанные с
неким центром (акцептором), термин применяется в биохимии для обозначения
агентов, соединяющихся с биологическими акцепторами — рецепторами,
иммуноглобулинами и др.) к 5-HT4-рецептору — прукалоприда (prucalopride).
Избирательность этого нового препарата значительно отличает его от старших
поколений альтернативных препаратов благодаря сведению к минимуму возможностей
побочных эффектов. Кроме того, концепция поиска аналогичных лигандов открывает
широкие возможности для дальнейшей разработки лекарственных препаратов и
создания агонист-специфических эффектов в различных типах клеток, тканей или
органов. Селективный агонист 5-HT4-рецепторов прукалоприд является
инновационным препаратом с привлекательным профилем безопасности для лечения
пациентов, страдающих гипомоторными расстройствами ЖКТ [36]. Прукалоприд имеет
высокое сродство и избирательность к 5-HT4-рецепторам ЖКТ. За время
существования препарата прукалоприд было проведено несколько крупных и
долгосрочных исследований, которые позволили в полной мере оценить риски и
преимущества использования прукалоприда при хронических запорах [36–38]. В целом
прием прукалоприда был связан с последовательным и значительным улучшением
удовлетворенности пациентов в их лечении, по оценке опросника качества жизни при
запорах (Patient Assessment of Constipation Quality of Life questionnaire —
PAC-QOL). Доля участников, получавших прукалоприд в дозе 2 мг в сутки, которые
отметили улучшение ≥ 1 пункт по 5-балльной подшкале PAC-QOL, составила 45,3%, по
сравнению с 21,3% среди тех больных, кто получал плацебо (р ≤ 0,001), но число
ответчиков почти во всех исследованиях было менее 50%. В ходе других испытаний —
PRU-США-11 и PRU-США-13 — не было выявлено никакого существенного различия между
прукалопридом и плацебо во всех суррогатных точках. Общая частота нежелательных
явлений была статистически достоверно чаще у пациентов, получавших прукалоприд
(72%), по сравнению с пациентами, принимавшими плацебо (59%) (отношение рисков
(ОР) 1,21, 95% доверительный интервал (ДИ): 1,06, 1,38). Неблагоприятные
события, которые наиболее часто сообщали пациенты, получавшие прукалоприд, были
головная боль (до 30%), тошнота (до 24%), диарея (до 5%), боли в животе и
метеоризм (до 23%), головокружение (до 5%) и инфекции верхних дыхательных путей
[39]. R. Cinca и соавт. сравнили эффективность, безопасность и влияние на
качество жизни макрогола и прукалоприда у 240 женщин с хроническими запорами,
которым другие слабительные не обеспечивали адекватную помощь. В этом
исследовании макрогол оказался более эффективным для лечения хронического
запора, чем прукалоприд, и лучше переносился [40]. В итоге можно сделать вывод,
что прукалоприд может назначать врач, имеющий опыт в лечении хронических
запоров, женщинам от 18 до 75 лет в том случае, если в их лечении не были
эффективны другие слабительные средства.
Важно знать, что не всегда у пациентов бывает дефицит серотонина, в ряде
случаев врач может сталкиваться с его избытком. У беспокойных
гастроэнтерологических пациентов, которые имеют повышенное содержание серотонина,
развивается аэрофагия, что вызывает увеличение воздушного пузыря в желудке и
приводит к раздражению рецепторного аппарата [41]. Повышенный уровень серотонина
обуславливает частую тошноту и рвоту вследствие активации блуждающего нерва,
диарею или спастический запор, гастроинтестинальные панические атаки, головную
боль, тремор, гипергидроз, волнение и тревогу, сердцебиение, нестабильное
артериальное давление, бессонницу.
Серотонин играет важную роль не только в регуляции моторики и секреции в ЖКТ,
усиливая его перистальтику и секреторную активность, но и является фактором
роста для некоторых видов симбиотических микроорганизмов, усиливает
бактериальный метаболизм в толстой кишке. Сами бактерии толстой кишки также
вносят некоторый вклад в секрецию серотонина кишечником, поскольку многие виды
симбиотических бактерий обладают способностью декарбоксилировать триптофан. При
дисбиозе и ряде других заболеваний толстой кишки продукция серотонина кишечником
значительно снижается. Массивное высвобождение серотонина из погибающих клеток
слизистой желудка и кишечника при воздействии цитотоксических химиопрепаратов
является одной из причин возникновения тошноты и рвоты, а также диареи при
химиотерапии злокачественных опухолей [42, 43].
Трудно переоценить роль серотонина в организме человека. В передней части
мозга под воздействием серотонина стимулируются области, ответственные за
процесс познавательной активности, а повышение серотонинергической активности
создает в коре головного мозга ощущение подъема настроения. Поступающий в
спинной мозг серотонин положительно влияет на двигательную активность и тонус
мышц, это состояние можно охарактеризовать фразой «горы сверну». Кроме
настроения, серотонин «отвечает» за самообладание или эмоциональную
устойчивость. Серотонин контролирует восприимчивость мозговых рецепторов к
стрессовым гормонам адреналину и норадреналину. У людей с пониженным уровнем
серотонина малейшие поводы вызывают обильную стрессовую реакцию. Отдельные
исследователи считают, что доминирование особи в социальной иерархии обусловлено
именно высоким уровнем серотонина [42, 43].
Заключение
Когда в организм поступает пища, в том числе содержащая триптофан,
увеличивается выработка серотонина, что повышает настроение. Мозг быстро
улавливает связь между этими явлениями и, в случае депрессии (серотонинового
голодания), незамедлительно «требует» дополнительного поступления пищи с
триптофаном или глюкозой. Наиболее богаты триптофаном продукты, которые почти
целиком состоят из углеводов, например, хлеб, бананы, шоколад, инжир, курага,
финики, изюм, арбузы и т. п. Перечисленные продукты давно известны и как
регуляторы кишечной перистальтики. Их дефицит в питании приводит к депрессиям и
проблемам ЖКТ, что можно часто наблюдать у людей, соблюдающих строгую
низкокалорийную диету. По этой причине прежде чем назначать пациенту
лекарственные препараты, повышающие уровень серотонина, необходимо уточнить
причину его дефицита. Знание о деталях строения серотониновых рецепторов,
несомненно, найдет применение в лечении пациентов некардиотоксичными аналогами
серотонина или препаратами, повышающими уровень серотонина, которые будут
выполнять свою целебную функцию и окажутся приятны во всех отношениях, например,
такие как шоколад [44]. Препараты, повышающие уровень серотонина в синаптической
щели и способствующие усилению его эффектов, относятся к группе
антидепрессантов. Сегодня они являются одними из самых назначаемых лекарств
врачами общей медицинской практики многих стран мира, в том числе Европы и
Северной Америки. Своевременное назначение антидепрессантов как в монотерапии,
так и в схемах лечения различных заболеваний, позволяет повысить эффективность
лечения основного заболевания и улучшить качество жизни пациентов, особенно у
пациентов гастроэнтерологического профиля.
Литература
- Medhus A. W., Sandstad O., Naslund E. at al. The influence of the
migrating motor complex on the postprandial endocrine response // Scand J
Gastroenterol. 1999. 34. Р. 1012–1018.
- Buchheit K. H., Engel G., Mutschler E., Richardson B. Study of
the contractile effect of 5-hydroxytryptamine (5-HT) in the isolated
longitudinal muscle strip from guinea-pig ileum. Evidence for two distinct
release mechanisms // Naunyn Schmiedebergs Arch Pharmacol. 1985. 329. Р.
36–41.
- Kim D. Y., Camilleri M. Serotonin: a mediator of the brain-gut
connection // Am J Gastroenterol. 2000. 95. Р. 2698–2709.
- Woollard D. J., Bornstein J. C., Furness J. B. Characterization
of 5-HT receptors mediating contraction and relaxation of the longitudinal
muscle of guinea-pig distal colon in vitro // Naunyn Schmiedebergs Arch
Pharmacol. 1994. 349. Р. 455–462.
- Yamano M., Ito H., Miyata K. Species differences in the
5-hydroxytryptamine-induced contraction in the isolated distal ileum // Jpn J
Pharmacol. 1997. 74. Р. 267–274.
- De Maeyer J. H., Lefebvre R. A., Schuurkes J. A. 5-HT4 receptor
agonists: similar but not the same // Neurogastroenterol Motil. 2008. 20. Р.
99–112.
- Hannon J., Hoyer D. Molecular biology of 5-HT receptors // Behav
Brain Res. 2008. 195. Р. 198–213.
- Kim D. Y., Camilleri M. Serotonin: a mediator of the brain-gut
connection // Am J Gastroenterol. 2000. 95. Р. 2698–2709.
- Berger M., Gray J. A., Roth B. L. The expanded biology of
serotonin // Annu Rev Med. 2009. 60. Р. 355–366.
- Hannon J., Hoyer D. Molecular biology of 5-HT receptors // Behav
Brain Res. 2008. 195. Р. 198–213.
- Crowell M. D. Role of serotonin in the pathophysiology of the
irritable bowel syndrome // Br J Pharmacol. 2004. 141. Р. 1285–1293.
- Gershon M. D. Plasticity in serotonin control mechanisms in the
gut // Curr Opin Pharmacol. 2003. 3. Р. 600–607.
- Bearcroft C. P., Perrett D., Farthing M. J. Postprandial plasma
5-hydroxytryptamine in diarrhoea predominant irritable bowel syndrome: a pilot
study // Gut. 1998. 42. Р. 42–46.
- Hansen M. B. Small intestinal manometry // Physiol Res. 2002. 51.
Р. 541–556.
- Fishlock D. J., Parks A. G., Dewell J. V. Action of
5-hydroxytryptamine on the human stomach, duodenum, and jejunum in vitro //
Gut. 1965. 6. Р. 338–342.
- Hopkinson G. B., Hinsdale J., Jaffe B. M. Contraction of canine
stomach and small bowel by intravenous administration of serotonin. A
physiologic response? // Scand J Gastroenterol.
1989. 24. Р. 923–932.
- Hansen M. B., Gregersen H., Husebye E., Wallin L. Effect of
serotonin and ondansetron on upper GI manometry in healthy volunteers //
Neurogastroenterol Motil. 2000. 12. Р. 281.
- Boerckxstaens G. E., Pelckmans P. A., Rampart M. at al.
Pharmacological characterization of 5-hydroxytryptamine receptors in the
canine terminal ileum and ileocolonic junction // J Pharmacol ExpTher. 1990.
254. Р. 652–658.
- Alberti E., Mikkelsen H. B., Larsen J. O., Jimenez M. Motility
patterns and distribution of interstitial cells of Cajal and nitrergic neurons
in the proximal, mid- and distal-colon of the rat // Neurogastroenterol Motil.
2005. 17. Р. 133–147.
- Sanders K. M. A case for interstitial cells of Cajal as
pacemakers and mediators of neurotransmission in the gastrointestinal tract //
Gastroenterology. 1996. 111. Р. 492–515.
- Thomsen L., Robinson T. L., Lee J. C. at al. Interstitial cells
of Cajal generate a rhythmic pacemaker current // Nat Med. 1998. 4. Р.
848–851.
- Park S. Y., Je H. D., Shim J. H., Sohn U. D. Characteristics of
spontaneous contraction in the circular smooth muscles of cat ileum // Arch
Pharm Res. 2010. 33. Р. 159–165.
- Crowell M. D. Role of serotonin in the pathophysiology of the
irritable bowel syndrome // Br J Pharmacol. 2004. 141 (8). Р. 1285–1293.
- Balestra B., Vicini R., Pastoris O. at al. 5-HT receptors and
control of intestinal motility: expression and hierarchic role // Poster
Session, Bologna. 2011.
- Read N. W., Gwee K. A. The importance of 5-hydroxytryptamine
receptors in the gut // Pharmacol Ther. 1994. Apr-May; 62 (1–2). Р. 159–173.
- Lucchelli A., Santagostino-Barbone M. G., Barbieri A. at al. The
interaction of antidepressant drugs with central and peripheral (enteric)
5-HT3 and 5-HT4 receptors // Br J Pharmacol. 1995. Mar; 114 (5). Р. 1017–1025.
- Ford A. C., Talley N. J., Schoenfeld P. S., Quigley E. M., Moayyedi P.
Efficacy of antidepressants and psychological therapies in irritable bowel
syndrome: systematic review and meta-analysis // Gut. 2009. Mar; 58 (3). Р.
367–378.
- Friedrich M., Grady S. E., Wall G. C. Effects of antidepressants
in patients with irritable bowel syndrome and comorbid depression // Clin Ther.
2010. Jul; 32 (7). Р. 1221–1233.
- Chial H. J., Camilleri M., Burton D. at al. Selective effects of
serotonergic psychoactive agents on gastrointestinal functions in health // Am
J Physiol Gastrointest Liver Physiol. 2003. 284. G130-G137.
- Turvill J. L., Connor P., Farthing M. J. The inhibition of
cholera toxin-induced 5-HT release by the 5-HT (3) receptor antagonist,
granisetron, in the rat // Br J Pharmacol. 2000. 130. Р. 1031–1036.
- Ruckebusch Y., Bardon T. Involvement of serotonergic mechanisms
in initiation of small intestine cyclic motor events // Dig Dis Sci. 1984. 29.
Р. 520–527.
- Haus U., Spath M., Farber L. Spectrum of use and tolerability of
5-HT3 receptor antagonists // Scand J Rheumatol Suppl. 2004. 119.
Р. 12–18.
- Ford A. C., Brandt. L. J., Young C. at al. Efficacy of 5-HT3
antagonists and 5-HT4 agonists in irritable bowel syndrome:
Systematic review and metaanalysis // Am J Gastroenterol. 2009. 104. Р.
1831–1843.
- US Food and Drug Administration. Glaxo Wellcome withdraws irritable bowel
syndrome medication // FDA Consum. 2001. 35. Р. 3.
- Johanson J. F., Drossman D. A., Panas R., Wahle A., Ueno R.
Clinical trial: phase 2 study of lubiprostone for irritable bowel syndrome
with constipation // Aliment. Pharmacol. 2008. 27. Р. 685–696.
- Camilleri M., Kerstens R., Rykx A., Vandeplassche L. A
Placebo-Controlled Trial of Prucalopride for Severe Chronic Constipation // N
Engl J Med. 2008. 358. Р. 2344–2354.
- Tack J., van Outryve M., Beyens G., Kerstens R., Vandeplassche L.
Prucalopride (Resolor) in the treatment of severe chronic constipation in
patients dissatisfied with laxatives // Gut. 2009; 58: 357–565.
- Quigley E. M., Vandeplassche L., Kerstens R., Ausma J. Clinical
trial: the efficacy, impact on quality of life, and safety and tolerability of
prucalopride in severe chronic constipation a 12-week, randomized,
double-blind, placebo-controlled study // Aliment Pharmacol Ther. 2009; 29:
315–328.
- http://www.pbs.gov.au/industry/listing/elements/pbac-meetings/psd/2012–7/prucalopride.pdf.
- Cinca R., Chera D., Gruss H. J., Halphen M. Randomised clinical
trial: macrogol/PEG 3350+electrolytes versus prucalopride in the treatment of
chronic constipation — a comparison in a controlled environment // Aliment
Pharmacol Ther. 2013. May; 37 (9). Р. 876–886.
- Буров Н. Е. Тошнота и рвота в клинической практике (этиология,
патогенез, профилактика и лечение) // Российский медицинский журнал. 2002. №
16. С. 390–395.
- Баринов Э. Ф., Сулаева О. Н. Роль серотонина в физиологии и
патологии желудочно-кишечного тракта // РЖГГК. 2012. Т. 21. № 2. С. 4–13.
- Ашмарин И. П., Ещенко Н. Д., Каразеева Е. П. Нейрохимия в
таблицах и схемах. М.: «Экзамен», 2007. 143 с.
- Palczewski K., Kiser P. D. As good as chocolate // Science. 2013.
340. Р. 562–563.
Статья опубликована в журнале
Лечащий Врач
Если вы заметили орфографическую, стилистическую или другую ошибку на этой странице, просто выделите ошибку мышью и нажмите Ctrl+Enter. Выделенный текст будет немедленно отослан редактору
|
|
|
|

