Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Дисфункция эндотелия и артериальная гипертония:
терапевтические возможности
Профессор В.С. Задионченко, к.м.н. Т.В. Адашева, А.П.
Сандомирская
МГМСУ им. Н.А. Семашко
 Решающая роль эндотелия в регуляции сократимости гладкомышечных клеток сосудов
была в полной мере осознана лишь после открытия Fuchgott и Zawadski. Они
продемонстрировали, что сосуд, находившийся в состоянии сократимости после
введения норадреналина, отвечает релаксацией на увеличение дозы ацетилхолина
только при наличии эндотелия. Напротив, при отсутствии эндотелиальных клеток в
ответ на ацетилхолин наблюдались вазоконстрикция либо отсутствие релаксации. Это
привело к открытию вазодилатирующей субстанции, освобождаемой
эндотелиальными клетками. Авторы не установили природу этого вещества и
обозначили его, как эндотелий–релаксирующий фактор. Позднее оно
было идентифицировано, как оксид азота [1,2,3,4].
Решающая роль эндотелия в регуляции сократимости гладкомышечных клеток сосудов
была в полной мере осознана лишь после открытия Fuchgott и Zawadski. Они
продемонстрировали, что сосуд, находившийся в состоянии сократимости после
введения норадреналина, отвечает релаксацией на увеличение дозы ацетилхолина
только при наличии эндотелия. Напротив, при отсутствии эндотелиальных клеток в
ответ на ацетилхолин наблюдались вазоконстрикция либо отсутствие релаксации. Это
привело к открытию вазодилатирующей субстанции, освобождаемой
эндотелиальными клетками. Авторы не установили природу этого вещества и
обозначили его, как эндотелий–релаксирующий фактор. Позднее оно
было идентифицировано, как оксид азота [1,2,3,4].
В настоящее время известно, что эндотелий контролирует сосудистый тонус, рост
гладкомышечных клеток, тромбообразование, фибринолиз и многие другие процессы.
Установлено, что эндотелий регулирует сосудистый тонус через освобождение
сосудорасширяющих и сосудосуживающих факторов и модулирует сократительную
активность гладкомышечных клеток [512]. К эндотелиальным факторам дилатации
относятся: фактор гиперполяризации эндотелия, простациклин I2 (PGI2),
монооксид азота (NO), натрийуретический пептид С типа, адреномедулин. К факторам
констрикции эндотелин, тромбоксан А2, простагландин F2a,
эндопероксиды и другие [9,10,12].
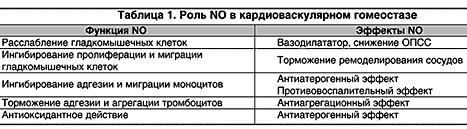
NO является основным вазодилататором, препятствующим тоническому сокращению
сосудов нейронального, эндокринного или локального происхождения (табл. 1)
[9,10,14,15,16,17].
В физиологических условиях преобладает освобождение релаксирующих факторов. В
нормально функционирующем эндотелии низкие уровни NO постоянно высвобождаются
для поддержания кровеносных сосудов в состоянии дилатации. Однако в определенных
кровеносных сосудах (периферические вены и крупные церебральные артерии)
нормальный эндотелий предрасположен к высвобождению сосудосуживающих веществ (супероксид
анион, тромбоксан А2). При различных сосудистых заболеваниях
способность эндотелиальных клеток освобождать релаксирующие факторы уменьшается,
тогда как образование сосудосуживающих факторов сохраняется или увеличивается,
т.е. формируется состояние, определяемое как дисфункция эндотелия
[9,10,18].
Оксид азота является старой молекулой, которая присутствует в природе уже
около ста миллионов лет и отлично сохранилась за весь период эволюции
биологических видов. Это очень лабильная молекула, время полужизни которой
составляет всего несколько секунд. NO является эссенциальным агентом для связи
между различными типами клеток, составляющими сердечнососудистую систему,
регулирует почечный и кардиоваскулярный гомеостаз [10,19,20,21,22].
В физиологических условиях NO постоянно вовлечен в адаптацию сосудистой
системы к повышенным метаболическим потребностям, физическим нагрузкам [6]. При
заболеваниях избыток NO отвечает за увеличение периферической вазодилатации при
вазоплегическом шоке, а недостаток NO может приводить к тяжелым заболеваниям,
включая артериальную гипертонию, ишемическую болезнь сердца и атеросклероз
[9,10,23,24,25].
NO предотвращает адгезию и агрегацию тромбоцитов, адгезию моноцитов, влияет
на структуру сосуда, что защищает сосудистую стенку и предотвращает
ремоделирование сосудов при различных патологических состояниях [9,26,27,28].
Оксид азота образуется под действием фермента NOсинтазы (NOS) путем окисления
терминального атома азота гуанидина в Lаргинине под каталитическим влиянием Са/кальмодулиназависимой
изоформы фермента NOсинтазы [29]. NOсинтаза существует в виде трех основных
изоформ, которые получили свое название по типу клеток, в которых они были
впервые обнаружены. Эти изоформы очищены, клонированы и охарактеризованы на
молекулярном уровне: нейрональная NOсинтаза (nNOS или NOS I), эндотелиальная
NOсинтаза (eNOS или NOS III) и NOсинтаза макрофагов или индуцибельная NOсинтаза
(iNOS или NOSII) [30]. Нейрональная и эндотелиальная NO синтазы являются
ферментами со стабильной активностью (т.е. стационарными, конститутивными), в то
время как активность макрофагальной или индуцибельной NOсинтазы в большей
степени регулируется цитокинами. Эндотелиальная NOсинтаза стабильно
экспрессируется в эндотелиальных клетках, помимо этого, она была обнаружена в
клетках эпителия почечных канальцев, в пирамидных клетках гиппокампа и в других
клетках [31,32,33].
Основная мишень NO в сосудистой системе гем растворимой гуанилатциклазы.
Активируя гуанилатциклазу, NO увеличивает образование цГМФ в гладкомышечных
клетках, тромбоцитах. цГМФ является главным внутриклеточным мессенджером в
сердечнососудистой системе и обусловливает расслабление сосудов, торможение
активности тромбоцитов и макрофагов [34,35].
Эндотелиальная дисфункция и артериальная гипертония
При артериальной гипертонии у человека была доказана эндотелиальная
дисфункция для периферической, коронарной микро и макроциркуляции и почечного
кровотока [51,52,53,54,55]. Хроническое ингибирование NO синтазы в эксперименте
быстро приводит ко всем органическим последствиям тяжелой и продолжительной
артериальной гипертензии, включая атеросклероз и сосудистые органные поражения
[37]. Эти экспериментальные данные подтверждают вовлечение NO в регуляцию АД,
следовательно его недостаток может приводить к гипертензии. Специфическая
инактивация гена эндотелиальной NOсинтазы сопровождается увеличением среднего АД
примерно на 1520 мм рт.ст. [38]. Доказано, что пациенты, страдающие гипертонией,
имеют меньший вазодилатирующий ответ на интраартериальное введение ацетилхолина
по сравнению с контрольной нормотензивной группой [39]. Установлено наличие
поражения эндотелийзависимой вазодилатации при эссенциальной гипертонии, которая,
повидимому, обусловлена нарушением синтеза и освобождением NO [40]. Есть данные
о связи повреждений системы LаргининNO с увеличением вазоконстрикторных
простагландинов. Доказано, что увеличение вазоконстрикторных простагландинов и
свободных радикалов вызывает уменьшение активности NO. Однако еще остается
множество вопросов о роли NO, механизмах его влияния на формирование и течение
артериальной гипертонии [9,10,44,71].
Экспериментальные данные:
при спонтанной АГ крыс (модель, наиболее близкая к эссенциальной АГ человека)
продукция NO повышается, но недостаточно, возможно, изза усиления его
инактивации, повышенного освобождения вазоконстрикторных простагландинов или
благодаря таким анатомическим изменениям, как утолщение интимы, которое
ингибирует действие NO на сосудистую стенку [9,10,37, 41,42,43].
на модели АГ у сольчувствительных крыс, получающих высокосолевой корм, не
выявлено повышения вазоконстрикторных простаноидов, что доказывает уменьшение
продукции NO [9,10,71].
Клинические данные:
при эссенциальной АГ эндотелиальная дисфункция вызвана одновременным
повреждением в системе LаргининNO и продукцией констрикторных простагландинов,
причем нарушение продукции NO первично, а увеличение вазоконстрикторов связано с
возрастом [9,10].
главным механизмом, приводящим к эндотелиальной дисфункции при АГ, является
продукция циклогеназозависимых простагландинов и свободных радикалов кислорода,
которые вызывают снижение активности NO [9,10,44].
Однако изменения эндотелиальной регуляции сосудистого тонуса у больных
артериальной гипертонией далеко не однозначны. Существуют различные точки зрения
на вопрос первичности эндотелиальной дисфункции при артериальной гипертонии
[45,46]. По данным некоторых авторов, наблюдаемая при АГ дисфункция эндотелия
является, скорее, следствием заболевания, чем его причиной, представляя
преждевременное старение кровеносных сосудов изза хронического воздействия
высокого АД [37,41,43,47].
Другие исследователи считают, что нарушение эндотелийзависимой вазодилатации
при АГ является первичным феноменом, так как, вопервых, обнаруживается у
потомков пациентов с эссенциальной гипертонией без повышенного артериального
давления, вовторых, отсутствует четкая корреляция с величиной АД, в третьих, не
нормализуется при снижении [48,49,50].
NO и сосудистое ремоделирование
Эндотелий освобождает вещества, которые поддерживают баланс между
ингибированием и стимуляцией факторов роста. NO относится к факторам,
ингибирующим рост. Дисфункция эндотелия с дефицитом NO, повышением экспрессии
факторов роста, локальных вазоактивных веществ, протеинов и протеиназ матрикса
может привести к сосудистому ремоделированию, повреждению структуры сосуда
[9,10].
Гипертензивные сосуды имеют утолщение средней оболочки, уменьшение просвета и
увеличение внеклеточного матрикса. Увеличение массы гладкомышечных клеток
повышает степень вазоконстрикции в ответ на нейрогормоны, приводит к повышению
периферического сосудистого сопротивления и таким образом способствует
стабилизации и усугублению артериальной гипертонии [56]. В крупных артериях
гипертрофия клеток и изменение внеклеточного матрикса уменьшают податливость и
эластичность сосудистой стенки. Утолщение сосудистой стенки, лейкоцитарное
пропитывание предрасполагает сосуды к развитию и прогрессированию атеросклероза
[56].
Изменение структуры сосудов с нарушением функции ведет к таким осложнениям,
как ишемия миокарда, инсульт, почечная недостаточность и т.д. [56,57].
Эндотелиальная дисфункция и инсулинорезистентность
Наличие тесной взаимосвязи между метаболическими нарушениями и
кардиоваскулярными заболеваниями не вызывает сомнения. Существует множество
исследований, рассматривающих тонкие механизмы влияния инсулинорезистенности и
гиперинсулинемии на уровень АД [58,59,60]. Установлено, что симпатическая
нервная система и путь LаргининаNO играют главную роль в посредничестве действия
инсулина на сердечнососудистую систему [59].
В настоящее время установлен и тот факт, что инсулинорезистентность и
эндотелиальная дисфункция, в том числе продукция NO, являются тесно
ассоциированными состояниями. Однако четко проследить причинноследственные связи
этих процессов пока не удается.
Инсулин обладает сосудистым протективным эффектом за счет активации
фосфатидилинозитол3киназы в эндотелиальных клетках и микрососудах, что приводит
к экспрессии гена эндотелиальной NOсинтазы и высвобождению NO эндотелиальными
клетками и инсулинобусловленной вазодилатации. Инсулин также содействует
повреждающим сосудистым эффектам через митогенактивированную протеинкиназу за
счет стимуляции различных факторов роста, что ведет к пролиферации и миграции
гладкомышечных клеток, продукции ими активатора плазминогена1 и усилению
процессов сосудистого ремоделирования и атеросклероза [60,61,62,63,64].
При инсулинорезистентности показано уменьшение инсулинопосредованной и
поражение эндотелийзависимой вазодилатации. Представленные данные дают основание
полагать, что эндотелиальная дисфункция является интегральным аспектом синдрома
инсулинорезистентности и способствует ее усугублению, увеличению реактивности
сосудов, что ведет к кардиоваскулярным осложнениям [58,60].
Дискутируется вопрос о причинноследственных взаимосвязях синдрома
инсулинорезистентности и эндотелиальной дисфункции. Несомненно,
инсулинорезистентность и эндотелиальная дисфункция, в том числе продукция NO,
тесно связаны друг с другом и формируют порочный круг, приводящий к
метаболическим и кардиоваскулярным заболеваниям.
Таким образом, эндотелий является новой терапевтический мишенью при
лечении сердечнососудистых заболеваний. И одним из путей коррекции
эндотелиальной дисфункции является фармакологическая стимуляция
эндотелийзависимого высвобождения монооксида азота [6568].
Вмешательства, корригирующие эндотелиальную дисфункцию при артериальной
гипертонии
Немедикаментозные методы воздействия
Нефармакологические вмешательства (диета, физические нагрузки, отказ от
курения), направленные на коррекцию эндотелиальной дисфункции, рекомендованы для
пациентов АГ [69].
В экспериментальных исследованиях было выявлено, что диета с высоким
содержанием жира приводит к развитию гипертонии за счет повышенного образования
свободных радикалов кислорода (супероксид анионов), инактивирующих NO [70].
Установлено, что благоприятный эффект на функцию сосудистого эндотелия
оказывают полиненасыщенные жирные кислоты, антиоксидантые витамины
(особенно токоферол и аскорбиновая кислота), фолиевая кислота, а также Lаргинин.
Они улучшают эндотелийзависимую вазодилатацию как у пациентов с высоким риском
кардиоваскулярных заболеваний, так и у здоровых без факторов риска [9,10,69].
Высокое потребление соли подавляет действие NO в периферических резистивных
сосудах на моделях АГ у животных [71]. В клинических исследованиях у пациентов с
сольчувствительной АГ показано снижение продукции NO [72].
Физические упражнения вызывают увеличение NO, как у нормотоников, так
и у пациентов с АГ [73,74]. В экспериментальных исследованиях на животных
выявлено, что после физических нагрузок происходит повышение эндотелиальной
NOсинтазы, увеличение продукции NO. Также на фоне физических нагрузок было
выявлено существование обратной связи: увеличение эндотелиального NO
стимулировало экспрессию супероксиддисмутазы, которая защищает NO от разрушения
свободными радикалами кислорода [75].
Курение является одним из факторов риска кардиоваскулярных заболеваний и
вызывает повреждение эндотелиальной функции [9,76]. Доказано нарушение
вазомоторной активности эндотелия коронарных артерий у курильщиков с длительным
стажем курения. Эндотелиальная дисфукнция коронарных артерий курильщиков
восстанавливалась при назначении Lаргинина, являющегося субстратом синтеза NO
[77]. При гиперхолестеринемии длительное курение усиливает эндотелиальную
дисфункцию за счет увеличения окисления ЛПНП [78]. Нарушение эндотелийзависимой
вазодилатации, вызванное курением, может быть обратимым у начинающих курильщиков
[79]. Пассивное курение также повышает кардиоваскулярный риск [9,80]. В
эксперименте показано, что эндотелиальная дисфункция, вызванная пасcивным
курением, уменьшалась при применении Lаргинина [80].
Ингибиторы АПФ
Обсуждаются, по крайней мере, два основных механизма влияния
ингибиторов АПФ (иАПФ) на эндотелиальную функцию [9,10, 81,82].
Известно, что иАПФ приводят к увеличению тканевого брадикинина.
Вазопротективные, антипролиферативные и антисклеротические свойства и, кроме
того, острые вазодилататорные эффекты иАПФ можно объяснить эндотелийзависимыми
реакциями, связанными со свойствами иАПФ предотвращать расщепление
брадикинина. Брадикинин является мощным стимулятором высвобождения
эндотелийзависимых расслабляющих факторов, таких как оксид азота,
эндотелийзависимый фактор гиперполяризации и простациклин (PGI2).
Эндотелиальный фактор гиперполяризации представляет собой нестойкий метаболит
арахидоновой кислоты, его высвобождение зависит от концентрации внутриклеточного
кальция и кальциймодуллина, и его влияние на эндотелийзависимое расслабление
связано с размером сосудов и наиболее значительно в небольших артериях.
Простациклин, образуясь в эндотелиальных клетках., активирует аденилатциклазу
гладкомышечных клеток, увеличивая образование цАМФ, расслабляющий эффект
которого усиливает вазодилатацию, вызываемую NO [8185]. Усиление
эндотелийзависимой релаксации в ответ на повышение локального брадикинина
объясняет острые вазодилатирующие эффекты иАПФ у больных с гипорениновой АГ
[9,10,86].
Другим механизмом воздействия иАПФ на эндотелиальную функцию является
блокада образования ангиотензина II (АТ II), который рассматривается как
индуктор окcидантного стресса. Экспериментально продемонстрировано увеличение
образования активных форм кислорода (супероксид анион) под действием АT II.
Механизмы действия АT II на продукцию супероксид аниона связаны со стимуляцией
НАДФН/НАДН оксидаз [87]. Таким образом, снижение АТ II приводит к уменьшению
оксидантного стресса, продукты которого снижают активность NO. Ангиотензин II во
многом обладает противоположным действием по отношению к NO и в настоящее время
признается практически его антагонистом. Ингибирование ангиотензинпревращающего
фермента может восстанавливать баланс между двумя вазоактивнами системами
ангиотензина II и оксида азота.
На моделях гипертензии у животных и при эссенциальной гипертонии у человека
доказано, что иАПФ улучшают ацетилхолинопосредованную и брадикининобусловленную
дилатацию артерий различной локализации (эпикардиальные артерии и микрососуды у
пациентов с ИБС и АГ, плечевая артерия, сосуды почек) [8894]. Способность иАПФ
улучшать эндотелиальную функцию и тормозить процессы атерогенеза впервые
продемонстрирована в исследовании TREND [93]. Это первое
клиническое исследование, подтвердившее данные многочисленных экспериментальных
работ о наличии у иАПФ эндотелиймодулирующих и антиатеросклеротических свойств.
В 6ти месячном рандомизированном исследовании у 129 больных с ИБС изучали
способность квинаприла восстанавливать нарушенную функцию коронарных артерий,
которую оценивали с помощью пробы с внутрикоронарным введением ацетилхолина при
коронарографии. Выявлено уменьшение на 1020% степени выраженности
вазоконстрикторных реакций после 6ти месячной терапии [95].
Блокаторы рецепторов ангиотензина II
Основным механизмом действия на систему NO блокаторов ангиотензиновых
рецепторов у больных АГ является, повидимому, блокада АТ1рецепторов,
приводящая к снижению продукции супероксидных радикалов, уменьшению связывания
NO и его накоплению. Так как стимуляция АТ1рецепторов способствует
образованию супероксидов, инактивирующих NO, а стимуляция АТ2рецепторов
приводит к вазодилатации и натрийурезу за счет активации системы брадикинина,
NO, цГМФ, то направленность эффекта ангиотензина ІІ (усиление синтеза или
инактивация NO) зависит от того, на какие рецепторы преимущественно он действует.
Поэтому очевидно, что на фоне блокады АТ1рецепторов создаются условия
для повышенного функционирования незаблокированных АТ2рецепторов, что
приводит к накоплению NO [96104].
Данные экспериментальных исследований о влиянии блокаторов ангиотензиновых
рецепторов на NO разноречивы. Так, на фоне назначения лозартана у крыс со
спонтанной гипертензией J. Cachoeiro и соавт. (1995) не обнаружили усиления
синтеза NO (об интенсивности образования NO судили по содержанию его клеточного
медиатора цГМФ в аорте). Другие исследователи наблюдали увеличение уровня цГМФ в
аорте крыс со спонтанной АГ под влиянием лозартана, из чего сделан вывод об
усилении синтеза NO [105]. На такой же модели АГ предварительное введение
лозартана полностью предотвращало влияние ангиотензина II на образование
супероксид аниона [106]. Установлено, что у крыс со спонтанной АГ повреждение
синтеза NO в надпочечниках способствовало возникновению и поддержанию
гипертензии. Доказано, что лозартан регулировал увеличение нейрональной
NOсинтазы в надпочечниках у крыс, восстанавливая таким образом синтез NO [107].
Клинические исследования пациентов с эссенциальной АГ показали улучшение
эндотелиальной функции резистивных артерий на фоне терапии лозартаном за счет
увеличения NO [108]. Имеются данные, что на фоне применения ирбесартана у
пациентов с АГ происходит повышение активности NOсинтазы в плазме и эритроцитах
и увеличение концентрации стабильных метаболитов NO [109,110]. Доказано, что
кандесартан у пациентов с эссенциальной АГ вызывал улучшение эндотелийзависимой
релаксации плечевой артерии за счет усиления тонического выделения NO [111].
Назначение валсартана приводило к улучшению эндотелиальной функции, нормализации
активности почечной ксантилоксидоредуктазы, увеличению продукции
брадикининопосредованного NO в почках [112]. Экспериментальные исследования на
крысах установили, что в ответ на уменьшение натрия и инфузию валсартана
происходит увеличение ангиотензина II, который стимулирует АТ2рецепторы,
что запускает каскад брадикинина и NO [113].
Антагонисты кальция
Антагонисты кальция дигидропиридинового ряда (АК) в эксперименте и в
клинических исследованиях улучшают эндотелийзависимую вазодилатацию за
счет увеличения NO (нифедипин, амлодипин, лацидипин, пранидипин,
фелодипин) [114129]. Установлено, что уменьшение Ca2+ в цитозоле и
вазодилатация на фоне АК обусловлены не только снижением трансмембранного
поступления ионов кальция в гладкомышечные клетки сосудов, но также и
NOцГМФопосредованным механизмом в эндотелиальных клетках [121]. Выявлено
несколько механизмов увеличения NO на фоне антагонистов кальция. Прандипин
достоверно увеличивал цГМФ в гладомышечных клетках, культивированных
одновременно с эндотелиальными клетками и не влиял на базальную экспрессию
эндотелиальной NO синтазы в эндотелиальных клетках; не оказывал эффекта при
наличии ингибитора NO синтазы (NGmonomethylLarginine). Однако прандипин
регулировал активность супероксид дисмутазы в эндотелиальных клетках, уменьшая
разрушение NO в стенке сосуда [128]. Очевидно, что основным механизмом
увеличения NO является антиоксидантное действие АК, увеличение активности
супероксиддисмутазы, уменьшение разрушения NO [125,128]. В эксперименте
установлено, что лацидипин регулировал экспрессию генов эндотелиальной NOS и
увеличивал уровень эндотелиальной NOсинтазы в ткани аорты [122,123,127].
Такие свойства АК дигидропиридинового ряда, как антиатеросклеротические (усиление
гидролиза холестерина, снижение внутриклеточной аккумуляции липидов),
антипролиферативные (подавление миграции и пролиферации гладкомышечных клеток и
макрофагов), в определенной мере антиагрегационные и обусловлены NO эффектом.
В настоящее время продолжается исследование ENCORE II
(Endothelial dysfunction as a therapeutic target), которое продемонстрирует
влияние антагонистов кальция и статинов на функцию эндотелия, а также позволит
оценить связь дисфункции эндотелия и ее фармакологического восстановления с
течением заболеваний коронарных артерий [128].
Другие гипотензивные препараты
Тиазидные диуретики приводили к повышению нейрональной NOсинтазы в
maculae densa и эндотелиальной NOсинтазы в почечных сосудах в экспериментальной
модели DOCAсолевой АГ у крыс, вызванной введением дезоксикортикостерона и
хлорида натрия [139].
Индапамид, помимо диуретического действия оказывает прямое
вазодилатирующее действие за счет своих антиоксидантных свойств, повышая
биодоступность NO, уменьшая его разрушение. Комбинированное лечение небольшими
дозами иАПФ (периндоприла) и индапамида сопровождалось увеличением базального
освобождения NO [140,141,142].
Доксазозин в экспериментальных исследованиях вызывал
эндотелийзависимую вазодилатацию, увеличивая NO через антиоксидантный эффект
[143,144].
Гормонозамещающая терапия у женщин в постменопаузе
В постменопаузе повышается риск возникновения артериальной гипертензии.
У женщин 4554 лет, страдающих климактерическим синдромом, увеличивается
частота АГ до 52,4% [145150]. Предполагают, что женские половые гормоны
играют важную роль в защите эндотелия [146158]. В экспериментах на животных и в
клинических исследованиях подтверждено, что уменьшение эстрогенов приводит к
дисфункции эндотелия [151]. Доказаны положительные эффекты эстрогенов на
эндотелиальную функцию: посредством коррекции липидного спектра крови,
увеличения ЛПВП и уменьшения ЛПНП [150]; улучшения ацетилхолиновой сосудистой
реактивности [151], в том числе в коронарных артериях у женщин с начальными
признаками ИБС; cтимуляции активности NO синтазы [152]; увеличения базального
уровня NO [153,154,155]. Однако в литературе имеются неоднозначные данные о
клинической эффективности гормонозамещающей терапии (ГЗТ). Проспективное
рандомизированное контролируемое клиническое исследование HERS
(Heart and Estrogen/Progestin Replacement Study) показало, что антиишемический
эффект эстрогенов связан с улучшением эндотелиальной функции и активацией
синтеза эндотелием простациклина [154]. Однако исследование не доказало
благоприятного влияния ГЗТ на первичную профилактику ИБС. Эти результаты
частично можно объяснить эффектами прогестерона, который поражает
эндотелийзависимую вазодилатацию коронарных артерий [155,156]. Несмотря на то,
что эстрогены проявляют ряд эндотелийзависимых эффектов, связанных с
вазодилатацией и NO, известно также их протромботическое и провоспалительное
действие, что может нейтрализовать другие положительные эффекты [157]. Таким
образом, необходимо дальнейшее подтверждение благоприятного действия эстрогенов
в профилактике кардиоваскулярных заболеваний у женщин в постменопаузе. В 2004
будут представлены результаты мультицентрового, плацебоконтролируемого, двойного,
слепого, ангиографического исследования The Womens Health Initiative
NIHsponsored, изучающего влияние эстрогенов на атеросклероз коронарных
артерий и кардиоваскулярных заболеваний с помощью ГЗТ [158]. В настоящее время в
мире проводится ряд исследований по вторичной профилактике ИБС у женщин, по
результатам которых можно будет сделать более определенные выводы по данной
проблеме.
Заключение
Таким образом, в настоящее время происходит накопление новых данных о
специфических механизмах эндотелиальной дисфункции при АГ. Происходит дополнение
и переосмысление действия традиционных гипотензивных препаратов с точки зрения
воздействия на эндотелий, раскрываются механизмы вазопротективного и
органопротективного действия кардиоваскулярных препаратов за счет модуляции
продукции NO. Все это открывает новые терапевтические горизонты, формирует новые
терапевтические мишени при различных кардиоваскулярных заболеваниях в том числе
артериальной гипертонии.
Литература:
1. Furchgott RF., Zawadzki JV. The obligatory role of endothelial cells in the
relaxation of arterial smooth muscle by acetylcholine. Nature 1980; 288: 373–376
2. Moncada S., Palmer R.M., Higgs E.A. The discovery of nitric oxide as the
endogenous nitrovasodilator. Hypertension 1988 Oct;12(4):36572
3. Luscher T.F., Noll.G. The pathogenesis of cardiovascular disease: role of
the endothelium as a target and mediator. Atherosclerosis 1995 Dec;118
Suppl:S8190
4. Luscher T.F., Barton M. Biology of the endothelium. Clin Cardiol 1997
Nov;20(11 Suppl 2):II310
5. Boulanger C., Vanhoutte P.M. [The role of the endothelium in the
regulation of vasomotor activity]. Arch Mal Coeur Vaiss 1991 Jan; 84 Spec No
1:3544
6. Rongen G.A, Smits P, Thien T. Endothelium and the regulation of vascular
tone with emphasis on the role of nitric oxide. Physiology, pathophysiology and
clinical implications. Neth J Med 1994 Jan;44(1):2635
7. Haller H. Endothelial function. General considerations. Drugs 1997;53
Suppl 1:110
8. Schiffrin E.L. The endothelium of resistance arteries: physiology and role
in hypertension.Prostaglandins Leukot Essent Fatty Acids 1996 Jan;54(1):1725
9. Carl J.Pepine, David S. Celermajer, Helmut Drexler Vascular health as a
therapeutic tagert in cardiovascular disease. University of Florida, 1998
10. JeanBaptiste Michel NO (Nitric oxide) and Cardiovascular Homeostasis 1999
Menarini International Industrie Farmaceutiche Riunite s.r.l. Paris
11. Luscher T.F. Endothelial control of vascular tone and growth. Clin Exp
Hypertens [A] 1990;12(5):897902
12. Luscher T.F. Endotheliumderived vasoactive factors and regulation of
vascular tone in human blood vessels. Lung 1990;168 Suppl:2734
13. Nagao T., Vanhoutte P.M. Endotheliumderived hyperpolarizing factor and
endotheliumdependent relaxations. Am J Respir Cell Mol Biol 1993 Jan;8(1):16
14. Palmer RMJ., Ferrige AG., Moncada S. Nitric oxide release accounts for
the biological activity of endotheliumderived relaxing factor. Nature.
1987;327:524526
15. Cooke J., Tsao P. Is nitric oxide an endogenous antiatherogenic molecule?
Arterioscler Thromb. 1994; 14: 653655
16. Grag UC., Hassid A. Nitric oxide generating vasodilators and 8bromocyclic
guanosine monophosphate inhibit mitogenesis and proliferation of cultured rat
vascular smooth muscle cells. J Clin Invest. 1989; 83:17741777
17. Luscher TF., Wenzel RR, Noll G. Local regulation of the coronary
circulation in health and disease: role of nitric oxide and endothelin Eur Heart
J 1995 May;16 Suppl C:518
18. Faraci FM., Heistad D.D. Regulation of the cerebral circulation: role of
endothelium and potassium channels. Physiol Rev 1998 Jan;78(1):5397
19. Tiritilli A Nitric oxide (NO), vascular protection factor. Biology,
physiological role and biochemistry of NO. Presse Med 1998 Jun 13;27(21):10614
20. Roland Govers and Ton J. Rabelink Cellular regulation of endothelial
nitric oxide synthase Am. J. Physiol. February 2001. 280: Vol. 280, Issue 2,
F193F206
21. Baylis C., Vallance P. Nitric oxide and blood pressure: effects of nitric
oxide deficiency. Curr Opin Nephrol Hypertens 1996 Jan;5(1):808
22. Ignarro LJ. Endotheliumderived nitric oxide: actions and properties,
FASEB J 1989 Jan;3(1):316
23. Moncada S., Palmer RM., Higgs EA. The discovery of nitric oxide as the
endogenous nitrovasodilator. Hypertension 1988 Oct;12(4):36572
24. Lin PJ., Chang CH. Endothelium dysfunction in cardiovascular diseases.
Chang Keng I Hsueh 1994 Sep;17(3):198210
25. Faraci FM., Heistad DD. Physiol Regulation of the cerebral circulation:
role of endothelium and potassium channels. Rev 1998 Jan;78(1):5397
26. Luscher T.F., Vanhoutte P.M. In: The endothelium: modulator of
cardiovascular function. Boca Raton, FL: CRC Press; 1990
27. Tschudi MR., Luscher TF. Nitric oxide: the endogenous nitrate in the
cardiovascular system Herz 1996 Jun;21 Suppl 1:5060
28. Luscher TF. Endotheliumderived nitric oxide: the endogenous
nitrovasodilator in the human cardiovascular system. Eur Heart J 1991 Nov;12
Suppl E:211
29. Palmer RMJ, Ashton DS., Moncada S. Vascular endothelial cells synthesize
nitric oxide from Larginine. Nature. 1988;333:664666
30. Moncada S., Higgs A., Furchott RE. XIV Inernational union of pharmacology
nomenclature in nitric oxide research. Phatmacol Rev 1997;49:137142
31. Boulanger CM. Endothelial NO synthase C R Seances Soc Biol Fil
1995;189(6):106979
32. Kader KN., Akella R., Ziats NP., Lakey LA., Harasaki H., Ranieri JP.,
Bellamkonda RV. eNOSoverexpressing endothelial cells inhibit platelet
aggregation and smooth muscle cell proliferation in vitro. Tissue Eng 2000 Jun;
6(3):24151
33. Kibbe M., Billiar T., Tzeng E. Inducible nitric oxide synthase and
vascular injury. Cardiovasc Res 1999 Aug 15;43(3): 6507
34. Rapoport RM., Draznin MB., Murad F. Endotheliumdependent relaxation in
rat aorta may be mediated through cyclic GMFdependent protein phosphorylation.
Nature 1983; 306: 174176
35. Busse R. Luckhoff A., Bassenge E. Endotheliumderived relaxing factor
inhibits platelet activation. NaunynSchmiedebergs Arch Pharmacol 1987; 336:
562566
36. Tiritilli A. Nitric oxide (NO), vascular protection factor. Biology,
physiological role and biochemistry of NO. Presse Med 1998 Jun 13;27(21):10614
37. Vanhoutte PM. Endothelial dysfunction in hypertension J Hypertens Suppl
1996 Dec;14(5):S8393
38. Gardiner SM., Compton AM., Bennet T., Palmer RMJ., Moncada S. Control of
regional blood flow by endotheliumderived nitric oxide. Hypertension 1990; 15:
486492
39. Panza JA. Endothelial dysfunction in essential hypertension. Clin Cardiol
1997 Nov;20(11 Suppl 2):II2633
40. Panza JA., Casino PR., Kilcoyne CM., Quyyumi AA. Role of
endotheliumderived nitric oxide in the abnormal endotheliumdependent vascular
relaxation of patients with essential hypertension Circulation. 1993; 87:
14681474
41. Noll G., Tschudi M., Nava E., Luscher TF. Endothelium and high blood
pressure. Int J Microcirc Clin Exp 1997 Oct;17(5):2739
42. Vanhoutte PM., Boulanger CM. Endotheliumdependent responses in
hypertension. Hypertens Res 1995 Jun;18(2):8798
43. Vanhoutte PM., Boulanger CM. Endotheliumdependent responses in
hypertension. Hypertens Res 1995 Jun;18(2):8798
44. Luscher TF., Boulanger CM., Dohi Y., Yang ZH. Endotheliumderived
contracting factors. Hypertension 1992 Feb;19(2):11730
45. Luscher T.F., Noll G. The pathogenesis of cardiovascular disease: role of
the endothelium as a target and mediator. Atherosclerosis 1995 Dec;118
Suppl:S8190
46. Van Zwieten PA. Endothelial dysfunction in hypertension. A critical
evaluation. Blood Press Suppl 1997;2:6770
47. Shimokawa H. Endothelial dysfunction in hypertension. J Atheroscler
Thromb 1998;4(3):11827
48. Taddei S., Salvetti A. Pathogenetic factors in hypertension. Endothelial
factors. Clin Exp Hypertens 1996 AprMay;18(34):32335
49. Taddei S., Virdis A., Ghiadoni L., Salvetti A. The role of endothelium in
human hypertension Curr Opin Nephrol Hypertens 1998 Mar;7(2):2039
50. Arnal JF., Michel JB., Harrison DG. Nitric oxide in the pathogenesis of
hypertension. Curr Opin Nephrol Hypertens 1995 Mar;4(2):1828
51. Linder L., Kiowski W., Buhler FR., Luscher TF. Indirect evidence for
release of endotheliumderived relaxing factor in human forearm circulation in
vivo: blunted response in essential hypertension. Circulation. 1990;81:17621767
52. Panza JA., Quyyumi AA., Brush JE., Epstein SE. Abnormal
endotheliumdependent vascular relaxation in patients with essential
hypertension. N Engl J Med. 1990;323:2227
53. Lyons D., Webster J., Benjamin N. The effect of antihypertensive therapy
on responsiveness to local intrarterial NGmonomethylLarginine in patients with
essential hypertension. J Hypertens. 1994;12:10471053
54. Taddei S., Virdis A., Mattei P., Salvetti A. Vasodilation to
acetylcholine in primary and secondary forms of hypertension. Hypertension.
1993;21:929933
55. Rizzoni D., Porteri E., Castellano M., Bettoni G., Muiesan ML., Tiberio
G., Giulini SM., Rossi GP., Bernini G., AgabitiRosei E. Endothelial dysfunction
in hypertension is independent from the etiology and from vascular structure.
Hypertension. 1998;31(pt 2):335341.
56. Dzau VJ., Gibbon GN. Endothelium and growth factors in vascular
remodeling of hypertension. Hypertension. 1991; 18 (suppl III): III 115III121
57. Gibbons GH., Dzau VJ. The emerging concept of vascular remodeling. N Engl
J Med.1994;330:14311438
58. Naruse M., Tanabe A., Takagi S., Tago K., Takano K. Insulin resistance
and vascular function. Nippon Rinsho 2000 Feb;58(2):3447
59. Lippincott William et al. Insulin, nitric oxide and sympathetic nervous
system: at the crossroad of metabolic and cardiovascular regulation Hypertension
1999;17:15171525
60. Cleland SJ., Petrie JR., Ueda S., Elliott HL., Connell JM. Insulin as a
vascular hormone: implications for the pathophysiology of cardiovascular disease
Clin Exp Pharmacol Physiol 1998 MarApr;25(34):17584
61. JC Stoclet., A Kleschyov., B Muller., C Lugnier. New insights into the
role of nitric oxide in cardiovascular protection. Exp Clin Cardiol
1997;2(2):9397
62. Kuboki K., Jiang ZY., Takahara N., Ha SW., Igarashi M., Yamauchi T.,
Feener EP., Herbert TP., Rhodes CJ., King GL. Regulation of endothelial
constitutive nitric oxide synthase gene expression in endothelial cells and in
vivo: a specific vascular action of insulin. Circulation 2000 Feb
15;101(6):67681
63. Shoemaker JK., Bonen A. Vascular actions of insulin in health and
disease. Can J Appl Physiol 1995 Jun;20(2):12754
64. Hsueh WA., Law RE. Insulin signaling in the arterial wall Am J Cardiol
1999 Jul 8;84 (1A):21J24J
65. Panza JA. Endothelial dysfunction in essential hypertension. Clin Cardiol
1997 Nov;20 (11 Suppl 2):II2633
66. Luscher TF., Noll G. Endothelial function as an endpoint in
interventional trials: concepts, methods and current data. Hypertens Suppl 1996
Sep;14(2):1119
67. Quyyumi AA. Endothelial function in health and disease: new insights into
the genesis of cardiovascular disease. Am J Med 1998 Jul 6;105(1A):3239
68. Simon A., Castro A., Kaski JC. Assessment of endothelial dysfunction and
its clinical usefulness.Rev Esp Cardiol 2001 Feb;54(2):2117
69. Allison A. Brown., Frank B Hu Dietary modulation of endothelial
function:implications for cardiovascular disease. American Journal of Clinical
Nutrition, 2001; 73 №4 673686.
70. Roberts CK, Vaziri ND, Wang XQ, Barnard RJ Enhanced NO inactivation and
hypertension induced by a highfat, refinedcarbohydrate diet.Hypertension 2000
Sep; 36(3) 4239
71. Kataoka H., Otsuka F., Ogura T., Yamauchi T., Kishida M., Takahashi M.,
Mimura Y., Makino The role of nitric oxide and the reninangiotensin system in
saltrestricted Dahl rats. H Am J Hypertens 2001 Mar;14(3):27685
72. Fujiwara N., Osanai T., Kamada T., Katoh T., Takahashi K., Okumura K.
Study on the relationship between plasma nitrite and nitrate level and salt
sensitivity in human hypertension: modulation of nitric oxide synthesis by salt
intake Circulation 2000 Feb 29;101(8):85661
73. Kingwell BA. Nitric oxidemediated metabolic regulation during exercise:
effects of training in health and cardiovascular disease. FASEB J 2000
Sep;14(12):168596
74. Yukihito Higashi., Shota Sasaki., Satoshi Kurisu., Atsunori Yoshimizu.,
Nobuo Sasaki., Hideo Matsuura., Goro Kajiyama., Tetsuya Oshima Regular Aerobic
Exercise Augments EndotheliumDependent Vascular Relaxation in Normotensive As
Well As Hypertensive Subjects Role of EndotheliumDerived Nitric Oxide Exercise
Relaxation Circulation. 1999;100:11941202.
75. Tohru Fukai, Martin R. Siegfried, Masuko UshioFukai, Yian Cheng, Georg
Kojda and David G. Harrison Regulation of the vascular extracellular superoxide
dismutase by nitric oxide and exercise training J Clin Invest, June 2000, Volume
105, Number 11, 16311639
76. Roxana Campisi, Johannes Czernin, Heiko Schoder, James W. Sayre, Fernando
D. Marengo, Michael E. Phelps, Heinrich R. Schelbert Effects of Longterm Smoking
on Myocardial Blood Flow, Coronary Vasomotion, and Vasodilator Capacity
Circulation 1998;98:119125
77. Roxana Campisi, Johannes Czernin, Heiko Schoder, James W. Sayre, Heinrich
R. Schelbert LArginine Normalizes Coronary Vasomotion in LongTerm Smokers
Circulation. 1999; 99:491497
78. Thomas Heitzer, Seppo YlaHerttuala, Jukka Luoma, Sabine Kurz, Thomas
Munzel, Hanjorg Just, Manfred Olschewski, Helmut Drexler Cigarette Smoking
Potentiates EndothelialDysfunction of Forearm Resistance Vessels in Patients
With Hypercholesterolemia Role of Oxidized LDL Circulation 1996;93:13461353
79. Celermajer DS., Sorensen KE,. Georgakopoulos D., et al. Cigarette smoking
is associated with doserelated and potentially reversible impairment of
endotheliumdependent dilation in healthy young adults. Circulation.
1993;88:21492155
80. Stuart J. Hutchison; Krishnankutty Sudhir; Richard E. Sievers; BoQing
Zhu;YiPing Sun; Tony M. Chou; Kanu Chatterjee; Prakash C. Deedwania;John P.
Cooke; Stanton A. Glantz; William W. Parmley Effects of LArginine on
Atherogenesis and Endothelial Dysfunction due to Secondhand Smoke Hypertension
1999; 34:4450
81. Scholkens B.A., Unger T. ACE Inhibitors, Endothelial function and
Atherosclerosis. Amsterdam Media Medica Publications. March 1993
82. Ulfendahl H.R., Aurell M. ReninAngiotensin/ Portland Press/ London. 1998
p.305
83. Bonner G., Preis S., Schunck U et al. Hemodynamic effects of bradykinin
on systemic and pulmonary circulation in healthy and hypertensive humans. J
Cardiovasc Pharmacol 1990;15 (suppl 6): 4656.
84. Busse R. Lamontagne D. Endotheliumderived bradykinin is responsible for
the increase in calcium produced by angiotensinconverting enzyme inhibitors in
human endothelial cells. NaunynSchmiedebergs Arch Pharmacol 1991;344:126129
85. AlhencGelas F., Tsai SJ., Callahan KS. et al., Stimulation of
prostaglandin formation by vasoactive mediators in cultured human endothelial
cells. Basic Res Cardiol 1982; 24:723742.
86. Griendling K.K., Minieri C.A., Ollerenshaw J.D. and Alexander R.W.
Angiotensin II stimulates NADH and NADPH oxidase activity in cultured vascular
smooth muscle cells. Circ. Res.1994;74:11411148
87. Pitt B., Pepine C., oNeill B., Haber H., Pressler M., Mancini GBJ.
Modulation of ACE inhibitor efficacy on coronary endothelial dysfunction by low
density lipoprotein cholesterol. J Am Coll Cardiol. 1997; 29 (2, suppl A):70A.
Abstract 7145
88. Clozel M., Kuhn H., Hefti F. Effects of angiotensin converting enzyme
inhibitors and of hydralazine on endothelial function in hypertensive rats.
Hypertension. 1990;16:532540.
89. Clozel M. Mechanism of action of angiotensin converting enzyme inhibitors
on endothelial function in hypertension. Hypertension 1991; 18:3742.
90. Creager MA., Roddy MA. Effects of captopril and enalapril on endothelial
function in hypertensive patients. Hypertension. 1994;24:499505.
91. Berkenboom G., Langer I., Carpentier Y., Grosfils K., Fontaine J.
Ramipril prevents endothelial dysfunction induced by oxidized lowdensity
lipoproteins. Hypertension.1997;30:371376
92. Prasad A., Husain S., Mincemoyer R., Panza A., Cannon RO., Quyyumi AA.
Coronary endothelial dysfunction in humans improves with angiotensin converting
inhibition. Circulation. 1996; 94 (8 supl I): I61. Abstract 348
93. Anderson TJ., Overhiser RW., Haber H., Charbonneau F.A. comparitive study
of four antihypertensive agents on endothelial function in patients with
coronary disease. J. Am Coll Cardiol. 1998;31 (2, suppl A):327A. Abstract.
94. Mancini GBJ., Henry Gc., Macaya C., et al. Angiotensinconverting enzyme
inhibition with quinapril improves endothelial vasomotor dysfunction in patients
with coronary artery disease: the TREND (Trial on Reversing Endothelial
Dysfunction) Study. Circulation.1996; 94:258265
95. Whitebread S., Mele M., Kamber B., de Gasparo M. Preliminary biochemical
characterization of two angiotension II receptor subtypes. Biochemic. Biophys.
Res. Commun. 1989; 163: 284291.
96. Chiu A.T., Herblin W.F., McCall D.E., Ardecky R.J., Duncia J.V., Pease
L.J., Wong P.C., Wexler R.R., Johnson A.L., Timmermans P. Identification of
angiotensin II receptor subtypes. Biochemic. Biophys. Res. Commun. 1989; 165:
196203.
97. Nakajima M.,Hutchinson H., Morishita R., Hayashida W., Zhang L.,Horiuchi
M.,Pratt R.E., Dzau V.J. The angiotensin II type 2 (AT2) receptor antagonizes
the growth effects ofthe AT1 receptor: Gain of functionstudy using in vivo gene
transfer. Proc.Natl.Acad.Sci.U.S.A.1995; 92: 1066310667.
98. Stoll M., Steckelings M., Paul M., Bottari S.R., Metzger R., Unger T. The
angiotensin AT2receptor mediates inhibition of cell proliferation in coronary
endothelial cells. J.Clin. Invest.1995; 95: 651657.
99. Booz G.W., Baker K.M. Role of type 1 and type 2 angiotensin receptors in
angiotensin IIinduced cardiomyocyte hypertrophy. Hypertension. 1996; 28: 635640.
100. Ford W.R., Clanachen A.S., Jugdutt B.I. Opposite effect of angiotensin
AT1 and AT2 receptor antagonists on recovery of mechanical function after
ischemiareperfusion in isolated working rat heats. Circulation. 1996; 94:
30873089
101. Gohlke P., Pees C., Unger T. AT2receptor stimulation increases aortic
cyclic GMP in SHRSP by a kinindependent mechanisms. Hypertension. 1998;
3:349355.
102. Chung O., Unger T. Angiotensin II receptor blockade and end organ
protection. Amer. J. Hypertension. 1999; 12: 150156
103. Robert M. Carey; ZhiQin Wang; Helmy M. Siragy Role of the Angiotensin
Type 2 Receptor in the Regulation of Blood Pressure and RenalFunction
Hypertension. 2000;35:15
104. Gohlke P., Zinz W., Scholkens B.A. et al. Cardiac and vascular effects
of longterm losartan treatment in strokeprone spontaneously hypertensive rats.
Hypertension. 1996; 28: 397402.
105. Welch WJ., Wilcox CS. receptor antagonist combats oxidative stress and
restores nitric oxide signaling in the SHR. Kidney Int 2001 Apr;59(4):125763
106. Qadri F., Arens T., Schwartz EC., Hauser W., Dominiak P.
Angiotensinconverting enzyme inhibitors and AT1receptor antagonist restore
nitric oxide synthase (NOS) activity and neuronal NOS expression in the adrenal
glands of spontaneously hypertensive rats Jpn J Pharmacol 2001 Apr;85(4):3659.
107. Ernesto L. Schiffrin, Jeong Bae Park, Rhian M. Touyz, Correction of
Arterial Structure and Endothelial Dysfunction in Human Essential Hypertension
by the Angiotensin Receptor Antagonist Losartan Circulation. 2000;101:1653.
108. Е.П. Свищенко, Н.М. Гулая, Л.В. Безродная, В.В. Коцеруба, В.В. Радченко,
Л.А. Мищенко, Е.А. Матова Влияние ирбесартана на суточный ритм артериального
давления и состояние системы оксида азота Институт кардиологии им. Н.Д.Стражеско
АМН Украины, Институт биохимии им. А.В. Палладина НАН Украины, г. Киев
(интернет)
109. Li P., Fukuhara M., Diz DI., Ferrario CM., Brosnihan KB. Novel
angiotensin II AT(1) receptor antagonist irbesartan prevents thromboxane
A(2)induced vasoconstriction in canine coronary arteries and human platelet
aggregation. J Pharmacol Exp Ther 2000 Jan;292(1):23846
110. Lorenzo Ghiadoni; Agostino Virdis; Armando Magagna; Stefano Taddei;
Antonio Salvetti Effect of the Angiotensin II Type 1 Receptor Blocker
Candesartan on Endothelial Function in Patients With Essential Hypertension
Hypertension. 2000; 35:501
111. Siragy HM, de Gasparo M, Carey RM Angiotensin type 2 receptor mediates
valsartaninduced hypotension in conscious rats. Hypertension 2000 May; 35(5):
10747.
112. Ledingham JM., Laverty R. Basilar artery remodelling in the genetically
hypertensive rat: effects of nitric oxide synthase inhibition and treatment with
valsartan and enalapril. Clin Exp Pharmacol Physiol 2000 Aug;27(8):6426
113. Habib JB., Bossaller C., Wells S., Williams C., Morrisett JD., Henry
PD.. Preservation of endotheliumdepent vascular relaxation in cholesterolfed
rabbit by treatment with the calcium blocker PN 200110. Circ Res 1986; 58:3059
114. Nakayama N., Ikezono K., Ohura M., Yabuuchi Y. Effects of the new
longacting dihydropyridine calcium antagonist pranidipine on the
endotheliumdependent relaxation in isolated rat aorta in vitro.
Arzneimittelforschung. 1993;43:12661270
115. Dohi Y., Criscione L., Pfeiffer K., Luscher TF. Angiotensin blockade or
calcium antagonists improve endothelial dysfunction in hypertension: studies in
perfused mesenteric resistence arteries. J. Cardiovasc Pharmacol 1994; 24:3729
116. Novosel D., Lang MG., Noll G., Luscher TF. Endothelial dysfunction in
aorta of spontaneously hypertensive, strokeprone rat: effects of therapy with
verapamil and trandolapril alone and in combination. J. Cardiovasc Pharmacol
1994; 24:97985
117. Takase H., Moreau P., Kung CF., Nava E.,Luscher TF. Antihypertensive
therapy prevents endothelial dysfunction in chronic nitric oxide deficiency.
Effect of verapamil and trandolapril. Hypertension 1996; 27:2531
118. Zhang X., Hintze TH. Amlodipine releases nitric oxide from canine
coronary microvessels: an unexpected mechanism of action of a calcium
channelblocking agent. Circulation. 1998;97:576580
119. Kishi Y., Watanabe T., Makita T., Sakita S., Watanabe R., Ashikaga T.,
Numano F. Effect of nifedipine on cyclic GMP turnover in cultured coronary
smooth muscle cells. J Cardiovasc Pharmacol. 1995;26:590595.
120. Yaoxian Ding, Nosratola D. Vaziri Calcium Channel Blockade Enhances
Nitric Oxide Synthase Expression by Cultured Endothelial Cells Hypertension.
1998; 32:718723
121. Ding, Y., Vaziri, N. D. Nifedipine and Diltiazem but Not Verapamil
UpRegulate Endothelial NitricOxide Synthase Expression. J. Pharmacol. Exp. Ther.
2000; 292: 606609
122. Xiu Q. Wang; Nosratola D. Vaziri Erythropoietin Depresses Nitric Oxide
Synthase Expression by Human Endothelial Cells Hypertension. 1999;33:894899
123. Maria Lorenza Muiesan; Massimo Salvetti; Cristina Monteduro; Damiano
Rizzoni; Roberto Zulli; Claudia Corbellini; Claudia Brun; Enrico AgabitiRosei
Effect of Treatment on FlowDependent Vasodilation of the Brachial Artery in
Essential Hypertension Hypertension. 1999; 33:575580
124. Berkels R., Egink G., Marsen TA. Bartels H., Roesen R., Klaus W.
Nifedipine increases endothelial nitric oxide bioavailability by antioxidative
mechanisms. Hypertension 2001; Feb;37(2):2405
125. Taddei S., Virdis A., Ghiadoni L., Uleri S., Magagna A., Salvetti S.
Lacidipine restores endotheliumdependent vasodilation in essential hypertensive
patients. Hypertension. 1997; 30:16061612.
126. Krenek, P., Salomone, S., Kyselovic, J., Wibo, M., Morel, N., Godfraind,
T. Lacidipine Prevents Endothelial Dysfunction in SaltLoaded StrokeProne
Hypertensive Rats. Hypertension 2001; 37: 11241128
127. Jin Yang; Keisuke Fukuo; Shigeto Morimoto; Tadaaki Niinobu; Toshimitsu
Suhara; Toshio Ogihara Pranidipine Enhances the Action of Nitric Oxide Released
From Endothelial Cells Hypertension. 2000; 35:82
128. Luscher T.F. (Endothelial dysfunction as a therapeutic target) The
ENCORE trials Euuropean Heart J Supplements 2000; 2 (Supplement D), D2025
129. Cherchi A. et al. Antianginal and antiischemic activity of nebivolol in
stable angina of effort. Drug Invest 1991; 3:Suppl 1:8698
130. Ruf G. et al. Determination of the antiischemic activity of nebivolol in
comparison with atenolol. Int J Cardiol 1994; 43:279285
131. Ulvenstam G. A single blind doseranging study of nebivolol in patients
with angina pectoris/ Drug Invest 1991; Suppl 1:199200
132. Gao YS., Nagao T., Bond RA., Janssens WJ., Vanhoutte PM. Nebivolol
induces endotheliumdependent relaxations of canine coronary arteries J
Cardiovasc Pharmacol 1991; Jun;17(6):9649
133. Cockcroft J.R., Chowienczyk P.J., Brett S.E.,Chen, Dupont A.G.,VanNueten,
L.Wooding S.J.,Ritter J.M. Nebivolol vasodilates human forearm vasculature:
evidence for an Larginine/NOdependent mechanism. J Pharmacol. Experimental
Therapeutics 1995; 274:106771
134. Parenti A., Filippi S., Amerini S., Granger HJ., Fazzini A., Ledda F.
Inositol phosphate metabolism and nitricoxide synthase activity in endothelial
cells are involved in the vasorelaxant activity of nebivolol. J Pharmacol Exp
Ther 2000; Feb;292(2):698703
135. Bowman AJ., Chen CP., Ford GA. Br Nitric oxide mediated venodilator
effects of nebivolol. J Clin Pharmacol 1994; Sep;38(3):199204
136. Dawes M., Brett SE., Chowienczyk PJ., Mant TG., Ritter JM. The
vasodilator action of nebivolol in forearm vasculature of subjects with
essential hypertension. Br J Clin Pharmacol 1999; Sep;48(3):4603
137. Broeders MA., Doevendans PA., Bekkers BC., Bronsaer R., van Gorsel E.,
Heemskerk JW., Egbrink MG., van Breda E., Reneman RS. van Der Zee R Nebivolol: a
thirdgeneration betablocker that augments vascular nitric oxide release:
endothelial beta(2)adrenergic receptormediated nitric oxide production.
Circulation 2000; Aug 8;102(6):67784
138. Troost R., Schwedhelm E., Rojczyk S., Tsikas D., Frolich JC. Nebivolol
decreases systemic oxidative stress in healthy volunteers. Br J Clin Pharmacol.
2000; Oct;50(4):3779
139. Ono Y., Ono H., Frohlich E.D. Hydrochlorothiazide exacerbates nitric
oxideblockade nephrosclerosis with glomerular hypertension in spontaneously
hypertensive rats. J Hypertens 1996 Jul;14(7):8238
140. Schini VB., Dewey J., Vanhoutte PM. Related Effects of indapamide on
endotheliumdependent relaxations in isolated canine femoral arteries. Am J
Cardiol 1990 May 2;65(17):6H10H
141. Junquero DC., Schini VB., Vanhoutte PM. Indapamide potentiates the
endotheliumdependent production of cyclic guanosine monophosphate by bradykinin
in the canine femoral artery. Am Heart J 1991 Oct;122(4 Pt 2):12049
142. Richard V., Joannides R., Henry JP., Mulder P., Mace B., Guez D.,
Schiavi P., Thuillez C. Fixeddose combination of perindopril with indapamide in
spontaneously hypertensive rats: haemodynamic, biological and structural
effects. J Hypertens 1996 Dec;14(12):144754
143. Swindell AC., Valentine JJ. Effects of doxazosin on dietinduced
hypercholesterolemia in C57BR/cdJ mice. Am J Cardiol 1987 May 29;59(14):29G34G
144. Yeates RA Rela Influence of doxazosin on the activity of the
endotheliumderived relaxing factor. Arzneimittelforschung 1994 Oct;44(10):111721
145. Kuller L.H., Matthews K.A., SuttonTyrrel K. et al. Coronary and aortic
calcification among women 8 years after menopause and their premenopausal risk
factors: the healthy women study. Artherioscler. Thromb. Vasc. Biol. 1999;19:
218998.
146. Кириченко А.А., Новичкова Ю.Н., Никулина Ж.С., Оганесян К.О., Сметник
В.П. Влияние терапии ливиалом на сердечнососудистую систему и липидный спектр
крови в постменопаузе. Русский медицинский журнал 2001, том 9, № 9 (128): 377381
147. Rilwan A., Ross A., Cooper A., et al. Oral and transdermal oestrogens
reduse impedance to blood flow equally in the cerebral circulation of
postmenopausal women. IV European Congress on Menopause, Vienna, Austria, 1997,
12
148. Stampfer MJ., Colditz GA., Willett WC., et al Postmenopausal estrogen
therapy and cardiovascular disease: tenyear followup from the NursesHealth
Study. N Engl J Med.1991; 325:756762
149. Marie Gerhard, Brian W. Walsh, Ahmed Tawakol, Elizabeth A. Haley, BA;
Shelly J. Creager, BSN; Ellen W. Seely, MD; Peter Ganz, Mark A. Creage.
Estradiol Therapy Combined With Progesterone and EndotheliumDependent
Vasodilation in Postmenopausal Women. Circulation. 1998;98:11581163
150. Hartmut Kleinert; Thomas Wallerath; Christian Euchenhofer; Irmgard
IhrigBiedert; Huige Li. Ulrich Forstermann Estrogens Increase Transcription of
the Human Endothelial NO Synthase Gene Analysis of the Transcription Factors
Involved Hypertension. 1998; 31:582588.
151. Guetta V., Quyyumi AA., Prasad A et al. The role of nitric oxide in
coronary vascular effects of estrogen in postmenopausal women. Circulation 1997;
96:2795801
152. Pernille Holm, Heidi L. Andersen, Malene R. Andersen, Elisabeth
Erhardtsen, Steen Stender The Direct Antiatherogenic Effect of Estrogen Is
Present, Absent, or Reversed, Depending on the State of the Arterial Endothelium
A Time Course Study in CholesterolClamped Rabbits Circulation. 1999;
100:17271733
153. George B. Stefano, Vincent Prevot, JeanClaude Beauvillain, Patrick
Cadet, Caterina Fimiani, Ingeborg Welters, Gregory L. Fricchione, Christophe
Breton, Philippe Lassalle, Michel Salzet, Thomas V. Bilfinger CellSurface
Estrogen Receptors Mediate CalciumDependent Nitric Oxide Release in Human
Endothelia. Circulation. 2000; 101:1594
154. Auer J., Berent R., Mayr H., Kirchgatterer A., Eber B Abteilung [Antiischemia
effect of estrogens]. [Article in German] Z Kardiol 2000; May;89(5):43441
155. Hulley S., Grady D., Bush T. et al. Randomized trial of estrogen plus
progestin for secondary prevention of coronary artery disease in postmenopausal
women. Heart and Estrogen/progestin Replacement Study (HERS) Research Group. J
Am Med Assoc 1998; 280:60513
156. Herrington D. Role of estrogens, selective estrogen receptor modulators
and phytoestrogens in cardiovascular protection. Can J Cardiol 2000; Aug;16
Suppl E:5E9E
157. Williams JK,. Adams MR. Estrogens, progestins and coronary artery
vasoreactivity. Certain progestins may oppose the favorable effects of estrogen
on the cardiovascular system of postmenopausal women. Nature Med 1997;3:2734
158. Folmar S., OatesWilliams F., Sharp P., Reboussin D., Smith J., Cheshire
K., Macer J., Klein KP., Herrington D. Recruitment of Participants for the
Estrogen Replacement and Atherosclerosis (ERA) Trial. A Comparison of Costs,
Yields, and Participant Characteristics from Community and HospitalBased
Recruitment Strategies. Control Clin Trials 2001; Feb;22(1):1325
Опубликовано с разрешения администрации Русского
Медицинского Журнала.

