Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Хронический гепатит С: клиника, диагностика, лечение
И. Г. Федоров, И. Г. Никитин, доктор медицинских
наук, профессор,
Г. И. Сторожаков, доктор медицинских наук, член-корреспондент РАМН
В настоящее время проблемой хронической HCV-инфекции интересуются как
врачи-специалисты, так и люди, никак не связанные с медициной.
От гепатита С во всем мире страдают по меньшей мере 200 млн человек.
Последствиями перенесенного заболевания могут быть хронический гепатит, цирроз и
первичный рак печени.
Эпидемиология
Распространенность хронической HCV-инфекции на земном шаре варьирует от 0,5
до 2%. Существуют регионы, для которых характерна более высокая
распространенность этого заболевания: 6% в Заире и Саудовской Аравии, 16% в
изолированных поселениях в Японии. В России наблюдается рост заболеваемости
гепатитом С (3,2 на 100 тыс. населения в 1994 году и 19,3 в 1999 году).
Источниками заражения вирусным гепатитом C служат больные острыми и хроническими
формами HCV-инфекции, причем в основном это люди, у которых отсутствует желтуха
и наблюдается бессимптомное или малосимптомное течение заболевания.
В настоящее время HCV чаще всего инфицируются молодые люди, преимущественно
мужчины в возрасте около 20 лет, примерно 40% из них заражаются при внутривенном
введении наркотиков. Основным путем инфицирования HCV является парентеральный.
Так, у 6,1% больных, которым производилось переливание крови и ее компонентов во
время кардиохирургических операций, развивался острый вирусный гепатит C, у 60%
из них гепатит принимал хроническую форму.
Существует и риск заражения гепатитом C половым путем, однако он невелик
(5-8%). Возможна передача HCV от матерей с острой или хронической формой
инфекции; это также редкое явление, встречается не чаще чем в 5-6% случаев. Риск
заражения вышеуказанными путями уступает таковому при гепатите В.
Приблизительно у половины больных путь инфицирования HCV установить не
удается.
Вирус гепатита С
Вирус гепатита С относится к семейству флавивирусов. Геном вируса представлен
однонитевой РНК протяженностью около 10 000 нуклеотидов. Вирус гепатита С
вызывает заболевание только у человека. В экспериментальных условиях
воспроизвести инфекцию можно у высших обезьян.
Популяция вируса неоднородна. Идентифицированы 6 генотипов (классификация по
Simmonds), более 90 субтипов и множество вариантов вируса, обозначаемых как
квазивиды. Зарегистрирована территориальная неравномерность циркуляции генотипов
вируса гепатита С. В России чаще всего выявляются генотипы 1b и 3а этого вируса.
Определение генотипов вируса гепатита С имеет большое значение для
практической медицины. Хотя до сих пор не установлено четкой корреляции между
генотипами и уровнем виремии, характеристиками пациента, тяжестью течения
заболевания, большинство исследователей соглашаются с выводами о значении
генотипов вируса как важного фактора, влияющего на эффективность противовирусной
терапии.
Вакцину против гепатита С создать пока не удалось из-за высокой изменчивости
вируса гепатита С (ВГС).
Патогенез
Считают, что вирус оказывает прямое цитопатическое действие и вызывает
иммуноопосредованное повреждение гепатоцитов. Высокая степень хронизации
вирусного гепатита С обусловлена некоторыми особенностями действия вируса:
- возможностью внепеченочной репликации вируса, включая иммунокомпетентные
клетки (клетки, предшественники гемопоэза, лимфоциты и моноциты периферической
крови, миофибробласты);
- гетерогенностью генотипов и частыми мутациями генома вируса;
- индукцией каскада иммунопатологических реакций;
- активизацией процессов перекисного окисления липидов в печени.
В течении хронической HCV-инфекции может происходить нейтрализация мажорного
варианта вируса, но тогда генерируются минорные варианты. Квазивиды HCV
представляют собой движущуюся мишень, которую ограничивает иммунная система
хозяина. Появление нового мажорного квазивида сопровождается повышением виремии
и увеличением титра Ig M антител к вирусным белкам. Постепенно и этот новый
мажорный вариант заменяется. Такой процесс приводит к периодической
волнообразной виремии, сопровождающейся обострением хронического гепатита С (ХГС)
и повышением уровня антител.
Возможно, антивирусному Т-клеточному ответу отведена центральная роль в
элиминации ВГC, так как нейтрализующие антитела, по-видимому, очень часто
оказываются неэффективными. Т-хелперные (Th) лимфоциты распознают вирусные
антигенные пептиды, представленные HLA-комплексом II класса на поверхностной
мембране антиген-презентирующих клеток. В зависимости от типа цитокинового
профиля Th-клетки делятся на две группы: Th1 и Th2. Первые продуцируют IFNg и
IL2, стимулируя Т-клеточный ответ и цитотоксическую Т-лимфоцитную активность, а
вторые продуцируют IL4 и IL10, стимулируя В-клеточный ответ. Таким образом,
Тh-лимфоциты играют существенную роль в регуляции иммунного ответа. У пациентов,
у которых болезнь перешла в хроническую стадию, в острой фазе
вирус-специфический Th ответ был ниже и преобладали цитокины типа Th2.
У хронически ВГC-инфицированных пациентов значительно увеличено содержание
вирусоспецифических Th2-клеток и их цитокинов. Нарушение баланса Th1/Th2
цитокиновой продукции может играть важную роль в иммунопатогенезе хронической
ВГC-инфекции. Показано снижение уровня IFNg и IL12 при ХГС. Этот дефицит
является следствием повышенного уровня IL10, предполагаемого отрицательного
регулятора для IFNg. Повышенное содержание Th2-клеток при ХГС может снижаться
при комбинированной терапии рибавирином и IFNa. Обнаружено, что у пациентов с
клинико-биохимическим улучшением после лечения IFNa произошло увеличение уровня
Th1-цитокинов.
Цитотоксические лимфоциты (CTL) играют, по-видимому, некоторую роль в
ограничении репликации ВГС. Этот ответ недостаточен для полной элиминации вируса
при хронической инфекции и, кроме того, может вызывать повреждение печени.
Известно, что CTL способны быстро опознавать и направленно лизировать клетки,
несущие ВГC-антигены, не провоцируя значительного воспаления, с помощью
перфоринового, FasL- и TNFα-базируемых механизмов.
ТNF, как предполагается, индуцируют апоптоз клеток, опосредуя высвобождение
свободных радикалов из митохондриальных электронно-транспортных путей и
модуляцию синтеза некоторых белков. Взаимодействие нуклеокапсидного белка ВГC с
внутрицитоплазматической частью рецептора TNFb, вероятно, представляет собой
эволюционно-отобранный механизм, с помощью которого вирус препятствует
преждевременному апоптозу клетки-хозяина. В отсутствие доступных модельных
клеточных культур прямая цитопатичность вируса гепатита С не может быть
исследована в полном объеме.
В подавляющем большинстве случаев острого гепатита С иммунной системе не
удается элиминировать вирус. До сих пор нет ясного представления о том, почему
это происходит. Очевидно, ВГС обладает эволюционно-закрепленными способностями,
обеспечивающими ему персистенцию.
Однако иммунная система может оказывать существенное влияние на ВГC-инфекцию.
В 15% случаев острого гепатита С она эффективно уничтожает вирус, а у хронически
ВГC-инфицированных обеспечивает умеренное ограничение инфекции в течение почти
20 лет. Возможно, ослабление какого-либо звена антивирусных иммунных механизмов
позволяет вирусу активно воздействовать на иммунную систему. Длительная
ВГC-персистенция может привести к развитию В-клеточных лимфопролиферативных
нарушений, таких, как смешанная криоглобулинемия, злокачественная не-Ходжкинская
лимфома и появление органоспецифических и неспецифических аутоантител. Таким
образом, хроническую ВГC-инфекцию следует рассматривать как мультисистемное
заболевание.
Диагностика
Лабораторная диагностика гепатита С основана на выявлении специфических
маркеров инфицирования ВГС (анти-ВГС-IgM/G, РНК ВГС) и должна проводиться
разрешенными МЗ РФ к применению диагностическими препаратами отечественного или
зарубежного производства в лабораториях, имеющих лицензию на проведение данного
вида лабораторных исследований.
HCV RNA — самый ранний маркер репликации вируса, определяемый с помощью
полимеразной цепной реакции (ПЦР) спустя несколько недель после заражения. Для
выявления анти-ВГС применяют иммуноферментный анализ (ИФА). В настоящее время
используют тест-системы третьего поколения ELISA-3. Подтверждающим методом
является рекомбинантный иммуноблотинг (RIBA). У 60% больных анти-ВГС
определяются в острой фазе, у 35% они появляются спустя 3-6 месяцев после
инфицирования, у 5% инфицированных лиц анти-ВГС не определяются.
Болезнь может протекать бессимптомно. Наиболее распространенным симптомом
является слабость. Целенаправленный опрос больных часто помогает выявить такие
факторы риска, как переливание крови, внутривенное введение наркотиков,
хронический гемодиализ и др. Кроме слабости больной может жаловаться на быструю
утомляемость, тяжесть в правом подреберье, боли в правом верхнем квадранте
живота, диспепсические явления.
Критериями постановки диагноза являются увеличение печени и селезенки,
гиперферментемия и анти-ВГС в крови в течение не менее 6 месяцев.
Гепатоспленомегалия выявляется не более чем у 50% обратившихся за помощью
больных, активность сывороточных трансаминаз редко превышает верхнюю границу
нормы в 6 раз. Следует обратить внимание на то, что активность сывороточных
трасаминаз не отражает степени изменений в печени: она может быть нормальной,
несмотря на значительные морфологические изменения. Концентрация РНК ВГС в
сыворотке имеет существенное значение для определения контагиозности и для
мониторинга результатов лечения. При наличии в крови HCV-РНК биопсия печени, как
правило, выявляет ряд изменений. Концентрация HCV-РНК в сыворотке, превышающая
105 молекулярных эквивалентов (копий) в 1 мл, наблюдается в активной фазе
заболевания и совпадает с пиками активности трансаминаз.
Наличие или отсутствие РНК ВГС, как правило, не является диагностическим
критерием хронического гепатита С и определяет фазу процесса (активный,
неактивный).
Для раннего выявления ГЦК у больных циррозом печени, особенно у мужчин старше
40 лет, каждые 6 месяцев определяют уровень сывороточного α-фетопротеина и
выполняют УЗИ печени.
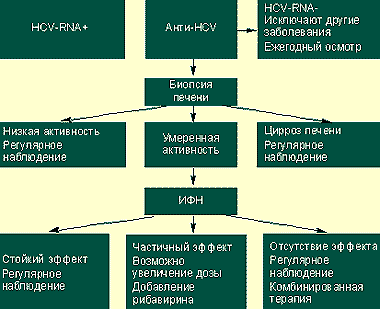
Алгоритм ведения HCV-положительных больных
Естественное течение и прогноз
Инфицирование ВГС приводит к развитию острого гепатита С, протекающего в
манифестной (желтушной) или чаще в латентной (безжелтушной) формах, которые
развиваются в соотношении 1:6. Около 17-25% больных острым гепатитом С
выздоравливают спонтанно, у остальных 75-83% развивается хронический гепатит С.
Большинство больных с биохимическими и иммунологическими признаками хронического
гепатита имеют слабовыраженную или умеренную степень
воспалительно-некротического поражения печени и минимально выраженный фиброз.
Примерно у 26-35% больных хроническим гепатитом С в течение 10-40 лет
развивается фиброз печени и может наступить смерть от цирроза печени и его
осложнений. У 30-40% больных с циррозом печени высок риск заболевания раком
печени.
Считается, что не более чем у 30% больных ВГС с минимальной морфологической
активностью через 20 лет возможно развитие цирроза печени. Таким образом,
больные, у которых при гистологическом исследовании биоптата печени выявляется
наличие минимального воспаления и минимального фиброза, нуждаются в динамическом
наблюдении.
Если персистенция РНК ВГС сохраняется более 6 месяцев, то спонтанное
разрешение хронической HCV-инфекции маловероятно.
Клиническая картина
У большинства больных с хроническим гепатитом С заболевание протекает
бессимптомно. Если жалобы существуют, то это чаще всего слабость, тупые боли в
правом подреберье, тошнота, снижение аппетита, кожный зуд, артралгии и миалгии.
Физикальный осмотр пациента помогает установить диагноз зачастую только на
стадии цирроза печени.
Внепеченочные проявления HCV-инфекции
Ассоциация хронического гепатита С с различными внепеченочными проявлениями —
хорошо известный врачам факт. Наиболее вероятным для большинства заболеваний и
синдромов, наблюдаемых при HCV-инфекции, представляется иммунный патогенез, хотя
конкретные механизмы во многом еще не выяснены. Доказанные и предполагаемые
иммунные механизмы включают:
- моно- или поликлональную пролиферацию лимфоцитов;
- образование аутоантител;
- отложение иммунных комплексов;
- секрецию цитокинов.
Частота иммуноопосредованных заболеваний и синдромов у больных хроническим
гепатитом С достигает 23%. Наиболее характерны аутоиммунные проявления для
больных с гаплотипом HLA DR4, который ассоциируется с внепеченочными
проявлениями при аутоиммунном гепатите. Этот факт подтверждает гипотезу о
триггерной роли вируса в инициации аутоиммунных процессов у генетически
предрасположенного индивидуума.
Заболевания, ассоциированные с HCV-инфекцией
Ассоциированные с продукцией или отложением иммуноглобулинов:
- Криоглобулинемия
- Лейкоцитокластерный васкулит
- Мембранозно-пролиферативный гломерулонефрит
- В-клеточная лимфома
- Плазмоцитома
- MALTома
Аутоиммунные:
- Тиреоидит
- Синдром Шегрена
- Гемолитическая анемия
- Тромбоцитопения
- Красный плоский лишай
Ассоциированные с неизвестным механизмом:
Выявление сывороточных аутоантител отражает наиболее частый феномен
аутоиммунизации при HCV-инфекции, который диагностируют у 40-65% больных. Спектр
аутоантител достаточно широк и включает ANA (до 28%), SMA (до 11%), анти-LKM-1
(до 7%), антифосфолипидные (до 25%), антитиреоидные (до 12,5%), ревматоидный
фактор, анти-ASGP-R и др. Чаще всего титры этих антител не достигают
диагностических значений, показательных для той или иной аутоиммунной патологии.
Анти-GOR являются антителами, специфичными для HCV-инфекции, и их выявляют не
менее чем у 80% больных. Эпитоп, распознаваемый анти-GOR, локализуется на пока
неидентифицированном ядерном белке, гиперэкспрессию которого наблюдают при
гепатоцеллюлярной карциноме. Выработка анти-GOR ассоциирована только с
HCV-инфекцией, но не с АИГ.
Аутоиммунные расстройства наблюдаются в среднем у 23% больных хроническим
гепатитом С. Наиболее часто встречаются патология щитовидной железы.
Гистологическое исследование печени
Гистологическая картина не является патогномоничной, при этом достаточно
часто выявляются характерные изменения. Отличительная особенность ее —
лимфоидные агрегаты или фолликулы в портальных трактах, которые могут быть как
изолированными, так и частью воспалительных изменений портальных трактов. По
клеточному составу эти агрегаты напоминают первичные лимфоидные фолликулы в
лимфатических узлах. Жировая дистрофия обнаруживается в 75% случаев. Кроме того,
выявляются следующие характерные изменения: негнойный холангит с лимфоидной и
плазмоклеточной инфильтрацией стенок протоков; лимфогистиоцитарная инфильтрация
перипортальной зоны; слабовыраженные ступенчатые некрозы; мостовидные некрозы
(обнаруживаются редко), пролиферация и активация сателлитных клеток печени,
пролиферация эпителия желчных канальцев.
Отмечено, что индекс гистологической активности (ИГА) и индекс фиброза (ИФ) у
больных хроническим гепатитом С с наличием жировой дистрофии достоверно выше,
чем у пациентов без сопутствующей жировой дистрофии. У 93% больных с жировой
дистрофией в гепатоцитах обнаруживался Core-протеин ВГС, при отсутствии жировой
дистрофии — лишь у 39%. Этим фактом подчеркивается роль Core-протеина в развитии
жировой дистрофии гепатоцитов.
Биопсия печени играет существенную роль в уточнении диагноза и оценке
активности и стадии заболевания.
РНК ВГС можно определить в ткани печени методом ПЦР.
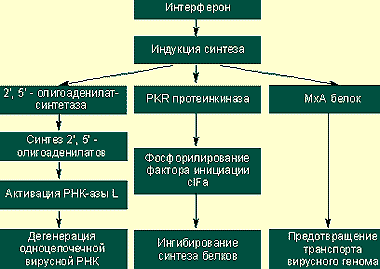
Предотвращение вирусной транскрипции и трансляции
Лечение
Основная цель лечения — предотвратить прогрессирование заболевания.
Режим отдыха, диета и прием витаминов не оказывают лечебного действия.
Отбор пациентов для лечения. Показанием к назначению терапии
интерфероном служит умеренное (но не минимальное) либо тяжелое воспаление и/или
фиброз. Решение о лечении пациентов с циррозом печени принимают индивидуально в
каждом конкретном случае. Больные, у которых гистологическая активность
минимальна, должны находиться под динамическим наблюдением, так как они имеют
хороший жизненный прогноз без лечения и очень низкий риск развития цирроза
печени через 10-20 лет.
Факторы, связанные с благоприятным эффектом противовирусной терапии при
хронической HCV-инфекции:
- Возраст моложе 45 лет
- Женский пол
- Отсутствие ожирения
- Срок инфицирования менее 5 лет
- Отсутствие коинфекции HBV
- Отсутствие иммунодепрессии
- Отсутствие алкоголизма
- Умеренное повышение АЛТ
- Отсутствие цирроза
- Низкое содержание железа в печени
- Низкий уровень HCV RNA в сыворотке
- Генотип 2 или 3
- Однородность популяции вируса
Больным с нормальным уровнем АЛТ и положительным тестом на HCV RNA без
результатов гистологического исследования противовирусное лечение проводить не
рекомендуется.
Основной препарат, эффективность которого в лечении гепатита С доказана, —
это интерферон альфа (ИФα).
В настоящее время принята оптимальная схема монотерапии ИФ: разовая доза
составляет 3 млн МЕ, ее вводят подкожно или внутримышечно 3 раза в неделю в
течение 3 месяцев. Через 3 месяца необходимо исследовать РНК ВГС. Если
результаты ПЦР положительные схему лечения меняют. Если же РНК не выявляется,
лечение продолжают до 12 месяцев. Стойкий положительный ответ в этом случае
регистрируется у 15-20% больных.
Оптимальная схема лечения хронического гепатита С в настоящее время — это
комбинация ИФa и рибавирина.
Согласно рекомендации согласительной конференции Европейской ассоциации по
изучению печени (1999), больным с впервые установленным диагнозом «хронический
гепатит С» и показаниями к лечению необходимо назначать ИФa в комбинации с
рибавирином следующими курсами:
- в течение 6 месяцев - при генотипах 2 и 3;
- в течение 6 месяцев - при генотипе 1 и низком уровне виремии;
- в течение 12 месяцев - при генотипе 1 и высоком уровне виремии.
Стойкий положительный ответ при комбинированном лечении ИФa с рибавирином
наблюдается в 40-60% случаев.
Суточная масса рибавирина составляет 1000-1200 мг в зависимости от массы
тела.
В последние годы для повышения эффективности интерферона применяют
пегилирование, которое заключается в присоединении к молекуле интерферона
полиэтиленгликоля. В итоге образуется ПЭГ-интерферон, имеющий более длительный
период полураспада. Предварительные данные свидетельствуют о большей
эффективности такого лечения по сравнению с терапией интерфероном альфа.
Одним из наиболее перспективных пегилированных интерферонов является пегасис
— ПЭГ-интерферон альфа-2а, соединенный с разветвленной молекулой
полиэтиленгликоля, молекулярная масса которого составляет 40 kDa, общий вес
молекулы — около 60 kDa. Особенности химической структуры данного препарата
определяют его фармакокинетические свойства и клиническую эффективность.
Молекула полиэтиленгликоля присоединена к альфа-интерферону посредством самой
стабильной амидной связи, это делает молекулу пегасиса чрезвычайно устойчивой к
действию петидаз и позволяет выпускать препарат в виде растворенной и готовой к
употреблению лекарственной формы. Особенностью молекулы полиэтиленгликоля
является способность активно связывать несколько молекул воды, что создает
вокруг химически структурной единицы пегасиса эффект «водного облака», делая ее
устойчивой во внутренней среде и сообщая препарату относительно небольшой объем
распределения. Это, в свою очередь, способствует тому, что отпадает
необходимость в коррекции дозы препарата в зависимости от массы тела пациента:
пегасис вводится один раз в неделю в дозе 180 мкг. Существенными преимуществами
препарата пегасис являются значительно лучшая переносимость и меньшая частота
побочных реакций, ассоциированных с системным действием альфа-интерферона, что
значительно улучшает качество жизни пациентов, получающих лечение по поводу
хронического гепатита С. Кроме того, в отличие от других пегилированных
интерферонов пегасис не требует существенной коррекции дозы в зависимости от
функционального состояния почек, что делает препарат незаменимым у пациентов с
сопутствующей хронической почечной недостаточностью.
Клиническая эффективность пегасиса оценена солидными широкомасштабными
многоцентровыми рандомизированными исследованиями. Было показано, что частота
доказанного ответа на лечение значительно превышает таковую по сравнению с
«короткими» интерферонами как в схемах монотерапии, так и в сочетании с
рибавирином. Особенно впечатляющими в этой связи являются результаты
этиопатогенетической терапии с использованием пегасиса в сочетании с рибавирином
у так называемой «трудной» категории пациентов, имеющих морфологические
проявления цирроза печени, 1b-генотип вируса, высокую виремию: частота
доказанного ответа на лечение у данной категории пациентов при использовании
пегасиса в сочетании с рибавирином может составлять около 40%, у иных категорий
пациентов этот показатель может превышать 75%, что ранее было практически
немыслимым результатом.
Другие противовирусные препараты в лечении хронического гепатита С
Имеются данные, свидетельствующие о положительном действии таких препаратов,
как ремантадин, урсодеоксихолевая кислота, пегилированные интерфероны, препараты
глициризиновой кислоты, однако эта информация нуждается в дальнейшей проверке.
Статья опубликована в журнале
Лечащий Врач

