Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Кардиомиопатии при первичной митохондриальной патологии. Подходы к лечению
И. В. Леонтьева, доктор медицинских наук
Московский НИИ педиатрии и
детской хирургии МЗ РФ
Кардиомиопатии (КМП) у детей относятся к тяжелым заболеваниям миокарда с
непрерывно прогрессирующим течением и с высокой смертностью [1-3]. До
последнего времени научные разработки по этой патологии были направлены на
совершенствование методов диагностики заболевания, определение стадий
клинического течения и поиск новых лекарственных препаратов для лечения
недостаточности кровообращения [4-8].
Достижения медицинской науки за последние десятилетия в области медицинской
генетики, биохимии и клинической морфологии помогли идентифицировать среди
ранее недифференцированных патологических состояний новый класс
митохондриальных заболеваний, обусловленных глубокими дефектами структуры и
функции митохондрий [9, 10]. Развитие представлений о митохондриальной
патологии позволило значительно расширить современные воззрения на патогенез
заболеваний миокарда. Появилась возможность выделить особую группу
метаболических митохондриальных КМП, что способствовало разработке
дифференцированной специфической терапии.
Митохондриальные заболевания характеризуются полиорганностью поражения и
проявляются в первую очередь поражением скелетных мышц, вовлечением в
патологический процесс других органов и тканей (мозга, сердца, печени, почек)
вариабельно, что приводит к гетерогенной клинической картине [9-14]. Описаны
КМП при типичных митохондриальных заболеваниях: синдромах MERRF [11, 13, 14],
MELAS [14-17], Кернса-Сейра [17, 18], митохондриальной миопатии [19]. Вместе с
тем митохондриальная дисфункция может быть не только причиной развития
полиорганной патологии, но и проявляться преимущественным поражением миокарда.
Экспериментальными и клиническими исследованиями последних лет установлено,
что при так называемых «идиопатических» кардиомиопатиях происходят нарушения
окислительного фосфорилирования, связанные со снижением активности
митохондриальной электронно-транспортной системы вследствие мутации
митохондриальной или ядерной ДНК. Существует предположение, что
митохондриальная дисфункция может являться патогенетической основой
кардиомиопатий, считающихся «идиопатическими» [14, 20-23]. Митохондриальные
КМП могут быть определены как заболевания миокарда, сопровождающиеся
структурными, количественными и функциональными нарушениями митохондрий либо
комбинацией этих нарушений [14, 20-23]. Установлено, что основой формирования
митохондриальных КМП являются мутации митохондриальной ДНК [20, 24-27].
Делеция, или точковая мутация, митохондриальной ДНК была выявлена в
исследовании, проведенном Ито Т. (1992) [24] среди больных с гипертрофической
или дилатационной кардиомиопатией и синдромом MELAS (митохондриальная
миопатия, лактат-ацидоз, инсультоподобные эпизоды). Суомалайнен (1992) [26]
приводит наблюдения за женщиной и ее сыном с дилатационной кардиомиопатией,
обусловленной мутацией митохондриальной ДНК. Casali с соавт. (1995) [27]
описывает новую мутацию митохондриальной ДНК в позиции 4300 tRNA(Ile),
ассоциирующейся с ГКМП и материнским наследованием.
Мутации митохондриальной ДНК приводят к нарушению транспорта электронов
вследствие патологии комплексов цепи дыхательных ферментов, что фенотипически
проявляется КМП. Так, описаны КМП при дефиците цитохром С-оксидазы [28],
снижении активности I и IV или II и III комплексов цепи дыхательных ферментов
митохондрий [29], низкой активности пальмитоил-коэнзим А дегидрогеназы,
связанной со снижением функции ацетил-коэнзим А дегидрогеназы длинных цепей
[30].
В отечественной детской кардиологической практике митохондриальные КМП при
жизни диагностируются недостаточно достоверно или остаются нераспознанными.
Отсутствуют критерии дифференцированного подхода к обследованию больных с КМП
для выявления митохондриальной недостаточности, не разработаны пути
метаболической коррекции нарушений клеточной энергетики.
Мы наблюдали 16 больных с митохондриальными синдромами Кернса-Сейра (8
детей), Барта (1), MELAS (2), MERRF (1), гистиоцитарной КМП (1), карнитиновой
КМП (2), с дефицитом II комплекса цепи дыхательных ферментов КМП (1 больной).
Программа исследования включала электрокардиографию, рентгенографию грудной
клетки, суточное холтеровское мониторирование, допплер-эхокардиографию,
позитронно-эмиссионную томографию (ПЭТ) сердца, неинвазивную оценку перфузии и
метаболизма миокарда, морфологический анализ биоптатов скелетной мышцы,
биохимическое определение в крови уровня лактата и пирувата. По показаниям
проводились электромиография и электроэнцефалография.
Синдром Кернса-Сейра впервые описан Кернсом в 1946 году
как заболевание с характерным клиническим симптомокомплексом: прогрессирующая
наружная офтальмоплегия, пигментная ретинопатия, КМП с нарушением проводящей
системы и развитием полного атриовентрикулярного блока. Более детальное
изучение этого заболевания принадлежит Сейру, в связи с чем с 1956 года этот
симптомокомплекс получил называние синдрома Кернса-Сейра. Пониманию природы
синдрома способствовали молекулярно-генетические исследования и обнаружение
мутаций митохондриальной ДНК [23, 31-34]. Впервые гистохимические и
ультраструктурные изменения мышечных волокон в виде феномена «рваных» красных
волокон (RRF), являющиеся важным критерием митохондриальной патологии, при
синдроме Кернса-Сейра были обнаружены в 1972 году в работе Олсона и соавт.
[35].
По нашим данным, при синдроме Кернса-Сейра при световой биопсии скелетных
мышц феномен RRF определяется в 25% мышечных волокон. Обнаруживаются и другие
маркеры митохондриальной патологии: субсарколемальные скопления липидов,
гликогена, кальция. Электронная микроскопия выявляет нарушения структуры
митохондрий: отсутствует часть митохондриальных крист, нарушено их обычное
расположение (рис. 1).

Рисунок 1. Синдром Кернса-Сейра.
А. Крупная митохондрия с деструкцией большинства крист и наличием сегмента
параллельно лежащих, регенирирующих крист. ЭМ.х110 000
Б. Наличие субсарколеммальных полос продуктов реакции на СДГ в поперечно
срезанных мышечных волокнах. Феномен RRF. Ув. 250
Клиническая манифестация синдрома Кернса-Сейра относится ко второму или
даже третьему десятилетию жизни. Этот феномен объясняется тем, что суммарная
функция митохондрий в течение длительного времени может оставаться
удовлетворительной [36]. При этом, чем раньше проявляется заболевание, тем оно
носит более генерализованный характер и имеет худший прогноз. Диффузные
патологические изменения в митохондриях различных органов и тканей объясняют
мозаичность клинической картины с вовлечением различных органов и систем.
Отмечается задержка физического и полового развития. Изменения со стороны кожи
проявляются ихтиозом с очагами гиперпигментации. Нарушения со стороны
опорно-двигательного аппарата характеризуются вальгусной девиацией голеней и
высоким сводом стопы. Наиболее выраженной является патология со стороны глаз.
Характерны наружная офтальмоплегия с птозом различной степени выраженности,
пигментный ретинит или пигментная дегенерация сетчатки. Птоз — наиболее
типичный признак [10]. Один из наиболее частых симптомов — мозжечковая
атаксия. У многих больных наблюдается умственная отсталость, однако степень
снижения интеллекта варьирует от умеренно выраженной до прогрессирующей
деменции. Описан случай инфаркта мозга у больного с синдромом Кернса-Сейра
[37]. Нарушения со стороны эндокринной системы включают дефицит гормона роста,
гипоганодизм, сахарный диабет, гипопаратиреоз, нарушение адреналового обмена
[31, 38 ].
Изменения сердечно-сосудистой системы являются облигатной составляющей
клинического симптомокомплекса синдрома Кернса-Сейра. Варианты и степень
выраженности нарушений со стороны сердечно-сосудистой системы определяют тяжесть
течения и прогноз синдрома Кернса-Сейра. Эти изменения в большинстве случаев
затрагивают проводящую систему сердца. В исследованиях Мюллера с соавт. [39]
обосновано преимущественное поражение проводящей системы сердца по сравнению с
миокардиальными нарушениями у больных с синдромом Кернса-Сейра, большей
представленностью мутаций митохондриальной ДНК в проводящей системе сердца в
отличие от клеток сократительного миокарда. Так, частота мутаций
митохондриальной ДНК у пациентов с синдромом Кернса-Сейра в клетках проводящей
системы составляет 35-40% по сравнению с клетками сократительного миокарда —
10-20% [40]. Поражение проводящей системы сердца чаще всего характеризуется
полным атриовентрикулярным блоком. В ряде случаев патология со стороны
сердечно-сосудистой системы при синдроме Кернса-Сейра долгое время остается
нераспознанной [41]. Иногда врачи проявляют серьезную озабоченность только при
появлении полной атриовентрикулярной блокады, приводящей к резкой брадикардии,
длительным паузам сердечного ритма с развитием синкопальных состояний —
приступов Морганьи-Адамса-Стокса. Наличие полного атриовентрикулярного блока, не
купированного своевременно имплантацией искусственного водителя ритма, является
непосредственной причиной гибели этих пациентов [38, 41]. С другой стороны, даже
имплантация искусственного водителя ритма не гарантирует благополучного
прогноза. Так, Н. А. Белоконь с соавт. (1988) [42] обследовали ребенка с
синдромом Кернса-Сейра, у которого на фоне полной атриовентрикулярной блокады
частота сердечных сокращений уменьшалась до 28 в минуту, что сопровождалось
развитием синкопальных состояний и потребовало имплантации искусственного
водителя ритма. Однако, несмотря на это, больной умер через 9 лет от
прогрессирующей сердечной недостаточности при удовлетворительном
функционировании пейсмекера. Полная атриовентрикулярная блокада помимо угрозы
возникновения приступов Морганьи-Адамса-Стокса приводит к возникновению
миокардиальной дисфункции с последующим возможным развитием недостаточности
кровообращения [38, 41]. Акэйк М. с соавт. (1997) подчеркивают, что высокий риск
возникновения миокардиальной недостаточности на фоне полного
атриовентрикулярного блока диктует необходимость имплантации пейсмекера типа DDD
в ранние сроки, не дожидаясь опасных для жизни нарушений в проводящей системе
сердца [43].
Под нашим наблюдением находилось 8 пациентов с синдромом Кернса-Сейра.
Изменения со стороны проводящей системы не всегда манифестируют полным
атриовентрикулярным блоком, возможно постепенное нарастание изменений со стороны
проводящей системы сердца, что наблюдалось в 4 случаях. Степень поражения
сердечно-сосудистой системы широко варьирует от дистального нарушения проведения
по правой или левой ножке пучка Гиса до полной атриовентрикулярной блокады.
Поражения проводящей системы сердца носят непрерывно прогрессирующий характер —
они начинаются с дистальной блокады ножек пучка Гиса, распространяясь на
атриовентрикулярный и синусовый узлы с развитием полной атриовентрикулярной
блокады и синдрома слабости синусового узла.
Нарушения проводящей системы сердца при синдроме Кернса-Сейра могут
сочетаться с изменениями в миокарде по типу КМП. Возможно формирование как
дилатационной (3 из 8 наблюдений), так и гипертрофической симметричной
необструктивной кардиомиопатии (2 из 8). Наиболее тяжелое поражение
сердечно-сосудистой системы отмечено у девочки 15 лет с синдромом Кернса-Сейра.
Наблюдалось диффузное прогрессирующее поражение проводящей системы сердца,
начиная с дистальной двухпучковой блокады ножек пучка Гиса и транзиторной
атриовентрикулярной блокады 1-й степени с последующим развитием блокады правой и
левой ножек пучка Гиса до полной атриовентрикулярной блокады с длительностью
периодов асистолии от 3 до 4 секунд и возникновением жизнеугрожающих
синкопальных состояний — приступов Морганьи-Адамса-Стокса, что потребовало
экстренной трансплантации искусственного водителя ритма. После имплантации ЭКС
частота сердечного ритма составила 86 ударов в минуту. Нарушения проводящей
системы сердца сопровождались развитием КМП, сочетающей как дилатацию полости
левого желудочка, так и симметричную гипертрофию левого желудочка без
обструкции. Особенности данного процесса следующие: развитие выраженной
миокардиальной дисфункции, резкое снижение контрактильной способности миокарда и
наличие обширных ишемических изменений в области переднебоковой стенки левого
желудочка (деформация желудочкового комплекса по типу QS V1-5). Развитие
миокардиальной дисфункции, снижение сократительной способности миокарда,
распространенные ишемические изменения резко ухудшают прогноз течения синдрома
Кернса-Сейра.
Синдром MELAS (митохондриальная миопатия — энцефалопатия — лактат-ацидоз,
инсультоподобные эпизоды)
В основе патогенеза синдрома лежат точковые мутации митохондриальной ДНК.
Мутация наиболее часто встречается в скелетной и сердечной мышцах, печени,
почках, поджелудочной железе, мозжечке и коре больших полушарий [14]. Дебют
заболевания вариабелен, наиболее часто это происходит между 6 и 10 годами.
Экстракардиальными клиническими симптомами являются судороги, рецидивирующие
головные боли, рвота, анорексия, непереносимость физических нагрузок,
инсультоподобные эпизоды, деменция, миопатический симптомокомплекс, признаки
периферической невропатии. При компьютерной томографии головного мозга
выявляются зоны инфарктов, преимущественно в области гемисфер, что и
обусловливает неврологическую симптоматику.
Под нашим наблюдением находились два пациента с синдромом MELAS. В одном из
этих случаев наследственность отягощена. Старший ребенок умер в возрасте 10 лет
(отмечались атрофия зрительного нерва, периодическая рвота, частые
мигренеподобные головные боли, выраженная мышечная слабость, утомляемость,
косоглазие), у матери — частые головные боли, непереносимость физических
нагрузок. Дебют заболевания в том и другом случае относился к 8 годам. Первые
симптомы — частые мигренеподобные головные боли, сопровождающиеся тошнотой и
рвотой. Изменения неврологического статуса характеризовались мышечной слабостью,
повышенной утомляемостью при физической нагрузке, нарушением походки:
пошатывание при ходьбе, неуверенность при выполнении координационных проб.
Впоследствии развились атаксия, нарушение речи (дизатрия, моторная дислалия),
частые мигренеподобные головные боли, двустороннее снижение слуха, судорожные
подергивания левой половины лица, сонливость. В 9 лет появились эпизоды тошноты,
рвоты, снижения аппетита, усилились мигренеподобные головные боли. В 10 лет на
фоне подъема температуры возник эпилептический статус, затем приступы стали чаще
сопровождаться потерей сознания, клоническими подергиваниями левых конечностей и
заведением левого глазного яблока кнаружи. Частота приступов в течение года
нарастала, и в 12 лет возник инсультоподобный эпизод, в левых конечностях
развился стойкий гемипарез. В одном случае отмечалось снижение остроты зрения.
На ЭЭГ определялась пароксизмальная активность в виде групп острых волн с
преимущественной локализацией в левой теменно-затылочной области. МРТ мозга:
ишемические очаги в области головки хвостатого ядра и в белом веществе головного
мозга кнаружи от внутренней капсулы слева. Нарушения зрения больше были
характерны для девочки — отмечались снижение остроты зрения и частичная атрофия
зрительного нерва. В 10 лет появились расходящееся косоглазие, птоз левого века,
мелкоамплитудный горизонтальный нистагм, слабость конвергенции с обеих сторон.
По данным аудиометрии, отмечалась двусторонняя нейросенсорная тугоухость.
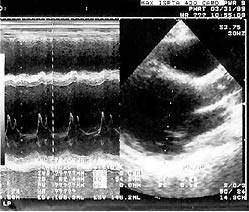
Рисунок 2. ЭхоКГ — дилатация полости левого желудочка (КДДлж =
56 мм), снижение сократительной способности миокарда (фр. выброса 0,34)
В одном случае изменения со стороны сердца характеризовались симметричной
ГКМП (Тзслж = Тмжп = 11 мм при норме 7 мм). Отмечались нарушения ритма —
эктопический предсердный ритм, суправентрикулярная экстрасистолия — по типу
три- и квадригеминии, нарушение процессов реполяризации. Наиболее тяжелое
течение заболевания отмечено у девочки 12 лет с дилатационной КМП. По данным
ЭКГ, резко выраженная синусовая тахикардия, нарушение процессов реполяризации
миокарда. Результаты ЭхоКГ выявили дилатацию левого желудочка (КДД = 56 мм при
норме 40 мм), снижение контрактильной способности миокарда (ФВ = 0,34 при
норме 0,60) (рис. 2). По данным позитронно-эмиссионной томографии, отмечена
дилатация полостей левого и правого желудочков, резкое снижение метаболизма
глюкозы в миокарде (накопление FDG18 стенками миокарда резко снижено во всем
миокарде, невозможно выделить стенки и полости левого желудочка К FDG18=
0,6-1,1 при норме 2,5, реакция на нагрузку глюкозой отсутствует) на фоне
нормальной перфузионной способности миокарда (рис. 3). Зафиксировано
выраженное снижение активности цикла Кребса.

Рисунок 3. Нарушение метаболизма глюкозы в миокарде, по данным
позитронно-эмиссионной томографии при синдроме Барта. Перфузия миокарда в
пределах нормы. Снижение метаболизма глюкозы — накопление FDG18 снижено (К
FDG18 =1,4 при норме 2,5)
По данным биохимического анализа крови, в том и другом случае отмечалось
повышение содержания молочной и пировиноградной кислот: содержание молочной
кислоты в исходе — 2,8 ммоль/л, через час после нагрузки глюкозой — 3,0, через
3 часа — 3,2 ммоль/л ; содержание пировиноградной кислоты в исходе — 0,34
ммоль/л (норма 0,05-0,09), через час — 0,28, через 3 часа — 0,24 ммоль/л; рН —
7,38. По данным биопсии скелетной мышцы, размеры большинства мышечных волокон
не изменены, имелись участки атрофии — до 20%, в них отмечены регионарные
некрозы и локальные участки повышения регенераторной активности по
интраволоконному типу. В 35% мышечных волокон при окраске на
сукцинатдегидрогеназу определяется выраженный позитивный феномен RRF (рис. 3).
При электронной микроскопии выявляются типичные участки пролиферирующих
митохондрий. Гликоген и липиды распределены равномерно, в значительном
количестве определяются конгломераты кальция. Цитохимическое исследование
обнаружило снижение активности СДГ в лимфоцитах периферической крови — 13 ед.
(норма 19-22 ед.).
Cиндром MERRF (миоклонус-эпилепсия и инфаркт мозга, RRF-волокна)
Сочетание миоклонус-эпилепсии с «рваными» красными волокнами скелетных мышц
обнаружили в 1973 году Циарис с соавторами, но в качестве синдрома MERRF он
был описан Фукухарой и его соавторами в 1980-м. В основе синдрома MERRF лежит
точковая мутация в позиции 8344 в гене лизиновой tРНК. При этом снижается
синтез белка, кодируемый митохондриальной ДНК, в первую очередь это касается
субъединиц цитохромоксидазы. Заболевание наследуется по митохондриальному
(материнскому) типу. Дебют MERRF вариабелен — от 3 до 63 лет.
Экстракардиальными симптомами, доминирующими в клинической картине, являются
миоклонус-эпилепсия, атаксия, деменция, потеря слуха и мышечная слабость. С
этих же симптомов заболевание может манифестировать. При компьютерной
томографии головного мозга выявляются множественные церебральные инфаркты.
Именно эти изменения и обусловливают основную неврологическую симптоматику. В
биоптатах скелетных мышц обнаруживаются типичные RRF.
Ферментно-гистохимический анализ выявляет недостаточность цитохром С-оксидазы.
При электронной микроскопии наблюдаются увеличение размеров митохондрий, их
деформация, липидные включения [13].
Под нашим наблюдением находился ребенок с синдромом MERRF. Изменения со
стороны сердца характеризовались симметричной гипертрофической КМП (Тзслж =
Тмжп = 12 мм при норме 7 мм). Отмечался синдром Вольфа-Паркинсона-Уайта, что
создавало предпосылки для возникновения жизнеугрожающих состояний.
Синдром Барта (кардиомиопатия с нейтропенией и гипостатурой)
В последнее десятилетие постоянно расширяется реестр митохондриальных
болезней. В 1983 году П. Г. Барт и соавторы описали Х-сцепленный рецессивный
фенотип, проявляющийся сочетанием скелетной миопатии, кардиомиопатии, задержки
роста с нейтропенией в раннем возрасте. Наследование заболевания Х-сцепленное
рецессивное. О митохондриальной природе заболевания говорят резко выраженные
нарушения строения митохондрий мышечной, сердечной ткани и других органов.
Заболевание возникает в раннем возрасте, на 5-7-м месяце жизни. Дети с данной
патологией имеют низкий вес при рождении и в дальнейшем инфантильный соматотип
(весо-ростовые показатели соответствуют 3-5 центилям), характерно отставание
костного возраста от паспортного на 1-2 года. Заболевание манифестирует
миопатическим синдромом. Изменения со стороны сердца могут характеризоваться
как симметричной гипертрофической, так и дилатационной кардиомиопатией. Именно
степень поражения сердечной мышцы определяет тяжесть и прогноз заболевания.
Нами наблюдался мальчик с синдромом Барта. Впервые изменения со стороны
сердца были выявлены в 1,5 года в виде симметричной необструктивной
гипертрофической КМП. По данным эхокардиографии, толщина межжелудочковой
перегородки — 12 мм, задней стенки левого желудочка — 10 мм при норме 5 мм.
При обследовании через год отмечено нарастание степени гипертрофии миокарда
(толщина задней стенки левого желудочка — 13 мм, толщина межжелудочковой
перегородки — 11,8 мм при норме 5,5 мм). На ЭКГ — повышение электрической
активности левого желудочка, снижение процесса реполяризации в миокарде (рис
4).

Рисунок 4. Нарушение метаболизма миокарда, по данным
позитронно-эмиссионной томографии при синдроме MELAS. Нормальная перфузия.
Накопление FDG18 резко снижено. Снижение активности цикла Кребса. Снижение
энергетического метаболизма вне связи с его кровоснабжением
Основными клиническими симптомами являлись задержка физического (рост <3
центилей, масса <10 центилей) и психомоторного развития и повышенная
утомляемость, отмечено умеренное отставание психоречевого развития. В
неврологическом статусе определялись гипомимия лицевых мышц, периодическое
поперхивание, нарушение произношения некоторых звуков. Выражены общая мышечная
гипотония и гипотрофия, снижение силы мышц.
Сухожильные рефлексы снижены, больше в верхних конечностях. Походка
изменена по типу утиной, ребенок с трудом поднимается по лестнице. В
психологическом статусе отмечена легкая задержка психического развития — IQ 80
ед. Электронейромиография: повышение числа полиморфных потенциалов, диффузные
изменения нервно-мышечного характера, миопатический тип кривой. Компьютерная
томография головного мозга — картина «пустого» турецкого седла. Содержание в
крови тиреотропного гормона и гормонов щитовидной железы было в пределах
нормы. При проведении пробы с клофелином дефицита соматотропного гормона не
обнаружено. Рентгенография трубчатых костей выявила остеопороз. Лейкоцитарная
формула по типу нейтропении. Проведенное биохимическое обследование ребенка
выявило гипогликемию (2,0-3,12 ммоль/л при N = 3,3–5,7). Отмечалось повышение
уровня молочной кислоты в сыворотке крови до 2,63 ммоль/л (при N = 1,0–1,7
ммоль/л), после нагрузки глюкозой содержание молочной кислоты повысилось до
4,16 ммоль/л, а также отмечался высокий уровень пировиноградной кислоты в
крови (0,17-0,23 ммоль/л при N = 0,05–0,09 ммоль/л). Выявлено нарушение
экскреции органических кислот, возникающее у больных с синдромом Барта как
следствие недостаточности митохондриальных энергетических процессов.
Наблюдается низкое содержание карнитина.
Митохондриальный генез патологии подтвержден данными биопсии скелетной
мышцы. Ребенку были назначены следующие препараты: L-карнитин — 500 мг/сут,
цитомак — 4,0 в/м 4 курса в год, коэнзим Q10 — 60 мг/сут, ноотропил — 0,4 г/сут.
При своевременной заместительной терапии препаратами, улучшающими
энергетический обмен в сочетании с диетой с низким содержанием жиров, были
отмечены положительная динамика со стороны сердечно-сосудистой системы,
уменьшение миопатического синдрома, улучшение показателей физического
развития, уменьшение степени гипертрофической кардиомиопатии, нормализация
толщины межжелудочковой перегородки (до 7,5 мм) и задней стенки левого
желудочка (до 7 мм), а также снижение экскреции жирных кислот.
Карнитиновая кардиомиопатия
Было установлено, что КМП могут сочетаться с резким снижением уровня
карнитина в митохондриях [44, 45]. В ряде случаев причиной ДКМП у детей может
быть генетический дефект транспорта карнитина [46]. Изолированная карнитиновая
КМП клинически проявляется с 3-5 месяцев, имеет плохой прогноз, смерть наступает
внезапно вследствие метаболического стресса. Асистолия связана с тяжелой
гипогликемией, возможна патологическая брадикардия, sinus-arrest из-за блокады
выхода [45]. Клинически отличить карнитиновую КМП от дилатационной аутоиммунного
генеза сложно. Дифференциальной диагностике помогают следующие
клинико-инструментальные показатели. Обычно при дилатационной кардиомиопатии
наблюдаются изолированная дилатация полостей без явлений гипертрофии и
выраженная гипокинезия стенок левого желудочка. При карнитиновой КМП наряду с
гипертрофией миокарда отмечаются дилатация левого желудочка и явления
фиброэластоза эндокарда. Характерными изменениями на ЭКГ являются «гигантские»
зубцы Т в левых грудных отведениях, превышающие зубец R желудочкого комлекса
[47].

Рисунок 5. Карнитиновая ДКМП. ЭхоКГ. Высокий вольтаж QRS,
смещение ST, высокий положительный двугорбый Т больше зубца R, гипертрофия
желудочков КДДлж= 65 мм, атриомегалия, фракция выброса — 0,20, гипокинез и
дискинез, митральная регургитация 2-3-й ст.
Нами наблюдались 2 больных с карнитиновой КМП. Приводим одно из наблюдений.
Больной А. 9 лет с карнитиновой недостаточностью, вызвавшей развитие
дилатационной кардиомиопатии. В возрасте 7 лет стал жаловаться на повышенную
утомляемость, слабость, потливость, появились жалобы на частые боли в животе,
выраженный миопатический синдром. Тогда же отмечались признаки недостаточности
кровообращения: одышка, сердцебиения, гепатомегалия. При рентгенологическом
обследовании выявлено увеличение размеров сердца, в основном за счет левых
отделов, КТИ до 56%. По данным ЭКГ, выявлено повышение электрической активности
миокарда левого желудочка. В стационаре по месту жительства был поставлен
диагноз: ДКМП. Назначено лечение: преднизолон, мочегонные, ККБ и поляризующая
смесь. Однако терапия оказалась неэффективной, нарастали явления недостаточности
кровообращения. Увеличивалась дилатация левого желудочка, границы сердца
расширены влево до переднеаксиллярной линии; на ЭКГ — синусовая тахиаритмия,
гипертрофия левых отделов сердца, резко выраженные ишемические нарушения в виде
«гигантских» зубцов Т. На ЭхоКГ — расширение полости левого желудочка (КДДлж =
66 мм при норме 41 мм), снижение сократительной способности миокарда (ФВ =
0,32), симметричная гипертрофия стенок левого желудочка (Тзслж = Тмжп = 12 мм
при норме 8 мм), легочная гипертензия. УЗИ брюшной полости: гепатомегалия,
расширение печеночных вен. На основании выраженного миопатического синдрома,
снижения толерантности к физической нагрузке, гепатомегалии, рефрактерной к
применению дигоксина и мочегонных препаратов, изменений со стороны сердца в виде
сочетания дилатации левого желудочка, снижения контрактильной способности
миокарда с явлениями гипертрофии стенок левого желудочка, усиления сигнала от
эндокарда и специфических изменений на ЭКГ в виде «гигантских» зубцов Т возникло
подозрение о развитии карнитиновой кардиомиопатии (рис. 5). В целях верификации
диагноза был определен уровень карнитина в плазме. Он был снижен до 18 ммоль/мл
при норме 25 ммоль/мл. В связи с этим в стандартную терапию дигоксином и
мочегонными препаратами был подключен L-карнитин (элькар раствор) из расчета 75
мг/кг. На фоне данной терапии состояние значительно улучшилось, уменьшились
явления недостаточности кровообращения до 1-й степени, сократились размеры
полости левого желудочка (КДДлж уменьшилась с 66 мм до 52 мм), увеличилась
контрактильная способность миокарда (фракция выброса выросла с 0,32 до 0,49).
Гистиоцитарная кардиомиопатия
Гистиоцитарная кардиомиопатия впервые была описана Д. Вотом в 1963 году как «арахноцитоз»
сердечной мышцы. Было установлено, что гистиоцитарная кардиомиопатия — это
типичное клиническое проявление дефицита цитохрома-В [21]. Клиническая
симптоматика заболевания проявляется с 3-недельного возраста, как правило, до 1
года, характеризуется внезапным возникновением тахиаритмий (желудочковой или
наджелудочковой локализации), частым развитием фибрилляции желудочков. Чаще
болеют девочки в соотношении 5:1. Несмотря на интенсивную терапию, больные
погибают через несколько недель после начала приступов желудочковой тахикардии.
При аутопсии обнаруживаются сочетание гипертрофии миокарда с дилатацией полости
левого желудочка, фиброэластоз сердца, при световой микроскопии отмечаются
необычные очаги «обесцвеченного» миокарда главным образом в желудочках, в
субэндо- и субэпикарде, меньше интрамурально, реже изменения могут наблюдаться и
в предсердиях, иногда группы трансформированных клеток встречаются в основании
створок митрального, трехстворчатого и аортального клапанов. Эти очаги содержат
удлиненные мышечные волокна, похожие на миофибрилы, так называемые
гистиоцитоподобные пенистые или онкоцитарные клетки. В цитоплазме
гистиоцитоидных клеток содержится большое количество липидов и гликогена. При
электронной микроскопии в гистиоцитоидных клетках наблюдается большое количество
митохондрий причудливой формы с низким содержанием цитохрома-В.
Приводим клиническое наблюдение больной 1 года 2 месяцев с гистиоцитарной
кардиомиопатией. Изменения со стороны сердца характеризовались дилатационной и
гипертрофической симметричной необструктивной кардиомиопатией, фиброэластозом
эндокарда, синдромом Вольфа-Паркинсона-Уайта, пароксизмальной
суправентрикулярной тахикардией.
Первая беременность матери протекала на фоне угрозы прерывания в 3-5 недель,
выраженного токсикоза, постоянной гипотонии. Во время беременности мать дважды
(в 4,5 мес. и в 7 мес.) перенесла грипп в тяжелой форме. На сроке 20 недель
находилась на стационарном лечении в связи с выраженной анемией (Нв = 60 г/л).
Роды преждевременные, на 36-й неделе, кесарево сечение из-за разрыва шейки матки
3-й степени, низко расположенной плаценты. Во время операции сильное
кровотечение. Девочка родилась с массой 2450 г, длиной 46 см, закричала сразу,
оценка по шкале Апгар 7/8 баллов. Были признаки морфофункциональной незрелости.
Через неделю после рождения у девочки впервые зарегистрирован приступ
пароксизмальной тахикардии с ЧСС 240 уд/мин, который протекал с признаками
недостаточности кровообращения, длился около суток, купирован в/в введением
изоптина. При обследовании выявлены значительное увеличение полостей сердца,
снижение сократительной функции миокарда, увеличение печени до 4 см. По данным
ЭхоКГ, выраженное расширение полости левого желудочка (КДДлж = 30 мм при норме
24 мм), снижение фракции выброса до 0,35, гипертрофия миокарда левого желудочка:
Тмжп = Тзслж = 9 мм при норме до 4 мм). Кроме того, отмечалось усиление сигнала
от эндокарда левого желудочка (фиброэластоз). На ЭКГ — феномен WPW, тип А. В
приступе регистрировалась суправентрикулярная реципрокная тахикардия. Приступ
купирован внутривенным введением изоптина. При выходе из приступа
регистрировалась длительная (около 3 секунд) асистолия. В стационаре
продолжались ежедневные приступы пароксизмальной тахикардии, которые далее
купировались внутривенным введением АТФ. Получала гормональную и метаболическую
терапию, сердечные гликозиды, мочегонные препараты. Сохранялась постоянная
тахикардия с ЧСС 160 уд/мин, на ЭКГ феномен WPW. Эхокардиографически
определялись дилатация полости левого желудочка (КДДлж = 32 мм при норме 24 мм),
снижение сократительной способности миокарда (ФВ = 0,35 при норме 0,70) и
симметричная гипертрофия миокарда левого желудочка (Тзслж = Тмжп = 9 мм при
норме 4 мм), усиление сигнала от эндокарда, признаки недостаточности
кровообращения НК IIБ степени. Для лечения назначены дигоксин, с
кардиотрофической целью актовегин, в качестве антиаритмических препаратов
кордарон, финлепсин. За 1,5 месяца лечения состояние девочки значительно
улучшилось: сократились размеры полостей сердца (до верхних значений возрастной
нормы), но сохранялась гипертрофия миокарда левого желудочка, исчезли признаки
недостаточности кровообращения, на ЭКГ феномен WPW приобрел транзиторный
характер. В возрасте 1 года 1 месяца проведена вакцинация ППМ. Через сутки у
ребенка внезапно возникла многократная рвота. Впервые с трехнедельного возраста
развился тяжелый приступ тахикардии с частотой более 240 уд/мин, девочка
госпитализирована в реанимационное отделение. На ЭКГ зарегистрирована политопная
желудочковая тахикардия. Наблюдались выраженная одышка, пастозность, постоянная
тахикардия с ЧСС 160 уд/мин, глухость сердечных тонов, увеличение печени до +4
см. Была вновь назначена, противоаритмическая терапия: дигоксин, кордарон,
финлепсин, мочегонные препараты фуросемид, триампур. Впервые возникло
синкопальное состояние во сне — девочка резко закричала, затем обмякла,
констатирована остановка дыхания и сердечной деятельности. После проведения
реанимационных мероприятий сердечная деятельность восстановлена, но сохранялась
политопная тахикардия. Через час вновь зарегистрирована остановка сердца,
девочка в сопорозном состоянии. В течение 2 часов еще 5 раз отмечались остановка
сердца, фибрилляция желудочков. Консервативное лечение и реанимационные
мероприятия дали временный эффект. Экстренно переведена в ИСХИ им. Бакулева для
повторной дефибрилляции и решения вопроса о восстановлении ритма хирургическим
путем. При проведении внутрисердечного электрофизиологического исследования во
время дачи наркоза в течение 5 секунд отмечалась асистолия с восстановлением
приступа политопной желудочковой тахикардии с ЧСС 240 уд/мин. При картировании
правого предсердия — наиболее ранняя зона активной стимуляции расположена в
межжелудочковой перегородке. При попытке частой стимуляции купировать пароксизм
тахикардии не удалось. Отмечались отдельные синусовые комплексы с
восстановлением приступа. Медикаментозное тестирование лидокаина и новокаинамида
не дало эффекта, достигнуто лишь небольшое урежение сердечных сокращений до 170
уд/мин. По данным ЭФИ, имела место полиморфная левожелудочковая тахикардия с
ретроградной вентрикуло-атриальной диссоциацией, по-видимому, эктопического или
триггерного характера. Преходящий синдром WPW, тип А. Ввиду полиморфности
тахикардии, обилия очагов эктопии хирургическое лечение было признано
бесперспективным. В отделении состояние девочки оставалось крайне тяжелым.
Попытки навязать ритм от наружного кардиостимулятора и проводимые реанимационные
мероприятия не привели к восстановлению сердечной деятельности. В результате
некупируемого приступа фибрилляции желудочков сердца наступила смерть от острой
сердечной недостаточности. Паталогоанатомический диагноз: Гистиоцитарная
кардиомиопатия младенческого возраста. Субэндо- и субэпикардиальная
трансформация миоцитов левого желудочка в гистиоподобные клетки, множественные
очаги гистиоподобных клеток в интрамуральных отделах обоих желудочков. Очаговая
жировая дистрофия миокарда левого желудочка. Фиброэластоз эндокарда левых
отделов сердца. Миогенная дилатация полостей сердца с расширением фиброзных
колец всех клапанов. Непрерывно рецидивирующая полиморфная левожелудочковая
тахикардия, неоднократно переходящая в фибрилляцию желудочков, преходящий
синдром WPW, тип А.
Гистологическое исследование миокарда выявило крупные комплексы
гистиоцитоподобных пенистых клеток с обилием липидных включений в цитоплазме
среди пучков нормальных кардиомиоцитов. Наличие липидов указывало на резкое
снижение окислительной способности миокарда, на его жировую дистрофию и
гипофункцию. Такое состояние свидетельствует о резком снижении активности
митохондриальных ферментов и предположительно указывает на наличие врожденной
первичной митохондриальной патологии. Таким образом, данное наблюдение
демонстрирует развитие кардиомиопатии, сочетающей черты дилатационной и
гипертрофической с фатальным нарушением сердечного ритма у ребенка с
гистиоцитарной кардиомиопатией. Найденные морфологические изменения в виде
большого содержания липидов и гликогена в сердечной мышце, изменения структуры
митохондрий в совокупности с литературными данными о дефиците при этой патологии
III ферментного комплекса цепи дыхательных ферментов митохондрий позволяют
предположить, что данные изменения обусловлены митохондриальной патологией.
Кардиомиопатии при дефиците П-комплекса цепи дыхательных ферментов
Сукцинат-конзимQ-оксиредуктаза является важным ферментным комплексом как
цикла трикарбоновых кислот, так и респираторной цепи митохондрий. Комплекс
состоит из 4 полипептидов: 2 больших полипептида представляют
сукцинатдегидрогеназу и 2 малых — b тип цитохрома. П-комплекс кодируется ядерной
ДНК; наследование аутосомно-рецессивное, Х-сцепленное рецессивное или
доминантное с неполной пенентрантностью (Ангелини, 1993).
Клинический фенотип дефицита П-комплекса характеризуется прогрессирующей
офтальмоплегией, энцефаломиопатией, атаксией, миоклоническими подергиваниями,
миопатией и/или энцефалопатией, вторичным дефицитом карнитина, лактат-ацидозом.
Изменения со стороны сердца проявляются кардиомиопатией. В 1993 году Ангелини
описывал двух братьев с митохондриальной миопатией и гипертрофической
кардиомиопатией. У 25-летнего пациента на ЭКГ отмечались желудочковая
тахикардия, фибрилляция предсердий, клиника отека легких. Синусовый ритм был
восстановлен только на фоне применения верапамила. Отмечалась кардиомегалия. По
данным эхокардиографии, обнаружилась необструктивная гипертрофическая
кардиомиопатия с преимущественной гипертрофией межжелудочковой перегородки.
Отмечались изменения опорно-мышечного аппарата в виде сколиоза, проксимального
лордоза, слабости мышц плечевого пояса. Миография подтвердила миогенный паттерн.
Второй брат 19 лет предъявлял жалобы на загрудинные боли. В возрасте 8 месяцев у
него был отмечен эпилептический приступ. Эхокардиография выявила асимметричную
необструктивную КМП, толщина межжелудочковой перегородки составляла 30 мм,
задней стенки левого желудочка — 19 мм. В неврологическом статусе отмечены
атаксия и гипотония мышц плечевого пояса. Электромиография подтвердила миогенный
паттерн. У матери этих пациентов также выявлен миогенный паттерн, по данным
электромиографии. Анализ mt-ДНК не выявил значимых изменений. При биопсии мышцы
выявлены ragged-red волокна, отложения липидов. Структура митохондрий нарушена:
дезориентация в расположении крист. Гистоферментный анализ биоптатов скелетной
мышцы установил снижение активности сукцинатдегидрогеназы на 35% по сравнению с
нормой и сукцинат-цитохромС-редуктазы на 47% по сравнению с контролем. Уровень
карнитина был нормальным в первом наблюдении и сниженным до 62% от нормы во
втором.
Под нашим наблюдением находился больной с гипертрофической симметричной
кардиомиопатией, необструктивной формой со вторичной дилатацией левого желудочка
на фоне выраженной миокардиальной дисфункции, с распространенным
кардиосклерозом, рефрактерной сердечной недостаточностью НК Пб Ш ст.,
недиференцированным объемным образованием в полости левого желудочка (тромб),
диффузными дистрофическими изменениями в печени, задержкой физического и
психического развития, которые обусловлены системной митохондриальной
патологией.
Мальчик родился массой 3400 г, длиной 52 см, закричал сразу с оценкой по
Апгар 8/8. Раннее развитие без особенностей. Манифестация заболевания относится
к 9 годам, когда появились жалобы на повышенную утомляемость, нарушения походки.
Отмечались задержка физического и психического развития, головные боли. На фоне
перенесенного ОРВИ отмечены резкое снижение физической активности, отсутствие
аппетита, миопатический синдром, резкое снижение массы тела, состояние
продолжало ухудшаться, появились симптомы недостаточности кровообращения П Б
степени. На ЭКГ — признаки гипертрофии левого желудочка, блокада передней левой
ножки пучка Гиса, ишемические изменения в миокарде. На ЭхоКГ — симметричная
гипертрофия миокарда, митральная регургитация 2-й степени, дилатация полости
левого желудочка, снижение сократительной способности миокарда (Тзслж = Тмжп =
28, КДД ЛЖ = 47 мм, ФВ = 0,40). Косвенные признаки легочной гипертензии —
расчетное давление в полости правого желудочка 60 мм рт. ст., объемное
образование в полости левого желудочка (тромб) (рис. 6). Присоединение
выраженной миокардиальной дисфункции у ребенка с ГКМП привело к резкому снижению
сократительной способности миокарда и развитию дилатационной кардиомиопатии.
Учитывая инфантильный соматотип ребенка, отставание в физическом и психическом
развитии, выраженную гепатомегалию, рефрактерную к проводимой терапии,
миопатический синдром, было выдвинуто предположение о миторхондриальном генезе
заболевания. В терапию на фоне мочегонных препаратов были включены капотен,
предуктал, эссенциале, аплегин. На этом фоне состояние несколько улучшилось,
уменьшилась тахикардия, одышка, печень сократилась до 4 см. Гистоферментный
анализ биоптатов скелетной мышцы выявил значительное снижение
сукцинат-цитохромС-редуктазы — на 43% по сравнению с контролем.

Рисунок 6. Аномалия 2-го комплекса цепи дыхательных ферментов.
ЭхоКГ. Концентрическая симметричная гипертрофия миокарда Тзслж = Тмжп = 28,
митральная регургитация 2-й ст., дилатация полости левого желудочка,
снижение фракции выброса (ФВ = 0,40)
Разработаны диагностические критерии, позволяющие предположить развитие
кардиомиопатий, связанных с энергетической несостоятельностью митохондрий.
Экстракардиальными критериями являются:
- инфантильный соматотип (масса и рост ребенка соответствуют 3-5 центилям);
- мышечная слабость, выявляемая в покое или после физической нагрузки;
- снижение толерантности к физической нагрузке;
- нарушения зрения (птоз);
- снижение слуха;
- инсультоподобные эпизоды неясного генеза;
- периодическая (циклическая) нейтропения;
- стойкое увеличение печени, рефрактерное к лечению сердечной
недостаточности на фоне приема сердечных гликозидов и диуретиков;
- увеличение уровня лактата и пирувата;
- повышенная экскреция органических кислот;
- снижение содержания карнитина в крови;
- ацидоз.
Особенностями кардиомиопатий, протекающих на фоне первичной митохондриальной
патологии, являются:
- нарушение проводящей системы сердца;
- злокачественные, рефрактерные к антиаритмическим препаратам желудочковые
аритмии у детей раннего возраста;
- сочетание дилатации полостей сердца и гипертрофии миокарда,
преимущественно задней стенки, с проявлениями фиброэластоза эндокарда;
- выявление гипертрофической кардиомиопатии в раннем возрасте;
- семейный характер заболевания;
- "гигантские" зубцы Т на ЭКГ в левых грудных отведениях.
Статья опубликована в журнале
Лечащий Врач
Если вы заметили орфографическую, стилистическую или другую ошибку на этой странице, просто выделите ошибку мышью и нажмите Ctrl+Enter. Выделенный текст будет немедленно отослан редактору
|
|
|

