Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Изучение микроэкологии влагалища (вагинального биотопа),
начатое более 100 лет тому назад А. Дедерлейном, показало, что настоящая
экосистема сложная, многокомпонентная, гормонально зависимая и легкоранимая.
Состояние ее динамического равновесия определяется, во-первых, уровнем
гликогена в клетках эпителия влагалища, который в свою очередь связан с
функциональным состоянием яичников, затем концентрацией лактофлоры, рН
влагалищного содержимого и состоянием местного иммунитета.
Наличие индигенной флоры является одним из основных механизмов
защиты половых путей от патогенных бактерий. Выраженный антагонистический
эффект в отношении широкого круга патогенов проявляют лактобациллы, которые
помимо образования молочной кислоты продуцируют перекись водорода, и
бактериоцины, угнетающие развитие посторонних микробов. Кроме того,
лактобактерии и неспорообразующие анаэробы проявляют высокую
конкурентоспособность в заселении экологической нищи. Имеет большое значение и
фактор адгезии индигенной флоры между собой и к поверхности эпителиоцитов.
Специфическое прикрепление обеспечивается как за счет выростов в виде пилей и
фимбрий, так и особыми химическими агентами— лектинами-гликопротеинами. В
результате таких взаимодействий формируется гликокаликс, защищающий микробный
пул от воздействия неблагоприятных факторов— антител, лизоцима, бактериофагов.
Все вышеперечисленное входит в понятие «колонизационная резистентность»,
означающее совокупность механизмов, придающих стабильность влагалищного
биотопа и предотвращающих заселение данной ниши.
В последнее десятилетие все больше внимания уделяется проблеме
микозов, актуальность ее обусловлена продолжающимся ростом заболеваемости
различными видами грибковой инфекции во всем мире, в частности, хроническими
кандидозами кожи и слизистых, висцеральными микозами с поражением
желудочно-кишечного тракта, респираторной системы и репродуктивных органов.
В акушерской и гинекологической практике прослеживается явная
тенденция увеличения числа заболеваемости инфекционными процессами нижнего
отдела гениталий, в частности бактериальным вагинозом и кандидозной инфекцией.
Последние два заболевания зачастую объединяют в понятие «дисбиоз влагалища»,
который можно определить как полимикробный инфекционный синдром,
представляющий собой патологию экосистемы влагалища, вызванную дисбалансом,
проявляющимся уменьшением количества ферментирующих лактобацилл с
одновременным увеличением количества условно-патогенных микроорганизмов.
В нашей стране вагинальный дисбиоз прочно занимает одно из
ведущих мест в структуре причин обращений пациенток на
амбулаторно-поликлинический этап оказания медицинской помощи населению.
Внедрение современных технологий в клиническую микробиологию позволило
существенно расширить представления специалистов и наглядно
продемонстрировать, что отрицательное воздействие эндогенных и экзогенных
факторов на микрофлору биотопов макроорганизма различной локализации, в том
числе влагалища, ведет к развитию разнообразных патологических процессов как
воспалительного, так и невоспалительного генеза. Несмотря на значительные
успехи, достигнутые в диагностике, терапии и профилактике дисбиозов влагалища,
их частота продолжает оставаться высокой (Стрижаков А. Н. с соавт., 2003;
Радзинский В. Е. с соавт., 2006; Кира Е. Ф. с соавт., 2007; Макаров О. В. с
соавт., 2007; Culligan P. J. et al., 2005; Klebanoff M. A. et al., 1991,
2005).
Одной из важных причин этого является рост числа
иммунодефицитных состояний, наблюдаемый на фоне ухудшения экологической
обстановки, нерационального питания, стрессов, «бума самодиагностики и
самолечения» с бесконтрольным применением лекарственных средств, в первую
очередь антибиотиков. Чаще всего генитальная инфекция обусловлена несколькими
патогенными факторами: вирусами, бактериями, грибами, простейшими, которые
вызывают схожие по клиническому течению, но различные по патогенезу и методам
лечения заболевания.
Многие авторы (Буданов П. В. с соавт., 2005; Бондаренко К. Р.
с соавт., 2007; Мальцева Л. И. с соавт., 2007; Eschenbach D. A., 2004),
изучавшие различные механизмы вагинального кандидоза, подчеркивают, что грибы
рода Candida нередко участвуют в различных микробных ассоциациях и могут
являться маркерами воспалительных заболеваний мочеполовых органов.
Подробная микробиологическая характеристика кандидозной
инфекции влагалища представлена в исследовании А. С. Анкирской и соавт.
(1998). Авторами выделены три микробиологических варианта вагинального
биоценоза при обнаружении дрожжеподобных грибов Candida: у 68% пациенток
установлена кандидозная моноинфекция; у 18,3%— грибы рода Candida вегетировали
в составе полимикробных ассоциаций, характерных для бактериального вагиноза; у
13,7%— при культуральном исследовании получен рост дрожжеподобных грибов в
титре менее 103 КОЕ/мл (при микроскопическом исследовании
клинического материала влагалища грибов не выявлено, лейкоцитарная реакция
отсутствует), что позволило авторам расценить данный вариант как «нормоценоз»
влагалища.
Анализ видового и количественного состава микрофлоры влагалища
пациенток с урогенитальным кандидозом позволил выделить В. И. Кисиной с соавт.
(1999) следующие типы вагинального микроценоза у обследованных женщин:
I тип. Выделение дрожжеподобных грибов рода
Candida с сохранением лактофлоры у 12,1% пациенток в концентрации 104–105
КОЕ/мл, у 18,97%— в концентрации 106–107 КОЕ/мл.
IIа тип. Выделение дрожжеподобных грибов рода
Candida в количестве 105–107 КОЕ/мл на фоне полимикробной микрофлоры с
наличием Gardnerella vaginalis и/или Mobiluncus, «ключевых» клеток,
снижения/отсутствия лактобацилл у 12,1% пациенток.
IIб тип. Картина микроценоза, аналогичная
таковой при типе IIа, в ассоциации с Mycoplasma hominis и/или Ureaplasma
urealyticum в количестве < 104 КОЕ/мл, со снижением/отсутствием лактофлоры у
13,8% пациенток.
III тип. Выделение дрожжеподобных грибов рода
Candida в количестве 104–106 КОЕ/мл в ассоциации с
Chlamydia trachomatis, с сохранением лактофлоры у 22,4% пациенток.
IVa тип. Выделение дрожжеподобных грибов рода
Candida в количестве 105–107 КОЕ/мл в ассоциации с С.
trachomatis, M.hominis и/или U.urealyticum, с сохранением лактофлоры у 8,6%
пациенток.
IVб тип. Выделение дрожжеподобных грибов рода Candida в
количестве 105–107 КОЕ/мл в ассоциации с М.hominis и/или
U.urealyticum, с сохранением лактофлоры у 24,1% пациенток.
Кроме этого, у 87,9% пациенток обнаружен один или несколько
факультативно-анаэробных микроорганизмов (стафилококки, коринебактерии,
кишечная палочка, энтерококки) в концентрации от 103 до 106
КОЕ/мл.
При анализе результатов изучения кишечного микроценоза
установлено умеренное уменьшение численности популяции бифидобактерий,
лактобактерий в сочетании с резким снижением содержания полноценных
Escherichia coli у 56,9% пациенток. Наряду с изменениями количественного
состава нормальной микрофлоры зарегистрированы и ее качественные сдвиги:
значительное увеличение количества лактозонегативных энтеробактерий у 53,4%
пациенток, Escherichia coli со сниженными ферментативными свойствами у 20,7%,
кокковых форм в количестве 106–108 КОЕ/мл (Staphilococcus
aureus, S.saprophiticus, S.epidermidis) у 77,6% пациенток. Повышенная
пролиферация дрожжеподобных грибов рода Candida в количестве 105–108
КОЕ/мл обнаружена в кишечнике у 46,6% обследованных.
Следует отметить, что манифестация кандидозной инфекции на
фоне уже имеющегося инфекционного процесса влагалища усугубляет течение
последнего и затрудняет лечение. Таким образом, формируется своеобразный
порочный круг: кольпиты любой этиологии способствуют активации
вульвовагинального кандидоза, который, в свою очередь, осложняет течение и
усложняет лечение кольпита, обусловленного бактериально-вирусной инфекцией
(Краснопольский В. И. с соавт., 2005; Мальцева Л. И. с соавт., 2004, 2007).
Все чаще приходится сталкиваться с необоснованными подходами к
диагностике и лечению вульвовагинального кандидоза, что объясняется, с одной
стороны, недостаточно полной осведомленностью врачей в вопросах современных
особенностей этиологии и патогенеза настоящего заболевания, с другой стороны,
излишне агрессивным лоббированием интересов производителей как оригинальных,
так и генерических антимикотиков. Одним из вопросов, важных для гинекологов,
сталкивающихся с проблемой кандидозной инфекции, является причина ее
резистентности к традиционным методам терапии.
Традиционными подходами к лечению вагинальных дисбиозов
следует признать различные методы, основанные на стадийности проводимого
лечения и базирующиеся на понятиях коррекции, элиминации и восстановления
влагалищного биотопа (Кира Е. Ф., 2001, 2007; Кондулукова И. А. с соавт.,
1999; Линева О. И. с соавт., 2005; Мельников В. А., 2007; Шляпников М. Е.,
2005, 2008). Применяемые для коррекции многокомпонентные препараты для
локального (интравагинального) введения всегда оставались популярны как среди
практикующих врачей, так и среди пациенток, благодаря высокой комплаентности,
относительно невысокой стоимости курса лечения в сочетании с достаточной
клинической и микробиологической эффективностью.
Одним из таких препаратов, появившихся в последнее время на
российском рынке, является «Метрогил Плюс» в виде вагинального геля,
содержащий наряду с традиционно используемым для лечения бактериального
вагиноза метронидазолом, антимикотический компонент— клотримазол, что дает
полное основание для использовании препарата в первую очередь для коррекции
бактериального вагиноза, сочетанного с микотической инфекцией. Обоснованным
следует считать введение в состав препарата именно клотримазола, поскольку,
согласно исследованием последних лет (Кудрина М. И. с соавт., 2005; Пестрикова
Т. Ю с соавт., 2005), параллельно с ростом резистентности грибов к
флуконазолам происходит процесс восстановления чувствительности к таким ранее
традиционно используемым на протяжении десятилетий препаратам, как нистатин и
клотримазол (Жестков А. В. с соавт., 2007; Шляпников М. Е. с соавт., 2008).
Дополнительным преимуществом препарата, выгодно отличающим его от большинства
вагинальных форм, следует отметить гелевую основу, способствующую максимально
равномерному распределению активных компонентов препарата на слизистой
оболочке влагалища и экзоцервикса.
Нами проведено проспективное исследование эффективности
использования препарата у 30 женщин репродуктивного возраста с
верифицированным состоянием дисбиоза влагалища.
При анализе жалоб, с которыми обратились пациентки, выявлено,
что большинство пациенток беспокоит наличие выделений из половых путей (60%),
выделения с неприятным запахом (20%), наличие зуда, жжения в области вульвы и
промежности (20%). У 4 пациенток (13,3%) выделения усиливались и начинали
беспокоить только после полового акта или перед менструацией. У 2 пациенток
(6,7%) выделения усиливались на фоне запоров кишечника (табл. 1).У 5 (16,6%)
пациенток жалобы отсутствовали. Диагноз был поставлен при профилактическом
обращении после гинекологического осмотра и микроскопии влагалищных выделений.
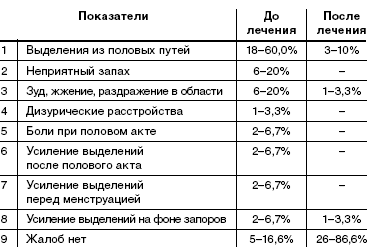
После пятидневного курса лечения препаратом «Метрогил Плюс» в
виде вагинального геля субъективные жалобы отсутствовали у 86,6% женщин. У 10%
сохранялись жалобы на выделения из половых путей: 1 случай (3,3%)— только
выделения, 1 случай (3,3%) выделения в сочетании с усиливающимся зудом, 1
случай (3,3%) жалобы на усиление выделений на фоне запора.
Характер выделений описан в табл. 2. До лечения у пациенток
при гинекологическом осмотре выделения носили следующий характер: в основном
обильные (56,6%), жидкие (33,3%) или пенистые (20%), серо-белые (40%) или
молочные (43,3%), с неприятным запахом(60%). У 3 женщин из 30 (10%) при
гинекологическом осмотре выделения соответствовали норме.
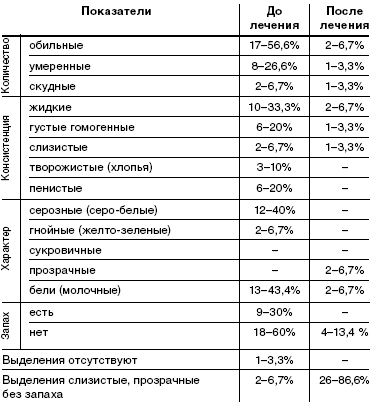
При осмотре после лечения препаратом «Метрогил плюс» в виде
вагинального геля у 26 (86,6%) пациенток выделения имели критерии нормы:
умеренные, слизистые, прозрачные, без запаха. У 4 пациенток (13,4%) выделения
имели патологический характер: обильные 6,7%, жидкие 6,7%. Серозных, гнойных,
пенистых, с неприятным запахом выделений после лечения не наблюдалось.
Из табл. 3 видно, что у большинства пациенток слизистая
влагалища при вагинальном дисбиозе не изменена (63,3%). Но у 26,6% пациенток
отмечалась гиперемия слизистой влагалища, у 6,7%— отечность, в 1 случае
(3,3%)— мацерация слизистой влагалища.

После лечения в 96,7% видимой патологии слизистой влагалища не
отмечается. В 1 случае (3,3%) сохранялась умеренная гиперемия.Эффективность
действия препарата по этому признаку составляет 91%.
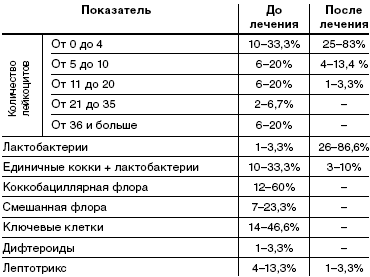
При анализе микроскопии влагалищного содержимого у пациенток
исследуемой группы до лечения в 20% в мазке большое количество лейкоцитов, в
60% коккобациллярная флора, в 46,6%— в мазке «ключевые клетки», в 23,3%
смешанная флора. Влагалищная флора, состоящая только из лактобактерий, в одном
случае— 3,3%.
После лечения у 86,6% пациенток влагалищная флора состояла
только из лактобактерий, лактобактерии с единичными кокками у 10% пациенток,
наличие лептотрикса отмечалось в 3,3% случаев. В 83,3% мазков лейкоциты были
единичные, большого количества лейкоцитов не отмечалось (табл. 4).
Степень чистоты влагалища до лечения в 96,7% случаев была IV;
II степени чистоты влагалища до лечения в исследуемой группе пациентов не
было. После курса лечения препаратом «Метрогил Плюс» в виде вагинального геля
в 76,6% случаев стала II степень чистоты.
Данные, приведенные в табл. 5, наглядно демонстрируют
достаточно высокий комплаенс использования препарата «Метрогил Плюс» в виде
вагинального геля.

Таким образом, на основании проведенного исследования можно
сделать вывод о высокой клинической и лабораторной эффективности использования
препарата «Метрогил Плюс» в виде вагинального геля при коррекции
дисбиотических состояний влагалищного биотопа. Наличие в составе препарата
двух высокоэффективных компонентов— метронидазола и клотримазола, гелевой
основы, обусловливающей равномерное распределение активных компонентов на
слизистой оболочке, в сочетании с высоким комплаенсом, предопределяют
максимально широкое применение Метрогила Плюс в качестве препарата «первой
линии» у женщин с вагинальными дисбиозами.

