Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Кость— это уникальная живая ткань, обладающая свойством
постоянного обновления и регенерации в процессе жизни человека. Появление
дисбаланса в процессах костного ремоделирования (резорбции и
костеобразования), возникающего в пожилом возрасте или по другим причинам,
может вызывать нарушение способности костной ткани к самообновлению, активное
снижение костной массы и развитие остеопороза (ОП).
ОП— это системное заболевание скелета, для которого характерно
снижение массы и прочности кости и повышение риска возникновения переломов. По
оценкам эпидемиологов, в России этим заболеванием страдают в среднем каждая
третья женщина и каждый пятый мужчина в возрасте старше 50 лет, что составляет
более 10 млн человек. Медико-социальное и экономическое значение ОП
определяется высокой частотой и тяжестью его осложнений— переломов, из которых
наиболее опасным считается перелом шейки бедра. В нашей стране пациенты с
переломом шейки бедра занимают 20% травматологических коек, 31–35% больных
погибают в течение первого года после перелома, а 78% выживших в течение
длительного времени нуждаются в постороннем уходе, т. е. фактически становятся
инвалидами.
Постменопаузальный ОП считается наиболее распространенным
типом заболевания, на который проходится около 80% всех случаев
диагностируемого ОП. В большинстве случаев ОП развивается бессимптомно и
первым его проявлением может стать перелом, возникший при минимальной травме
или даже без таковой. Перелом— причина болей, костных деформаций, ограничения
объема движений, потребности в постоянном медицинском уходе, психологических и
других проблем, приводящих к значительному снижению качества жизни. У 10%
пожилых женщин обнаруживаются тяжелые остеопоротические переломы тел позвонков
и еще 50% имеют умеренно выраженные компрессионные деформации. Такие пациентки
жалуются на постоянные боли в спине, значительное уменьшение роста,
сгорбливание, снижение настроения, депрессию и другие психоэмоциональные
расстройства. При подтверждении наличия компрессионных переломов тел позвонков
на рентгенограмме позвоночника вопрос о назначении терапии женщине в
постменопаузе может быть решен даже без проведения костной денситометрии. При
отсутствии данных за переломы в анамнезе диагноз и тактика лечения могут быть
определены только на основании денситометрического обследования позвоночника и
шейки бедра и анализа специфических факторов риска ОП.
Наиболее значимыми параметрами, которые должны оцениваться у
женщины в постменопаузе при определении риска ОП и переломов, являются
возраст, масса тела, наличие переломов в возрасте старше 50 лет, семейный
анамнез ОП и перелома шейки бедра, прием пероральных глюкокортикоидов и других
препаратов, ятрогенных в отношении ОП, курение, злоупотребление алкоголем,
наличие хронических заболеваний, осложняющихся развитием вторичного ОП.
Учитывая повышение предрасположенности к переломам в пожилом возрасте в целом,
у женщин старше 65 лет при наличии вышеуказанных факторов риска вопрос о
назначении терапии ОП может решаться независимо от показателей минеральной
плотности кости (МПК), определенных с помощью костной денситометрии. В более
ранние периоды менопаузы рекомендации по лечению могут даваться только после
денситометрического обследования.
Современные подходы к лечению ОП предполагают воздействие на
костный обмен с позиций «живой» костной ткани, т.е. сохранение нормального
баланса в процессах костного ремоделирования, необходимого для поддержания
оптимальных количественных и качественных характеристик костной ткани в
пожилом возрасте. Единственным препаратом для лечения ОП, оказывающим двойной
разнонаправленный эффект на костный метаболизм (стимулирующее действие на
костное формирование и уменьшение активности резорбции), является стронция
ранелат.
Стронция ранелат (Бивалос)— принципиально новый препарат для
терапии постменопаузального ОП. В течение двух последних десятилетий
многочисленные экспериментальные и клинические исследования продемонстрировали
уникальную способность стронция ранелата одновременно стимулировать
образование и замедлять резорбцию кости, а также показали высокую
эффективность препарата в восстановлении костной массы и снижении риска
переломов у больных постменопаузальным ОП.
Механизм действия стронция ранелата при ОП
Стронций также, как и кальций, является элементом четвертой
группы периодической системы элементов. По физико-химическим свойствам сходен
с кальцием, имеет высокое сродство к костной ткани и избирательно
накапливается в скелете: 99% стронция, присутствующего в организме,
концентрируется в костях. Стронция ранелат содержит два атома стабильного
стронция, связанных с органической (ранеловой) кислотой, — такая формула
обеспечивает оптимальную биодоступность и переносимость препарата.
Стронция ранелат— единственный препарат, позитивное влияние
которого на оба процесса костного ремоделирования как в фундаментальных, так и
в клинических исследованиях достоверно доказано. В частности, в
экспериментальных работах показано стимулирующее воздействие на процесс
костеобразования. В культуре клеток свода черепа новорожденных крыс после
24-часового экспонирования препарата в растворе стронция ранелата наблюдалось
усиление репликации преостеобластов в зрелые остеобласты, повышение активности
функционирующих остеобластов и достоверное увеличение процесса
костеобразования на 30–35%. Также показано увеличение репликации и
дифференциации остеобластов костной ткани человека, вероятно, за счет влияния
на кальций-чувствительные рецепторы преостеобластов. Имеются данные и о
повышении дифференцировки и увеличении продолжительности жизни остеоцитов—
клеток, осуществляющих трофическую и структурную функции в костной ткани и,
таким образом, влияющих на качество кости.
Одновременно со стимуляцией костеобразования, стронция ранелат
уменьшает скорость костной резорбции, замедляя дифференцировку
клеток-предшественниц в зрелые остеокласты за счет влияния на систему
регулирования костного ремоделирования «RANK-RANKL-остеопротегерин». Стронция
ранелат усиливает продукцию остеобластами белка остеопротегерина, который
блокирует взаимодействие RANK и RANKL на преостеокластах, тем самым подавляя
созревание остеокластов и снижая активность резорбции кости. Выработка
остеопротегерина значительно уменьшается с возрастом, в частности, в
постменопаузе на фоне дефицита эстрогенов; с этим отчасти связывают усиление
костной резорбции и развитие ОП у женщин в постменопаузе. Таким образом,
стронция ранелат воздействует на физиологические регуляторные механизмы, не
нарушая функционирование и жизнеспособность костных клеток.
Двойное влияние препарата на процессы костного ремоделирования
было подтверждено в клинических работах. В исследовании SOTI (Spinal
Osteoporosis Therapeutic Intervention), в которое было рандомизировано 1649
женщин c подтвержденным постменопаузальным ОП, уже через 3 месяца лечения
стронция ранелатом отмечено достоверное повышение костно-специфической
щелочной фосфатазы (КС-ЩФ), свидетельствующее о стимуляции костеобразования, и
параллельное снижение уровня С-телопептида коллагена типа I (СТх)— маркера
активности резорбции. Аналогично в исследовании TROPOS (TReatment Of
Peripheral OSteoporosis), в которое была включена 5091 женщина в возрасте
старше 70 лет, на фоне всего периода терапии стронция ранелатом уровень КС-ЩФ
был достоверно выше, а маркера резорбции N-телопептида коллагена типа I (NTх)—
ниже, чем у пациенток в группе плацебо. Данные гистоморфометрического анализа
биопсийного материала после 5 лет лечения стронция ранелатом достоверно
подтверждают его стимулирующий эффект на костеобразование (увеличение
остеобластических поверхностей на 38% и повышение скорости минерализации в
трабекулярной и кортикальной кости на 8% и 11% соответственно в сравнении с
плацебо) и подавляющее влияние на резорбцию (снижение числа эндостальных
эрозированных поверхностей, трабекулярных остеокластических поверхностей и
общего количества остеокластов).
Таким образом, стронция ранелат обладает уникальным свойством
двойного разнонаправленного влияния на процессы костного ремоделирования, в
отличие от препаратов других фармакологических групп, что немаловажно с
позиций физиологического воздействия на «живую» костную ткань при лечении ОП.
Улучшая баланс между резорбцией и костеобразованием, стронция ранелат повышает
степень минерализации кости и увеличивает толщину участков минерализации в
новой костной ткани. Вновь образованная кость характеризуется высоким
качеством— по данным биопсий, проводимых в рамках различных клинических
исследований, на фоне терапии стронция ранелатом в костной ткани не было
выявлено признаков остеомаляции или дефектов минерализации, в частности, не
обнаружено признаков увеличения толщины остеоида, гиперминерализации или
задержки первичной минерализации.
Клиническая эффективность стронция ранелата при
постменопаузальном ОП
Лечение постменопаузального ОП направлено на снижение риска
развития переломов костей, повышение МПК и прочности костной ткани. Кроме
того, важной целью медикаментозной терапии является уменьшение болевого
синдрома в спине, расширение двигательной активности и улучшение качества
жизни пациентов. Главным критерием эффективности любого препарата,
применяемого при лечении ОП, является снижение риска возникновения новых
переломов, доказанное в ходе проведения двойных слепых контролируемых
исследований при длительности терапии не менее 3 лет. Клиническая
эффективность и безопасность стронция ранелата была убедительно
продемонстрирована в нескольких широкомасштабных клинических испытаниях,
проводившихся в 75 клинических центрах 12 стран мира, с участием 9196 женщин в
постменопаузе, лечившихся стронция ранелатом до 8 лет включительно.
Стронция ранелат показал хорошие данные по профилактике
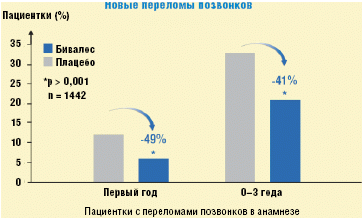
переломов любых локализаций. В исследовании SOTI у пациенток с
постменопаузальным ОП достоверное уменьшение вероятности возникновения
переломов позвонков уже через 1 год приема препарата составило 49% (р<0,001),
а через 3 года— 41% (р<0,001) (рис. 1).
Другое крупное исследование— TROPOS подтвердило эффективность
стронция ранелата в профилактике переломов тел позвонков, а также
продемонстрировало его эффективность в снижении риска периферических переломов
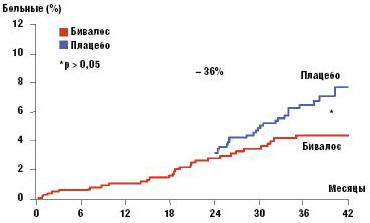
у женщин в постменопаузе. В частности, через 3 года было обнаружено
достоверное по сравнению с плацебо снижение риска всех непозвоночных переломов
на 16%, а в группе пациенток с высоким риском перелома шейки бедра (МПК шейки
бедра по Т-критерию ≤–3,0)— уменьшение числа больных, у которых возник перелом
этой локализации, на 36% (р<0,05) (рис.2).
К стронция ранелату не развивается резистентность, и его
антипереломная эффективность не ослабевает даже при длительной терапии— до 5–8
лет. Анализ результатов продолжительного лечения стронция ранелатом женщин,
страдающих постменопаузальным ОП, показал, что через 5 лет риск развития
позвоночных переломов достоверно снижается на 24% (р<0,001), непозвоночных
переломов— на 15% (р=0,03), а перелома шейки бедра у пациенток в возрасте 74
лет и старше— на 43% (р=0,036). При наблюдении пациенток, принимавших стронция
ранелат до 8 лет, отмечена стабильно высокая приверженность терапии (87,9%) и
сохранение антипереломной активности. Важно, что эффективность стронция
ранелата не зависит от степени тяжести ОП, наличия в анамнезе переломов
позвонков, массы тела, соотношения факторов риска и исходной активности
костного ремоделирования. В последних Европейских клинических рекомендациях по
диагностике и лечению постменопаузального ОП (2008 г.) стронция ранелат
представлен как один из препаратов с самой широкой и доказанной эффективностью
по снижению риска переломов различных локализаций.
Стронция ранелат способствует выраженному приросту МПК как в
осевом, так и в периферическом скелете. Достоверное повышение МПК по сравнению
с плацебо наблюдается уже через 6 месяцев лечения, а через 3 года повышение
минеральной насыщенности костной ткани составляет 14,4% в поясничных
позвонках, 8,3% в шейке бедра и 9,8% в бедре в целом по сравнению с плацебо (p<0,001)
(рис. 2)]. В среднем, при лечении стронция ранелатом можно ожидать ежегодный
прирост МПК в позвоночнике на 4%, в шейке бедра— на 2%. При этом отмечена
четкая корреляция между увеличением МПК при лечении стронция ранелатом и его
эффективностью в предотвращении переломов. Так, на каждый 1% увеличения МПК
шейки бедра риск возникновения нового перелома позвонков в течение 3 лет
снижается на 3%. Таким образом, увеличение МПК на фоне терапии стронция
ранелатом может служить маркером клинической эффективности лечения.
Улучшение субъективного самочувствия и качества жизни больных—
одна из важнейших целей терапии ОП. Стронция ранелат— первый препарат, влияние
которого на все аспекты качества жизни пациенток с ОП исследовалось
целенаправленно. Препарат достоверно снижает риск развития клинических
переломов позвонков, сопровождающихся патологической симптоматикой (болями в
спине, уменьшением роста, ограничением двигательной активности) через год
лечения на 52% (р=0,003), через 3 года— на 38% (р<0,001). На фоне терапии
уменьшается число больных, испытывающих боли в спине (через 12 месяцев— на
29%, р=0,03, через 3 года— на 32%, р = 0,006), а также количество пациенток с
уменьшением роста. В целом препарат позитивно влияет как на физические, так и
на психоэмоциональные аспекты качества жизни, значительно улучшая общее
самочувствие лечившихся пациентов ОП по сравнению группой плацебо (р<0,05).
Опыт применения Бивалоса (стронция ранелата) в России
Стронция ранелат зарегистрирован в Российской Федерации в 2005
г. под коммерческим названием «Бивалос». Широкое назначение Бивалоса в
отечественной клинической практике в течение 3 лет подтвердило высокую
эффективность, хорошую переносимость и удобство применения препарата у женщин,
страдающих постменопаузальным ОП.
В российском многоцентровом годичном исследовании изучалась
эффективность Бивалоса у 60 женщин в периоде постменопаузы с подтвержденным
системным ОП. Результаты работы убедительно продемонстрировали позитивное
влияние препарата на прирост МПК в различных участках скелета: в среднем на
4,7% в позвоночнике (p<0,000001), на 2,0% в шейке бедра (p<0,0001) и на 3,1% в
проксимальном отделе бедра в целом (p<0,000001). Также были получены данные,
соотносимые с результатами международных исследований, о достоверном
разнонаправленном изменении уровня маркеров костеобразования (КС-ЩФ) и
резорбции (СТх) и улучшении качества жизни больных. Более 70% врачей и
пациентов оценили терапию Бивалосом как хорошую и более 90%— высоко оценили
переносимость препарата.
Быстрое наступление клинической эффективности и улучшение
общего самочувствия пациентов при назначении терапии ОП— важный фактор для
мотивации больных ОП на долгосрочное лечение. Опыт применения Бивалоса в
МОНИКИ им. М. Ф. Владимирского с включением 40 женщин с установленным
постменопаузальным ОП показал, что значимое повышение МПК можно ожидать уже
через 6 месяцев после начала лечения: в среднем на 4,4% в позвоночнике (p<0,001)
и на 2,4% в шейке бедра (p<0,05). Бивалос способствует снижению уровня СТх и
повышению концентрации остеокальцина в течение первых месяцев лечения, что
подтверждает данные о двойном механизме действия препарата на костное
ремоделирование. При анкетировании пациенток с помощью вопросника QUALEFFO-41,
уже через 3 месяца женщины отметили достоверное уменьшение болей в спине (p<0,001),
подвижности (p=0,01) и суммарного показателя качества жизни (p<0,05), а через
6 месяцев— указали расширение социальной активности (p<0,05) и повышение общей
оценки собственного здоровья (p<0,05).
Таким образом, опыт применения Бивалоса в России подтвердил
высокую эффективность препарата по воздействию на костную массу, влиянию на
процессы костного метаболизма и качество жизни больных. Удобство применения в
сочетании с высокой эффективностью обеспечивают высокую приверженность лечению
при долгосрочной терапии постменопаузального ОП. С позиций фармакоэкономики,
стронция ранелат характеризуется выгодным соотношением
«эффективность/стоимость» в странах Европы, поэтому клинико-экономическую
целесообразность применения Бивалоса для лечения женщин с постменопаузальным
ОП в России можно считать вполне обоснованной.
Рекомендации по приему стронция ранелата
Препарат не имеет значимых противопоказаний к назначению и
характеризуется хорошей переносимостью. В исследованиях SOTI и TROPOS за 3
года наблюдения не было отмечено достоверной разницы в частоте побочных
реакций между группами больных, принимавших стронция ранелат и плацебо.
Наиболее частыми побочными эффектами при приеме стронция ранелата являются
тошнота (6,6% против 4,3% в группе плацебо), диарея (6,1% против 3,6%
соответственно) и головная боль (3,0 против 2,4% соответственно). Указанные
побочные эффекты, как правило, не требуют прекращения терапии и самостоятельно
проходят в течение первых 3 месяцев. Имеются данные, что в редких случаях
могут наблюдаться венозные тромбозы и тромбоэмболии— 0,9% против 0,6% в группе
плацебо, однако вероятность развития тромбозов при лечении стронция ранелатом
не превышает средние популяционные данные (у женщин в возрасте 70–79 лет он
составляет 0,82%, а в целом в популяции после 75 лет— 1,2%). Препарат не
повышает риск развития серьезных осложнений со стороны верхних отделов
желудочно-кишечного тракта (язвы, эрозивного гастрита и эзофагита и др.).
Из-за отсутствия опыта применения препарат не следует назначать женщинам
детородного возраста и пациенткам с клиренсом креатинина менее 30 мл/мин.
Рекомендуемая схема приема стронция ранелата— ежедневно в
дозировке 2 г (1 саше) через 2 часа после ужина. Стронция ранелат можно
сочетать (но не принимать одномоментно) с препаратами кальция (1000 мг/сут) и
витамина D (400–800 МЕ/сут). У пожилых женщин и больных с умеренным нарушением
функции печени и почек коррекции дозы не требуется.
Заключение
С современных позиций лечения постменопаузального ОП, стронция
ранелат (Бивалос)— инновационный лекарственный препарат, физиологически
регулирующий функцию клеток костной ткани и активность процессов костного
ремоделирования— резорбции и костеобразования. Сохраняя свойства «живой
костной ткани», у больных постменопаузальным ОП Бивалос достоверно снижает
риск развития позвоночных и периферических переломов, включая перелом шейки
бедра, значительно повышает МПК и увеличивает прочность кости. Препарат
демонстрирует хорошую эффективность, переносимость и удобство применения даже
при длительных сроках лечения— 8 лет и более.
В настоящее время стронция ранелат позиционируется как
препарат первой линии лечения постменопаузального ОП в странах Евросоюза и
Восточной Европы, Австралии, Гонконге, Сингапуре и др. Стронция ранелат
включен в Американские, Европейские и Российские клинические рекомендации по
диагностике и лечению остеопороза.

