Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
В настоящее время ВИЧ-инфекция у детей является одной из
актуальнейших проблем во всем мире. Первоначально в нашей стране она была
обусловлена внутрибольничной заболеваемостью, а в последние годы — рождением
детей ВИЧ-инфицированными женщинами. Более 90% детской ВИЧ-инфекции является
результатом именно перинатальной трансмиссии вируса.
Больные ВИЧ-инфекцией дети и их близкие нуждаются в
профессиональной лечебно-реабилитационной поддержке их социального
функционирования и оптимального качества жизни. Эта работа должна быть прежде
всего направлена на «обновление взглядов» как на больных детей, так и их
родителей. Очень важно не оставлять их в социальной изоляции, ведь порой
вторичные проблемы негативно действуют на больного и его родственников не
меньше, чем само заболевание.
По данным Федерального научно-методического центра по
профилактике и борьбе со СПИДом, в России на 31 декабря 2006 г.
зарегистрировано 2093 ребенка с подтвержденным диагнозом «ВИЧ-инфекция», из
них 169 детей — в Москве [4].
По данным МГЦ СПИД за последние 10 лет произошло уменьшение
числа детей с врожденной ВИЧ-инфекцией. Так, если в 2001 году, когда
химиопрофилактика вертикальной трансмиссии ВИЧ-инфекции только начинала
проводиться, число ВИЧ-инфицированных детей составляло 8%, то в 2006 году —
всего 1,5%. Таких результатов удалось добиться благодаря введению в практику
схемы профилактики согласно протоколу от 1996 г. PACTG 076 (Pediatric AIDS
Clinical Trial Group), который основан на назначении беременной женщине
Азидотимидина — антиретровирусного препарата из группы нуклеозидных
ингибиторов обратной транскриптазы.
Однако даже своевременное проведение химиопрофилактики не
исключает полностью возможность перинатальной передачи ВИЧ-инфекции от матери
плоду.
К факторам, повышающим риск передачи ВИЧ от матери к ребенку,
относятся:
-
высокий уровень вирусной нагрузки матери;
-
поздние стадии ВИЧ-инфекции у матери;
-
преждевременное излитие околоплодных вод с безводным промежутком более 4
часов;
-
инвазивные вмешательства, повреждающие плод;
-
эпизиотомия;
-
родоразрешение через естественные родовые пути (при вирусной нагрузке
более 1000 копий/мл перед родами);
-
недоношенность (гестационный возраст менее 37 недель);
-
грудное вскармливание.
При отсутствии профилактики перинатальной передачи ВИЧ, риск
заражения составляет 30–40% [3].
Причинами отсутствия химиопрофилактики во время беременности и
родов могут быть: диагностика ВИЧ-инфекции только во время родов, употребление
наркотических веществ во время беременности, добровольный отказ от
профилактики, в т. ч. по религиозным убеждениям, беременность до внедрения в
практику профилактики вертикальной передачи ВИЧ и домашние роды.
Особенности клинических проявлений ВИЧ-инфекции у детей
определяются стадией онтогенеза, на которой произошло инфицирование плода ВИЧ
в организм (внутриутробно или интранатально) и от возраста ребенка в случае
постнатального заражения.
При заражении плода в позднем перинатальном периоде или
ребенка после рождения течение ВИЧ-инфекции почти не отличается от взрослых.
Целью данной работы является оценка эффективности общей и
высокоактивной антиретровирусной терапии (ВААРТ) у детей с врожденной
ВИЧ-инфекцией.
Задачи
-
Выявить наиболее частые клинические проявления у детей с врожденной
ВИЧ-инфекцией.
-
Выявить оппортунистические и сопутствующие заболевания у детей с
врожденной ВИЧ-инфекцией.
-
Проанализировать динамику показателей CD4-лимфоцитов до начала ВААРТ и
через 3 месяца.
-
Сравнить уровень вирусной нагрузки в динамике: до начала ВААРТ и через 3
месяца.
-
Определить влияние ВААРТ на течение оппортунистических заболеваний.
-
Выявить причины неэффективности ВААРТ.
Нами проанализированы 60 случаев врожденной ВИЧ-инфекции у
детей в возрасте от 1 месяца до 7 лет, в т. ч.: 30 амбулаторных карт детей,
состоящих на диспансерном учете в московском городском центре СПИД (МГЦ СПИД);
30 историй болезни детей, находящихся на стационарном лечении в МГЦ СПИД.
По результатам анализа амбулаторных карт и историй болезни
нами были выявлены следующие наиболее часто встречающиеся клинические
проявления врожденной ВИЧ-инфекции у детей: поражение ЦНС, лимфаденопатия,
гепатолиенальный синдром, интерстициальные изменения в легких, анемия,
гипотрофия, недоношенность.
Поражение ЦНС в нашем исследовании наблюдалось у 75% детей.
Установлено, что ВИЧ является не только иммунотропным, но и нейротропным
вирусом и проникает через гематоэнцефалический барьер на ранних этапах
инфекционного процесса в организме, поражая олигодендроциты и астроциты,
нейроциты, микроглию, макрофаги, клетки эндотелия кровеносных сосудов,
фибробластоподобные клетки мозга. Указанные клетки имеют рецептор CD4 и
считаются прямыми клетками-мишенями для ВИЧ. Патоморфологические изменения
головного мозга при ВИЧ-инфекции могут быть охарактеризованы как
альтернативно-дистрофические, с периваскулярным отеком, дистрофией нейронов,
очаговой демиелинизацией и циркуляторными нарушениями.
У обследованных нами ВИЧ-инфицированных детей наблюдался
полиморфизм клинических неврологических проявлений.
В начале заболевания отмечались астеноневротический и
цереброастенический синдромы. Для этой стадии СПИДа характерной была
ВИЧ-энцефалопатия. Также было установлено, что тяжесть поражения нервной
системы более выражена у детей первого года жизни.
ВИЧ-энцефалопатия — тяжелое заболевание, затрагивающее все
функции ЦНС. При подострой прогрессирующей энцефалопатии утрачиваются ранее
приобретенные умения и навыки. Вялотекущая прогрессирующая энцефалопатия
замедляет или прекращает формирование новых навыков, не затрагивая при этом
старых. Обе формы прогрессирующей энцефалопатии резко замедляют психомоторное
развитие. Дети с непрогрессирующей энцефалопатией продолжают приобретать новые
навыки, но медленнее, чем здоровые сверстники.
Одновременно поражение ЦНС проявлялось грубой задержкой
психомоторного развития, синдромом гипервозбудимости и гидроцефальным
синдромом.
Клиническая манифестация ВИЧ-инфекции у детей разнообразна и
зачастую неспецифична. Нами установлено, что лимфаденопатия, ассоциированная с
гепатоспленомегалией, является одним из наиболее ранних признаков врожденной
ВИЧ-инфекции. Так, персистирующая генерализованная лимфаденопатия выявлена в
64% случаев, а гепатолиенальный синдром — в 38% случаев. Сочетание обоих
синдромов наблюдалось у 36% детей.
Интерстициальные изменения в легких были у 25% детей, они
развивались в результате многократно перенесенных ранее пневмоний различной
этиологии.
Из гематологических проявлений чаще всего отмечалась анемия
(24% больных), что было связано с приемом антиретровирусного препарата из
группы нуклеозидных ингибиторов обратной транскриптазы ВИЧ — «Зидовудина».
Гипотрофия (от I до III степени) была выявлена у 18% больных,
недоношенность отмечалась в 14% случаев.
Из сопутствующих заболеваний чаще встречались хронический
вирусный гепатит С и туберкулез, а из оппортунистических заболеваний —
грибковые поражения кожи и слизистых, пневмоцистная пневмония, герпетическая
инфекция, цитомегаловирусная инфекция.
Грибковые поражения кожи и слизистых отмечались у 38% детей.
Наиболее частая этиология — грибы рода Candida.
Чаще всего наблюдался оральный кандидоз, которому сопутствовал
ангулярный хейлит, когда в углах рта возникали мацерации, эрозии, трещины. По
краям трещин иногда отмечался гиперкератоз. Для детей, больных ВИЧ/СПИДом,
характерно рецидивирующее течение орофарингеального кандидоза. В зависимости
от степени иммунодефицита (определяется по количеству CD4-лимфоциов), было
отмечено возникновение рецидивов через несколько месяцев, недель, а иногда и
дней после отмены антимикотической терапии. Продолжительность периодов
ремиссии была индивидуальна у каждого больного.
Наиболее опасная оппортунистическая инфекция, пневмоцистная
пневмония, наблюдалась у 26% детей. Пневмоцистная пневмония может развиться в
любом возрасте, но у наблюдавшихся нами больных почти в половине случаев
приходилась на первые 6 месяцев жизни.
Обычно она развивалась остро, проявляясь одышкой и кашлем.
Однако в некоторых случаях сначала появлялся кашель, и в течение нескольких
дней к нему присоединялось постепенно нарастающее тахипноэ. Вначале появлялось
навязчивое покашливание, затем кашель становился коклюшеподобным, особенно в
ночное время. У ребенка отмечалась прогрессирующая слабость, снижение
аппетита, бледность кожного покрова, цианоз носогубного треугольника.
Температура тела в начале заболевания была нормальной или субфебрильной [1,
5].
При физикальном исследовании выявлялись тахипноэ, одышка,
влажные и сухие хрипы. При прогрессировании пневмонии, возможно, возникала
легочно-сердечная недостаточность.
Рентгенологические изменения, характерные для пневмоцистной
пневмонии в виде снижения прозрачности легких, появления симметричных теней в
виде крыльев бабочки, «ватных легких», определялись менее чем у половины
больных.
Диагноз пневмоцистной пневмонии был основан на обнаружении
возбудителя в мокроте, в материале, полученном при бронхоальвеолярном лаваже
или биопсии легкого. У большинства детей пневмоцистная пневмония сочеталась с
другими оппортунистическими заболеваниями.
Для лечения применялся Бисептол (сульфаметоксазол +
триметоприм), который назначался при первом подозрении на пневмоцистную
пневмонию до получения результатов микробиологического исследования.
Профилактика пневмоцистной пневмонии проводилась тем же препаратом всем детям,
рожденным ВИЧ-инфицированными женщинами в возрасте от 6 недель до 4 месяцев до
исключения диагноза «ВИЧ-инфекция». ВИЧ-инфицированным детям первичная
профилактика пневмоцистной пневмонии проводилась в течение первого года жизни.
Дальнейшее проведение профилактики рекомендуется детям при уровне
CD4-лимфоцитов < 15%. У детей, перенесших пневмоцистную пневмонию,
рекомендуется пожизненная профилактика [5].
У ВИЧ-инфицированных детей могут наблюдаться различные
поражения кожи.
В 8% случаев была выявлена инфекция кожного покрова,
обусловленная вирусом Varicella-Zoster. На фоне иммунодефицита наблюдалось
тяжелое генерализованное течение инфекции с полиорганными поражениями.
Цитомегаловирусная инфекция отмечалась у 7% детей. Клинически
манифестация заболевания сопровождалась разнообразной симптоматикой — от
сиалоаденита и лимфаденита до тяжелых диссеминированных форм.
Хронический вирусный гепатит С был выявлен у 16% детей и
обусловлен вертикальной трансмиссией вируса от матери плоду.
Туберкулез отмечался в 5% случаев. Случаи заболевания были
обусловлены трансплацентарным путем инфицирования.
Диагностика врожденной ВИЧ-инфекции
Диагноз ВИЧ-инфекции у ребенка может быть установлен при
получении двух положительных результатов ПЦР в двух образцах крови, взятых в
разные дни. ПЦР-диагностика проводится: в первые 48 часов жизни, в 14 дней
жизни, в 1–2 месяца, в 3–6 месяцев [5].
ВИЧ-инфекцию можно исключить: при 2 и более отрицательных
результатах ПЦР на ВИЧ (один в возрасте до 1 месяца, один — старше 4 месяцев);
при 2 и более отрицательных серологических тестах на антитела к ВИЧ в возрасте
старше 6 месяцев при отсутствии грудного вскармливания.
На основании приказа Минздрава РФ № 606 от 19.12.2003 г.,
ребенок может быть снят с диспансерного учета по ВИЧ-инфекции в возрасте 18
месяцев при отрицательном результате исследования на антитела к ВИЧ методом
ИФА, отсутствии гипогаммаглобулинемии, отсутствии клинических проявлений
ВИЧ-инфекции.
Лечение
Основным компонентом лечения больных ВИЧ-инфекцией является
антиретровирусная терапия, с помощью которой можно добиться контролируемого
течения заболевания, то есть состояния, при котором удается остановить
прогрессирование болезни. Антиретровирусная терапия должна проводиться
пожизненно, непрерывно. В процессе лечения проводятся обследования, цель
которых — контроль его эффективности и безопасности. В плановом порядке эти
обследования проводятся через 4 и 12 недель после начала лечения, впоследствии
— каждые 12 недель.
Лекарственная терапия ВИЧ-инфекции включает в себя базисную
терапию (которая определяется стадией заболевания и уровнем CD4-лимфоцитов), а
также терапию вторичных и сопутствующих заболеваний [2].
В настоящее время придерживаются рекомендаций, разработанных
Рабочей группой по антиретровирусной терапии и лечению ВИЧ-инфекции у детей
(создана Национальным центром ресурсов Центра Франсуа-Ксавье Банью,
Медицинским и стоматологическим университетом Нью-Джерси (UMDNJ), Управлением
ресурсов и служб здравоохранения (HRSA) и Национальным институтом
здравоохранения (NIH) США), согласно которым всех ВИЧ-инфицированных детей
разделяют на 3 возрастных группы (до 12 месяцев, от 1 года до 5 лет и 5 лет и
старше) [5].
Детям до 12 месяцев рекомендуется начинать антиретровирусную
терапию, независимо от клинических проявлений, количества CD4-лимфоцитов и
уровня вирусной нагрузки.
Детям от 1 года до 5 лет и старше 5 лет проведение
антиретровирусной терапии рекомендуется:
-
при наличии СПИДа или наличии симптомов, соответствующих стадии С и
большей части симптомов стадии B (по классификации CDC, 1994 г.),
независимо от количества CD4-лимфоцитов и уровня вирусной нагрузки;
-
при уровне CD4-лимфоцитов < 25% у детей от 1 года до 5 лет и уровне
CD4-лимфоцитов < 350 клеток/мм3 у детей > 5 лет, независимо от клинических
симптомов и уровня вирусной нагрузки;
-
детям в возрасте 1 год и старше, которые находятся на стадиях N, A или
имеют следующие симптомы стадии В: единственный эпизод тяжелой
бактериальной инфекции или лимфоидную интерстициальную пневмонию при
уровне CD4-лимфоцитов ≥ 25% у детей от 1 года до 5 лет или уровне
CD4-лимфоцитов ≥ 350 клеток/мм3 у детей > 5 лет и уровне вирусной нагрузки
≥ 100 000 копий/мл.
Антиретровирусную терапию можно временно не назначать детям, у
которых нет клинических проявлений ВИЧ-инфекции или они слабо выражены, при
уровне CD4-лимфоцитов ≥ 25% у детей от 1 года до 5 лет или уровне
CD4-лимфоцитов ≥ 350 клеток/мм3 у детей > 5 лет и уровне вирусной нагрузки <
100 000 копий/мл.
ВААРТ назначается ребенку пожизненно.
Терапия проводится не менее чем тремя препаратами с режимом
приема 2–3 раза в день.
Применяются следующие группы антиретровирусных препаратов:
-
Препараты, блокирующие процесс обратной транскрипции (синтез вирусной ДНК
на матрице вирусной РНК), — ингибиторы обратной транскриптазы. Среди них
выделяют две группы препаратов:
-
нуклеозидные ингибиторы обратной транскриптазы (НИОТ) (измененные молекулы
нуклеозидов), встраивающиеся в синтезируемую цепочку ДНК и прекращающие ее
дальнейшую сборку: зидовудин (Азидотимидин)**, фосфазид*, ставудин*,
диданозин**, зальцитабин*, ламивудин**, абакавир*, Комбивир (ламивудин +
зидовудин);
-
ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ), блокирующие
необходимый для осуществления обратной транскрипции вирусный фермент —
обратную транскриптазу: эфавиренз*, невирапин**.
-
Препараты, блокирующие процесс формирования полноценных протеинов ВИЧ и, в
конечном итоге, сборку новых вирусов — ингибиторы протеазы (ИП) ВИЧ:
саквинавир, индинавир, нелфинавир**, ритонавир*, лопинавир/ритонавир**.
-
Препараты, воздействующие на рецепторы, используемые вирусом для
проникновения ВИЧ в клетку хозяина, — ингибиторы слияния.
Многие из этих препаратов применяются в виде разных
лекарственных форм (в том числе предназначенных для лечения детей младшего
возраста). Кроме того, зарегистрированы комбинированные препараты, содержащие
два и более препарата в одной таблетке (капсуле).
При выборе оптимальной схемы терапии для конкретного больного
принимается во внимание: эффективность и токсичность препаратов, возможность
их сочетания между собой, переносимость препаратов пациентом, удобство приема
препаратов — кратность приема, сочетание антиретровирусных препаратов с
препаратами, которые применяются (или, возможно, будут применяться) для
лечения имеющихся у пациента вторичных и сопутствующих заболеваний.
Комбинация из двух препаратов НИОТ является основой различных
схем антиретровирусной терапии.
Для детей рекомендуются схемы терапии, включающие 2 НИОТ и 1
ИП или 2 НИОТ и 1 ННИОТ.
В дальнейшем, при эффективной ВААРТ, уровень вирусной нагрузки
должен быть ниже уровня определения, но возможны подъемы, не превышающие 1000
копий/мл (рис. 1).
В результате проведенного анализа амбулаторных карт и историй
болезни детей с врожденной ВИЧ-инфекцией, получающих антиретровирусную
терапию, было установлено, что в среднем уже через 3 месяца от начала лечения
наблюдалось снижение уровня вирусной нагрузки ниже уровня определения (ниже
400 копий в мл), а количество CD4-лимфоцитов повышалось (рис. 2).
Эффективность специфической терапии определялась:
-
готовностью пациента и его семьи к началу ВААРТ;
-
соблюдением правил назначения ВААРТ;
-
удобной лекарственной формой препарата;
-
предупреждением лекарственных взаимодействий;
-
своевременным выявлением побочного действия ВААРТ.
Если ВААРТ является неэффективной и это не связано с
нарушением режима приема препарата, приемом лекарств антагонистов и т. п.,
рекомендуется проведение теста на резистентность вируса к лекарственным
препаратам и назначение новой схемы терапии с учетом результатов этого теста.
На 2007 г. из 169 детей, состоящих на учете в МГЦ СПИД, 100
детей получают ВААРТ. Отсутствие приверженности, т. е. неготовность семьи к
проведению ВААРТ, несоблюдение режима приема препаратов было в 1-м случае, что
привело к летальному исходу.
Положительный тест на резистентность к ВААРТ был у 5 детей
(13%). Схема лечения была пересмотрена.
Клинический пример. М. А., 2 года 11 месяцев. Дата рождения:
18.03.05 г. Находилась в детском отделении с 31.03.05 г. по 3.03.06 г. с
диагнозом: ВИЧ-инфекция, стадия вторичных заболеваний IIIВ: генерализованная
цитомегаловирусная инфекция, рецидивирующая пневмония, распространенная
грибковая инфекция, анемия, энцефалопатия смешанного генеза, грубая задержка
психомоторного и физического развития, истощение IV ст., гидроцефальный
синдром, глубокая недоношенность, лимфаденопатия, гепатолиенальный синдром.
Ребенок от ВИЧ-инфицированной матери 25 лет, 7 беременностей
(5 медицинских абортов), 2 преждевременных родов в домашних условиях, в
женской консультации не наблюдалась. Профилактику во время беременности не
получала. Вес при рождении 1280 г, рост 42 см. Состояние при поступлении
тяжелое за счет острой дыхательной недостаточности, обусловленной пневмонией с
ателектазами.
За время нахождения в стационаре многократно болела ОРЗ и
пневмониями с обструктивным синдромом. С сентября 2005 г. полисегметарная
пневмония рецидивирующего течения, плевропневмония, в ноябре 2005 г.
деструктивная правосторонняя пневмония. С января 2006 г. интерстициальные
изменения в легких, плевральные спайки.
Иммунный статус на 18.06.05 г.: CD4 – 920 (19%), вирусная
нагрузка 6 000 000 копий/мл. С мая 2005 г. проводилась специфическая терапия:
Вирасепт + Эпивир ТриТиСи + Калетра. Иммунный статус на 3.03.06 г.: CD4 – 1480
(20%), вирусная нагрузка 7300 копий/мл. На фоне лечения состояние
стабилизировалось, ребенок выписан в удовлетворительном состоянии под
амбулаторное наблюдение.
Выводы:
-
Чаще всего врожденная ВИЧ-инфекция проявляется симптомами поражения ЦНС,
лимфаденопатией, гепатоспленомегалией.
-
Из оппортунистических инфекций ведущими являются грибковые поражения кожи
и слизистых, пневмоцистная пневмония, а из сопутствующих заболеваний —
хронический вирусный гепатит С.
-
На фоне приема ВААРТ отмечалась положительная клиническая динамика и
улучшение специфических лабораторных показателей: на 12–24 неделе лечения
количество CD4-лимфоцитов повысилось в среднем на 5% от исходного уровня,
в то время как уровень вирусной нагрузки снизился до неопределяемого (<
400 копий/мл).
-
Отмечался постепенный регресс вторичных заболеваний в результате
проводимой специфической терапии в сочетании с ВААРТ.
-
Причинами неэффективности ВААРТ были:
— отсутствие приверженности;
— развитие резистентности к проводимой терапии (отмечалось в 13% случаев).
Литература
-
Рахманова А. Г., Воронин Е. Е., Фомин Ю. А. ВИЧ-инфекция у детей. 2003.
-
Покровский В. В., Ермак Т. Н., Беляева В. В., Юрин О. Г. ВИЧ-инфекция:
клиника, диагностика и лечение. 2000.
-
Кулаков В. И., Баранов И. И. ВИЧ: профилактика передачи от матери ребенку.
2003.
-
Покровский В. В., Ладная Н. Н., Соколова Е. В., Буравцова Е. В., Кравченко
А. В. ВИЧ-инфекция. Информационный бюллетень № 30. 2007.
-
Peter Havens, Russell Van Dyke, Geoffrey Weinberg. Guidelines for the Use
of Antiretroviral Agents inPediatric HIV Infection. 2008.
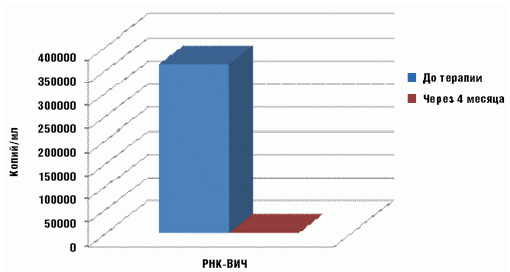
Рис. 1. Динамика уровня вирусной нагрузки через 4 месяца
после терапии
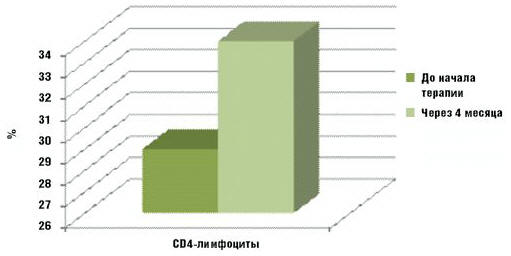
Рис. 2. Динамика уровня CD4-лимфоцитов через 4 месяца
после терапии

