Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Пробиотики: новые грани хорошо знакомых средств
М. А. Ливзан, доктор медицинских наук, профессор
ГОУ ВПО «Омская государственная медицинская академия Росздрава», Омск
Бифидобактерия была впервые изолирована Анри Тиссье
(Пастеровский институт) у новорожденного, получавшего грудное кормление, и
названа им Bacillus bifidus communis. Тиссье утверждал, что бифидобактерии могут
заменить протеолитические бактерии, вызывающие диарею, и рекомендовал введение
бифидобактерий новорожденным, страдающим от этого синдрома. Термин «пробиотики»
впервые был введен в 1965 г. Лилли и Стиллуэллом; в противоположность
антибиотикам, пробиотики были описаны как микробные факторы, стимулирующие рост
других микроорганизмов.
В соответствии с определением рабочей группы ВОЗ к пробиотикам
относят живые микроорганизмы, которые при применении в адекватных количествах
вызывают улучшение здоровья организма-хозяина. Они подразделяются по количеству
входящих в состав препарата культур на монокомпонентные (Бифидумбактерин,
Энтерол, Бактисубтил и т. д.) и поликомпонентные (Линекс), а также по свойству
пробиотической культуры на самоэлиминирующиеся антагонисты (Энтерол, Бактисубтил)
и на бифидосодержащие, лактосодержащие и колисодержащие. Так, например, препарат
Линекс относится к поликомпонентным бифидо- и лактосодержащим пробиотикам, так
как содержит три пробиотических микроорганизма Bifidobacterium infantis,
Lactobacillus acidophilus и Enterococcus faecium. Входящие в его состав
лактобактерии и энтерококк преимущественно колонизируют тонкую кишку, а
бифидобактерии — толстую, поэтому пробиотические культуры наиболее физиологично
поддерживают колонизационную резистентность и способствуют выполнению функций
индигенной кишечной микрофлоры.
К доказанным эффектам пробиотиков относят [1]:
-
активацию локальных макрофагов для увеличения презентации антигенов B
лимфоцитам и увеличения производства секреторного иммуноглобулина А (IgA)
местно и системно;
-
модулирование цитокиновых профилей;
-
переваривание пищи и конкуренцию за питательные вещества с патогенами;
-
изменение локальной pH для создания невыгодного местного окружающего
пространства для развития патогенов;
-
производство бактериоцинов для подавления патогенов;
-
устранение супероксидных радикалов;
-
стимуляцию продукции эпителиального муцина;
-
усиление барьерной функции кишечника;
-
конкуренцию с патогенами за адгезию.
-
модификацию патогенных токсинов.
Помимо пробиотиков, средства коррекции микробиоты включают также
пребиотики и синбиотики. Пребиотики представляют собой стабилизаторы среды
обитания и стимуляторы роста нормальной микрофлоры. В эту группу входят
препараты, относящиеся к различным фармакотерапевтическим группам, но обладающие
общим свойством — способностью стимулировать рост и развитие нормальной
микрофлоры кишечника. К пребиотикам относят лактулозу, глюкозу, протеины,
камедь, аминокислоты, витамины и минералы, инулин, каолин, пищевые волокна,
дрожжи [2]. Лактулоза — синтетический дисахарид, не встречающийся в природе, в
котором каждая молекула галактозы связана b-1,4-связью с молекулой фруктозы.
Лактулоза попадает в толстый кишечник в неизмененном виде (лишь около 0,25–2,0%
всасывается в неизмененном виде в тонкой кишке) и служит питательным субстратом
для сахаролитических бактерий. В процессе бактериального разложения лактулозы на
короткоцепочечные жирные кислоты (молочная, уксусная, пропионовая, масляная)
снижается рН содержимого толстой кишки. За счет этого же повышается осмотическое
давление, ведущее к задержке жидкости в просвете кишки и усилению ее
перистальтики. Лактулоза способствует нормализации стула у пациентов с
хроническими запорами и может назначаться длительно. Одним из наиболее
перспективных пребиотических веществ является инулин (полисахарид растительного
происхождения, который содержится в топинамбуре), который избирательно
стимулирует рост бифидобактерий и лактобацилл, подавляет рост условно-патогенных
микроорганизмов, а также способствует нормализации моторной функции кишечника.
Его комбинация с пробиотическими культурами — основа для создания эффективных
синбиотических средств (например, в состав Линексбио включен инулин с
олигофруктозой, а также с пробиотическими бактериями L. acidophilus (LA-5) и
Bifidobacterium animalis subsp. lactis (BB-12)).
Микробные ассоциации желудочно-кишечного тракта характеризуются
сложной иерархической структурой, различными межвидовыми отношениями и
многоступенчатыми метаболическими процессами, конечным результатом которых
являются биологически активные соединения — микробные метаболиты. Наиболее
точными методами оценки состояния микробиоты и ее функциональной активности
являются аспирация содержимого и посев биоптатов из слизистой тонкой и толстой
кишки на питательные среды; неинвазивный дыхательный тест с лактулозой,
исследование уровня летучих жирных кислот в кале, газожидкостная хроматография
малодоступны на сегодняшний день в широкой клинической практике, в связи с чем
назначение средств, способствующих нормализации микробиоценоза, определяется
прежде всего клинической ситуацией [3].
К наиболее доказанным клиническим рекомендациям по использованию
пробиотиков относятся следующие [4]:
-
Пробиотики эффективны для профилактики антибиотик-ассоциированной диареи
(уровень доказательности A). Наиболее целесообразно использование
Saccharomyces boulardii и L. rhamnosus GG.
-
В соответствии с результатами крупномасштабного Кокрановского обзора и
метаанализа, включивших исследования диареи вирусной этиологии и диареи
путешественников, терапия пробиотиками снижает как продолжительность (по
меньшей мере, на 30 часов), так и тяжесть симптомов диареи (уровень
доказательности А).
-
В соответствии с проведенными до настоящего времени исследованиями, у
пациентов с синдромом раздраженного кишечника терапия пробиотиками снижает
выраженность болевого синдрома и вздутие живота (уровень доказательности B).
-
У детей из группы риска возникновения атопии пробиотики могут предотвращать
развитие атопического дерматита (уровень доказательности В), а также
существуют предварительные доказательства эффективности купирования
симптомов атопического дерматита при использовании пробиотиков.
Механизм действия пробиотиков на молекулярном уровне активно
изучается [5]. Известно, что практически все микроорганизмы взаимодействуют с
клетками макроорганизма через так называемые Toll-подобные рецепторы (TLR) —
семейство мембранных гликопротеинов, присутствующих на макрофагах, нейтрофилах,
дендритных клетках, эпителиоцитах (рис. 1).
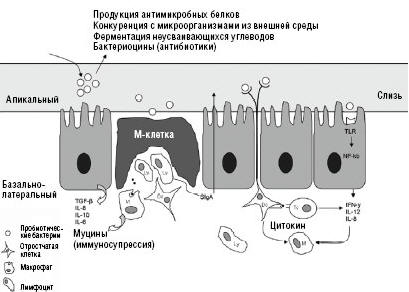
Сигналы патогенных микробов и представителей индигенной флоры
воспринимаются этими рецепторами по-разному. При реакции TLR на соответствующий
структурный паттерн разрывается его комплекс с ингибитором (Tollip), и TLR
передает стимулирующий импульс на белок NFkB, вследствие чего последний
транспортируется в ядро клетки. Активация NFkB приводит к переключению
дифференцировки Th0-лимфоцитов на Thl-путь и стимуляции выработки
провоспалительных цитокинов. Назначение пробиотиков ингибирует активацию NFkB за
счет предупреждения его ингибитора lkВ-альфа. По-разному воспринимается и
микробная ДНК патогенов и комменсалов. Олигонуклеотиды, в которых содержатся
неметилированные динуклеотиды, что свойственно патогенной и условно-патогенной
микрофлоре, улавливаются TLR с последующей стимуляцией воспалительного ответа.
Эукариоидная ДНК и метилированные динуклеотиды, свойственные
индигенной флоре, не воспринимаются TLR и не активируют иммунный ответ.
Очевидно, что разные штаммы пробиотиков способны по-разному восприниматься
МALT-системой, более того, восприятие каждого из препаратов может быть
индивидуально. Тем не менее, большинство проведенных клинических и
экспериментальных исследований свидетельствуют о том, что пробиотические штаммы
лактобактерий (LGG, L. acidophylus), E. faecium, S. thermophylus воспринимаются
TLR и стимулируют воспалительный ответ, усиливая выработку Th1 и IL-1,
INF-альфа. Они стимулируют фагоцитарную активность нейтрофилов и выработку SIgА.
В то же время бифидобактерии оказывают стимулирующее воздействие на Th-reg и,
соответственно, выработку TGF-бета, IL-10, способствуя формированию
иммунологической толерантности. Этот процесс сопровождается снижением синтеза
IgE и усилением синтеза SIgA. Наиболее активно повышают уровень IL-10 В. longum,
B. bifidum, B. infantis. Пробиотики, в состав которых входят симбионтные штаммы
бактерий, аэробы и анаэробы, вероятно, могут оказывать более многоплановое и
мощное иммуномодулирующее действие, чем монокомпонентные препараты.
Иммунорегулирующее действие пробиотиков расширяет возможности их
использования и раскрывает широкие перспективы для применения в разных
клинических ситуациях [6]. Так, в новом международном согласительном документе
по применению про- и пребиотиков (htpp://www.worldgastroenterology.org) в число
нозологических форм, при которых показан прием препаратов этой группы, включены
воспалительные заболевания кишечника, а также обсуждается эффективность
пробиотической терапии при аутоиммунных заболеваниях.
Не менее интересным представляется и рассмотрение роли
микробиоты кишечника в регуляции обменных процессов, а также роль нарушения
индигенной микрофлоры кишечника в развитии нарушения липидов (ожирения, гипер- и
дислипидемии) и углеводного обмена (сахарный диабет, нарушение толерантности к
глюкозе) (рис. 2) [7].
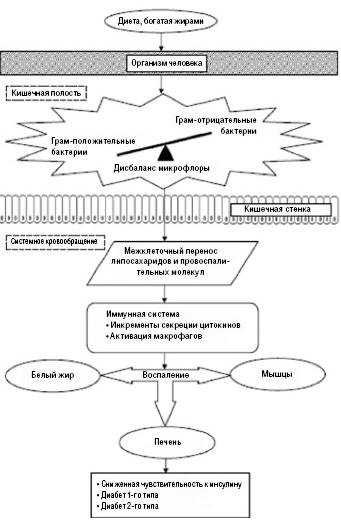
Известно, что главным физиологическим механизмом холестеринового
гомеостаза является экскреция желчных кислот с желчью в процессе их
энтерогепатической циркуляции по принципу «обратной связи», регламентирующему
внутрипеченочный синтез стероида и его метаболизм в желчные кислоты. При
синдроме избыточного бактериального роста микробиота толстого кишечника при
помощи ферментативного аппарата бактерий нарушает метаболизм желчных кислот в
цикле их энтерогепатической циркуляции, приводя в итоге к дислипопротеидемии.
Основным органом-мишенью при этом становится печень.
Установлено, что при дислипидемии (облитерирующем атеросклерозе,
жировой инфильтрации печени, метаболическом синдроме и др.) происходят
выраженные дисбиотические изменения кишечника с понижением общего уровня летучих
жирных кислот и повышением анаэробного индекса, характерных для угнетения
резидентной микрофлоры кишечника. Таким образом, создается «порочный круг»:
нарушение микроэкологии кишечника — нарушение энтерогепатической циркуляции
желчных кислот — нарушение функции печени — нарушение обмена липидов — нарушение
структуры печени (жировая инфильтрация, фиброз) — нарушение обмена липидов —
поддержание (усугубление) нарушенного кишечного дисбиоза [9]. Эти данные
позволяют экспертам Международной организации гастроэнтерологов рассматривать в
качестве возможных показаний к назначению пробиотиков и пребиотиков заболевания
сердечно-сосудистой системы, а также обмена веществ (ожирение, сахарный диабет).
Таким образом, с течением времени пробиотики не только не
утратили своей актуальности, но и демонстрируют в клинической практике свои
новые свойства, позволяющие расширить горизонты профилактики, эффективной и
безопасной терапии заболеваний, нормализации деятельности иммунной системы и
обмена веществ.
Литература
-
Всемирная Гастроэнтерологическая ассоциация. Практические рекомендации.
Пробиотики и пребиотики. Май 2008. http://www.worldgastroenterology.org/assets/downloads/ru/pdf/guidelines/19_probiotics_prebiotics_ru.pdf.
-
Шендеров Б. А. Медицинская микробная экология и функциональное питание. Том
I: Микрофлора человека и животных и ее функции. М.: Издательство ГРАНТЪ,
1998. 288 с.
-
Jonkers D., Stockbrugger R. Review article: Probiotics in gastrointestinal
and liver diseases. 2007 Dec;26 Suppl. 2: 133–48.
-
Kligler B., CohrssAliment Pharmacol Theren A. Probiotics. Am Fam Physician.
2008; 78: 1073–1078.
-
Borivant M., StroberW. The mechanism of action of probiotics. Curr Opin
Gastroenterol. 2007 Nov; 23 (6): 679–92.
-
Gill H., Prasad J. Probiotics, immunomodulation, and health benefits. Adv
Exp Med Biol. 2008; 606: 423–54.
-
Eamonn P. Culligan, Colin Hill, Roy D. Sleator. Probiotics and
gastrointestinal disease: successes, problems and future prospects Gut
Pathogens 2009, 1:19 doi: 10.1186/1757–4749–1-19.
-
Huey-Shi Lye, Chiu-Yin Kuan, Joo-Ann Ewe, Wai-Yee Fung and Min-Tze Liong.
The Improvement of Hypertension by Probiotics: Effects on Cholesterol,
Diabetes, Renin, and Phytoestrogens *Int. J. Mol. Sci. 2009, 10, 3755–3775;
doi:10.3390/ijms10093755.
-
Vitali B., Ndagijimana M., Cruciani F., Carnevali P. Impact of a synbiotic
food on the gut microbial ecology and metabolic profiles BMC Microbiology
2010, 10:4 doi: 10.1186/1471–2180–10–4.
Статья опубликована в журнале
Лечащий Врач

