Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ)
– хроническое заболевание, которое вследствие
развития характерных для рефлюкса симптомов
(изжоги и регургитации) существенно снижает
качество жизни пациентов и чревато развитием
осложнений (пептические стриктуры пищевода,
пищевод Баррета, аденокарцинома пищевода) [13, 29,
35]. В спектр симптомов заболевания могут также
входить «внепищеводные» проявления, под которыми
понимают проявления со стороны других органов и
систем, патогенетически обусловленных
гастроэзофагеальным рефлюксом (ГЭР)
(например, эрозии эмали зубов, хронический кашель,
бронхиальная астма, хронический фарингит и др.)
[41].
Модификация образа жизни и диеты является одним
из компонентов лечения ГЭРБ, которое, помимо
этого, включает назначение антисекреторных
препаратов и в ряде случаев прокинетиков и
антацидов. Рекомендации по диете больным ГЭРБ
разработаны с помощью эмпирического подхода и
теоретических данных. Обычно пациентам
рекомендуется исключение переедания, острых и
соленых блюд, уменьшение объема пищи, принимаемой
за один раз [2, 13, 41]. Однако накопленные за
последнее время сведения свидетельствуют о
возможности применении и других подходов, в
частности обогащение рациона пищевыми
волокнами (ПВ) с целью уменьшения
выраженности симптомов у этих больных [6].
Цель настоящей публикации –
проанализировать имеющиеся в настоящее время
данные о влиянии пищевых волокон на развитие
проявлений и течение заболевания у больных ГЭРБ.
Проведен поиск в системе Medline/PubMed
ключевыми словами: food, dietary patterns,
nutrients, nutrition, dietary fiber в комбинации с
gastroesophageal reflux, GERD. Выбраны
исследования, удовлетворяющие следующим
требованиям: публикация должна содержать данные
клинического наблюдения или быть результатом
мета-анализа, при этом необходимыми условиями
считается наличие характеристики группы
наблюдения, применявшихся методов и полученных
результатов.
Предпосылки эффективности обогащения
рациона больных ГЭРБ пищевыми волокнами в
отношении уменьшения выраженности проявлений
заболевания. Теоретическими предпосылками
положительного влияния ПВ на течение ГЭРБ может
являться то, что они могут связывать содержащийся
в пище оксид азота (NO), который, в свою
очередь, обладает расслабляющим влиянием на
нижний пищеводный сфинктер (НПС) [24, 37].
Недостаток в пище волокон ассоциирован также с
повышением риска развития грыжи пищеводного
отверстия диафрагмы (ГПОД), наличие которой
обусловливает увеличение частоты развития
симптомов заболевания [9]. По-видимому, это
связано с ослаблением моторики желудка,
замедлением эвакуации содержимого при дефиците
пищевых волокон и вследствие этого перерастяжением
желудка, что способствует увеличению опасности
развития ГПОД [21, 23, 33].
С другой стороны, замедление эвакуации приводит
к более длительному нахождению содержимого в
просвете желудка, росту внутрижелудочного
давления, постпрандиальной гиперсекреции, что
непосредственно увеличивает риск возникновения ГЭР
[16, 22, 43]. Повышение внутрижелудочного давления
зависит и от других факторов, в частности от
интенсивности секреции желудочного сока.
В одном из исследований была показана
способность гуаровой смолы, а также других
растворимых ПВ способствовать уменьшению
кислотообразования и увеличению скорости эвакуации
желудочного содержимого, что может быть полезным в
плане уменьшения риска развития симптомов ГЭРБ
[20]. Кроме того, отдельные ПВ обладают
способностью связывать желчные кислоты, которые
считаются одним из патогенетических факторов
развития эрозивного эзофагита, пищевода Баррета,
аденокарциномы пищевода [10, 17, 25, 40]. Таким
образом может достигаться протективный эффект в
отношении этих проявлений и осложнений ГЭРБ (рис.
1).
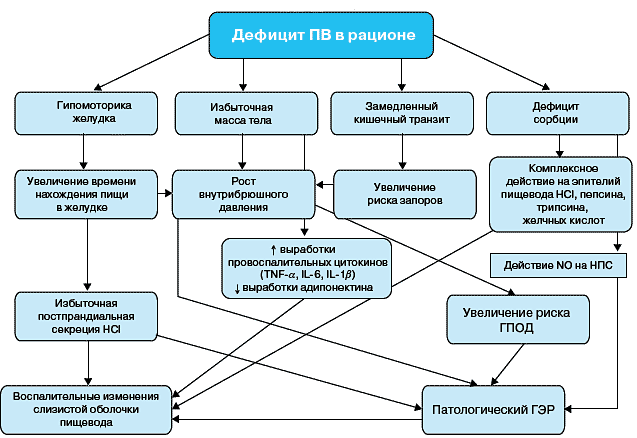
Рис. 1. Роль
пищевых волокон в патогенезе ГЭРБ: HCl – соляная
кислота; TNF-α – фактор некроза опухоли α; IL –
интерлейкин; NO – оксид азота; НПС – нижний
пищеводный сфинктер; ГПОД – грыжа пищеводного
отверстия диафрагмы; ГЭР – гастроэзофагеальный
рефлюкс
Другим потенциальным механизмом положительного
действия ПВ при ГЭРБ является опосредованное
влияние путем нормализации массы тела
(МТ) больных. Действительно, ряд работ
свидетельствует о тесной взаимосвязи ожирения и
проявлений ГЭРБ. Так, при оценке роли различных
факторов в развитии симптомов заболевания S.
Nandurkaretal и соавт. выявили корреляцию лишь в
отношении индекса массы тела (ИМТ) обследуемых, в
то время как различные пищевые факторы, а также
уровень физической активности не влияли на
возникновение изжоги [30]. Возможным
патогенетическим механизмом, лежащим в основе
указанной взаимосвязи, является то, что наличие
ожирения по абдоминальному типу может
сопровождаться повышением внутрибрюшного давления,
тем самым обусловливая увеличение давления в
желудке [27, 32, 42]. При ожирении часто
наблюдается укорочение пищевода и дислокация НПС и
диафрагмы относительно друг друга, что может
способствовать возникновению ГПОД [15].
Кроме того, немаловажна роль самого
висцерального жира, который является метаболически
активным. В частности, под его влиянием может
снижаться уровень цитокинов в крови, оказывающих
защитную роль, например адипонектина, в то время
как содержание провоспалительных факторов –
фактора некроза опухоли-α (ФНО-α), интерлейкинов
IL-1β, IL-6 – повышается [11, 36, 38].
По данным мета-анализа эпидемиологических
исследований по выявлению взаимосвязи ожирения,
ГЭРБ и ассоциированных с ней состояний, было
установлено, что избыток массы тела (в пределах
>25, но ≤30 кг/м2) и ожирение (ИМТ>30
кг/м2) были тесно взаимосвязаны с
симптомами ГЭРБ. Так, отношение шансов
(ОШ) наличия симптомов заболевания у пациентов с
избыточной МТ составило 1,43; 95%
доверительный интервал (ДИ) 1,158–2,677, а у
лиц с ожирением соответственно 1,94; 95% ДИ 1,468–
2,566. Аналогично у пациентов с избыточной МТ ОШ
наличия рефлюкс-эзофагита составило 1,76; 95% ДИ
1,156–2,677, а аденокарциономы пищевода – 1,52;
95% ДИ 1,147–2,009. В то же время у лиц с
ожирением ОШ развития аденокарциномы пищевода было
еще выше и составило 2,78; 95% ДИ 1,850–4,164
(рис. 2) [19].
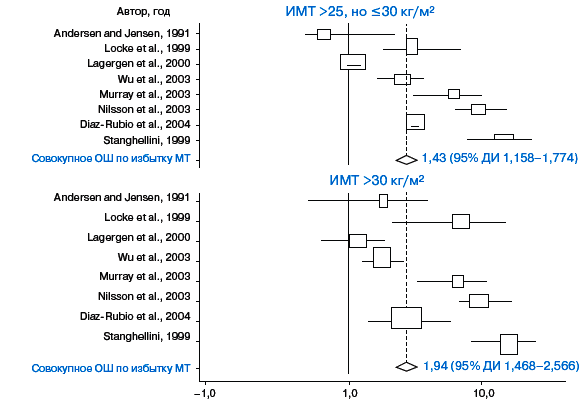
Рис. 2.
Взаимосвязь индекса массы тела и риска развития
симптомов ГЭРБ
Также было показано наличие прямой зависимости
между изменением массы тела (в сторону как
увеличения, так и уменьшения) и частотой
возникновения симптомов ГЭРБ. В проспективном
исследовании C.A. Fraser-Moodie и соавт. (n=34,
ИМТ исходно >23 кг/м2) при снижении
массы тела у больных ГЭРБ (в 80% в среднем на 4
кг) отмечалось уменьшение частоты и выраженности
симптомов. В группе с прибавкой МТ за время
исследования (n=7) у 3 человек симптомы
ГЭРБ стали более выраженными, а у 4 их проявления
уменьшились. При проведении корреляционного
анализа авторы выявили достоверную прямую
взаимосвязь средней силы между снижением МТ и
уменьшением выраженности симптомов ГЭРБ (r=0,548,
p<0,001) [18].
В популяционном исследовании E. Rey и соавт. в
ходе телефонного опроса случайно выбранных
респондентов в возрасте 49–79 лет оценивались
частота, выраженность и давность симптомов ГЭРБ в
совокупности с данными о росте, массе тела и ее
изменении за прошедший год [34]. Установлено, что
частота впервые появившихся за последний год
симптомов напрямую зависела от выраженности
увеличения массы тела: в случаях прибавки более 5
кг за год она составила 14,4%, ≤5 кг – 8,2%, а у
тех, у кого увеличения массы тела не было, – 5,4%.
При этом ОШ наличия новых симптомов ГЭРБ у
респондентов с прибавкой МТ ≤5 кг составило 1,5
(95% ДИ 0,9–2,4), а существовавших ранее – 1,1
(95% ДИ 0,8–1,4), в то время как при показателе >5
кг ОШ наличия как вновь появившихся, так и
существовавших ранее симптомов было больше – 3,0
(95% ДИ 1,6–6,0) и 1,3 (95% ДИ 0,8–2,1)
соответственно.
Полученные результаты позволили авторам
исследования сделать вывод о том, что независимо
от исходного ИМТ увеличение массы тела является
фактором риска развития симптомов ГЭРБ.
С другой стороны, результаты эпидемиологических
исследований свидетельствуют о том, что
употребление пищевых волокон (в виде
цельнозернового хлеба) имеет протективные свойства
в отношении развития ожирения. Так, в мета-анализе,
включавшем 2 поперечных (более 100 000 человек) и
4 проспективных исследования (более 100 000
человек), установлено, что вне зависимости от пола
риск развития или наличия ожирения у пациентов с
высоким потреблением ПВ оказался меньше по
сравнению с теми, у кого в рационе их содержание
было меньше нормального уровня потребления (14
г/1000 ккал в сутки) – относительный риск составил
0,77 (95% ДИ 0,68–0,87) [5]. В этой же работе
показано, что высокий уровень потребления ПВ
снижал риск развития ожирения на 30%.
Данные мета-анализа 16 рандомизированных
клинических исследований подтвердили, что
обогащение рациона пищевыми волокнами
(преимущественно нерастворимыми) способствует
более эффективному снижению массы тела по
сравнению с контрольными диетами без добавления ПВ
(рис. 3) [6].
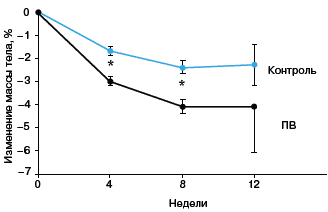
Рис. 3. Влияние
обогащения рациона пищевыми волокнами на
эффективность снижения массы тела по сравнению с
контрольными диетами. Мета-анализ данных 16
исследований. Значения представлены в формате M±m.
Значимые различия (*) выявлены на 4-й (p=0,0063) и
8-й (p=0,0088) неделях
Итак, рассмотренные нами выше факты
свидетельствуют о наличии обоснованных предпосылок
потенциальной пользы использования пищевых волокон
у больных ГЭРБ. Однако есть ли прямые
свидетельства взаимосвязи между потреблением ПВ и
риском развития симптомов заболевания, а также
влияния модификации рациона на течение
заболевания?
Данные эпидемиологических исследований.
В исследовании HUNT2, проведенном в Швеции с
участием 65 363 человек старше 20 лет, ответивших
на вопросник, в том числе касавшийся диетических
привычек и наличия изжоги, выявлена линейная
корреляция между частотой изжоги и потреблением ПВ.
Оказалось, что те из респондентов, которые
употребляли хлеб с содержанием пищевых волокон не
менее 7% его сухой массы, испытывали изжогу
практически в 2 раза реже по сравнению с теми, кто
использовал в пищу преимущественно белый хлеб, в
котором количество ПВ не превышало 2% (ОШ 0,5; 95%
ДИ 0,4–0,7) – см. таблицу [31].
Количество
потребляемых пищевых волокон и риск развития
симптомов ГЭРБ
| Сухой вес
(%) пищевых волокон в хлебе |
Отношение
шансов развития симптомов ГЭРБ (95% ДИ) |
1–2 (белый хлеб, мало
волокон)
4–7 (умеренное количество волокон)
6–10 (много волокон)
14–16 (твердый хлеб)
|
1,0
(группа сравнения)
0,7
(0,6–0,9)
0,5
(0,4–0,7)
0,5
(0,4–0,7)
p для
тренда <0,0001
|
В исследовании H.B. El-Serag отношение шансов
наличия симптомов ГЭРБ в группе с большим
потреблением ПВ по сравнению с теми, у кого оно
было незначительным, составило 0,72 (95% ДИ
0,53–0,99, p=0,04). Авторам не удалось найти
достоверных отличий по потреблению ПВ между
группами обследованных, имевших симптомы ГЭРБ и с
отсутствием таковых, – 8,5±3,2 г/1000 ккал по
сравнению с 9,2±4,0 г/1000 ккал соответственно (р=0,097).
В этом исследовании не выявлено также различий по
количеству ПВ в рационах групп с наличием
эрозивного эзофагита и без повреждений слизистой
пищевода – 9,0±3,1 по сравнению с 9,0±4,0 (р=0,962)
[14].
Данные эпидемиологических исследований
свидетельствуют о том, что риск возникновения
таких осложнений ГЭРБ, как пищевод Баррета и
аденокарцинома пищевода, пропорционально снижается
в зависимости от увеличения количества
потребляемых овощей и фруктов, которые являются
одними из основных источников ПВ в рационе. Так, в
популяционном исследовании выявлено, что у
пациентов, в рационе которых количество овощных
блюд было больше (8,3 порций в сутки), риск
возникновения пищевода Баррета был на 73% ниже по
сравнению с теми, у кого количество
овощных/фруктовых блюд в день не превышало двух
(ОШ обнаружения пищевода Баррета составило 0,27,
95% ДИ 0,15–0,50) [26]. В этом же исследовании
установлено, что каждая порция овощей и фруктов в
рационе снижает риск возникновения пищевода
Баррета на 14% (ОШ=0,86; 95% ДИ 0,80–0,93), а риск
диагноза ГЭРБ – на 10%.
В другом исследовании, проведенном в Ирландии с
включением 710 респондентов (224 больных с
пищеводом Баррета, 226 – с аденокарциномой
пищевода и 260 практически здоровых лиц),
оказалось, что количество порций овощей в неделю
было больше у практически здоровых лиц – в среднем
20, чем у пациентов с пищеводом Баррета – в
среднем 18,7 (p=0,04). В рационе больных с
пищеводом Баррета также содержалось меньше
фруктов, чем в группе контроля (11,9 порций в
неделю по сравнению с 14,2 соответственно, р<0,001).
В этой же работе отмечено, что по сравнению с
контрольной группой больные с аденокарциномой
пищевода потребляли меньше фруктов (в среднем 11,2
порций в неделю, p<0,001), количество потребляемых
овощей достоверно не отличалось (в среднем 20,6
порций в неделю, р=0,348) [7]. Однако, по данным
кросс-секционного исследования, не выявлено
различий по количеству порций овощей и фруктов,
потребляемых в среднем за сутки, между группами с
отсутствием или наличием симптомов ГЭРБ, а также с
наличием или отсутствием эзофагита [14].
Работ, в которых было бы оценено влияние
модификации диеты с увеличением количества ПВ на
течение ГЭРБ, нами не найдено. В то же время,
несмотря на имеющиеся противоречия, выявленные
данные свидетельствуют о том, что увеличение
количества пищевых волокон в рационе может
способствовать уменьшению частоты возникновения
симптомов ГЭРБ у этой группы больных. Кроме того,
повышенное потребление ПВ может оказывать защитный
эффект относительно развития осложнений
заболевания – пищевода Баррета и аденокарциномы
пищевода.
Учитывая отсутствие достоверных сведений,
требуется проведение дополнительных исследований,
оценивающих влияние как отдельных представителей
этой группы пищевых факторов, так и их воздействие
в целом на течение ГЭРБ.
Заключение
Насколько нам известно, настоящая работа
является первой в отечественной литературе
попыткой провести систематический обзор
наблюдений, касающихся влияния пищевых волокон на
течение ГЭРБ. К сожалению, имеющиеся материалы
далеко неполные и требуют дальнейшего рассмотрения
в специально спланированных проспективных
исследованиях. В частности, мы не нашли ни одной
работы, в которой оценивалось бы влияние
модификации рациона больных ГЭРБ с обогащением его
пищевыми волокнами на развитие симптомов
заболевания и одного из его объективных признаков
– гастроэзофагеальных рефлюксов, регистрируемых
при помощи суточной пищеводной рН-метрии или рН-импедансометрии.
Тем не менее, как косвенные данные о влиянии
пищевых волокон на патогенетические факторы ГЭРБ,
так и результаты эпидемиологических исследований
свидетельствуют о том, что использование ПВ в
модификации рациона больных ГЭРБ может оказывать
положительное воздействие.
Следует отметить, что в настоящее время нет
информации о том, какие именно пищевые волокна
(растворимые, нерастворимые), какое их количество
и химический состав обладают бόльшим эффектом на
проявления заболевания. Также не ясно, какой
способ использования ПВ более предпочтителен:
увеличение потребления богатых пищевыми волокнами
продуктов или увеличение суточной квоты ПВ путем
назначения лекарственных препаратов или
биологически активных добавок. В большей части
рекомендаций по питанию указывается, что
предпочтительным является первый [4, 28, 39].
Однако реальное потребление ПВ сложнее поддается
контролю; ни в одном из исследований не доказана
бόльшая результативность такого подхода. Напротив,
в нескольких исследованиях отмечалась бόльшая
клиническая эффективность (например, в отношении
снижения массы тела, контроля гликемии,
липопротеидов крови) при использовании ПВ в виде
лекарственных средств (псиллиум, мукофальк) [5, 8,
12]. Кроме того, лекарственные препараты ПВ могут
применяться параллельно с диетическими
рекомендациями для увеличения эффективности
коррекции диеты. Еще одним преимуществом
упомянутого «лекарственного» источника ПВ –
псиллиума – является высокое содержание слизей в
составе препарата, поскольку они обладают
буферными свойствами, связывая кислоту желудочного
сока и оказывая «обволакивающий» эффект на
слизистую оболочку желудка [1].
Учитывая, что патогенетические факторы, лежащие
в основе ГЭРБ, многообразны, необходимо также
проведение дополнительного анализа, способного
выделить отдельные группы пациентов, у которых
обогащение рациона пищевыми волокнами могло бы
принести наибольшую пользу (например, больные ГЭРБ
с ожирением или при сочетании ГЭРБ с замедленным
кишечным транзитом) [3].
Список литературы:
1. Ардатская М.Д. Клиническое
применение пищевых волокон: Метод. пособие. – М.,
2010. – 48 с.
1. Ardatskaya M.D. The clinical application
of the dietary fibers: Practical manual. – Мoscow,
2010. – 48 p. [in Russian]
2. Гастроэзофагеальная рефлюксная болезнь:
Учебно-методическое пособие / Под ред. Маева И.В.
– М.: ВУНМЦ, 2000. – 52 с.
2. The gastroesophageal reflux disease: Practical
manual / Ed. by Mayev I.V. – Мoscow: Educational,
scientific and methodological center for
continuing medical and pharmacological education,
2000. – 52 p. [in Russian]
3. Янова О.Б., Машарова А.А. Гастроэзофагеальная
рефлюксная болезнь в сочетании с хроническим
запором у пожилых больных // Клин. геронтол. –
2008. – № 14. – С. 26–29.
3. Yanova O.B., Masharova A.A. The
gastroesophageal reflux disease combined with
chronic coprostasia of the elderly patients. //
Clin. Gerontol. – 2008. – № 14. – P. 26–29. [in
Russian]
4. American Diabetes Association. Nutrition
principles and recommendations in diabetes //
Diabetes Care. – 2004. – Vol. 27 (suppl.). – P.
36–46.
5. Anderson J.W. Dietary fiber and
associated phytochemicals in prevention and
reversal of diabetes // Nutraceuticals, glycemic
health and type 2 diabetes / Eds. Pasupuleti
V.K., Anderson J.W. – Ames, Iowa: Blackwell
Publishing Professional, 2008. – P. 111–142.
6. Anderson J.W., Baird P., Davis R.H. et
al. Health benefits of dietary fiber // Nutr. Rev.
– 2009. – Vol. 67 (4). – P. 188–205.
7. Anderson L.A., Watson R.G.P., Murphy S.J.
et al. Risk factors for Barrett’s esophagus and
esophageal adenocarcinoma: Results from the FINBAR
study // World J. Gastroenterol. – 2007. – Vol. 13
(10). – P. 1585–1594.
8. Birketvedt G.S., Shimshi M., Erling T.,
Florholmen J. Experiences with three
different fiber supplements in weight reduction //
Med. Sci. Monit. – 2005. – Vol. 11. – P. 15–18.
9. Burkitt D.P., James P.A. Low-residue
diets and hiatus hernia // Lancet. – 1973. – Vol.
2. – P. 128–130.
10. Champion G., Richter J.E., Vaezi M.F.
et al. Duodenogastroesophageal reflux:
relationship to pH and importance in Barrett’s
esophagus // Gastroenterology. – 1994. – Vol. 107.
– P. 747–754.
11. Cnop M., Landchild M.J., Vidal J. et
al. The concurrent accumulation of intraabdominal
and subcutaneous fat explains the association
between insulin resistance and plasma leptin
concentrations: distinct metabolic effects of two
fat compartments // Diabetes – 2002. – Vol. 51. –
P. 1005–1015.
12. Cummings J.H. The effect of dietary
fiber on fecal weight and composition // Dietary
fiber in human nutrition / Ed. Spiller G.
– Boca Raton, FL: CRC Press, 2001. – P. 183–252.
13. Dent J., Brun J., Fendrick A.M. et al.
An evidencebased appraisal of reflux disease
management – the Genval Workshop Report // Gut. –
1999. – Vol. 44 (suppl. II). – P. 1–16.
14. El-Serag H.B., Satia J.A., Rabeneck L.
Dietary intake and the risk of gastroesophageal
reflux disease: a cross sectional study in
volunteers // Gut. – 2005. – Vol. 54 (1). – P.
11–17.
15. El-Serag H.B., Tran T., Richardson P.,
Ergun G. Anthropometric correlates of
intragastric pressure // Scand. J. Gastroenterol.
– 2006. – Vol. 41. – P. 887–891.
16. Emerenziani S., Sifrim D.
Gastroesophageal reflux and gastric emptying,
revisited // Curr. Gastroenterol. Rep. – 2005. –
Vol. 7 (3). – P. 190–195.
17. Fein M., Peters J.H., Chandrasoma P.
et al. Duodenogastroesophageal reflux induces
esophageal adenocarcinoma without exogenous
carcinogen // J. Gastrointest. Surg. – 1998. – Vol.
2 (3). – P. 260–268.
18. Fraser-Moodie C.A., Norton B., Gornall C.
et al. Weight loss has an independent beneficial
effect on symptoms of gastroesophageal reflux in
patients who are overweight // Scand. J.
Gastroenterol. – 1999. – Vol. 34. – P. 337–340.
19. Hampel H., Abraham N.S., El-Serag H.B.
Metaanalysis: obesity and the risk for
gastroesophageal reflux disease and its
complications // Ann. Intern. Med. – 2005. – Vol.
143. – P. 199–211.
20. Harju E. Guar gum benefits duodenal
ulcer patients by decreasing gastric acidity and
rate of emptying of gastric contents 60 to 120
minutes postprandially // Am. Surg. – 1984. – Vol.
50. – P. 668–672.
21. Holoway R.H., Hongo M., Berger K. et
al. Gastric distension: a mechanism for
postprandial gastroesophageal reflux //
Gastroenterology. – 1985. – Vol. 89. – P. 779–784.
22. Iwakiri K., Kobayashi M., Kotoyori M.
et al. Relationship between postprandial
esophageal acid exposure and meal volume and fat
content // Dis. Dig. Sci. – 1996. – Vol. 41. – P.
926–930.
23. Kahrilas P.J., Shi G., Manka M., Joehl
R.J. Increased frequency of transient lower
esophageal sphincter relaxation induced by gastric
distension in reflux patients with hiatal hernia
// Gastroenterology. – 2000. – Vol. 118. – P.
688–695.
24. Karamanolis G., Tack J. Nutrition and
motility disorders // Best Pract. Res. Clin.
Gastroenterol. – 2006. – Vol. 20 (3). – P.
485–505.
25. Kirby R.W., Anderson J.W., Sieling B.
et al. Oat-bran intake selectively lowers serum
low-density lipoprotein cholesterol concentrations
of hypercholesterolemic men// Am. J. Clin. Nutr. –
1981. – Vol. 34. – P. 824–829.
26. Kubo A., Levin T.R., Block G. et al.
Dietary antioxidants, fruits, and vegetables and
the risk of Barrett’s esophagus // Am. J.
Gastroenterol. – 2008. – Vol. 103 (7). – P.
1614–1623.
27. Lambert D.M., Marceau S., Forse R.A.
Intra-abdominal pressure in the morbidly obese //
Obes. Surg. – 2005. – Vol. 15. – P. 1225–1232.
28. Lichtenstein A.H., Appel L.J., Brands M.
et al. Diet and lifestyle recommendations revision
2006: a scientific statement from the American
Heart Association Nutrition Committee //
Circulation. – 2006. – Vol. 114. – P. 82–96.
29. Locke G.R., Talley N.J., Fett S.L. et
al. Prevalence and clinical spectrum of
gastroesophageal reflux: a population-based study
in Olmstead County, Minnesota // Gastroenterology.
– 1997. – Vol. 112. – P. 5–12.
30. Nandurkar S., Locke G.R. 3rd.,
Fett S. et al. Relationship between body mass
index, diet, exercise and gastroesophageal reflux
symptoms in a community // Aliment. Pharmacol.
Ther. – 2004. – Vol. 20 (5). – P. 497–505.
31. Nilsson M., Johnsen R., Ye W. et al.
Lifestyle related risk factors in the etiology of
gastroesophageal reflux // Gut. – 2004. – Vol. 53.
– P. 1730–1735.
32. Pandolfino J.E., El-Serag H.B., Zhang Q.
et al. Obesity: a challenge to esophagogastric
junction integrity // Gastroenterology. – 2006. –
Vol. 130. – P. 639–649.
33. Penangini R., Carmagnole S., Cantu P.
et al. Mechanoreceptors of the proximal stomach:
Role of triggering transient lower esophageal
sphincter relaxation // Gastroenterology. – 2004.
– Vol. 126. – P. 49–56.
34. Rey E., Moreno-Elola-Olaso C., Artalejo
F.R. et al. Association between weight gain
and symptoms of gastroesophageal reflux in the
general population // Am. J. Gastroenterol. –
2006. – Vol. 101. – P. 229–233.
35. Ronkainen J., Aro P., Storskrubb T.
et al. Gastroesophageal reflux symptoms and
health-related quality of life in the adult
general population – the Kalixanda study //
Aliment. Pharmacol. Ther. – 2006. – Vol. 23. – P.
1725–1733.
36. Ryan A.M., Duong M., Healy L. et al.
Obesity, metabolic syndrome and esophageal
adenocarcinoma: epidemiology, etiology and new
targets // Cancer Epidemiol. – 2011. – Vol. 35
(4). – P. 309–319.
37. Terry P., Lagergren J., Ye W. et al.
Inverse association between intake of cereal fiber
and risk of gastric cardia cancer //
Gastroenterology. – 2001. – Vol. 120. – P.
387–391.
38. Tselepis C., Perry I., Dawson C. et
al. Tumour necrosis factor-alpha in Barrett’s
esophagus: a potential novel mechanism of action
// Oncogene. – 2002. – Vol. 21. – P. 6071–6081.
39. US Department of Agriculture (USDA), US
Department of Health and Human Services. Dietary
Guidelines for Americans. Washington, DC: USDA;
2005.
40. Vaezi M.F. Duodenogastroesophageal
reflux // The Esophagus / Eds. Castell D.O.,
Richter J.E. – Philadelfia: Lippincott,
Williams, Wilkins, 1999. – P. 421–436.
41. Vakil N., Zanten V.S., Kahrilas P.
The Montreal definition and classification of
gastroesophageal reflux disease: A global
evidence-based consensus // Am. J. Gastroenterol.
– 2006. – Vol. 101. – P. 1900–1920.
42. Vries D.R., Herwaarden M.A., Smout A.J.,
Samsom M. Gastroesophageal pressure gradients
in gastroesophageal reflux disease: relations with
hiatal hernia, body mass index, and esophageal
acid exposure // Am. J. Gastroenterol. – 2008. –
Vol. 103. – P. 1349–1354.
43. Yamashita Y., Mason R.J., Demeester T.R.
Postprandial acid reflux is reduced by delayed
gastric emptying // J. Smooth Muscle Res. – 2003.
– Vol. 39 (4). – P. 87–93.

