Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Отдаленные результаты
хирургического лечения пациентов с рефлюкс –
эзофагитом
Н.Е. Шабанова1,2,
В.М. Дурлештер1,2, Н.В. Корочанская1,2,
Р.М. Тлехурай1,2, Л.Г. Дряева1,
И.Ю. Свечкарь1,2, В.В. Рябчун1,
Р.Б. Беретарь1,2, А.И. Пономарева1,2
1 - Государственное бюджетное учреждение
здравоохранения «Краевая клиническая больница №2»
2 - Государственное бюджетное образовательное
учреждение высшего профессионального обучения
«Кубанский государственный медицинский университет»
Министерства здравоохранения Российской федерации
Резюме: В статье приведены данные
обследования и лечения пациентов с рефлюкс -
эзофагитом. Всем пациентам была выполнена
лапароскопическая арефлюксная операция. Проведенный
клинический анализ выявил уменьшение и(или)
исчезновение ведущих клинических симптомов
гастроэзофагеальной рефлюксной болезни после
проведенного хирургического вмешательства.
Ключевые слова: гастроэзофагеальная
рефлюксная болезнь, рефлюкс - эзофагит, пищевод
Барретта, формирование арефлюксной кардии.
Введение.
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) в
настоящее время широко распространена в мире. По
данным Института Gallop (США) в среднем один раз в
месяц жалуются на изжогу 44% американцев, ежедневно
ее испытывают 7% и вынуждены прибегать к самолечению
18% [25]. Около 20% больных страдают тяжелым
рефлюксом, который вызывает такие осложнения, как
пищевод Барретта (ПБ) (10–15%), изъязвление (2–7%),
стриктура (4–20%), кровотечение (2%) [3, 9, 22-23].
Одним из звеньев патогенеза развития ГЭРБ
является гастроэзофагеальный рефлюкс (ГЭР),
приводящий к развитию рефлюкс – эзофагита (РЭ).
Главной проблемой лечения РЭ остается необходимость
длительного назначения больших доз антисекреторных
лекарственных препаратов и проведение основной (не
менее 6–12 недель) и поддерживающей терапии.
Стандартом лечения ГЭРБ в последние 10–15 лет
признаны ингибиторы протонной помпы [5, 26]. Следует
отметить, что проводимая консервативная терапия РЭ,
направленная на снижение секреции хлористоводородной
кислоты желудком, не влияет на функцию нижнего
пищеводного сфинктера. Завершение медикаментозного
лечения приводит к возникновению рецидива
заболевания через 1 месяц в 50% случаев, а в течение
года – в 58–85% [4-5, 7-8]. В последние годы во всем
мире отмечен рост интереса к хирургическим методам
лечения РЭ, основным из которых следует считать
создание арефлюксной кардии.
Проведение арефлюксного хирургического
вмешательства является единственным методом, который
позволяет восстановить функцию нижнего пищеводного
сфинктера (НПС) и устранить гастроэзофагеальный
рефлюкс (ГЭР) и его последствия [6].
В настоящее время существует большое число
оперативных методик, применяемых при лечении РЭ. Тем
не менее, данные литературы свидетельствуют о
неудовлетворенности хирургов и больных их
результатам [1-2, 6].
Цель исследования: оценить отдаленные
результаты хирургического лечения больных с РЭ после
устранения грыжи пищеводного отверстия диафрагмы (ГПОД)
и формирования арефлюксной кардии.
Материал и методы исследования
При составлении дизайна исследования формирование
клинических групп проводили таким образом, чтобы
можно было оценить эффективность хирургического
лечения у пациентов с РЭ и ПБ.
С этой целью нами было обследовано 213 больных с
РЭ, в возрасте от 24 до 76 лет, находившихся на
лечении в МБУЗ Городская больница № 2 «КМЛДО» г.
Краснодара (с 2013 г. и по настоящее время – ГБУЗ «ККБ
№2») в 2008 – 2014 годах. Пациентам было проведено
хирургическое лечение - устранение ГПОД и
формирование арефлюксной кардии лапаротомным
доступом; с 2011 года выполняется лапароскопическое
антирефлюксное вмешательство по разработанной и
используемой в клинике технологии (приоритетная
справка № 2013122121 от 14.05.2013г.). Показанием
для хирургического лечения всех больных является
тяжелый РЭ, в том числе осложненный ПБ и
резистентный к консервативной терапии, а также
наличие ГПОД. Сроки наблюдения за пациентами после
хирургического лечения составили более трех лет.
Всем больным проводили комплексное исследование
через 1, 3 , 6 месяцев после операции, затем
ежегодно. Пациенты были разделены на две группы.
Первую группу (n=142) составили больные, у которых
диагностирован РЭ без ПБ, во 2–ую вошли пациенты с
РЭ, осложненным ПБ (n=71). У всех больных изучили
клинические проявления РЭ и провели комплекс
диагностических исследований. Выполняли
рентгеноскопию и рентгенографию желудочно-кишечного
тракта на рентгенаппарате c электронно-оптическим
преобразователем. Узкоспектральную эндоскопию
(видеоинформационная система с цифровым анализатором
изображения фирмы «Olympus» Evis Exera GIF–160 и GIF–H–180,
Япония) с хромоскопией (прижизненная окраска
слизистой оболочки (СО) пищевода растворами
метиленового синего 1% и Люголя 1%) с последующей
биопсией измененной слизистой и морфологической
оценкой СО пищевода. Иммуногистохимическое (ИГХ)
исследование срезов биопатов СО включало
исследование на секреторные муцины MUC2, MUC5AC,
маркеры цитокератинов СК7 и СК20 (белки цитоскелета
эпителия), а также на Ki67 – ядерный антиген
пролиферирующих клеток с целью дифференциальной
диагностики реактивной пролиферации и дисплазии в СО
ПБ и определения типа метаплазии СО пищевода.
Суточное рН–мониторирование проводили с помощью
прибора «Гастроскан–24» фирмы “Исток-Система” г.
Фрязино. Оценивали: среднее значение рН, % общего
времени с рН < 4, число продолжительных рефлюксов >
5 мин (рефл./сут.), наибольшую продолжительность
рефлюкса (мин), обобщенный показатель De Meester.
Статистическую обработку полученных данных
производили на IBM – совместимом компьютере на базе
Intel Pentium IV с использованием пакета прикладных
программ Microsoft Exсel и программы
«Статистика–7.0» для Windows XP (версия 2002).
Результаты
Анализ клинической картины продемонстрировал, что
у больных 1–ой группы после проведенной операции
через 1–3 месяца достоверно снизились жалобы на
изжогу (43,0% и 15,7%, p < 0,05). Частота симптомов
отрыжки воздухом и кислым достоверно уменьшилась
через 3 месяца после хирургического вмешательства
(67,7% и 29,5%, p < 0,05). Симптом дисфагии до
операции встречался у 15,3% пациентов, а через 3
месяца после хирургического лечения – у 33,4%
больных, что связано с перенесенной операцией. После
оперативного вмешательства дисфагия характеризуется
легким течением. Болевой симптом встречался в
течение всего срока послеоперационного наблюдения
реже и с меньшей интенсивностью.
Во 2–ой клинической группе частота изжоги (78,9%)
и отрыжки воздухом и кислым (89,5%) достоверно
уменьшались через 1– 3 месяца после операции (25,1%
и 17,4%, p < 0,05). Встречаемость дисфагии и одышки
уменьшалась в течение всего срока послеоперационного
наблюдения и наблюдалась через 1 год у 9,3%
пациентов. Частота болевого симптома снижалась в
течение всего периода наблюдения, боли в животе
отмечены в 9,7% случаев через 1 год после
оперативного вмешательства, при этом характер болей
изменялся схожим образом с таковым у пациентов без
ПБ. Дисфагия в отделенном периоде встречалась у 4
(5,6%) больных. Все остальные клинические симптомы
имели тенденцию к снижению на каждом этапе
наблюдения в обеих группах.
Таким образом, проведенный клинический анализ
выявил уменьшение и(или) исчезновение основных
клинических симптомов РЭ после проведенного
оперативного лечения в течение ближайшего и
отдаленного послеоперационного периодов.
По результаты полипозиционной рентгенографии
желудочно–кишечного тракта с контрастированием
бариевой взвесью через 1–3 месяца после
хирургического лечения восстанавливалось плотное
смыкание кардии. В течение 1 года диспансерного
наблюдения ГПОД не выявлялись; данная
рентгенологическая картина оставалась без изменений
и на протяжении последующего диспансерного
наблюдения (рис. 1).
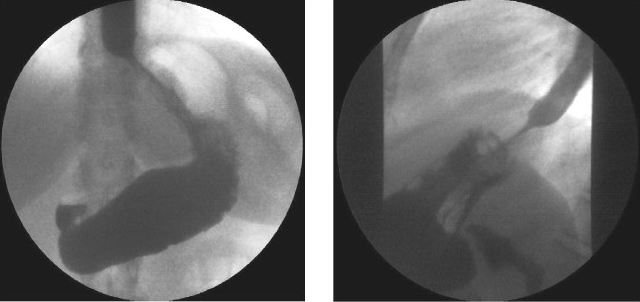
Рис. 1. Полипозиционная рентгенография
пищевода и желудка. Кардия смыкается, признаков ГПОД
и ГЭР нет. Слева – вид стоя, справа – в левом
лопаточном положении
Рецидив ГПОД возник у 2,4% пациентов (n=5) от
общего количества к третьему году наблюдения, что
было связано с наличием избыточного веса,
сопутствующей патологией и несоблюдением врачебных
рекомендаций.
По данным эндоскопической картины до
хирургического вмешательства у пациентов в 1–й
группе, относительно 2-й, достоверно чаще
встречалось плотное смыкание кардии (26,4% и 6,7%) и
достоверно реже - воспалительные изменения в
двенадцатиперстной кишке (16,7% и 48,9%). Наличие
желчи в желудке натощак во 2-й группе встречалось
достоверно чаще, по сравнению с 1-ой (7,2% и 24,5%).
При проведении эндоскопического исследования через
1–3 месяца, далее ежегодно у всех пациентов отмечено
плотное смыкание кардии. Рецидив РЭ при проведении
эндоскопии к третьему году динамического наблюдения
возник в 1–й группе у 13,4% (n=19) больных и во 2–ой
– у 15,5% (n=11), соответственно.
Результаты гистологического исследования СО
пищевода у больных 2-ой группы представлены в
таблице 1.
Таблица 1. Результаты
морфологического исследования слизистой оболочки у
пациентов с пищеводом Барретта (n=71)
Виды метаплазии
|
Виды сегментов, абс (%)
|
Всего
абс (%) |
ультракороткий
сегмент
(n=27)
|
короткий
сегмент
(n=35)
|
длинный
сегмент
(n=9) |
| Желудочная метаплазия |
6 (22,2) |
9 (25,7) |
3(5,6) |
18 (25,4) |
| Кишечная метаплазия |
10(37,1) |
15 (42,9) |
4 (2,8) |
29 (40,8) |
| Желудочно-кишечная метаплазия |
11 (40,7) |
11 (31,4) |
2 (22,2) |
24(33,8) |
| Всего |
27 (38,0) |
35 (49,3) |
9 (12,7) |
71 (100) |
Из данных таблицы 1 следует, что у 40,8%
пациентов встречался кишечный тип метаплазии, у 33,8
% – желудочно-кишечный. Кишечный тип метаплазии
обладает более высоким злокачественным потенциалом и
его наличие повышает риск развития аденокарциномы
пищевода (АКП). У пациентов с желудочной метаплазией
интенсивную реакцию на MUC5AC дают поверхностные
эпителиоциты, эпителиоциты желез кардиального типа
окрашиваются умеренно, при этом распределение
продукта реакции диффузное. Лишь в зоне вокруг ядра
типируются мелкие гранулы. В поверхностных
эпителиоцитах и в псевдобокаловидных клетках гранулы
локализуются преимущественно в апикальной части
клеток. При выявлении цитокератинов положительную
реакцию на СК7 обнаруживают только поверхностные
эпителиоциты. В то же время при выявлении
цитокератина СК20 окрашиваются как поверхностные,
так и железистые эпителиоциты кардиальных желез.
Собственные железы пищевода характеризуются
отрицательной экспрессией этих цитокератинов (рис.
2).
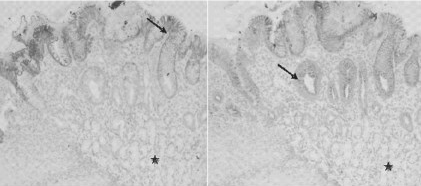
Рис. 2. Пищевод Барретта с желудочной
метаплазией. Выявление СК7 (А) (указано стрелкой) в
поверхностных эпителиоцитах. Выявление СК20 в
поверхностных и железистых (Б) эпителиоцитах
(указано стрелкой). Отрицательная экспрессии в
собственно железах пищевода (звездочка). Увеличение
х100
У пациентов с наличием кишечной метаплазии СО в
зоне ПБ появляются бокаловидных клеток; такие
участки метаплазии наиболее часто (63,6 %)
встречаются при коротком сегменте ПБ. Оказалось, что
у 12 пациентов имеет место завершенная кишечная
метаплазия. При этом бокаловидные клетки этих зон
обнаруживают присутствие как кишечного муцина MUC2,
так и желудочного MUC5AC, а секрет этих клеток
содержит нейтральные муцины и сиаломуцины (рис 3).

Рис. 3. Пищевод Барретта с кишечной
метаплазией. Интенсивная экспрессия MUC5AC.
Бокаловидные клетки с «MUC-негативным участком»
(стрелка). Увеличение х100
При завершенной кишечной метаплазии, как правило,
имеет место смещение зоны пролиферации вниз и
большинство Ki67 позитивных ядер выявляются в
клетках, расположенных в области дна желез.
Незавершенный тип кишечной метаплазии был выявлен у
16 больных. При этом бокаловидные клетки этих зон
характеризуются наличием желудочного муцина MUC5AC,
кишечного муцина MUC2, однако здесь между
бокаловидными клетками появляются цилиндрические
клетки, экспрессирующие MUC5AC; метка Ki67
встречалась в клетках различных отделов желез. У
всех пациентов с кишечной метаплазией, вне
зависимости от типа метаплазии, при окраске на СК7
положительная реакция обнаруживается только в
поверхностных отделах метаплазированного эпителия, в
то время как при окраске на СК20 положительную
реакцию дают как поверхностные эпителиоциты, так и
глубже лежащие железы с бокаловидными клетками (рис.
4,5)
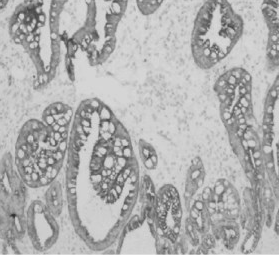
Рис. 4. Пищевод Барретта с кишечной
метаплазией. Положительная реакция на СК20;
увеличение х100
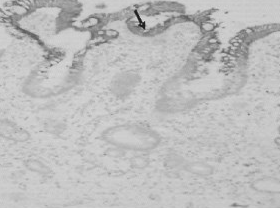
Рис. 5. Пищевод Барретта с кишечной
метаплазией Выявление СК7 (стрелка) в эпителиоцитах
поверхностных отделов слизистой; увеличение х100
При оценке результатов хирургической коррекции РЭ,
осложненного ПБ, оказалось, что формирование
арефлюксной кардии имело своим исходом эпидермизацию
очагов желудочной метаплазии только при
ультракоротком сегменте ПБ у трех пациентов. Для
остальных пациентов была характерна частичная
эпидермизация очагов желудочной метаплазии,
исчезновение диспластических изменений,
обусловленных острыми воспалительными процессами в
слизистой.
Эффект хирургической коррекции ПБ для 80%
пациентов с желудочной метаплазией был связан с
увеличением уровня содержания желудочного MUC5AC в
составе эпителиоцитов желез кардиального типа, тогда
как кишечный муцин в эпителиоцитах этих
метаплазированных зон не выявлялся. Экспрессия Ki 67
в ядрах базального слоя многослойного плоского
эпителия при его появлении характерна почти для 90%
ядер, что может указывать на усиление процесса
регенерации по пути формирования многослойного
пласта, свойственного нормальному пищеводу. Однако у
трех больных с желудочной метаплазией под
многослойным плоским эпителием сохранялись участки
метаплазии. Эпителиоциты этих зон не экспрессируют
кишечный муцин, а ядра не обнаруживают
пролиферативной активности Ki 67. Вместе с тем
клетки этих метапластических зон начинают
дифференцироваться по желудочному типу с ИГХ
выявляемыми в составе их секрета нейтральными и
сиаломуцинами.
Результаты хирургической коррекции у пациентов на
фоне кишечной метаплазии в исходном статусе
показали, что через 2 месяца после операции
распределение MUC2 и MUC5AC практически не меняется
и соответствует исходному. Тоже самое наблюдается в
распределении цитокератинов (СК7 и СК20) и
пролиферативного ядерного маркера Ki 67. Этот
феномен прослеживается на протяжении всех сроков
наблюдения. Показателем позитивных изменений к концу
первого года после операции является увеличение
числа ядер (более 80%) в эпителиоцитах базального
слоя многослойного плоского эпителия зон
эпидермизации, обнаруживающих положительную реакцию
на Ki 67. Эпителиоциты метаплазированных очагов под
зоной эпидермизации экспрессируют как желудочный,
так и кишечный муцины с ИГХ выявляемыми
сульфомуцинами, однако антиген пролиферативной
активности в ядрах эпителиоцитов желез не
выявляется.
Проведенный анализ результатов суточной рН –
метрии показал, что через 3 месяца после
хирургического лечения достоверно (р < 0,05)
снизились следующие показатели суточной рН–метрии
пищевода: % общего времени с рН < 4 – почти в 3 раза
в 1–ой группе и в 5 – во 2-ой; наибольшая
продолжительность рефлюкса – почти в 4 раз 1–ой и в
7 – во 2–ой; число продолжительных рефлюксов более 5
минут – в 3 раза в 1–ой и почти в 5 – во 2–ой;
индекс De Meester уменьшился в среднем в 5 раз и
среднее значение рН в нижней трети пищевода
достоверно (р<0,05) повысилось до 6,5 в обеих
группах (рис. 6.а – 6.д).
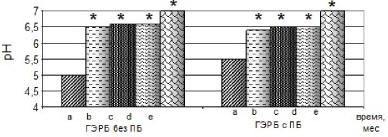
Рис. 6а. Среднее значение рН в нижней трети
пищевода больных гастроэзофагеальной рефлюксной
болезнью
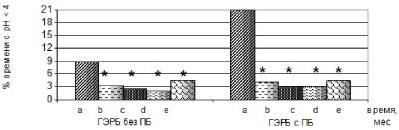
Рис. 6б. Процент общего времени с рН < 4 в
нижней трети пищевода больных гастроэзофагеальной
рефлюксной болезнью
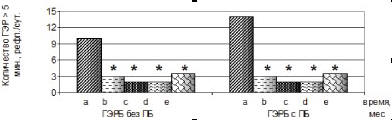
Рис. 6в. Число продолжительных рефлюксов более
5 минут в нижней трети пищевода больных
гастроэзофагеальной рефлюксной болезнью
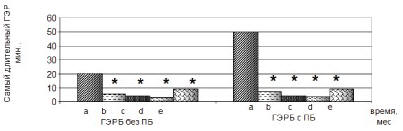
Рис. 6г. Наибольшая продолжительность рефлюкса
в нижней трети пищевода больных гастроэзофагеальной
рефлюксной болезнью
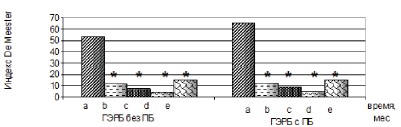
Рис. 6д. Индекс De Meester в нижней трети
пищевода больных гастроэзофагеальной рефлюксной
болезнью. Группы больных в зависимости от сроков
послеоперационного наблюдения: a – до операции, b –
через 2 месяца после операции, c – через 6 месяцев,
d – через 1 год, e – норма, * – р<0,05 по
сравнению с группой до операции
Полученные данные подтверждают, что после
оперативного лечения показатели суточной рН-метрии
эзофагогастрадуоденального комплекса достигают
нормативных значений, что свидетельствует об
устранении патологического рефлюкса и подтверждает
арефлюксность сформированной кардии в ближайшем и в
отдаленном послеоперационных периодах.
Обсуждение и выводы
В 90–х годах XX столетия отмечен новый этап
развития антирефлюксной хирургии
пищеводно-желудочного перехода, что было связано с
внедрением в клиническую медицину эндоскопических
технологий. По литературным данным лапароскопическая
фундопликация имеет широкое распространение, так как
данная методика менее агрессивна и у больных
наблюдается более короткий период восстановления по
сравнению с лапаротомией [9, 11-18, 20-21].
В литературе имеются данные, что при выполнении
рН-метрии в отдаленном периоде у 16,7% индекс
DeMeester значительно повышен, у 83,3% он остается в
норме [19]. Имеющиеся данные в публикациях совпадают
с результатами исследования наших пациентов.
Положительные результаты после лапароскопической
фундопликаций по Nissen на сегодняшний день отмечены
у 87–95% пациентов и это подтверждается данными
эндоскопии и полипозиционной рентгенографии
[9-10,24-25]. J.Y.Liu, S. Woloshin [38] опубликовали
исследование отдаленных результатов после
проведения фундопликаций по Nissen, которые
оценивали сами пациенты. Удовлетворенность
результатами операции отмечена у 83%
прооперированных больных [25].
Сравнительный анализ лапаротомного и
лапароскопического методов операции создания
арефлюксной кардии не проводили, так как это не
входило в цели нашего исследования. В настоящее
время проводится анализ различных методик
используемых в нашей клинике, который будет
представлен в последующих публикациях.
Итак, своевременное проведение хирургического
лечения у больных РЭ по предложенной методике
обеспечивает арефлюксность конструкции вновь
созданной кардии. Всем пациентам с РЭ необходимо
длительное динамическое наблюдение в отдаленном
послеоперационном периоде и проведение ежегодного
полного комплекса исследований, обязательно
включающего полипозиционную рентгенографию,
эндоскопию с биопсией и иммуногистохимическое
исследование СО. Эффект формирования арефлюксной
кардии у пациентов с ПБ при наличии желудочной
метаплазией проявляется усилением экспрессии MUC5AC
у 80% больных и появлением очагов эпидермизации с Ki
67 позитивными ядрами в базальном слое сквамозного
пласта у 100% прооперированных, что свидетельствует
об активации процесса адаптации и регенерации.
Наблюдение в отдаленном послеоперационном периоде за
пациентами позволяет предотвратить развитие
аденокарциномы пищевода.
Информация об авторах
- Шабанова Наталья Евгеньевна – к.м.н., врач –
терапевт, ассистент кафедры клинической
фармакологии и функциональной диагностики ГБОУ
ВПО «КубГМУ» Минздрава России. 50080 Краснодар
ул.Уральская 160 кв193, 8(918)437-65-25
nshabanоvа1980@mаil.ru
- Дурлештер Владимир Моисеевич – д.м.н.,
зам.главного врача по хирургии ГБУЗ «ККБ № 2»,
профессор кафедры хирургии № 1 ФПК и ППС ГБОУ
ВПО «КубГМУ» Минздрава России
- Корочанская Наталья Всеволодовна – д.м.н.,
руководитель гастроэнтерологического центра ГБУЗ
«ККБ № 2», главный внештатный гастроэнтеролог
Краснодарского края, профессор кафедры хирургии
№ 1 ФПК и ППС ГБОУ ВПО «КубГМУ» Минздрава России
- Тлехурай Руслан Махмудович – к.м.н., врач –
эндоскопист, отделения эндоскопии ГБУЗ «ККБ №
2», ассистент кафедры хирургии № 1 ФПК и ППС
ГБОУ ВПО «КубГМУ» Минздрава России
- Дряева Людмила Геннадьевна – к.м.н.,
заведующая патологоанатомическим отделением ГБУЗ
«ККБ № 2»
- Свечкарь Игорь Юрьевич – врач – хирург,
хирургического отделения № 4 ГБУЗ «ККБ № 2»,
аспирант кафедры хирургии № 1 ФПК и ППС ГБОУ ВПО
«КубГМУ» Минздрава России
- Рябчун Вадим Валерьевич – к.м.н., врач –
хирург, ГБУЗ «ККБ № 2»
- Беретарь Руслан Батырбиевич - врач – хирург,
хирургического отделения № 4 ГБУЗ «ККБ № 2»,
аспирант кафедры хирургии № 1 ФПК и ППС ГБОУ ВПО
«КубГМУ» Минздрава России
- Пономарева Ася Игоревна – д.м.н., профессор,
заведующая кафедрой клинической фармакологии и
функциональной диагностики ГБОУ ВПО «КубГМУ»
Минздрава России.
Список литературы
- Богданов Д.Ю., Матвеев Н.Л., Мацак В.А.
Исследование эффективности лапароскопических
фундопликаций при хирургическом лечение ГЭРБ //
Эндоскопич.хиирургия. – 2008. – Т. 14.№3. –
С.27-34.
- Луцевич О.Э., Галлямов Э.А., Преснов К.С.,
Гвоздик В.В., Макушин А.А. Выбор способа
эндохирургических антирефлюксных вмешательств
при гастроэзофагеальной рефлюксной болезни //
Альманах Института хирургии им. А.В.
Вишневского. – 2012. – Т. 7. №1. – С. 117-118.
- Маев И.В., Вьючнова Е.С., Лебедева Е.Л. и
др. Гастроэзофагеальная рефлюксная болезнь:
Уч.-мет. пос. М.: Изд. ВУНЦ МЗ РФ. 2000.
- Минушкин О.Н., Масловский Л.В., Аникина
Н.Ю., Шулешова А.Л. Оценка эффективности и
безопасности двух режимов поддерживающей терапии
рабепразолом у пациентов с ГЭРБ 0 и I степени //
Экспер. и клин, гастроэнтерол. 2005. №2. С.
29-36.
- Надинская М.Ю. Рабепразол (париет) в лечении
гастроэзофагеальной рефлюксной болезни с позиции
медицины основанной на научных доказательствах
// Рос. журн. гастроэнтерол., гепатол.,
колопроктол. 2004. №1. С. 2-12.
- Пучков К.В., Филимонов В.Б. Грыжи
пищеводного отверстия диафрагмы. – М.: «Медпрактика
– М», 2003. – 171 с.
- Старостин Б.Д. Эффективность поддерживающей
терапии при гастроэзофагеальной рефлюксной
болезни // Рос. журн. гастроэнтерол., гепатол.,
колопроктол. 2006. № 5. С. 13.
- Трухманов А.С. Новейшие данные о рефлюксной
болезни пищевода. Успехи консервативного лечения
// Рос. журн. гастроэнторол., гепатол.,
колопроктол. 1997. №1. С. 39-44.
- Черноусов Ф.А., Шестаков А.Л., Егорова Л.К.
Результаты фундопликаций при лечении
рефлюкс-эзофагита // Вестник хирургической
гастроэнтерологии. - 2009. - № 4. - С. 64-69.
- Anvari М., Allen С. Five-year comprehensive
outcomes evaluation in 181 patients after
laparoscopic Nissen fundoplication // J. Am.
Coll. Surg. 2003. V. 196 (1). P. 51-57;
discussion. P. 57-58.
- Anvari M., Allen C, Bonn A. Laparoscopic
Nissen fundoplication is a satisfactory
alternative to long-term omeprazole therapy //
Br. J. Surg. 1995. V. 82. P. 938-942.
- Bais J.E., Bartekman J.F., Bonjer H.J. et al.
Laparoscopic or conventional Nissen
fundoplication for gastro-oesophageal reflux
disease: randomised clinical trial // Netherl.
Antirefl . Surgery Stud. Group. Lancet. 2000. V.
355. P. 170-174.
- Bell R.C., Hanna P., Mills M.R., Bowrey D.
Patterns of success and failure with
laparoscopic Toupet fundoplication // Surg.
Endosc. 1999. V. 13(12). P. 1189-1194.
- Catarci M., Gentileschi P., Papi C. et al.
Evidence-based appraisal of antireflux
fundoplication // Ann. Surg. 2004. V. 239 (3).
P. 325-337.
- Dallemagne В., Weerts J.M., Jehaes C,
Markiewicz S. Causes of failures of laparoscopic
antirefl ux operations // Surg. Endosc. 1996. V.
10. P. 305-310.
- Draaisma W.A., Rijnhart-de Jong H.G.,
Breeders LA. et al. Five-year subjective and
objective results of laparoscopic and
conventional Nissen fundoplication: a randomized
trial // Ann. Surg. 2006. V. 244. P. 34-41.
- Furnee E.J.B., Draaisma W.A., Breeders LA.,
Hein G. Gooszen Surgical Reintervention After
Failed Antirefl ux Surgery: A Systematic Review
of the Literature // J. Gastrointest. Surg.
2009. V. 13(8). P. 1539-1549.
- Furnee E.J.B., Draaisma W.A., Breeders LA.
et al. Surgical Reintervention After Antireflux
Surgery for Gastroesophageal Reflux Disease. A
Prospective Cohort Study in 130 Patients // Arch.
Surg. 2008. V. 143(3). P. 267-274.
- Khajanchee Y.S., O'Rourke R.W., LockhartB.
et al. Postoperative Symptoms and Failure After
Antireflux Surgery // Arch. Surg. 2002. V 137.
P. 1008-1014.
- Perdikis G, Hinder R., Lund R. et al.
Laparoscopic Nissen fundoplication: Where do we
stand? // Surg. Laparosc. Endoscop. 1997. V. 7.
P. 17-21.
- Rantanen Т.К., Sab J.A., Salminen J.T.,
Kellokumpu I.E. Functional Outcome After
Laparoscopic or Open Nissen Fundoplication. A
Follow-up Study //Arch. Surg. 1999. V. 134. P.
240-244.
- Richardson W.S., Trus T.L., Hunter J.G.
Laparoscopic antireflux surgery // Surg. Clin.
N. Am. 1996. V. 76. P. 437-458.
- Romagnuolo J., Meier M.A., Sadowski D.C.
Medical or surgical therapy for erosive reflux
esophagitis: costutility analysis using a Markov
model//Ann. Surg. 2002. V. 236. P. 191-202.
- Salminen P.T.P., Hiekkanen H.I. et al.
Comparison of long-term outcome of laparoscopic
and conventional nissen fundoplication: a
prospective randomized study with an 11-year
follow-up // Ann. Surg. 2007. V. 246(2). P.
201-216.
- Salminen P. Т., Laine S. O., Ovaska J. T.
Late subjective results and symptomatic outcome
after laparoscopic fundoplication // Surg.
- Soper N.J., Dunnegan D. Anatomic
fundoplication failure after laparoscopic
antireflux surgery // Ann. Surg. 1999. V. 22. P.
669-677.
Статья опубликована на сайте
http://www.gastroscan.ru

