Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Многоликая острая респираторная инфекция: от основных
возбудителей к выбору препаратов
М. С. Савенкова, доктор медицинских наук, профессор
РГМУ, Москва
Острые респираторные заболевания (ОРЗ) у детей и взрослых по своей частоте и
эпидемической распространенности занимают первое место среди всех болезней. Дети
разного возраста в норме 2–3 раза в год болеют ОРЗ. Частота респираторных
заболеваний может быть объяснима многообразием вирусов и пневмотропных
возбудителей бактериального происхождения. За последние 30 лет, благодаря
развитию миробиологии, генно-инженерных методов, произошли значительные
изменения в структуре респираторных инфекций. Если в прежние годы, выставляя
ребенку диагноз острой респираторной вирусной инфекции, мы были уверены, прежде
всего, в наличии хорошо изученных и известных возбудителей — таких как грипп,
парагрипп, аденовирус, респираторно-синтициальный вирус (РСВ), риновирус, то на
сегодняшний день следует учитывать и внутриклеточных возбудителей — хламидий и
микоплазм, вирусов группы герпеса, других возбудителей — легионелл, бокавирусов
(табл. 1).
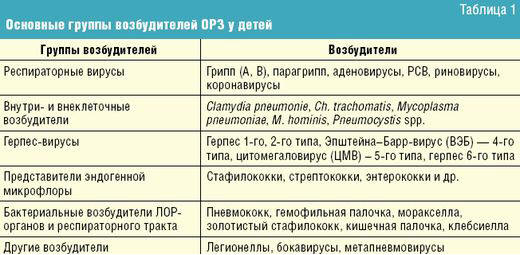
Выделенных возбудителей объединяет легкость передачи, способность к
изменчивости и нестойкость постинфекционного иммунитета. Исходя из этих
соображений, до получения результатов лабораторных исследований, очевидно,
целесообразнее употреблять более обобщенный термин «ОРЗ» — «острое респираторное
заболевание» или «РЗ» — «респираторное заболевание».
Ежегодно эпидемиологический состав вирусов меняется. В среднем, насчитывается
более 200 видов респираторных вирусов: гриппа, парагриппа, РСВ, адено-, рино-,
корона-, энтеровирусы. Доля респираторных вирусов может быть различной и зависит
нередко от географических особенностей той или иной страны или города. Так, в
Калифорнии преобладают риновирусы (30–50%), в России — на долю гриппа приходится
30–50%, в период эпидемии этот показатель увеличивается [1, 2]. По данным
Санкт-Петербургской государственной медицинской академии по частоте
инфицирования грипп составляет 15% (тип А — 12%, В — 3%), парагрипп — до 50%,
аденоинфекции — до 5%, РСВ — 4%, микоплазма — 2,7%, энтеровирусы — 1,2%,
смешанные инфекции — около 23% случаев [3]. У детей первого полугодия жизни 70%
бронхиолитов обусловлены РСВ. После перенесенной тяжелой РСВ инфекции возможно
развитие рецидивирующего течения, которое резко увеличивает вероятность развития
бронхиальной астмы [4].
От каких факторов зависит инфицирование теми или иными возбудителями Можно
перечислить основные: возраст, частота заболеваний, уровень поражения слизистых
респираторного тракта (верхних дыхательных путей (ВДП), нижних дыхательных путей
(НДП)), сезонность, состояние лимфоглоточного кольца и слизистых полости рта.
Для детей раннего возраста большую роль играет преморбидный фон и тесный контакт
с инфицированными родителями.
Особую группу составляют «часто болеющие дети» (ЧБД), для которых характерен
смешанный характер течения и большая частота эпизодов респираторных заболеваний
в течение года.
Частые респираторные заболевания у ребенка — хорошо это или плохо Ответ на
данный вопрос не может быть однозначным, и в этом случае вполне закономерно
существование противоположных мнений. С одной стороны, респираторные заболевания
способствуют формированию иммунитета. С другой стороны, рецидивирующие
заболевания нижних дыхательных путей, особенно у детей первых трех лет жизни,
определенно связаны с развитием бронхоспазма к 7 годам. Однако частые
респираторные заболевания приводят к повышению сенсибилизации организма и
развитию хронической патологии (бронхиальной астмы, аденоидитов, тонзиллитов,
синуситов, обструктивных бронхитов, рецидивирующего синдрома крупа), которые, в
свою очередь, способствуют формированию функциональных нарушений со стороны
сердечно-сосудистой и бронхолегочной системы [5–7].
Клинические симптомы острых респираторных заболеваний во многом схожи:
гипертермия, катаральные явления (насморк, кашель), головная боль, гиперемия
зева, конъюнктивит, увеличение регионарных лимфоузлов, боли в животе, рвота,
артралгии.
Несмотря на схожую клиническую картину, имеются и определенные различия, как
в клинических симптомах, так и в продолжительности инкубационного периода. Так,
для гриппа инкубационный период может быть очень коротким от 2–5 часов до 7
суток. Грипп является острым инфекционным заболеванием с коротким инкубационным
периодом, внезапным началом, выраженной интоксикацией. Клиника риновирусной
инфекции развивается спустя 10–12 часов. При аденовирусной инфекции и
заболеваниях внутриклеточной этиологии инкубационный период может быть более
продолжительным — от 2 до 14 дней. Для герпесвирусных инфекций инкубационный
период может быть различным по продолжительности — от 1–2 суток до трех недель.
Известно, что возбудители имеют определенный тропизм к отдельным участкам
слизистой респираторного тракта, тем самым определяя основную симптоматику
заболевания. Так, для вируса гриппа свойственно поражение эпителия верхних
(задняя стенка глотки) и нижних (трахеобронхит) дыхательных путей, включая
паренхиму легких (пневмонию). РСВ инфекция чаще поражает детей второго полугодия
жизни с развитием бронхообструкции и бронхиолита. Для аденовирусной инфекции,
наряду с обильным серозным отделяемым при кашле, характерно наличие
конъюнктивита, полиаденита, возможна гепатомегалия. При парагриппозной инфекции
у детей в возрасте 6–18 мес жизни чаще поражается слизистая гортани, именно
поэтому они чаще госпитализируются в стационар с обструктивным ларингитом
(синдромом крупа). Риновирусная инфекция преимущественно поражает слизистую носа
с развитием насморка, чихания, заложенности носа.
Лихорадочный период при острых респираторных вирусных инфекциях также
различный: при гриппе — гипертермия (38–40 °C) — 1–2 дня, парагриппе — 37,5–38 °C
(до 5 суток), аденовирусной инфекции (лихорадочный период с размахами до 38–39 °C
в течение двух недель). При риновирусной инфекции температурная реакция
незначительно выражена, чаще субфебрильная.
Хламидийная и микоплазменная инфекции характеризуются кашлем «коклюшеподобного»
характера, с одновременным увеличением лимфоузлов, нередко конъюнктивитом.
Температурная реакция чаще не выражена. Заболевания хламидийной и микоплазменной
этиологии нередко носят рецидивирующий характер, сопровождаются функциональными
нарушениями со стороны сердечно-сосудистой и бронхолегочной систем [8].
Нередко заболевания вирусной и внутриклеточной этиологии сопровождаются
активацией эндогенной микрофлоры (Staphylococcus aureus, S. pneumoniae, S.
viridans) либо присоединением грамотрицательных возбудителей типа H. influenzae,
Moraxella catarrhalis.
Осложнения бактериального характера (синуситы, отиты, пневмонии) возникают у
детей раннего и пубертатного возраста и связаны с особенностями развития
иммунной системы. Лимфоглоточное кольцо с момента рождения у ребенка играет
огромную роль и выполняет защитную функцию от респираторных вирусов, бактерий,
грибов. Ранний возраст отличается своеобразием функции иммунной системы. В этом
возрасте происходит переориентация иммунного ответа на инфекционные агенты с
превалирования Th2 ответа, свойственного новорожденным и детям первых месяцев
жизни, на Th1 ответ, свойственный взрослым [9]. У детей с рецидивирующими и
хроническими заболеваниями имеет место дисфункция микробиоциноза и местного
иммунитета слизистой рото- и носоглотки. К особенностям иммунной системы ЧБД
следует отнести нарушение процессов интерферонообразования, снижение уровня
секреторного иммуноглобулина (sIgA), лизоцима, снижение В клеточного и
Т-клеточного иммунитета [10].
Известно также и негативное влияние частого использования антибактериальных
препаратов у ЧБД, которые подчас назначаются без предварительного обследования,
формируя не только сенсибилизацию, но и дисбактериоз и резистентность выделенной
микрофлоры.
Лечение ОРЗ. Основные группы препаратов
Антибактериальная терапия. Основными показаниями для назначения антибиотиков
является риск развития бактериальных осложнений: ранний детский возраст,
гипертермия более трех дней, болевой синдром при развитии отита, подозрение на
пневмонию.
Практика показала, что для успешного лечения детей необходимо знание
микробиологических и серологических результатов, без учета которых возможно
формирование тяжелых и хронических форм заболеваний из-за нерационального по
продолжительности курса антибактериальной терапии. В связи с риском развития
тяжелых осложнений, особенно у детей раннего возраста и новорожденных,
значительно ограничены показания для многих групп антибиотиков: аминогликозидов
(ото- и нефротоксичность), хлорамфеникола (апластическая анемия),
сульфаниламидов и ко-тримоксазола (ядерная желтуха), цефтриаксона (ядерная
желтуха). Нежелательные реакции отмечены при приеме эритромицина (тошнота,
рвота) [11].
За последние 20 лет, благодаря смене грамположительной микрофлоры на
грамотрицательных и внутриклеточных возбудителей, на фармацевтическом рынке
появились новые антибактериальные средства (защищенные бета-лактамные
антибиотики — цефалоспорины, макролиды, карбапенемы, гликопептиды, фторхинолоны).
Следует также учитывать рост резистентности стафилококков, пневмококков,
гемофильных палочек и других грамотрицательных микроорганизмов [11].
Проблема резистентности микроорганизмов к антимикробным препаратам является
социальной и рассматривается в различных ее аспектах. В этой связи изучается
резистентность микроорганизмов не только в стационарах (например, заболеваний,
вызванных метициллинрезистентным стафилококком S. aureus — MRSA,
энтеробактериями), но и во внебольничной среде. Наблюдается неблагоприятная
тенденция к концентрации резистентных штаммов в детских коллективах (детских
домах и детских садах).
По данным Козлова Р. С. (2009), в целом по стране резистентность пневмококков
к пенициллину составляет 10%, в то время как в детских домах она достигает
80–90%. В России, в отличие от стран Западной Европы, США, Юго-Восточной Азии,
сохраняется благоприятная ситуация с чувствительностью к бета-лактамам,
макролидам, фторхинолонам [12].
Не случайно лечение тяжелых госпитальных инфекций требует постоянного
мониторинга результатов тестов на чувствительность к антибактериальным
препаратам in vitro. Для профилактики возникновения устойчивых штаммов следует
каждые 1–2 года производить смену лекарственных средств, наиболее часто
используемых в больнице, что уменьшит вероятность появления резистентных штаммов
[12].
При развитии у ребенка респираторного заболевания любой инфекционной природы
педиатру следует ответить на ряд вопросов:
- Нужен ли антибиотик
- Какой антибиотик следует использовать, каковы пути его введения в организм
- Какова продолжительность курса терапии
- Каковы критерии излеченности
Принципы выбора эмпирического антибиотика базируются на знании основных
возбудителей как в стационаре, так и в амбулаторной практике. Перед назначением
антибиотика следует оценить «факторы со стороны больного» и ряд «факторов
возбудителя».
«Факторы больного»:
- аллергологический анамнез;
- состояние функции печени и почек;
- наличие сопутствующих заболеваний;
- прием других лекарственных средств;
- тяжесть болезни;
- возраст;
- локализация патологического процесса;
- у сексуально активных девочек оценивают прием контрацептивов.
«Факторы возбудителя»:
- вероятный возбудитель (вирус или бактерия);
- чувствительность микроорганизма к противомикробным средствам.
Известно, что эффективность проводимой терапии во многом зависит от знания
основных патогенов сегодняшнего дня. С 2000 года нами ежегодно проводится
скрининг основных возбудителей на основе комплекса серологических и
микробиологических методов. За этот период времени было обследовано более двух с
половиной тысяч детей и более 300 взрослых. Исследование проводили на базе
Морозовской больницы г. Москвы, РГМУ, МНИИЭМ им. Н. Г. Габричевского МЗ РФ, НИИ
физико-химической медицины Минздравмедпрома РФ. Серологическая диагностика
проводилась методом иммуноферментного анализа (ИФА) у детей (амбулаторно и в
стационаре) с рецидивирующими заболеваниями верхних и нижних дыхательных петей,
ЛОР-органов. Иммуноферментная диагностика включала определение иммуноглобулинов
классов IgG и IgM для следующих инфекций: хламидиоза (Ch. pneumoniae, Ch.
trachomatis, Ch. psittaci), микоплазмоза (M. pneumoniae, M. hominis),
токсоплазмоза, вируса простого герпеса 1 го, 2 го типа (Herpes simplex Type 1,
Herpes simplex Type 2), ВЭБ — вирус герпеса 4 го типа (Epstein-Barrvirus Human
herpes Type 4), вирус герпеса человека 5 го типа (Cytomegalovirus, Human herpes
Type 5). Всего было обследовано 516 детей разного возраста, выделено 810
возбудителей.
На рис. 1 представлена тенденция преобладающих возбудителей последних четырех
лет (с 2007 по 2010 гг.).
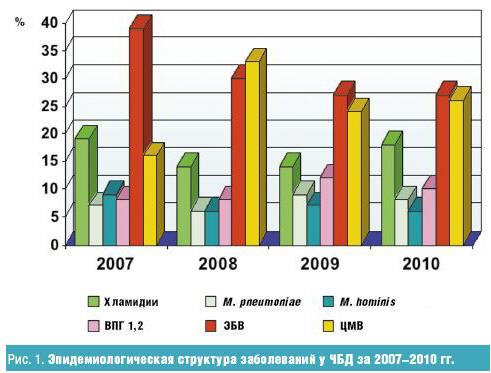
При оценке изменений в структуре возбудителей, которые происходили с 2000
года, было выявлено уменьшение преобладающих в то время внутриклеточных
возбудителей и увеличение герпесвирусных. Эти изменения происходили благодаря
активному внедрению макролидов для лечения хламидийных и микоплазменных инфекций
с конца прошлого века. С 2004 года происходит увеличение количества детей с
герпесвирусным инфицированием. На рисунке данная тенденция сохраняется
(2007–2010 гг.): преобладают ВЭБ и ЦМВ инфекции. Данная тенденция должна
учитываться, так как ряд заболеваний имеет смешанную этиологию, без четкого
знания которой невозможен грамотный выбор терапии.
Учитывая основные требования, предъявляемые к назначению антибактериальных
препаратов, наиболее эффективными и безопасными для детей принято считать группу
аминопенициллинов, цефалоспоринов и макролидов.
Амоксициллин — полусинтетический пенициллин широкого спектра действия,
угнетающий синтез бактериальной стенки. Оказывает воздействие не только на
грамположительные, но и на грамотрицательные микроорганизмы. Амоксициллин в
настоящее время по-прежнему продолжает рассматриваться как препарат первой линии
при бронхитах, пневмонии, синусите, тонзиллите, среднем отите [13, 14]. Механизм
устойчивости грамотрицательных бактерий к бета-лактамам связан с продукцией
бета-лактамаз широкого спектра, разрушающих бета-лактамное кольцо. Для
преодоления резистентности в настоящее время используются комбинированные
препараты, содержащие в своем составе антибиотик и ингибитор бета-лактамаз (клавуланат,
сульбактам, тазобактам).
В педиатрической практике известны также и нежелательные действия клавуланата
на систему пищеварения (диарея, диспептические явления), на долю которых
приходится 18–20%. «Защищенные» аминопенициллины — амоксициллин и амоксициллин/клавуланат,
согласно рекомендациям ВОЗ и Минздрава РФ, включены в Перечень необходимых и
важнейших лекарственных средств РФ и стандартов лечения больных. В последние
годы, благодаря инновационной технологии, в основе которой происходит
равномерная дисперсия частиц по новой технологии «Солютаб», был создан ряд
препаратов: Флемоксин Солютаб, Флемоклав Солютаб.
Данная технология позволяет повысить всасывание клавулановой кислоты до
62–66%, а действующее вещество в неизмененном виде максимально всасывается в
зоне воспаления [15, 16]. Амоксицилли/сульбактам (Трифамокс ИБЛ) выпускается для
детей в виде суспензии, расширяет спектр активности амоксициллина за счет
устойчивых к нему штаммов, связывается с белками плазмы и проявляет синергизм с
другими бета-лактамными антибиотиками. Сульбактам обладает большей устойчивостью
к изменениям pH-среды, чем клавуланат, по этой причине его следует применять у
часто болеющих детей [15, 16].
Цефалоспорины относятся к бета-лактамным антибиотикам широкого спектра
действия. Выделяют 4 поколения цефалоспоринов для парентерального введения и
перорального приема (табл. 2).
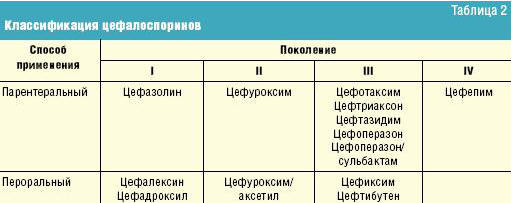
Для выбора правильной этиотропной терапии необходимо ориентироваться в
некоторых различиях спектра цефалоспоринов. Цефалоспорины I поколения проявляют
чувствительность в основном к стрептококкам (S. pneumoniae, S. pyogenes) и
стафилококкам. По уровню антипневмококковой активности они уступают
цефалоспоринам последующих поколений и аминогликозидам. По этой причине спектр
их применения ограничен.
Спектр действия цефалоспоринов II поколения шире: они более активны в
отношении стафилококков, а также грамотрицательных микроорганизмов: Neisseria
spp., E. coli, Shigella spp., Salmonella spp., P. mirabilis, Klebsiella spp.).
На практике цефалоспорины II поколения активно применяют при пневмониях,
инфекциях мочевыводящих путей, инфекциях кожи и мягких тканей.
Парентеральные цефалоспорины III поколения (цефотаксим, цефтриаксон — 50–100
мг/кг/сут в 3–4 введения) проявляют высокую активность в отношении
стрептококков, стафилококков, гонококков, менингококков, энтеробактерий, H.
influenzae, M. catarrhalis. C учетом спектра действия их рекомендуется применять
при тяжелых инфекциях: пневмонии, менингите, сепсисе, нозокомиальных инфекциях.
Цефалоспорин IV поколения (цефепим) по своим базовым характеристикам близок к
цефалоспоринам III поколения. Отличие заключается в способности цефепима
проникать через внешнюю мембрану грамотрицательных бактерий и относительной
устойчивости к гидролизу хромосомными бета-лактамазами. Поэтому цефепим
проявляет высокую активность в отношении P. aeruginoza, а также в отношении
микроорганизмов — гиперпродуцентов хромосомных бета-лактамаз (Enterobacter spp.,
Serratia spp., Citrobacter spp., Morganella morganii, Providencia stuartii).
Из пероральных цефалоспоринов на сегодняшний день в нашей стране и за рубежом
хорошо зарекомендовал себя пероральный цефалоспорин III поколения — цефиксим (Супракс)
[17]. Обладая широким спектром действия, применяется в амбулаторной и
стационарной практике при заболеваниях ЛОР-органов, дыхательных путей (верхних и
нижних), заболеваниях мочевыводящих путей.
Макролиды являются на сегодняшний день практически единственной группой
антибиотиков, в отношении которой высокочувствительны внутриклеточные
инфекционные агенты. Макролиды обладают уникальной способностью к концентрации в
тканях и очагах воспаления, причем наиболее интенсивно они накапливаются в
миндалинах, лимфоузлах, легких, плевральной жидкости, органах малого таза,
суставах. Макролиды целесообразно применять не только при внутриклеточных
инфекциях (хламидийной, микоплазменной, токсоплазменной и т. д.) этиологии, а
также при смешанных вариантах. К ним высокочувствительны стрептококки,
пневмококки, стафилококки, хламидии, микоплазмы, легионеллы, гонококки; умеренно
чувствительны энтерококки, Helicobacter pylori, боррелии, микобактерии (кроме M.
tuberculosis), токсоплазма, анаэробы; гемофильная палочка к большинству
препаратов слабочувствительна. Устойчивы к макролидам метициллинрезистентные
стафилококки, E. faecium, Enterobacnteriaceae, P. aeruginosae, Acinetobacter.
Макролиды представлены тремя группами:
- I группа — 14 членные (эритромицин, кларитромицин, рокситромицин);
- II группа — 15 членные (азитромицин);
- III группа — 16 членные (джозамицин, спирамицин, мидекамицин).
Суточные дозы и кратность введения макролидов:
Внутрь:
- азитромицин 10 мг/кг/сут 5–10 сут однократно;
- джозамицин 30–50 мг/кг/сут/ в 3 приема;
- кларитромицин 7,5–15 мг/кг/сут в 2 приема;
- мидекамицин 30–50 мг/кг/сут в 3 приема;
- роксимтомицин 5–8 мг/кг/сут в 2 приема;
- эритромицин 40–50 мг/кг/сут в 3–4 приема.
Парентерально:
- кларитромицин 7,5 мг/кг (не более 1 г) в 2 введения детям старше 28 дней;
- эритромицин 40–50 мг/кг/сут в 3 введения (92%).
В России на протяжении 20 последних лет накоплен огромный опыт применения
азитромицина (Сумамеда) — первого представителя группы 15 членных макролидов (азалидов).
Одними из первых работ были работы, которые касались лечения заболеваний
ЛОР-органов (отитов, тонзиллита, фарингита). Позднее появились работы по
активному применению азитромицина при заболеваниях верхних и нижних дыхательных
путей у взрослых и детей. В последние годы значительно расширились рамки
применения азитромицина при таких заболеваниях как коклюш, скарлатина, инфекции
кожи и дерматозы, кишечные инфекции. Широкое применение азитромицина можно
объяснить активностью в отношении большинства грамположительных и
грамотрицательных кокков. Однако наибольшую популярность азитромицин получил в
связи с особой чувствительностью к внутриклеточным патогенам (Chlamydia
trachomatis, Ch. pneumoniae, Mycoplasma pneumoniae, Mycoplasma hominis,
Ureaplasma urealyticum, Legionella pneumophila), простейшим (Toxoplasma gondii),
спирохетам (Treponema pallidum, Borrelia burgdorferi), рикетсиям (Bartonella
henselae).
Еще одним положительным феноменом, описанным в последние годы, следует
считать иммуномодулирующий эффект макролидов [18]. Это воздействие складывается
из ряда этапов. Так, азитромицин способен подавлять продукцию интерлейкина-8 (провоспалительного
цитокина), тем самым способствуя дегрануляции нейтрофилов и лизису бактерий.
Макролиды повышают продукцию интерлейкина-10 (противовоспалителиного цитокина),
снижают образование медиаторов воспаления [18].
В проведенных нами ранее сравнительных исследованиях была показана
эффективность макролидов у детей с хламидийной инфекцией. Наиболее высокой она
была у джозамицина (96,5%), азитромицина (93,4%), мидекамицина (93,4%),
рокситромицина (92%), клиндамицина (93,4%) и кларитромицина (92%). Наименее
результативен был эритромицин (56%).
Джозамицин относится к 16 членным макролидам, созданным на основе технологии
«Солютаб» — диспергируемых таблеток, обеспечивающих равномерную дисперсию частиц
действующего вещества. Джозамицин в настоящее время активно применяется при
заболеваниях ЛОР-органов (ангине, в том числе стрептококковой), скарлатине,
отитах, синуситах, инфекциях нижних дыхательных путей — бронхитах, пневмонии,
обусловленной внутриклеточными возбудителями, коклюше, инфекциях кожных покровов
и мягких тканей, инфекциях мочеполовой системы, в стоматологии [19, 20].
Противовирусная терапия
У детей арсенал средств, используемых для лечения респираторных заболеваний
вирусной этиологии, ограничен. На сегодняшний день для лечения и профилактики
гриппа Всемирной Организацией Здравоохранения рекомендовано применение
препаратов только этиотропного действия: блокаторов ионных каналов (римантадин,
амантадин) и ингибиторов нейраминидазы (осельтамивир и занамивир).
Ремантадин у нас в стране начал применяться с 1975 года для лечения гриппа А.
Многочисленные исследования изучения клинической и профилактической
эффективности Ремантадина свидетельствуют об уменьшении интоксикации,
катаральных явлений, уменьшении общей продолжительности заболевания, тяжести
течения более чем на 50% [21]. Резистентность к препарату формируется чаще при
лечении в терапевтической дозе и равна 10–20%. У современных пандемических
вирусов гриппа H1N1 выявлено две мутации во фрагментах белка М2, в связи с чем
ВОЗ и Минздравсоцразвития РФ не рекомендуют применение римантадина (Орвирема в
сиропе для детей) в пандемический период.
Осельтамивир — первый ингибитор нейраминидазы, по сравнению с Релензой
обладает более высокой биодоступностью (30–100%) [22]. Клиническое исследование
по применению осельтамивира показало его высокую эффективность при раннем приеме
препарата — в первые 36 часов. Прием осельтамивира в качестве профилактического
средства не рекомендован и связан с возможным развитием побочных осложнений
(диареей, тошнотой, болями в животе и развитием отита) [23].
Арбидол относится к противовирусным препаратам, сходным по механизму действия
с предыдущими. Арбидол, в отличие от амантадина и римантадина, ингибирует
освобождение самого нуклеокапсида от наружных белков, нейраминидазы и липидной
оболочки. Таким образом, он действует на ранних стадиях вирусной репродукции.
Арбидол подавляет репликацию вируса гриппа А на 80%, В на 60% и С на 20% и может
применяться у детей с двухлетнего возраста [24].
Препарат относится еще и к индукторам интерферона, способствуя повышению
общего количества Т-лимфоцитов и Т-хелперов. Применяется при гриппе в качестве
профилактического средства и для лечения, предотвращая тяжелое течение,
продолжительность заболевания и сокращая частоту осложнений. Арбидол совместим с
другими противовирусными препаратами, антибиотиками.
Интерферонопрофилактике гриппа в прежние годы в литературе было посвящено
много работ. Ранее проводилось распыление интерферона в носовые ходы для
профилактики гриппа и других ОРВИ, однако он быстро выводится из респираторного
тракта благодаря действию реснитчатого мерцательного эпителия. В последние годы
активно применялся препарат Анаферон детский для лечения и профилактики ОРЗ,
препараты рекомбинантного интерферона (Виферон). Интерфероны активно
используются при респираторных вирусных заболеваниях — гриппе, парагриппе, РСВ и
аденовирусных инфекциях, риновирусных инфекциях.
В последние годы для лечения детей с ОРВИ, а также герпесвирусными
заболеваниями стал активно применяться инозин пранобекс. В настоящее время на
фармацевтических рынках присутствует более 10 наименований препарата:
Isiorinosine, Groprinisin, Immunovir и др. Инозин пранобекс (Изопринозин®)
относится к метаболитам натуральных пуринов.
Противовирусное действие инозина пранобекс связано с подавлением репликации
ДНК и РНК вирусов путем связывания с рибосомой клетки и изменением ее
стереохимического строения. Иммуномодулирующий эффект обусловлен стимуляцией
функциональной активности Т-лимфоцитов, Т-хелперов, естественных киллеров.
Препарат увеличивает продукцию интерлейкинов, стимулирует биохимические процессы
в макрофагах, повышает синтез антител, инициирует продукцию интерферонов,
уравновешивает баланс клеточного и гуморального иммунитета.
Рекомендуемая доза взрослым — 6–8 таблеток в день. Детям — 50 мг/кг массы
тела в сутки в 2–4 приема в течение 5–10 дней (при необходимости суточную дозу
препарата увеличивают до 100 мг/кг). При герпесвирусных инфекциях проводят
несколько курсов по 10 дней (1–2–3).
Инозин пранобекс изучался у детей в комплексной терапии ОРВИ, при
бронхиальной астме, у больных с атопическим дерматитом [25–27]. Применение
инозина пранобекс у ЧБД после санации очагов хронической инфекции снижало
частоту эпизодов ОРЗ в 3 раза, частоту рецидивирующего бронхита в 2,3 раза и
хронического фарингита — в 2,5 раза. Впоследствии у этих детей значительно
сокращался прием антибактериальных препаратов [27].
Как уже было сказано в начале статьи, одними из основных патогенов у детей с
респираторными заболеваниями на сегодняшний день становятся герпес-вирусы, в
лечении которых большинство врачей испытывают определенные трудности. В этом
отношении инозин пранобекс (Изопринозин) в течение последних лет применяется у
больных герпес-вирусами (герпесом 1 го, 2 го типа, ВЭБ и ЦМВ) [28].
Нами было проведено изучение сравнительной эффективности противовирусных
препаратов (ацикловир, Арбидол, иозин пранобекс и индуктора интерферона —
циклоферона) у 115 детей с рецидивирующими заболеваниями респираторного тракта,
у которых было подтверждено герпесвирусное инфицирование (рис. 3). В
исследование были включены дети от 1 года до 15 лет. Основные диагнозы детей
представлены в табл. 3.
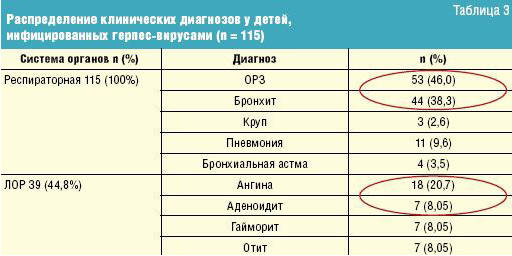
У большинства ЧБД преобладали ОРЗ (46%) и бронхиты (38,3%), у которых также
имела место и ЛОР-патология (44,8%).
Всем детям было проведено серологическое обследования для подтверждения
герпетических (герпес 1-го, 2-го типа, ЦМВ, ЭБВ, герпес 6-го типа) и
внутриклеточных (хламидийной, микоплазменной, токсоплазменной) инфекций.
Как видно на рис. 2, большинство детей с респираторной патологией было
инфицировано герпес-вирусами (ЭБВ — 63,5%, ЦМВ — 59,1%).
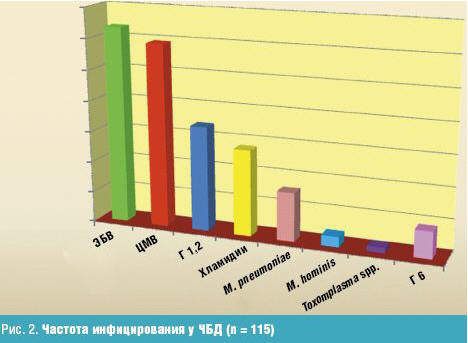
Меньше детей было инфицировано герпес-вирусами 1-го, 2-го и 6-го типа
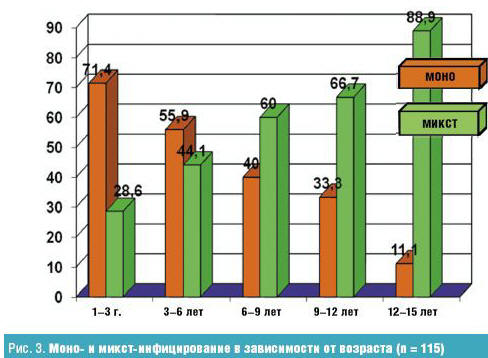
(соответственно 33,9% и 8,7%). Следует отметить, что для детей любого возраста
характерно было смешанное инфицирование (герпесвирусное + внутриклеточное) (рис.
3).
У 58 детей с рецидивирующими заболеваниями респираторного тракта
герпесвирусной (смешанной) этиологии нами было проведено лечение следующими
препаратами: ацикловиром (14), арбидолом (12), изопринозином (22), циклофероном
(10). Группы детей были рандомизированы по возрасту и основным диагнозам. Выбор
данных противовирусных препаратов был обусловлен выделенными герпесвирусами:
- Изопринозин (инозин пранобекс) — 50–100 мг/кг в течение 10 дней;
- Арбидол — 0,05–0,1 × 4 раза в течение 7 дней;
- Ацикловир — 100 мг × 3 раза — 7 дней;
- Циклоферон (меглумина акридонацетат) — 150 мг (по возрасту 1–3 таблетки в
день) по схеме: 1-й, 2-й, 4-й, 6-й, 8-й, 11-й, 14-й, 17-й, 20-й, 22-й дни.
Результаты проведенного лечения нами были оценены через два месяца по
динамике серологических показателей (рис. 4).
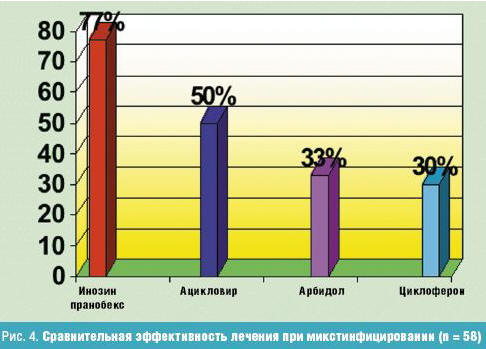
Как показали проведенные исследования, лучший результат был получен при
лечении детей Изопринозином (эффект составил 77%). При лечении другими
препаратами он был значительно ниже: Ацикловир (50%), Арбидол (33%), Циклоферон
(30%). Очевидно, для лечения детей с герпесвирусными и смешанными инфекциями
одним из препаратов выбора в настоящее время следует считать инозин пранобекс.
Перспективным с нашей точки зрения является применение Изопринозина у детей
раннего возраста в лечении различных форм герпесвирусных заболеваний, особенно в
связи со скорым появлением суспензионной формы.
Таким образом, острую респираторную инфекцию на сегодняшний день
действительно можно назвать многоликой с позиции этиологических факторов. Именно
знание последних будет определять выбор противовирусной, антибактериальной или
комбинированной терапии.
Литература
- Острые респираторные заболевания у детей: лечение и профилактика.
Научно-практическая программа. М., 2002. 70 с.
- Зайцев А. А., Синопальников А. И. Рациональная фармакотерапия острых
респираторных вирусных инфекций // Consilium Medicum. 2010. Т. 10. № 10, с.
80–86.
- Романцов М. Г., Сологуб Т. В., Шульдякова О. Г. Грипп и ОРВИ у детей.
Современные подходы к терапии и экстренной профилактике // Consilium Medicum.
Педиатрия. 2007. № 2, с. 18–22.
- Valkonen H., Waris M., Ruohola A. et al. Recurrent wheezing after
respiratory syncytial virus or non-respiratory syncytial virus bronhiolitis in
infancy: a 3 year follow-up // Allergy. 2009. V. 64. P. 680–686.
- Иванова Н. А. Часто болеющие дети // Русский медицинский журнал. 2008, т.
16, № 4, с. 183–185.
- Самсыгина Г. А., Коваль Г. С. Часто болеющие дети. Проблемы диагностики,
патогенеза и терапии // Детский врач. 2008, № 6, с. 5–10.
- Булгакова В. А., Балаболкин И. И., Ушакова В. В. Современное состояние
проблемы часто болеющих детей // Педиатрическая фармакология. 2007, т. 4, № 2.
с. 48–52.
- Савенкова М. С., Савенков М. П. Антибактериальная терапия респираторного
хламидиоза у детей // Consilium Medicum. Педиатрия. 2007, № 2, с. 30–35.
- Майкл Гриппи. Патофизиология легких. Изд. 2 е. М.: Из-во «Бином» 2005,
303.
- Вавилова В. П., Перевощикова Н. К. Образовательная программа для педиатров
и врачей общей практики «реабилитация часто болеющих детей». Издатель:
Международный фонд охраны здоровья матери и ребенка. М., 2004, 24.
- Практическое руководство по антиинфекционной химиотерпии. Под ред.
Страчунского Л. С., Белоусова Ю. Б., Козлова С. Н. М.: 2002, 381.
- Козлов Р. С. Резистентность к антимикробным препаратам как реальная угроза
национальной безопасности /В сб. трудов XV Российского национального конгресса
«Человек и лекарство». 2009, т. 1, с. 225–232.
- Страчунский Л. С., Решедько Г. К. Рекомендации по оптимизации
антимикробной химиотерапии нозокомиальных инфекций, вызванных
грамотрицательными возбудителями в ОРИТ: Пособие для врачей. Смоленск: Богес,
2002.
- Моисеев С. В. Место защищенных аминопенициллинов в лечении внебольничных
инфекций // Клин. фармакол. 2007, т. 16, № 2, с. 33–36.
- Зайцев А. А., Колобанова Е. В., Синопальников А. И. Внебольничные инфекции
дыхательных путей: место защищенных аминопенициллинов // Лечащий Врач. 2008, №
5, с. 75–79.
- Савенкова М. С., Афанасьева А. А., Неижко Л. Ю., Абдуллаев А. К. Опыт
применения амоксициллина/сульбактама (Трифамокса ИБЛ®) у часто болеющих детей
// Антибиотики и химиотер. 2008, т. 53, № 5–6, с. 35–41.
- Савенкова М. С. Значение и место оральных цефалоспоринов III поколения в
педиатрической практике // Consilium Medicum. Приложение к журналу Педиатрия.
2007, т. 10, № 2, с. 62–66.
- Карпов О. И. Макролиды: новая парадигма — фармакодинамика/иммуномодуляция
// Клин. Фармакология и терапия. 2005. № 5. с. 20–23.
- Popa G., Gafitanu E. Oral disintegrating tablets. A new, modern, solid
dosage form // Rev. Med. Chir. Soc. Med. Nat. lasi. 2003, 107: 497–502.
- Мухина М. Ф., Белоусов Ю. Б. Вильпрафен-Солютаб: современный подход к
лечению внебольничной пневмонии // Трудный пациент. 2009, т. 7, № 10, с.
31–34.
- Киселев О. И., Ершов Ф. И., Быков А. Т., Покровский В. И. Пандемия гриппа
2009/10: противовирусная ткрапия и тактика лечения.
Санкт-Петербург–Москва–Сочи. 1010. 65 с.
- Деева Э. Г. Грипп. На пороге пандемии. Руководство для врачей. Изд. «Геотар-Медиа».
2008. 198 с.
- Киселева Н. М., Кузьменко Л. Г. Противовирусные препараты в общей практике
// Лечащий Врач. 2007, № 9, с. 61–64.
- Осидак Л. В., Зарубаев В. В., Образцова Е. В. и др. Изопринозин в терапии
ОРВИ у часто болеющих детей // Детские инфекции. 2008, № 4. с. 35–41.
- Булгакова В. А., Балаболкин И. И., Седова М. С. и др.
Клинико-иммунологическая эффективность применения инозина пранобекс при острых
респираторных инфекциях у детей с атопической бронхиальной астмой //
Педиатрическая фармакология. 2010, т. 7, № 3, с. 98–105.
- Сергеев Ю. В., Малышев А. Ю., Сергеев А. Ю. Изопринозин в терапии больных
атопическим дерматитом // Иммунология, аллергология и инфектология. 1999, № 1,
с. 53–57.
- Маркова Т. П. Применение изопринозина для профилактики повторных
респираторных инфекций у часто болеющих детей // Фарматека. 2009, № 6, с.
46–49.
- Симованьян Э. Н., Денисенко В. Б., Григорян А. В. Часто болеющие дети:
оптимизация программы лечения // Педиатрия. 2007, т. 86, № 3, с. 75–81.
Статья опубликована в журнале
Лечащий Врач

