Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Результаты
хирургического лечения грыж пищеводного отверстия
диафрагмы
Г.А. Журбенко
(jurbiк1@уаndex.by), А.С. Карпицкий (bоb@brеst.by),
С.В. Панько (sppankаm@gmаil.com), А.М. Шестюк (shеstuk@gmаil.com)
УЗ «Брестская областная больница», Брест, Беларусь
Введение. На
фоне традиционно выполняемых фундопликаций в лечении
скользящих диафрагмальных грыж актуальными остаются
вопросы совершествования способов операций,
восстанавливающих острый угол Гиса.
Цель работы: разработать методику
хирургического лечения грыж пищеводного отверстия
диафрагмы, восстанавливающую острый угол Гиса.
Материал и методы. Пациенты (n=74) были
разделены на основную группу (I) (n=45), им
выполнялся разработанный метод операции, и
контрольную (II) (n=29), у 26 пациентов применена
методика Тoupet, у 3 – Nissen. Анкеты GERD-Q и
GERD-HRQL использованы у всех пациентов I-й группы
перед операцией, при выписке и через 6-12, 12-18 и
18-24 месяца после лечения. Пациенты II-й группы
анкетированы через 6-12 месяцев после операции.
Результаты. По результатам анкетирования
через 6-12 месяцев статистически значимой разницы в
группах не выявлено: GERD-Q, p<0,386; GERD-HRQL, p<0,1089.
В основной группе отмечена тенденция к уменьшению
баллов в анкете GERD-Q при сравнении до и после
операции, р<0,0001. Из 16 (55%) пациентов II группы,
госпитализированных после операции, рецидив выявлен
у 9, повторно оперированы 7 пациентов. В I группе
стационарно обследованы 20 (43,3%) пациентов,
рецидив выявлен у 2, операций не было.
Выводы. Эффективность предложенной техники
оперативного лечения грыж пищеводного отверстия
диафрагмы в ранние сроки сравнима с методом Тoupet,
однако при оценке отдалённых результатов
характеризуется меньшим количеством рецидивов.
Ключевые слова: грыжа пищеводного
отверстия диафрагмы, гастроэзофагеальная рефлюксная
болезнь, лапароскопическая фундопликация.
Введение
В настоящее время доказано, что грыжи пищеводного
отверстия диафрагмы (ГПОД) занимают одну из ведущих
позиций в возникновении гастроэзофагеальной
рефлюксной болезни (ГЭРБ) [1]. Возможность такой
взаимосвязи Филип Эллисон рассматривал ещё в
середине XX века [2]. Предпосылками к патологическим
желудочно-пищеводным рефлюксам являются
анатомические особенности пищеводно-желудочного
перехода при наличии скользящей грыжи. При этом
основное внимание отводится расположению так
называемого «кислотного кармана» относительно ножек
пищеводного отверстия диафрагмы (ПОД). В норме
«кислотный карман» находится в фундальной части
желудка, где при антиперистальтических движениях
концентрируется желудочный рефлюктат.
Смещению «кислотного кармана» и дна желудка в
задне-нижнее средостение способствует разрушение
анатомических антирефлюксных механизмов зоны
пищеводно-желудочного перехода (ПЖП). Прежде всего
это развитие диастаза ножек ПОД и растяжение
френоэзофагеальной мембраны, что приводит к смещению
абдоминальной части пищевода в средостение,
деформации зоны угла Гиса, уменьшению объёма дна
желудка [3]. Разрушение анатомического барьера зоны
пищеводно-желудочного перехода является основной
причиной формирования хиатальной грыжи и в конечном
итоге способствует росту количества
гастроэзофагеальных рефлюксов [4]. Таким образом,
расположение «кислотного кармана» и размер ГПОД
тесно связаны друг с другом и будут являться
основными факторами, обуславливающими развитие
патологического желудочно-пищеводного рефлюкса и
клиники ГЭРБ [5].
Суммируя вышесказанное, можно предположить, что
патогенетически обоснованным методом лечения
пациентов с клинически манифестированной ГЭРБ на
фоне ГПОД будет хирургическое вмешательство.
Назначаемая в такой ситуации консервативная терапия
эффективна при условии постоянного и длительного
приёма медикаментозных препаратов, основными из
которых являются ингибиторы протонной помпы (ИПП)
[6]. При несоблюдении указанных условий, отказе от
поддерживающего лечения риск рецидива ГЭРБ в течение
26 недель может достигать 80%, в течение года –
90-95%. Из этого следует обязательная необходимость
в постоянной поддерживающей терапии ГЭРБ или
принятия решения о хирургическом вмешательстве [7,
8, 9].
В рекомендациях Американской ассоциации
эндоскопических хирургов (SAGES) касательно ГПОД в
2010 г. отмечен положительный эффект при выполнении
лапароскопической фундопликации у 85-93% пациентов с
неэффективной медикаментозной терапией (SAGES
Guidelines, 2010) [10]. Основными методиками
оперативных пособий на сегодняшний день, по-прежнему
остаются фундопликации Nissen и Toupet [11].
Наряду с фундопликациями заслуживают внимания
также антирефлюксные операции по формированию
острого угла Гиса [12, 13]. Их отличительной
особенностью в дополнение к основным техническим
требованиям выполнения фундопликаций является
обязательное низведение пищевода в брюшную полость в
зону более высокого внутрибрюшного давления, а также
формирование острого угла Гиса и дна желудка [14].
Цель работы: разработать и предложить
методику хирургического лечения грыж пищеводного
отверстия диафрагмы, восстанавливающую острый угол
Гиса.
Материал и методы
Все пациенты, включённые в исследование (n=74), в
зависимости от выполненной методики антирефлюксной
операции были разделены на две группы: первая –
основная группа (I) (n=45) – пациентам выполнялся
разработанный метод лапароскопической клапанной
эзофагофундорафии, вторая – контрольная группа (II)
(n=29) – 26 пациентов, им применена
лапароскопическая парциальная методика по Тупе (Toupet),
и 3 пациентам – тотальная фундопликация по Ниссену (Nissen).
Пациенты контрольной группы были прооперированы в
период с марта 2009 по апрель 2012 г.
С апреля 2012 г. в клиническую практику внедрена
методика лапароскопической клапанной
эзофагофундопликации, применяемая в основной группе
до мая 2014 г.
Возраст пациентов – от 20 до 81 года. Средний
возраст в первой группе варьировал в пределах
55±14,0 лет, во второй – 50±10,3 года. По гендерному
признаку пациенты разделились следующим образом: в
первой группе было 13 мужчин и 35 женщин, во второй
– 13 мужчин и 16 женщин. Группы были однородными по
полу и возрасту. Формирование групп сравнения
произведено по простым критериям.
Нами предложена методика антирефлюксного
вмешательства – клапанная эзофагофундорафия,
относящаяся к операциям, восстанавливающим острый
угол Гиса. Основной отличительной особенностью
техники оперативного пособия является формирование
антирефлюксного механизма на всю длину низведённого
в брюшную полость и фиксированного при помощи
нити-держалки дистального отдела пищевода.
Вначале по ходу этапа мобилизации на протяжении 5
см от кардии полностью освобождаются передняя и
задняя стенки дна желудка с формированием
ретроэзофагеального пространства (рис. 1).
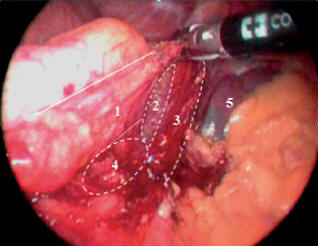
Рис. 1. Мобилизация на уровне левой
диафрагмальной ножки: 1 – пищевод; 2 – зона после
рассечения френоэзофагеальной мембраны слева; 3 –
левая диафрагмальная ножка; 4 – зона сформированного
ретроэзофагеального кармана слева; 5 – селезёнка
После мобилизации правой диафрагмальной ножки и
удаления у всех пациентов ретроэзофагеальной липомы
пищевод берётся на нить-держалку, концы которой
выводятся на переднюю брюшную стенку в левом
подреберье (рис. 2).
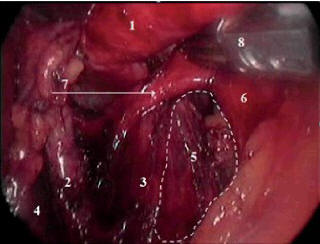
Рис. 2. Завершение этапа мобилизации: 1 –
пищевод; 2 – правая диафрагмальная ножка; 3 – левая
диафрагмальная ножка; 4 – I сегмент печени (pars
facida вскрыта); 5 – правое ретроэзофагеальное
пространство; 6 – задняя стенка желудка; 7 – задняя
ветвь блуждающего нерва; 8 – аппарат «ЛИГАШУ»,
отводящий пищевод
Острый угол Гиса формируется на всю длину
абдоминизированного отдела пищевода. Вначале 3-4
швами острый угол Гиса формируется по задней стенке,
затем 4-5 швами по левой боковой стенке пищевода.
Таким образом, в антирефлюксном механизме участвует
¼ часть окружности пищевода по его заднелевой стенке
(рис. 3).
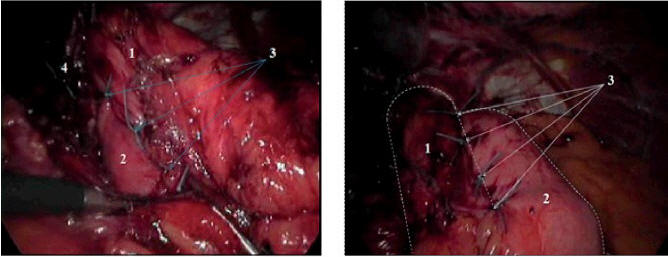
Рис. 3. Окончательный вид сформированного
антирефлюксного механизма: а – по задней стенке
пищевода, 1 – пищевод; 2 – дно желудка, формирующее
угол Гиса по задней стенке пищевода; 3 – швы,
формирующие угол Гиса по задней стенке пищевода; 4 –
ушитые ножки пищеводного отверстия диафрагмы; б – по
левой-боковой стенке пищевода: 1 – пищевод; 2 – дно
желудка, формирующее угол Гиса по левой-боковой
стенке пищевода; 3 – швы, формирующие угол Гиса по
левой-боковой стенке пищевода распределению
(положительный тест W Шапиро-Уилка, p<0,001).
Восстановленное дно желудка в предлагаемом
способе выполняет роль накопительного пространства
для жидкого и газового рефлюктата. Содержимое
желудка при рефлюксе попадает в область дна за счёт
градиента давления между объёмом полости
восстановленного дна и просветом на уровне
пищеводно-желудочного перехода. Антирефлюксный
эффект осуществляется за счёт смещения дупликатуры
стенки дна желудка и пищевода, учавствующей в
формировании угла Гиса (90° заднелевой стенки
пищевода), в сторону просвета пищевода.
Для статистической обработки полученных данных
использовали программу Stats Direct 2.7.2, методы
непараметрической статистики, так как данные не
подчиняются нормальному
Для анализа количественных данных использовали
U-критерий Манна-Уитни, для анализа качественных
показателей использовали таблицы сопряженности и
критерий χ2 (с поправкой Иейтса при степени свободы
υ=1) при значении более 5, при значении менее 5
применяли точный критерий Фишера, для сравнения
нескольких групп – критерий Н Крускала-Уоллиса (p<0,05),
для сравнения результатов до и после лечения
использовали критерий Уилкоксона W (p<0,05), для
выявления связей – коэффициент корреляции Спирмена
(силу связи считали слабой, если r≤0,25, средней – r=0,26–0,75,
сильной – r≥0,76) (Р – сравнение с таблицей
критических значений). Результаты представлены в
виде Me (25; 75).
Данные опросников, выраженные в балльном
эквиваленте, относятся к интервальным шкалам.
Результаты интервальных шкал и шкал соотношения
представлены в виде Ме (25; 75). Для анализа связи
использованы такие показатели непараметрической
статистики, как критерий Манна-Уитни,
Крускала-Уоллиса, Вилкоксона наравне с χ2, критерием
Фишера и построением таблиц сопряженности. Кроме
того, для анализа результатов в шкалах, где
вариантов значений 20 и более, использовали
показатели непараметрической статистики анализа
количественных данных.
Результаты и обсуждение
Для клинической оценки эффективности
хирургического лечения скользящих грыж пищеводного
отверстия диафрагмы использовался диагностический
алгоритм, включающий применение адаптированных
анкет-опросников GERD-Q (gastroesophageal refux
disease-questionaire) [15] и GERD-HRQL (gastroesophageal
refux disease-health-related quality of life) [16].
Анкета GERD-Q включает шесть показателей, каждый из
них оценивается от 0 до 3 баллов: изжога и
регургитация свидетельствуют в пользу диагноза ГЭРБ
(характеристики ГЭРБ по Монреальскому определению),
тошнота и эпигастральная боль – проявления, ставящие
диагноз ГЭРБ под сомнение, нарушение сна и
необходимость в дополнительных медикаментах.
Результатом использования анкеты GERD-HRQL
является определение так называемого индекса «GERD-HRQL».
Это суммарный показатель баллов по 10 строкам
таблицы. Оценка каждого из пунктов проводится от «0»
(лучший показатель, или показатель «здоровье») до
«5» баллов (худший показатель, или «нездоровье»). В
опроснике GERD-Q пограничной суммой баллов для
постановки диагноза ГЭРБ и определения показаний к
операции является «8» и более, соответственно, для
анкеты GERD-HRQL эта сумма баллов составляет больше
«25».
Анкетирование проводилось всем пациентам I-й
группы перед операцией, при выписке из стационара и
в сроки 6-12, 12-18 и 18-24 месяца после
оперативного вмешательства. Пациенты II-й группы
были анкетированы один раз, в сроки от 6 до 12
месяцев. Результаты выполненных операций в обеих
группах оценивались также при помощи
фиброэзофагогастроскопии, полипозиционной
рентгеноскопии пищевода и желудка, суточной
рН-метрии.
При сравнении результатов анкетирования через
6-12 месяцев после оперативного лечения в группе
контроля клинически отмечены жалобы на изжогу у 7
пациентов (24,1%), χ2=9,8, p<0,0003. У пациентов
основной группы при анкетировании за этот же период
времени после операции жалобы на изжогу 1-2 раза в
неделю предъявили 5 (11%) пациентов. Семь пациентов
контрольной группы (24,1%) указали на наличие
отрыжки не чаще 1 раза в неделю, в основной группе
отрыжка беспокоила 10 (22,2%) пациентов 1-2 раза в
неделю. Регургитация, как симптом, встречалась у 4
(13,8%) пациентов контрольной группы и у одного
(2,2%) – основной. Боли в верхней части живота 1-2
раза в неделю беспокоили 5 (17,2 %) пациентов
контрольной и 8 (17,8%) пациентов основной групп.
Жалобы на вздутие в животе также не чаще 2 раз в
неделю предъявили 6 (20,7%) пациентов контрольной и
9 (19,6%) – основной групп, p<0,001.
Среднее значение суммы баллов по всем анкетам
GERD-Q при анкетировании через 6-12 месяцев после
оперативного лечения у пациентов контрольной группы
составило «7» (6:10), в анкетах GERD-HRQL «4»
(1:13,5). У пациентов основной группы анкетирование
проводилось как до операции, так и в сроки от 6 до
12 месяцев после ее выполнения. Перед хирургическим
лечением среднее значение суммы баллов по опросникам
GERD-Q составило «12» (11:14), а по опросникам
GERD-HRQL – «39» (32:44) баллов. После операции
средняя сумма баллов в анкетах GERD-Q была «7»
(5:9), в опросниках GERD-HRQL – «12» (10:12) баллов,
что свидетельствует о статистически достоверном
клиническом эффекте проведенных антирефлюксных
вмешательств. По опроснику GERD-Q статистическая
достоверность p<0,0001, GERD-HRQL – p<0,0001. Однако
при сравнении результатов анкетирования в двух
группах по обоим опросникам за период 6-12 месяцев
после операции статистически значимой разницы в
результатах не выявлено: GERD-Q p<0,386; GERD-HRQL p<0,1089.
По критерию «удовлетворённость качеством жизни» в
конце анкеты GERD-HRQL после операции 19 (65,5%)
пациентов контрольной группы оценили своё
самочувствие как «удовлетворительное», 4 (13,8%) как
«нейтральное», 6 (20,7%) пациентов как
«неудовлетворительное», χ2=8,655172, p<0,0342. Если
сравнивать с основной группой, то 32 (70%) пациента
оценили качество жизни в эти же сроки как
«удовлетворительное», 12 (26%) как «нейтральное» и 2
(4%) как «неудовлетворительное», χ2=45,478261, p<0,0001.
При сравнении результатов лечения в анкете GERD-HRQL
по показателям «удовлетворён», «нейтрально», «не
удовлетворён» качеством жизни за период 6-12 месяцев
после операции выше свое качество жизни оценивали
пациенты основной группы, p<0,0013.
При дальнейшей оценке результатов лечения в
основной группе пациентов, сравнивая суммы
получаемых баллов в обеих анкетах, отмечена
статистически значимая тенденция по уменьшению этой
суммы в опроснике GERD-Q при анкетировании через
6-12 и 18-24 месяца, р<0,0001. При этом в анкете
GERD-Q отмечена четкая положительная корреляция
между результатами сразу после операции и через 6-12
месяцев, коэффициент Спирмена составил R=0,41, р<0,0054
(связь средней силы), при сравнении результатов
через 12-18 и 18-24 месяца также выявлена
положительная корреляция, R=0,46, р<0,01 (связь
средней силы). В результатах анкетирования по
опроснику GERD-HRQL до операции и сразу после ее
завершения корреляции не выявлено, а через 6-12
месяцев получена положительная корреляция, R=0,37, р<0,01
(связь средней силы).
Для проведения контрольного обследования с целью
оценки результатов хирургического лечения в первые 6
лет после операции повторно были госпитализированы
16 (55%) пациентов контрольной группы. При этом у 9
(31%) пациентов клинически выявлен рецидив
рефлюксной болезни. У 5 пациентов рецидив
гастроэзофагеального рефлюкса доказан по результатам
суточной рН метрии. Интегральный показатель De
Mister у них превышал 14,75. У двух пациентов
рецидив ГЭРБ был доказан по результатам
полипозиционной рентгеноскопии пищевода и желудка.
После проведенного комплексного консервативного
лечения длительный положительный эффект получен
только у двух пациентов. Семерым (24%) из девяти
выполнено повторное антирефлюксное вмешательство по
собственной методике. Сроки повторной операции у
шести пациентов колебались от 2,5 до 6 лет. Один
пациент повторно прооперирован через 22 месяца после
первичного вмешательства.
Из основной группы для контрольного обследования
в течение 5 лет после антирефлюксной операции были
госпитализированы 20 (43,4%) пациентов. Клиника
рецидива рефлюксной болезни выявлена у 2 (4,3%)
пациентов. У одного из них рецидив скользящей
диафрагмальной грыжи был заподозрен по результатам
ФЭГДС. Другой пациентке выполнена суточная рН-метрия,
не подтвердившая наличие гастроэзофагеального
рефлюкса (интегральный показатель De Mister равнялся
2,3 при норме ниже 14,75). В обоих случаях получен
удовлетворительный долговременный результат от
проведенной полноценной консервативной терапии, что
не потребовало повторного антирефлюксного
вмешательства.
Выводы
- Анализ хирургического лечения пациентов с
грыжами пищеводного отверстия диафрагмы при
применении традиционных методик и разработанной
клапанной эзофагофундорафии показывает
значительную эффективность антирефлюксных
операций в первые 6-12 месяцев, проявляющуюся
отсутствием основных клинических проявлений ГЭРБ
и улучшением качества жизни.
- Оценка результатов оперативного лечения
данной категории пациентов на более поздних
сроках (5-6 лет после операции) свидетельствует
о рецидивах рефлюксной болезни в контрольной
группе у 31% пациентов и лишь у 4% – в основной
группе. Повторная хирургическая коррекция ГЭРБ
потребовалась, соответственно, в 24% случаев в
контрольной группы и 0% – в основной.
- Восстановление естественного антирефлюксного
барьера в зоне пищеводно-желудочного перехода с
тщательным соблюдением отработанных технических
приёмов предлагаемой операции у пациентов
основной группы позволяет обеспечить
долговременный положительный эффект после
оперативного вмешательства и уменьшить риск
рецидива скользящей диафрагмальной грыжи.
Литература
- The role of the hiatus hernia in
gastro-оesophageal refux disease / C. Gordon [et
al.] // Alimentary Pharmacology & Therapeutics.
– 2004. – Vol. 20, № 7. – Р. 719-732.
- Allison, P. R. Refux esophagitis, sliding
hiatal hernia, and the anatomy of repair / P. R.
Allison // Surgical Gynecology and Obsterics. –
1951. – Vol. 92, № 4. – Р. 419-431.
- Янова, О. Б. Современное понимание
патофизиологических аспектов ГЭРБ и подходы к ее
фармакотерапии / О. Б. Янова // Врач. – 2013. –
№ 3. – С. 23.
- Mehta, S. Prospective trial of laparoscopic
Nissen fundoplication versus proton pump
inhibitor therapy for gastroesophageal refux
disease: Seven-year follov-up / S. Mehta //
Journal of Gastrointestinal Surgery. – 2006. –
Vol. 10, № 9. – P. 1312-1317.
- Effect of azithromycin on acid refux, hiatus
hernia and proximal acid pocket in the
postprandial period / W. O. Rohof [et al.] //
Gut. – 2012. – Vol. 61, № 12. – Р. 1670-1677.
- Степанов, Ю. М. Новые возможности и
перспективы лечения гастроэзофагальной
рефлюксной болезни / Ю. М. Степанов, И. Я.
Будзак, Арби Мохамед // Сучасна
гастроентерологiя. – 2007. – № 6 (38). – С.
30-35.
- Трухманов, А. С. Диагностика и лечение
гастроэзофагеальной рефлюксной болезни / А. С.
Трухманов // Терапевтический архив. – 2011. – №
8. – С. 48-54.
- Medical treatments for the maintenance
therapy of refux oesophagitis and endoscopic
negative refux disease / C. Donnellan [et al.]
// Cochrane Database of Systematic Reviews. –
2004. – Vol. 4. – P. 32-45.
- Non-erosive refux disease - denning the
entity and delineating the management / I. M.
Modlin [et al.] // Digestion. – 2008. – Vol. 78,
№ 1. – P. 1-5.
- Surgical Treatment of Gastroesophageal Refux
Disease / F. Tosato [et al.] // Advances in
Endoscopic Surgery. – 2011. – № 11. – Р.
259-290.
- Kim, D. Surgical Treatment of GERD. Where
Have We Been and Where Are We Going? / D. Kim,
V. Velanovich // Clinical Gastroenterology. –
2014. – Vol. 43. – P. 135-145.
- Лапароскопическая фиксация угла Гиса
ксеноперикардиальной лентой в хирургии
гастроэзофагеальнной рефлюксной болезни / О. А.
Баулина [и др.] // Новости хирургии. – 2014. –
Т. 22, № 2. – С. 164-170.
- Никитенко, А. И. Анализ результатов
эндовидеохи-рургического лечения грыж
пищеводного отверстия диафрагмы / А. И.
Никитенко, А. Г. Родин, В. А. Овчинников //
Эндоскопическая хирургия. – 2012. – № 5. – С.
3-7.
- Опыт оперативного лечения грыж пищеводного
отверстия диафрагмы / А. Г. Родин [и др.] //
Клиническая медицина. – 2012. – № 4. – С. 89-93.
- Jones, R. Development of the GerdQ, a tool
for the diagnosis and management of
gastro-oesophageal refux disease in primary care
/ R. Jones, О. Junghard, J. Dent // Alimentary
Pharmacology & Therapeutics. – 2009. – Vol. 30.
– P. 1030-1038.
- Quality of life scale for gastroesophageal
refux disease / V. Velanovich [et al.] //
Journal American College of Surgeons. – 1996. –
Vol. 183, № 3. – P. 217-224.
References
- Gordon C, Kang JY, Neild PJ, Maxwell JD. The
role of the hiatus hernia in gastro-оesophageal
refux disease. Alimentary Pharmacology &
Therapeutics. 2004;20(7):719-732.
- Allison PR. Refux esophagitis, sliding
hiatal hernia, and the anatomy of repair.
Surgical Gynecology and Obsterics.
1951;92(4):419-431.
- Janova OB. Sovremennoe ponimanie
patofziologicheskih aspektov GJeRB i podhody k
ee farmakoterapii [The modern understanding of
the pathophysiological aspects of GERD and its
approach to pharmacotherapy]. Vrach [Doctor].
2013;3:23. (Russian).
- Mehta S. Prospective trial of laparoscopic
Nissen fundo-plication versus proton pump
inhibitor therapy for gastro-esophageal refux
disease: Seven-year follov-up. Journal of
Gastrointestinal Surgery. 2006;10(9):1312-1317.
- Rohof WO, Bennink RJ, de Ruigh AA, Hirsch DP,
Zwinderman AH, Boeckxstaens GE. Effect of
azithromy-cin on acid refux, hiatus hernia and
proximal acid pocket in the postprandial period.
Gut. 2012;61(12):1670-1677.
- Stepanov JuM, Budzak IJa, Mohamed Arbi.
Novye voz-mozhnosti i perspektivy lechenija
gastrojezofagalnoj refjuksnoj bolezni [The new
possibilities and prospects for treatment of
gastroesophageal refux disease]. Suchasna
gastroenterologija [Modern Gastroenterology].
2007;6(38):30-35. (Russian).
- Truhmanov AS. Diagnostika i lechenie
gastrojezofa-gealnoj refjuksnoj bolezni [Diagnosis
and treatment of gastroesophageal refux disease].
Terapevticheskij arhiv [Therapeutic Archive].
2011;8:48-54. (Russian).
- Donnellan C, Sharma N, Preston C, Moayyedi
P. Medical treatments for the maintenance
therapy of refux oesoph-agitis and endoscopic
negative refux disease. Cochrane Database of
Systematic Reviews. 2004;4:32-45.
- Modlin IM, Hunt RH, Malfertheiner P,
Moayyedi P, Quigley EM, Tytgat GNJ, Tack J,
Holtmann G, Moss SF. Nonerosive refux
disease-denning the entity and delineating the
management. Digestion. 2008;78(1):1-5.
- Tosato F, Marano S, Mattacchione S, Luongo B,
Paltrinieri G, Mingarelli V, Vasapollo L.
Surgical Treatment of Gastroesophageal Refux
Disease. Advances in Endoscopic Surgery.
2011;11:259-290.
- Kim D, Velanovich V. Surgical Treatment of
GERD. Where Have We Been and Where Are We Going?
Clinical Gastroenterology. 2014;43:135-145.
- Baulina OA, Ivachev AS, Baulin VA, Baulin AA,
Krejmer VD. Laparoskopicheskaja fksacija ugla
Gisa ksenoperikardialnoj lentoj v hirurgii
gastrojezofagealnnoj refjuksnoj bolezni [Laparoscopic
fxation of the angle of His with xeno
pericardial ribbon in the surgery of
gas-troesophageal refux disease]. Novosti
Khirurgii [News Surgery]. 2014;2(22):164-170. (Russian).
- Nikitenko AI, Rodin AG, Ovchinnikov VA.
Analiz rezul-tatov jendovideohirurgicheskogo
lechenija gryzh pishhev-odnogo otverstija
diafragmy [The analysis of the results of
endovideo surgical treatment to hernia of the
esophageal opening of the diaphragm].
Jendoskopicheskaja hirurgija [Endoscopic Surgery].
2012;5:3-7. (Russian).
- Rodin AG, Nikitenko AI, Bazaev AV, Domnin MA.
Opytoperativnogo lechenija gryzh pishhevodnogo
otverstija di-afragmy [The experience in
surgical treatment to hernia of the esophageal
opening of the diaphragm]. Klinicheskaja
medicina [Сlinical Medicine]. 2012;4:89-93. (Russian).
15. Jones R, Junghard О, Dent J. Development of
the GerdQ, a tool for the diagnosis and
management of gastro-oesophageal refux disease
in primary care. Alimentary Pharmacology &
Therapeutics. 2009;30:1030-1038. 16. Velanovich
V, Vallance SR, Gusz JR, Apia JV, Habus MA.
Quality of life scale for gastroesophageal
re-fux disease. Journal American College of
Surgeons. 1996;183(3):217-224.
Статья опубликована на сайте
http://www.gastroscan.ru

