Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Оценка иммуномодулирующей активности комбинированных
препаратов с содержанием цинка и эхинацеи
Х. Х. Шарафетдинов, доктор медицинских наук
Т. Б. Сенцова, доктор медицинских наук, профессор
НИИ питания РАМН, Москва
Успехи биохимии, клеточной биологии, геномики, протеомики, метаболомики и
других фундаментальных наук существенно расширили представления о биологической
роли как отдельных макро- и микронутриентов, так и целого ряда минорных
биологически активных компонентов пищи, не только участвующих в регуляции
функциональной активности различных органов и систем, но и играющих важную роль
в снижении риска развития острых и хронических заболеваний.
Общепризнано, что дефицит микронутриентов — витаминов, микроэлементов,
отдельных полиненасыщенных жирных кислот и др. является одной из причин,
приводящих к резкому снижению резистентности организма к неблагоприятным
факторам окружающей среды физической, химической и биологической природы,
нарушению функционирования систем антиоксидантной защиты и развитию
иммунодефицитных состояний. Для большинства населения России характерно резкое,
практически до минимально возможного уровня, снижение энерготрат,
сопровождающееся столь же резким снижением потребности в энергии и, как
следствие, в пище, являющейся единственным источником энергии. В то же время
потребность в других жизненно важных пищевых веществах, в частности в
микронутриентах, существенно изменилась, что является объективной причиной, по
которой современный человек не может получить микронутриенты в необходимых
количествах даже при использовании адекватных рационов из традиционных
натуральных пищевых продуктов [4].
Одной из причин снижения неспецифической резистентности к неблагоприятным
факторам окружающей среды является недостаточная обеспеченность организма
минорными биологически активными компонентами пищи, абсолютно необходимыми для
формирования адекватного иммунного ответа и поддержания адаптационного
потенциала. Снижение неспецифической резистентности организма не только
определяет повышение риска развития таких заболеваний, как сердечно-сосудистые,
онкологические, сахарный диабет 2-го типа, но и сопровождается возрастанием
частоты возникновения простудных заболеваний, особенно в условиях неправильного
питания, при повышенных нервно-эмоциональных нагрузках и т. д.
Биологически активная добавка (БАД) к пище ТераФлю Иммуно применяется в
качестве дополнительного источника витамина C и цинка, а также источника
гидроксикоричных кислот для поддержания иммунитета и профилактики острых
респираторных заболеваний (ОРЗ).
Как известно, аскорбиновая кислота (витамин С) необходима для нормального
течения окислительно-восстановительных процессов в организме, стимулирует
защитные силы, воздействует на факторы иммунной системы, улучшает усвоение
железа. По данным многих авторов, витамин С регулирует иммунологические реакции
(активирует синтез антител, С3-компонента комплемента, интерферона),
способствует активации фагоцитоза, повышает сопротивляемость организма
инфекциям, оказывает противовоспалительное, противоаллергическое и
антиоксидантное действие, а также тормозит высвобождение и ускоряет деградацию
гистамина, угнетает образование простагландинов и других медиаторов воспаления и
анафилаксии [5, 8, 9].
Цинк необходим для нормального роста и полового развития, функционирования
иммунологических реакций, нормального течения процессов заживления, репарации,
биосинтеза белка и нуклеиновых кислот. Цинк участвует в регуляции экспрессии
ряда генов, образовании и созревании Т-клеток, обладает антиоксидантными
свойствами [2, 6, 7, 10].
Эхинацея пурпурная (Echinacea purpurea) — многолетнее растение из семейства
астровые, или сложноцветные (Asteraceae). Эхинацея содержит эфирное масло,
гликозид эхинакозид, гидроксикоричные кислоты, бетаин, инулин, смолу и другие
биологически активные вещества, оказывающие бактерицидное, ранозаживляющее,
повышающее фагоцитарную активность, стимулирующее центральную нервную систему
действие. Эхинацея способствует активации неспецифических факторов защиты
организма и клеточного иммунитета, улучшает обменные процессы, повышает
фагоцитарную активность макрофагов и хемотаксис гранулоцитов, способствует
высвобождению цитокинов, увеличивает продукцию интерлейкина-1 макрофагами,
ускоряет трансформацию В-лимфоцитов в плазматические клетки, усиливает
антителообразование и Т-хелперную активность [5].
Дизайн и методы исследования
Целью проводимых на базе клиники НИИ питания РАМН исследований является
изучение эффективности БАД ТераФлю Иммуно в процессе 3-недельного наблюдения.
Задачами исследования являлись:
- оценка переносимости и безопасности применения БАД ТераФлю Иммуно;
- оценка влияния БАД ТераФлю Иммуно на динамику иммунологических параметров
и показатели качества жизни здоровых добровольцев в процессе 3-недельного
наблюдения.
Рандомизированное, параллельное, контролируемое исследование выполнено на
двух группах условно здоровых людей (основная группа и группа сравнения) по 30
человек в каждой группе.
Участники исследования в основной группе получали БАД ТераФлю Иммуно в
дозировке по 2 пакетика в сутки в течение 3 недель. В группе сравнения
исследуемая БАД к пище не применялась.
В исследование включались добровольцы в соответствии с критериями включения и
исключения из исследования.
Критерии включения:
Возраст участников исследования от 25 до 69 лет.
Отсутствие острых или декомпенсированных хронических заболеваний, требующих
интенсивного лечения, аллергических заболеваний.
Информированное согласие добровольцев на участие в исследовании.
Критериями исключения:
Возраст добровольцев моложе 25 лет и старше 69 лет.
Острые или обострения хронических заболеваний, требующие интенсивной терапии.
Отказ от участия в исследовании.
В процессе 3-недельного наблюдения у всех добровольцев до и после применения
БАД ТераФлю Иммуно, наряду с ежедневной оценкой самочувствия и переносимости
исследуемой БАД, определялось содержание в сыворотке крови IgG, IgA, IgМ, С3, С4
компонентов комплемента методом лазерной нефелометрии на анализаторе с
использованием коммерческих антисывороток той же фирмы.
Исследование концентрации секреторных IgA в слюне проводилось до применения
БАД ТераФлю Иммуно, через 10 и 21 день после ее приема. Секреторные IgA в слюне
определялись методом иммуноферментного анализа (ИФА) с учетом результатов на
спектрофотометре Tecan Sunrise (Австрия) при использовании тест-систем BCM
Diagnostics (США).
Оценка качества жизни проводилась опросным методом (вопросник SF-36) до и
после приема БАД ТераФлю Иммуно. Задавались вопросы, отражающие общее состояние
здоровья, функционирование организма, обусловленное эмоциональным состоянием,
изменение здоровья за последние 3 недели и др.
Результаты исследований и их обсуждение
После завершения рандомизации были составлены основная группа и группа
сравнения по 30 человек в каждой, сопоставимые по возрасту, полу,
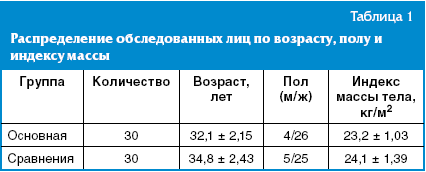
антропометрическим показателям. Данные распределения по возрасту, полу и индексу
массы тела представлены в табл. 1.
Переносимость БАД ТераФлю Иммуно была хорошая у 28 из 30 участвовавших в
исследовании, каких-либо неблагоприятных побочных явлений у них не отмечено,
отказов от приема БАД к пище не было.
У 2 человек, принимавших БАД ТераФлю Иммуно, отмечались диспептические
явления, выражавшиеся в появлении тошноты и неприятных ощущений в области
эпигастрия, которые носили слабо выраженный характер и не потребовали отмена
приема исследуемой БАД к пище.
Следует отметить, что все включенные в исследование лица, принимавшие БАД
ТераФлю Иммуно, отмечали приятный вкус без появления послевкусия.
В процессе 3-недельного наблюдения у обследованных лиц основной группы и
группы сравнения не отмечено возникновения ОРЗ.
Динамика содержания IgG, IgА, IgМ, С3, С4 компонентов комплемента в сыворотке
крови у обследованных лиц основной группы и группы сравнения представлена в
табл. 2.
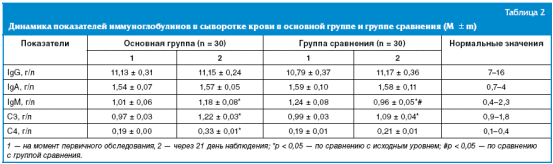
Из табл. 2 следует, что на момент первичного обследования содержание IgG, IgА,
IgМ в сыворотке крови как в основной группе, так и в группе сравнения
определялось в пределах нормы. На фоне приема БАД ТераФлю Иммуно у здоровых
добровольцев, включенных в исследование, отмечено достоверное повышение
содержания IgМ, С3 и С4 компонентов комплементов в сыворотке крови в среднем на
8,5%, 20,5% и 42,4% от исходного уровня соответственно (p < 0,05), тогда как в
группе сравнения содержание IgМ в сыворотке крови снизилось на 22,6% (p < 0,05),
С3 компонент комплемента повысился на 10,1% (p < 0,05). Статистически значимых
изменений в содержании IgG и IgА в сыворотке крови у обследованных лиц в
процессе наблюдения не отмечено. Полученные результаты свидетельствуют об
активации факторов специфического иммунитета за счет повышения содержания IgM в
сыворотке крови и об активации комплементарного бактериолиза, т. е.
сбалансированности противомикробного иммунитета за счет увеличении С3, С4
компонентов комплемента.
Динамика содержания IgА в слюне в основной группе и группе сравнения в
процессе наблюдения представлена в табл. 3.

Из данных табл. 3 следует, что в основной группе на фоне приема БАД ТераФлю
Иммуно через 21 день наблюдения отмечено достоверное повышение содержания
секреторных IgА в слюне в среднем на 18,5% от исходного уровня (p < 0,05), в то
время как в группе сравнения имела место четкая тенденция к снижению содержания
секреторных IgА в слюне относительно исходного уровня. Полученные данные
свидетельствуют об активация местного иммунитета за счет увеличения концентрации
секреторных IgА в слюне.
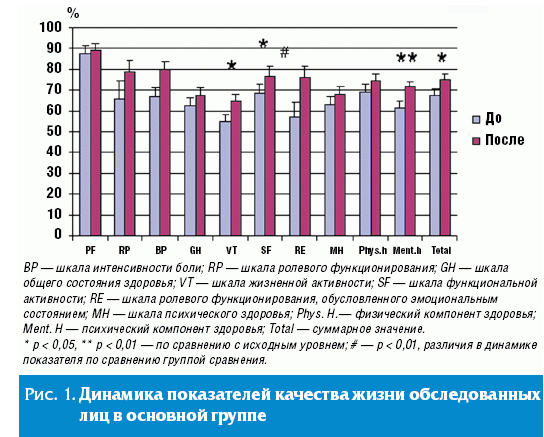
При оценке качества жизни в основной группе (рис. 1) наблюдался достоверный,
статистически значимый прирост уровня качества жизни по шкалам социального
функционирования (SF) (р < 0,05), жизненной активности (VT) (р < 0,05),
психологического компонента здоровья (Ment. H) (р < 0,01), суммарного значения (Total)
(р < 0,05).
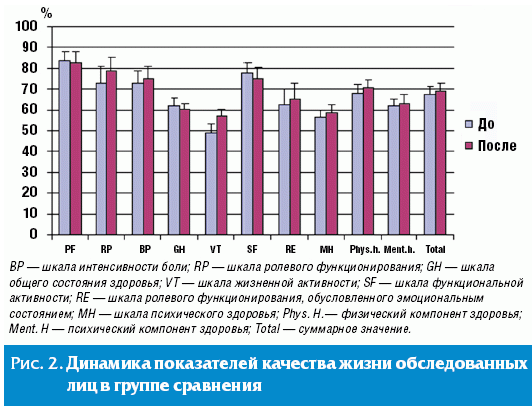
Динамика показателей качества жизни в группе сравнения оказалась менее
выраженной (рис. 2). В отличие от данных, полученных в основной группе, в группе
сравнения не отмечено достоверного повышения показателя по шкале
работоспособности, при этом прирост по шкале
социального функционирования (SF) был достоверно больше относительно такового
в группе сравнения (+11,8% против –4,4%, р < 0,001).
Таким образом, клинические исследования показали выраженный адаптационный и
иммуномодулирующий эффект БАД ТераФлю Иммуно, адаптационный эффект которого
проявлялся в интактности изменений содержания IgG и IgA в сыворотке крови,
иммуномодулирующий эффект — в увеличении содержания С3, С4 компонентов
комплемента и секреторных IgА в слюне.
Выводы
- Проведенное исследование показало удовлетворительную переносимость БАД к
пище ТераФлю Иммуно в дозировке по 2 пакетика в сутки в течение 3 недель;
каких-либо неблагоприятных побочных явлений у включенных в исследование
практически здоровых лиц не отмечено.
- Применение БАД ТераФлю Иммуно приводило к достаточно выраженному
адаптационному и иммуномодулирующому эффекту, проявляющемуся как активацией
факторов специфического иммунитета (за счет повышения содержания IgM в
сыворотке крови на фоне интактности изменений содержания IgG и IgA) и
комплементарного бактериолиза (за счет увеличении С3, С4 компонентов
комплемента в сыворотке крови), так и активацией местного иммунитета (за счет
увеличения концентрации секреторных IgА в слюне).
- Динамика показателей качества жизни здоровых лиц, принимавших ТераФлю
Иммуно, оказалось достоверно лучше (особенно по шкалам социального
функционирования, жизненной активности, психологического компонента здоровья),
чем у лиц группы сравнения.
- Результаты проведенной оценки эффективности БАД ТераФлю Иммуно позволяют
рекомендовать прием в дозировке по 2 пакетика в сутки для формирования
адекватного иммунного ответа и поддержания адаптационного потенциала.
Литература
- ВМА, Хельсинская декларация: Рекомендации для врачей по проведению
биомедицинских исследований с вовлечением человека, 1964 (дополнения 1975,
1983, 1989, 1996 гг.).
- МР 2.3.1.2432–08. Нормы физиологических потребностей в энергии и пищевых
веществах для различных групп населения Российской Федерации.
- МР 2.3.1.1915–04. Рекомендуемые уровни потребления пищевых и биологически
активных веществ. М., 2004. 36 с.
- Лечебное питание: современные подходы к стандартизации диетотерапии / Под
редакцией В. А. Тутельяна, М. Г. Гаппарова, Б. С. Каганова, Х. Х.
Шарафетдинова. 2-е изд., перераб. и доп. М.: Издательство «Династия», 2010.
304 с.
- Регистр лекарственных средств России РЛС. Энциклопедия лекарств. 18-й вып.
/ Гл. ред. Г. Л. Вышковский. М.: РЛС-МЕДИА, 2009. 1296 с.
- Справочник по диетологии / Под ред. В. А. Тутельяна, М. А. Самсонова. М.:
Медицина, 2002.
- Hambidge M. Human zinc deficiency // J. Nutr. 2000. Vol. 130 (5 S
Suppl.). P. 1344 S-1349 S.
- McGregor G. P., Biesalski H. K. Rationale and impact of vitamin C
in clinical nutrition // Curr. Opin. Clin. Nutr. Metab. Care. 2006. Vol. 9. P.
697–703.
- Padayatty S. J., Katz A., Wang Y. et al. Vitamin C as an
Antioxidant: Evaluation of Its Role in Disease Prevention // Journal of the
American College of Nutrition. 2003. Vol. 22. P. 18–35.
- Powell S. R. The antioxidant properties of zinc // J. Nutr. 2000.
Vol. 130 (5S Suppl.). P. 1447 S-14454 S.
Статья опубликована в журнале
Лечащий Врач

