Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Роль непрерывного мониторирования глюкозы в оценке
адекватности инсулинотерапии у детей и подростков с сахарным диабетом 1-го типа
Н. В. Болотова, доктор медицинских наук, профессор
Н. Ю. Филина, кандидат медицинских наук
Л. В. Скучаева
ГБОУ ВПО СГМУ им. В. И. Разумовского Минздравсоцразвития России, Саратов
Сахарный диабет (СД) — синдром хронической гипергликемии, который приводит к
расстройству всех видов обмена веществ и обуславливает развитие поздних
сосудистых осложнений. Целью лечения больных с СД является достижение
максимально возможной компенсации нарушений углеводного обмена [5, 8]. От
степени этих нарушений зависит прогноз заболевания, ранняя инвалидизация и
преждевременная смертность пациентов с диабетом [1, 3]. С внедрением средств
самоконтроля и распространением школ сахарного диабета процент детей с
нормальным уровнем гликированного гемоглобина стал увеличиваться [2, 10]. Однако
у большинства пациентов не удается добиться стойкой компенсации заболевания, что
требует детального анализа причин декомпенсации и поиска средств их устранения
[6]. Новые технологии, пришедшие в диабетологию в последние десятилетия, открыли
возможности долгосрочной оценки колебаний сахара в крови у пациентов с
нарушением углеводного обмена. Одним из таких методов является непрерывное
мониторирование глюкозы при помощи сиcтемы Continuose Glucose Monitoring System
(CGMS) [9]. Эта система позволяет получить детальную информацию о вариабельности
гликемии в течение суток и является примером использования новых технологий в
клинической практике, способных облегчить подбор и коррекцию дозы
сахароснижающей терапии и улучшить качество гликемического контроля [4, 7].
Цель исследования: оценить роль применения системы
мониторирования глюкозы CGMS в достижении компенсации углеводного обмена у детей
с СД 1-го типа.
Пациенты и методы
Обследовано 60 детей с сахарным диабетом 1-го типа, в возрасте от 11 до 15
лет. Оценка степени компенсации углеводного обмена проводилась в соответствии с
критериями ISPAD Clinical Practice Consensus Guidelines 2009.
В зависимости от степени компенсации углеводного обмена все пациенты были
разделены на две группы: 1-я группа — 28 детей с субкомпенсированным диабетом
(HbА1с 7,5–9,0%), средний возраст — 13,57 ± 1,54 года, 2-я группа —
32 пациента с декомпенсированным диабетом (HbА1с > 9,0%), средний
возраст — 13,84 ± 1,35 года. Группы сопоставимы по половому составу и
длительности диабета. Основная часть детей (86,7%) получала многоразовые
инъекции инсулина по интенсифицированной схеме, 8 пациентов (13,3%) осуществляли
введение ультракороткого инсулина посредством инсулиновой помпы.
Для выявления причин декомпенсации углеводного обмена использовали систему
непрерывного мониторирования глюкозы CGMS, фирмы Medtronic Minimed (США). Этот
метод, в сопоставлении с точечными измерениями посредством глюкометра,
обеспечивает информацию о величине, продолжительности, частоте и причинах
изменений глюкозы в крови, позволяя, таким образом, более адекватно осуществлять
контроль за лечением больных СД. Система постоянного мониторирования глюкозы
CGMS дает возможность круглосуточно (288 раз в сутки) контролировать уровни
гликемии, с количественным анализом и графическим представлением полученных
результатов на протяжении 3–4 дней, что позволяет составить четкое представление
о характере метаболизма глюкозы в организме и наметить рациональные пути
лечения. Сенсор системы CGMS фиксируется подкожно, тестирование глюкозы
происходит автоматически в интерстициальной жидкости. Сравнительная оценка
уровня глюкозы проводилась в следующие периоды:
- Период А (08.00–14.00 часов).
- Период В (14.00–17.00 часов).
- Период С (17.00–22.00 часа).
- Период D (22.00–03.00 часа).
- Период E (03.00–06.00 часов).
- Период F (06.00–08.00 часов).
Диапазон для нормогликемии устанавливался от 3,9 до 10 ммоль/л (рекомендации
Shichiri M. с соавт., 2000; Bode B. W. с соавт., 2005), для гипергликемии —
уровень глюкозы более 10 ммоль/л, для гипогликемии — уровень глюкозы менее 3,9
ммоль/л. Проведена оценка препрандиального уровня гликемии, что означало анализ
данных за период в 60 мин до начала приема пищи, зафиксированного монитором.
Оценка постпрандиального периода означала анализ данных за период в 180 мин от
начала приема пищи, зафиксированного монитором.
Статистическая обработка результатов проводилась в операционной системе
Windows 98 с использованием статистической программы XLSTATS version 4,0 (Rodney
Carr, Австралия, 1998). Для расчета достоверности различия количественных
показателей в однородных группах использовался t-критерий Стьюдента, в группах с
неоднородным распределением признака — критерий Манна–Уитни. Для сравнения
распределения качественных показателей в исследуемых группах детей использовался
точный критерий Фишера. Различия считали достоверными при р < 0,05.
Результаты и обсуждение
В данном исследовании проведен анализ причин развития декомпенсации сахарного
диабета 1-го типа у детей на основании изучения гликемии, полученной при
проведении непрерывного мониторирования глюкозы. В качестве одной из причин
декомпенсации рассматривалась длительность диабета, которая составляла от 3
месяцев до 10 лет. При сопоставлении уровня компенсации и длительности болезни
была выявлена корреляционная зависимость между длительностью заболевания
диабетом и уровнем гликированного гемоглобина r = 0,701, р < 0,0001, что
подтверждается и исследованиями других авторов [1, 3]. Медиана продолжительности
заболевания диабетом в 1-й группе составила — 2,5 (2,0; 4,5) года, во 2-й группе
8,0 (6,0; 9,0) лет. Достоверность различий между 1-й и 2-й группами: р = 0,001,
z = 3,004. В группе с субкомпенсированным диабетом длительность заболевания у
21,43% детей составляла от 3 месяцев до 1 года, у 50,00% пациентов — от 1 года
до 5 лет, у 28,57% больных — от 5 до 10 лет. В группе с декомпенсированным СД
увеличивалось количество детей с более длительным стажем заболевания: 68,75%
пациентов с длительностью диабета от 5 до 10 лет, 18,75% детей, заболевших более
10 лет назад, 6,25% больны от 3 месяцев до 1 года и 6,25% с длительностью
диабета от 1 года до 5 лет. Однако у пациентов с небольшим стажем диабета (от 6
месяцев до 1 года и от 1 до 5 лет) отмечалась как компенсация, так и
декомпенсация обменных процессов в различной степени выраженности, что
свидетельствует о наличии других, более важных факторов, вызывающих ее. Различий
по возрастному и половому составу в группах исследования выявлено не было, что
исключает влияние этих факторов на отсутствие компенсации диабета.
Далее проведен анализ результатов суточного мониторирования уровня глюкозы в
обследуемых группах детей с оценкой амплитуды колебаний гликемии в течение
суток, до и после приема пищи, длительности и частоты эпизодов гипо- и
гипергликемий.
По данным CGMS пациенты 1-й группы менее половины времени суток (11,76 часа)
находились в состоянии нормогликемии, более 45% времени суток (11,04 часа) у них
зафиксировано состояние гипергликемии, на долю эпизодов гипогликемии приходилось
5% суток (1,2 часа) (рис. 1).
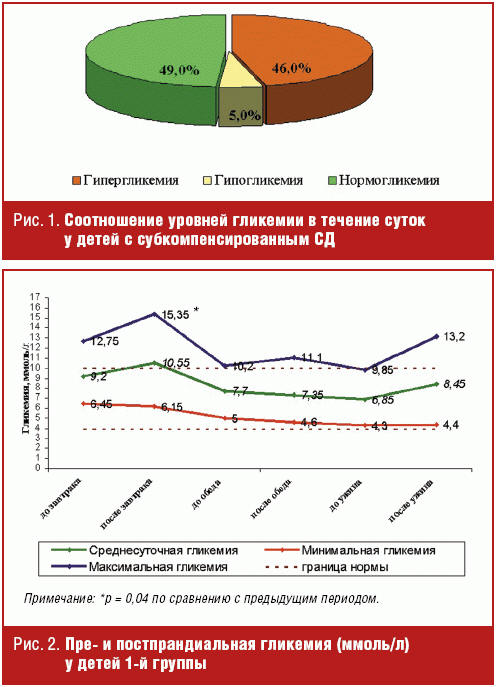
Уровень среднесуточной гликемии у детей 1-й группы не выходил за границу
рекомендуемых целевых показателей (3,9–10,0 ммоль/л), однако максимальная
гликемия резко превышали верхнюю границу. Так, постпрандиальная гликемия после
завтрака у 57,1% превышала 15,0 ммоль/л, что оставалось не выявленным при
обычном 4-кратном контроле.
Средний уровень глюкозы по данным СGMS перед приемами пищи составлял 9,2, 7,7
и 6,85 ммоль/л — перед завтраком, обедом и ужином соответственно. Уровень
глюкозы после приема пищи — 10,55, 7,35 и 8,45 ммоль/л соответственно, что
укладывалось в диапазон целевой посталиментарной гликемии (5,0–11,0 ммоль/л).
Однако у 42,9% детей гликемия в течение 3 часов после завтрака и ужина хотя и не
выходила за границу 11,0 ммоль/л, но не возвращалась к исходным значениям до
приема пищи. Показатели пре- и постпрандиальной гликемии детей с
субкомпенсированным СД по данным непрерывного мониторирования представлены на
рис. 2.
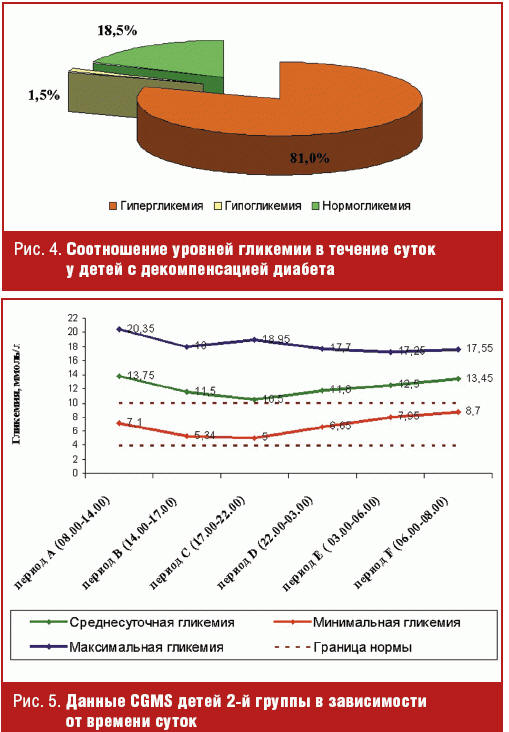
Для более детального представления о состоянии углеводного обмена у детей с
субкомпенсацией были проанализированы данные СGMS в течение суток. Результаты
исследования гликемического профиля детей 1-й группы в эти периоды представлены
на рис. 3.
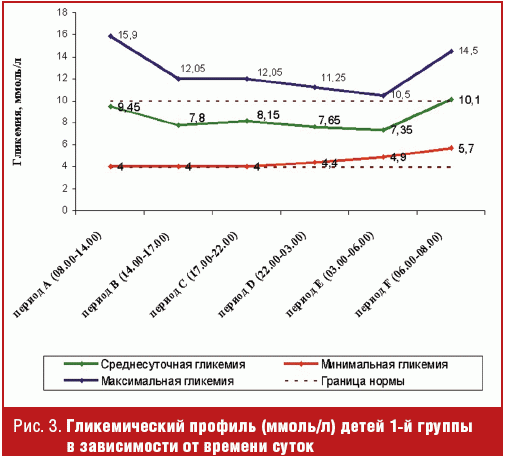
Как свидетельствуют данные CGMS, максимальные показатели гликемии в течение
суток резко превышали рекомендуемый целевой диапазон (3,9–10,0 ммоль/л).
Среднесуточная гликемия была стабильна с 14:00 до 06:00 (периоды В-Е) и имела
небольшую амплитуду колебания от 7,0 до 8,45 ммоль/л, однако с 06:00 до 14:00
(периоды F-A) отмечался подъем гликемии до 10,1 ммоль/л. Максимальные и
минимальные показатели гликемии также повышались в ранние утренние часы и
сохранялись на высоких цифрах до обеденного времени, указывая на наличие
«феномена утренней зари». При индивидуальном анализе кривых СGMS «феномен
утренней зари» выявлен у 32,1% детей, которым требовалось дополнительное
подведение ультракороткого инсулина в предутренние часы.
У 8 пациентов (28,6%) выявлены скрытые ночные гипогликемии, которые являлись
причиной развития последующих эпизодов гипергликемии в 21,4% случаев, что
требовало пересмотра схемы введения ночного базисного инсулина со снижением
дозы.
Таким образом, данные СGMS помогли выявить следующие причины гипергликемии у
детей с субкомпенсированным диабетом: недостаточность дозы ультракороткого
инсулина, вводимого перед основными приемами пищи у 57,1% пациентов; наличие
«феномена утренней зари» у 32,1% детей, что связано с повышенной активностью
контринсулярных гормонов в предутренние часы и возможно обусловлено
особенностями возрастного периода (пре- и пубертат); наличие скрытых ночных
гипогликемий у 28,6% детей.
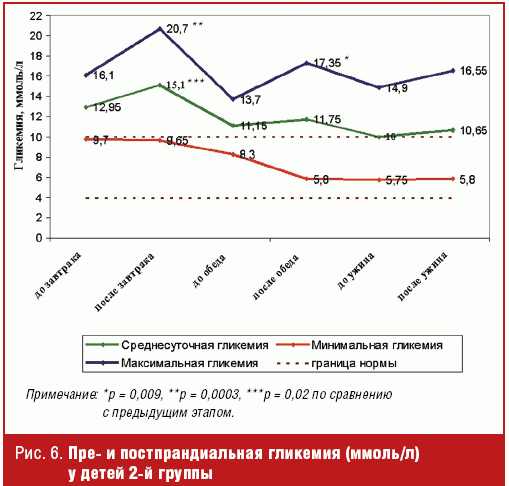
При анализе данных СGMS детей 2-й группы установлено, что более 19 часов (что
составляет 81% от времени суток) они находились в состоянии стойкой
гипергликемии и только незначительное время (4,44 часа) у них отмечалось
состояние нормогликемии. Эпизоды гипогликемии в этой группе встречались редко,
на них приходилось 1,5% времени суток — 0,36 часа (рис. 4).
Данные суточных кривых глюкозы пациентов 2-й группы показывают наличие
гипергликемии в течение всех временных периодов суток, что отличается от данных
пациентов 1-й группы и указывает на выраженный дефицит базисного
(пролонгированного) инсулина (рис. 5).
Среднесуточная гликемия у детей 2-й группы резко превышала рекомендуемый
целевой диапазон (3,9–10,0 ммоль/л). Нарастание гликемии начиналось с вечернего
периода времени (период С), продолжалось в течение всей ночи (периоды D, E, F),
достигая максимума в утренние часы, что подтверждает выраженный дефицит
базисного инсулина как причину декомпенсации диабета у пациентов 2-й группы.
У всех детей данной группы отмечалась гипергликемия натощак и резкое
превышение целевых значений гликемии перед приемами пищи. Средний уровень
глюкозы крови перед едой составлял 12,95, 11,15 и 10,0 ммоль/л перед завтраком,
обедом и ужином соответственно. Уровень посталиментарной гликемии составил 15,1,
11,75 и 10,65 ммоль/л соответственно, что превышало как исходные цифры гликемии
до приема пищи, так и верхнюю границу рекомендуемого целевого диапазона
(5,0–11,0 ммоль/л) (рис. 6).
Как видно из представленной на рис. 6 кривой CGMS, у большинства детей с
декомпенсированным диабетом в течение 3 часов после утреннего приема пищи
отмечалось увеличение средних показателей гликемии с 12,95 до 15,1 ммоль/л,
достоверное (р = 0,009) увеличение максимальных показателей гликемии с 16,1 до
20,7 ммоль/л (р = 0,0003), при этом цифры минимальных показателей гликемии до и
после завтрака практически не отличались: 9,7 и 9,65 ммоль/л. В течение 3 часов
после обеда и ужина средние показатели гликемии превышали целевые и исходные
показатели до приема пищи.
Эти данные свидетельствуют о несоответствии количества вводимого болюсного
инсулина с количеством употребляемых в пищу углеводов, что наряду с дефицитом
базисного инсулина является причиной декомпенсации. «Феномен утренней зари» у
пациентов данной группы не регистрировался, т. к. гипергликемия в утренние часы
сочеталась с гипергликемией в течение всей ночи. Синдром гипогликемии не являлся
причиной декомпенсации диабета у пациентов 2-й группы, а был ее следствием,
поскольку зафиксированные эпизоды снижения гликемии отмечались после введения
корректирующих доз инсулина на гипергликемию и носили редкий характер.
Таким образом, причины отсутствия компенсации диабета у детей с
субкомпенсацией и с декомпенсацией углеводного обмена были различными, что
требовало и различных подходов к проведению коррекции инсулинотерапии.
Основными причинами гипергликемии у детей с субкомпенсированным диабетом
являлись: недостаточность дозы ультракороткого инсулина, вводимого перед
основными приемами пищи у 57,1% пациентов, наличие «феномена утренней зари» у
32,1% детей, наличие скрытых ночных гипогликемий у 28,6% детей.
Причиной декомпенсации углеводного обмена у детей 2-й группы являлся дефицит
инсулина, как болюсного, так и базисного, что требовало пересмотра схемы всей
инсулинотерапии.
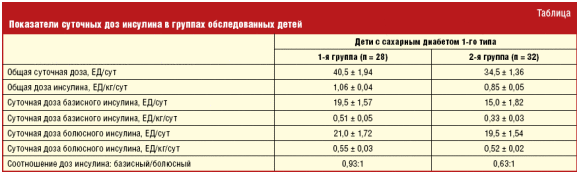
При анализе суточных доз базисного и болюсного инсулина установлено, что у
детей 2-й группы суточная доза как общего, так и базисного инсулина была
значительно ниже аналогичного показателя детей 1-й группы, что подтверждает
дефицит базисного инсулина как причину более выраженной декомпенсации в этой
группе (табл.).
При сопоставлении данных гликемии, полученных глюкометром с данными CGMS,
следует отметить, что 4–5-кратные точечные измерения, которые производит пациент
при обычном самоконтроле, пригодны лишь для поддержания хорошей компенсации
углеводного обмена. В ситуациях, требующих решения вопроса о коррекции
инсулинотерапии, при отсутствии компенсации, точечные измерения не всегда дают
полную информацию о динамике колебаний гликемии и могут, напротив, создавать
ложные представления о гликемии у больного [6]. Например, выявленные в
исследовании ситуации скрытой гипогликемии и «феномен утренней зари» требуют
верификации с помощью системы суточного мониторирования.
Таким образом, использование новых систем непрерывного определения уровня
глюкозы позволяет более детально изучить состояние гликемии в течение суток, что
крайне важно при решении вопроса о тактике изменения дозы инсулина в терапии СД
1-го типа у детей.
Литература
- Андрианова Е. А., Ширяева Т. Ю., Александрова И. И., Сунцов Ю. И.
Оценка степени метаболической компенсации и распространенности диабетических
осложнений в российской популяции детей и подростков (итоги проекта «Скрининг
осложнений сахарного диабета и оценка лечебной помощи больным») // Сахарный
диабет. 2009. № 3. С. 37–42.
- Дедов И. И., Балаболкин М. И. Новые возможности компенсации
сахарного диабета типа 1 и профилактики его сосудистых осложнений. М.:
ИМА-пресс, 2003.
- Дедов И. И., Сунцов Ю. И., Болотская Л. Л. и др. Скрининг
осложнений сахарного диабета как метод оценки лечебно-профилактической помощи
больным // Сахарный диабет. 2006. № 4. С. 38–42.
- Древаль А. В. Лечение сахарного диабета и сопутствующих
заболеваний. М.: Эксмо, 2010. 352 с.
- Мельник А. В., Аметов А. С. Управление сахарным диабетом: роль
постпрандиальной гипергликемии и возможности ее коррекции // Русский
медицинский журнал. 2007. Т. 15. № 27. С. 20–53.
- Boland Elizabeth, Monsod T. and al. Limitations of conventional
metods of self-monitoring of blood glucose: lessons learned from 3 days of
continuous glucose sensing in pediatric patients with type 1 diabetes //
Diabetes Care. 2001, 24: 1858–1862,
- Gross T. M. MastrototaroJ: Efficacy and reliability of the
continuous glucose monitoring system // Diabetes Technol Ther. 2000, 2 (Suppl.
1): 19–26.
- ISPAD and International Diabetes Federation (European Region)/Z. La-ron (ed).
Consensus guidelines for the management of insulin-dependent (Type 1) diabetes
mellitus (IDDM) in childhood and adolescence. Tel Aviv: Freund Publishing
House Ltd., 1995.
- MastrototaroJ: The MiniMed Continuous Glucose Monitoring System (CGMS) (review
Article) // J Pediatr Endocrinol Metab. 1999, 12 (Suppl. 3): 751–758.
- The Diabetes Control and Complications Trial Research Group: The effect of
intensive tritment of diabetes on the development and progression of long-term
complications in insulin = dependent diabetes mellitus // N. Engl J Med. 1993,
329: 977–986.
Статья опубликована в журнале
Лечащий Врач

