
Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Влияние
холецистэктомии на функцию сфинктера Одди
В.А. Ступин,
А.М. Хоконов, Ж.В. Басарболиева, М.А. Хоконов
Проведено проспективное
клинико-инструментальное исследование 119
пациентов с желчнокаменной болезнью (ЖКБ) и 71
пациента с постхолецистэктомическим синдромом (ПХЭС),
перенесших холецистэктомию (ХЭ) 2-45 лет назад.
Установлен полиморфизм клинической картины ПХЭС,
представленной постоянным болевым синдромом
(56,3%) и периодической болью (43,7%) в сочетании
с диспепсическими явлениями и
моторно-эвакуаторными нарушениями, при этом
клинические симптомы в 1,2-3,7 раза чаще
встречались в отдаленном периоде (>14 лет после ХЭ)
вне зависимости от вида перенесенной операции. У
77,5% пациентов с ПХЭС выявлена различная
органическая и функциональная патология ЖКТ, при
этом через год после операции распространенность
патологии ЖКТ составляет 15,1%, через 2-14 –
73,9%, через 15-45 лет – 84,0%. Согласно
манометрическим данным, функциональные
расстройства сфинктера Одди при ПХЭС,
проявляющиеся повышением давления и амплитуды
сокращений сфинктера Одди, а также холедоха и
двенадцатиперстной кишки в наибольшей степени
характерно для пациентов с ПХЭС с пролонгированным
болевым синдромом. Установлено, что спустя 10 и
более лет после исчезновения
резервуарно-накопительной функции желчного
нарастает дисфункция сфинктера Одди, коррелируя с
развитием патологии ЖКТ в отдаленном периоде.
Ключевые слова: сфинктер Одди;
постхолецистэктомический синдром; холецистэктомия;
манометрия.
Введение
Желчнокаменная болезнь (ЖКБ) – одно из самых
частых заболеваний желудочно-кишечного тракта (ЖКТ),
распространенность которого варьирует от 10% до
35% и зависит от пола, возраста, генетических и
средовых факторов [3, 9, 12, 14]. Одним из
наиболее распространенных методов лечения ЖКБ
является холецистэктомия (ХЭ), нередко приводящая
к развитию постхолецистэктомического синдрома (ПХЭС).
ПХЭС – многогранное, сложное и противоречивое
патологическое состояние, представляющее
определенные трудности в диагностике,
характеризуется сохранением симптоматики со
стороны ЖКТ после проведения ХЭ и наблюдается по
данным на фоне структурной или функциональной
аномалии сфинктера разных авторов у 5-90%
пациентов, наиболее частым является болевой
синдром [5, 10, 13].
Потенциальные причины ПХЭС многочисленны. Одной
из них является дисфункция сфинктера Одди (ДСО),
который представляет собой гладкомышечную
структуру, покрывающую и контролирующую
терминальный отдел главного протока поджелудочной
железы и общего желчного протока в месте впадения
в двенадцатиперстную кишку [1, 6]. Частота
развития ДСО после ХЭ достигает 45% [2, 7, 16],
что вызывается новыми физиологическими условиями
функционирования в результате исчезновения
резервуарной функции желчного пузыря, а также
операционной травмы. После ХЭ чаще встречается ДСО
билиарного типа, предполагаемым механизмом которой
является отсутствие резервуара для накопления
объема желчи и обеспечения давления в фазу
сокращения желчных путей [1, 8].
Другой возможной причиной является нарушение
целостности нервов во время ХЭ, обеспечивающих
функционирование сфинктера Одди [4]. При этом
наличие ДСО у пациентов с интактным желчным
пузырем, ставит под сомнение однозначность этой
теории. В 10-20% случаев симптомы билиарной боли
возникали в этой популяции и до проведения
операции [15], что может быть связано с наличием
других нарушений со стороны ЖКТ, таких как синдром
раздражённой кишки и/или неязвенная диспепсия.
Кроме того, у многих пациентов может быть
микролитиаз, который коррелирует с ДСО [1].
Несмотря на внедрение новых хирургических,
фармакологических и физиотерапевтических методов
лечения ДСО, эффективность остается низкой, что
может быть связано с низким применением золотого
стандарта диагностики ДСО – манометрии, для
контроля эффективности терапии, а также с
недостаточно изученным патофизиологическим
механизмом процесса пищеварения у пациентов,
перенесших ХЭ.
Цель: улучшение результатов диагностики
и лечения больных, перенесших холецистэктомию по
поводу ЖКБ, на основании комплексного изучения
влияния операции на функцию сфинктера Одди.
Материал и методы исследования
Проведено проспективное
клинико-инструментальное исследование с включением
190 пациентов с ЖКБ и ПХЭС в возрасте от 20 до 86
лет (средний возраст составил 61,2±13,7 лет,
медиана – 62 года), в том числе 32 мужчин (16,8%)
и 158 женщин (83,2%). У 119 (62,6%) пациентов была
диагностирована ЖКБ, в том числе у 76 (40,0%) –
хронический калькулезный холецистит (ХКХ), 43
(22,6%) – острый калькулезный холецистит (ОКХ); 71
пациент (37,4%) перенес в анамнезе ХЭ по поводу
ЖКБ и имели постоянный или периодический болевой
синдром (группа ПХЭС). На момент включения в
исследование самыми молодыми были пациенты с ОКХ,
старшими – ПХЭС. Пациенты с ЖКБ чаще, чем пациенты
с ПХЭС имели избыточную массу тела, что особенно
было характерно для группы ХКХ (табл. 1).
Таблица 1. Распределение
пациентов с ЖКБ и ПХЭС по полу и возрасту
| |
OKX (n=43)
|
ХКХ (n=76)
|
ПХЭС (n=71)
|
р
|
| Пол: - мужчины - женщины |
5 (11,6%) 38 (88,4%) |
23 (30,3%) 53 (69,7%) |
4 (5,6%) 67 (94,4%) |
<0,05 |
| Возраст |
58,3±14,9, Ме=57 |
56,3±12,5, Ме=60 |
68,1±10,7, Ме=70 |
<0,05 |
| Индекс массы тела |
26,9±2,4, Ме=27 |
28,1±2,5, Ме=28 |
25,6±2,3, Ме=25 |
<0,05 |
100 пациентов с ЖКБ (65 человек с ХКХ и 35 с
ОКХ) были прооперированы. 19 пациентов с ЖКБ,
госпитализированных в плановом порядке, после
дообследования от предложенного оперативного
лечения отказались, им проводилась только
консервативная терапия.
Пациентам с ПХЭС была выполнена открытая или
лапароскопическая холецистэктомия 2-45 лет назад,
в среднем (медиана) 14 лет назад. При этом у 4
(5,6%) пациентов ХЭ была выполнена 2-3 года назад,
12 (16,9%) – 4-9 лет, 30 (42,3%) – 10-14 лет и 25
(35,2%) – 15 и более лет назад. На момент
проведения операции наиболее частым возрастным
диапазоном включенных в исследование пациентов был
50-59 лет, при этом возраст пациентов с ПХЭС на
момент проведения ХЭ был сопоставим с возрастом
больных ЖКБ.
Пациентам чаще всего выполняли
лапароскопическую холецистэктомию (ЛХЭ) – 61,6% (n=117),
в том числе 68,4% при ХКХ, 53,5% при ОКХ, 59,2% в
группе ПХЭС. Открытая ХЭ была выполнена 31 (16,3%
пациенту, в том числе в 4-х случаях группы ЖКБ и
27 (38,0%) в группе ПХЭС. Эндоскопическая
папиллосфинктеротомия (ЭПСТ) была выполнена 4
больным (9,3%) с ОКХ, 1 (1,3%) пациенту из группы
ХКХ, а также ранее ЭПСТ была проведена 2 пациентам
(2,8%) с ПХЭС. Пункцию желчного пузыря проводили 8
пациентам (18,6%) с ОКХ и 8 (10,5%) с ХКХ (табл.
2).
Таблица 2. Распределение
пациентов с ЖКБ и ПХЭС по оперативному лечению
| Хирургическое лечение |
ОКХ
|
ХКХ
|
ПХЭС
|
Всего
|
| ЛХЭ |
23 (53,5%) |
52 (68,4%) |
42 (59,2%) |
117 (61,6%) |
| Открытая ХЭ |
0 |
4 (5,3%)
|
27 (38,0%)
|
31 (16,3%) |
| ЭПСТ |
4 (9,3%)
|
1 (1,3%)
|
2 (2,8%)
|
7 (3,7%)
|
| Пункция желчного пузыря |
8 (18,6%)
|
8 (10,5%)
|
0 |
16 (8,4%)
|
| Не было операции |
8 (18,6%)
|
11 (14,5%)
|
0 |
19 (10,0%)
|
При госпитализации всем пациентам с ОКХ
проводили терапию, соответствующую стандартам
лечения данной категории пациентов в условиях
стационара. Пациенты с ХКХ были направлены
поликлиникой и прооперированы нами в плановом
порядке в первые сутки после поступления.
Пациентам с ПХЭС проводили стандартную терапию
болевого синдрома и причины возникновения ПХЭС.
Оценку состояния пациентов с ПХЭС проводили на
госпитальном этапе, пациентов с ЖКБ – при
госпитализации и выписке, а также через год, на
основе комплексного
клиническо-лабораторно-инструментрального
обследования, включающего: анамнез и жалобы,
анкетирование; клинический осмотр; общий
клинический и биохимический анализ крови;
ультразвуковое исследование (УЗИ) органов брюшной
полости; дуоденоскопию; эндоскопическую манометрию;
по показаниям РПХГ, ЭГДС, колоноскопию.
Манометрия выполнялась следующим образом.
Пациента укладывали на левый бок, левую руку
отводили за спину. Дуоденоскоп вводили до глубины
двенадцатиперстной кишки, к области большого
дуоденального соска, и после аспирации
инсуфлированного ранее воздуха регистрировали
давление в ДПК. После этого катетеризировали
манометрическим катетером большой дуоденальный
сосок и проникали в холедох, где также измеряли
давление и амплитуду сокращения. В следующей
стадии катетер медленно извлекали с шагом 2 мм в 2
минуты и устанавливали в сфинктере Одди и измеряли
в нем давление, а также на каждом порте амплитуду
фазовых сокращений сфинктера (в процессе
извлечения катетера встречалась зона высокого
давления; после того, как все порты катетера
попадут в зону высокого давления, происходит
регистрация давления в течение трёх-пяти минут).
На заключительном этапе катетер извлекали. Когда
порты достигали ДПК, давление падало и повторно
регистрировали дуоденальное давление.
Результаты исследования и их обсуждения
Анализ жалоб установил полиморфизм клинической
картины ПХЭС, которая была представлена постоянным
болевым синдромом (56,3%) и периодической болью
(43,7%) в сочетании с диспепсическими явлениями и
моторно-эвакуаторными нарушениями: ощущением
тяжести (40,9%), тошнотой (39,5%), рвотой (8,5%),
изжогой (26,7%), сухостью/горечью во рту (25,3%),
метеоризмом (22,5%), отрыжкой (19,7%), диареей
(21,1%), запорами (9,9%). Жалобы на боль и
диспепсические явления пациентов с ПХЭС не от вида
перенесенной операции (табл. 3).
Таблица 3. Зависимость жалоб
и диспепсических явлений у пациентов с ПХЭС от
давности и вида операции, от патологии ЖКТ
| |
Периодическая боль
|
Постоянная боль
|
Всего
|
| N (%) |
31 (43,7%)
|
40 (56,3%)
|
71 (100%)
|
|
Давность операции (р=0,468) |
| 2-3 лет |
3 (9,7%)
|
1 (2,5%)
|
4 (5,6%)
|
| 4-9 лет |
6 (19,4%)
|
6 (15,0%)
|
12 (16,9%)
|
| 10-14 лет |
12 (38,7%)
|
18 (45%)
|
30 (42,3%)
|
| 15-45 лет |
10 (32,2%)
|
15 (37,5%)
|
25 (35,2%)
|
| В среднем |
14,4±5,0; Ме=14
|
15,1±8,9; Ме=14
|
>0,05 |
|
Вид операции (р=0,707) |
| открытая ХЭ |
14 (45,2%)
|
13 (32,5%)
|
27 (38,0%)
|
| ЛХЭ |
15 (48,4%)
|
27 (67,5%)
|
42 (59,2%)
|
| ЭПСТ |
2 (6,5%)
|
0 |
2 (2,8%)
|
Клинические симптомы в 1,22-3,67 раза чаще
встречались в отдаленном периоде (>14 лет после ХЭ)
вне зависимости от вида перенесенной операции
(рис. 1).
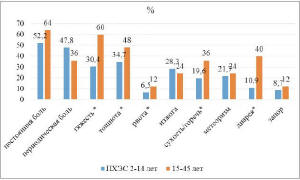
Рис. 1. Клиническая картина ПХЭС у
пациентов, оперированных в разные сроки (* –
межгрупповое различие при р<0,05; критерий х2)
Результаты интервью показали, что лишь 4 (5,6%)
пациента с ПХЭС строго соблюдали диету, 44 (62,0%)
старались соблюдать предписанный пищевой режим, 23
(32,4%) диету не соблюдали и их пищевой режим не
изменился после ХЭ. К последним в большинстве
случаев относились пациенты с ожирением I-III
степени.
Анализ жалоб пациентов с ЖКБ в дооперационном
периоде установил болевой синдром у 83,2%
пациентов (у 100% больных с ОКХ и 73,7% больных с
ХКХ). При ОКХ боль чаще носила постоянный характер
(79,1%), при ХКХ – периодический (80,4%; p<0,05).
Локализация и иррадиация боли были сопоставимы в
группах ОКХ и ХКХ, чаще боли локализовались в
правом подреберье (27,7%) и эпигастрии (28,6%).
Через год у пациентов с ЖКБ клинические
проявления наблюдались у 18,5% пациентов, чаще у
неоперированных больных (57,9%) и после пункции
желчного пузыря (43,8%), реже после ЭПСТ (20,0%),
ЛХЭ (4,0%), из 4-х больных, перенесших открытую ХЭ,
никто жалоб через год не предъявлял (p<0,05).
Таким образом, частота встречаемости ПХЭС через
год после ХЭ составила 6,8%.
Следовательно, нарушение процесса пищеварения
актуально не только для больных с конкрементами в
желчном пузыре, но и для прооперированных по этому
поводу пациентов, что в большей степени
проявляется спустя 14 лет после операции, причем
частота болевого синдрома и диспептических явлений
сопоставима с показателями у неоперированных
больных.
Одновременно с этим, частота органической
патологии прогрессировала пропорционально времени,
прошедшему после ХЭ. Так, данные инструментальных
и лабораторных исследований позволили установить,
что органическая и функциональная патология ЖКТ
встречалась у 77,5% пациентов с ПХЭС:
рецидивирующий панкреатит (29,6%), папиллит
(19,7%), антральный рефлюкс-гастрит (14,1%),
парафатеральный дивертикул (8,5%), холедохолитиаз
(7,0%), желчный энтероколит (7,0%), стеноз БДС
(4,2%), полип БДС (4,2%), цирроз печени (1,4%),
рак желудка (1,4%), рак печени (1,4%), рак
ободочной кишки (1,4%). Через год после операции
распространенность патологии ЖКТ составила 15,1%,
через 2-14 – 73,9%, через 15-45 лет – 84,0%.
Значимо больше патологии ЖКТ было выявлено у
пациентов, перенесших ХЭ более 14 лет назад, у
которых панкреатит был выявлен в 2,03 раза чаще,
желчный энтероколит в 2,79 раза чаще, антральный
рефлюкс эзофагит в 2,76 раза чаще, парафатеральный
дивертикул в 1,85 раза чаще, чем у пациентов,
оперированных 2-14 лет назад (p<0,05). Цирроз
печени и онкология выявлены у больных,
оперированных 15-45 лет назад (рис. 2).
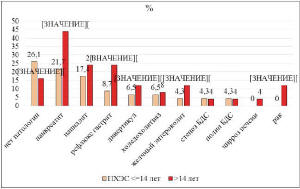
Рис. 2. Распространенность патологии ЖКТ у
пациентов, перенесших ХЭ в разные сроки давности
(* – межгруппое различие при р<0,05)
Анализ проводимого ранее специализированного
лечения установил, что 45,1% (n=32) пациентов с
ПХЭС в течение последнего года были
госпитализированы, включая 24 (33,8%) человек,
которые госпитализировались по поводу болей в
животе. Из них 9 человек (12,7%) были
госпитализированы с диагнозом ПХЭС, острый
панкреатит, 7 человек (9,9%) – с диагнозом при
выписке «острый гастродуоденит», 4 человека (5,6%)
– «синдром раздраженного кишечника», 2 человека
(2,8%) – «почечная колика», 2 (2,8%) – «язва
желудка». Кроме этого, с болями в животе постоянно
амбулаторно наблюдались в институте
гастроэнтерологии 5 (7,0%) пациентов, из которых 2
человека наблюдались по поводу
постхолецстэктомического рецидивирующего
панкреатита, 1 – по поводу антрального рефлюкс
гастрита, 1 – желчного энтероколита, 1 – стеноза
БДС.
Важно отметить, что в течении года до момента
настоящей госпитализации лечение проводилось у 35
(49,3%) пациентов с ПХЭС. Чаще всего пациенты
принимали спазмолитики (n=20; 28,1%), ингибиторы
протоновой помпы (напр., омез) (n=10; 14,1%) и
ферментные препараты (напр., мезим) (n=14; 19,7%).
При этом 17 (23,9%) пациентов с ПХЭС постоянно
принимали фармакологические препараты, а 18
(25,4%) человек лечились периодически курсами (1-3
раза в год) и для купирования боли и
диспептических явлений. Проводимое лечение не было
эффективно в большинстве случаев, что связано в
том числе с ошибками диагностики (рис. 3).
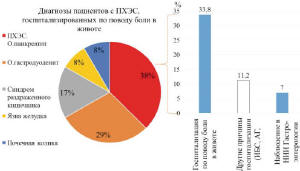
Рис. 3. Госпитализация пациентов с ПХЭС за
последний год
Проведенное нами комплексное обследование,
включающее данные УЗИ брюшной полости,
дуоденоскопии, ЭГДС и т.д, не выявило большинство
диагнозов, указанных в выписках.
У пациентов с ЖКБ наиболее часто был
диагностирован полип БДС (у 8 (10,5%) пациентов с
ХКХ и у 4 (9,3%) пациентов с ОКХ), другие виды
патологии встречались у 11 (9,2%) больных:
парафатеральный дивертикул (n=3; 2,5%; 1 при ОКХ и
2 при ХКХ), стеноз БДС (n=5; 4,2%; 4 при ОКХ и 1
при ХКХ), папиллит (n=3; 2,5%). Отсутствие
органической патологии ЖКТ при госпитализации
пациентов с ЖКБ было в 96 (80,7%) случаев. Через
12 месяцев у 18 (15,1%) пациентов была выявлена
патология ЖКТ. Панкреатит был диагностирован у 2
(1,7%) пациентов, папиллит – у 3 (2,5%),
парафатеральный дивертикул – у 3 (2,5%), полип БДС
– у 10 (8,4%).
Распространенность органической и
функциональной патологии ЖКТ через 2-14 лет после
ХЭ в 3,83 раза больше, а через 15-45 лет – в 4,35
раза больше, чем при ЖКБ в дооперационном периоде
(р<0,05). Распространенность патологии ЖКТ в 4,89
раза больше через 2-14 лет после ХЭ, в 5,56 раза
больше через 15-45 лет по сравнению с
распространенностью органической и функциональной
патологии ЖКТ через год после ХЭ (рис. 4).
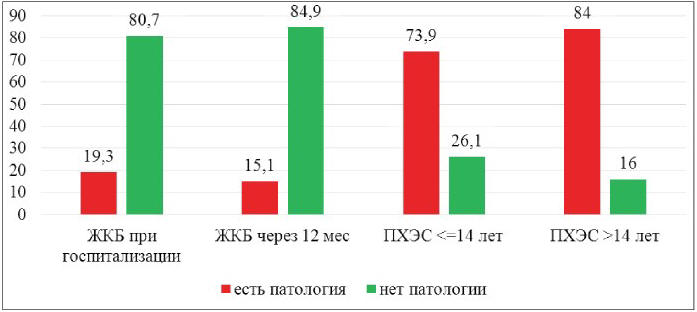
Рис. 4. Патология ЖКТ в динамике (%)
Влияние ХЭ на функцию сфинктера Одди изучали с
помощью эндоскопической манометрии, выполненной в
динамике.
Анализ манометрических показателей установил,
что при ПХЭС выше нормы среднее давление в
холедохе в 1,24 раза, среднее давление в сфинктере
Одди в 1,71 раза при стабильных амплитудах
сокращений сфинктера, холедоха, ДПК и давлении в
ДПК. У пациентов с ЖКБ значимо повышены среднее
давление в холедохе в 2,13 раза, давление в
сфинктере Одди в 1,63 раза, амплитуда сокращений
сфинктера в 1,21 раза и давление в ДПК в 2,90 раза
относительно нормы; максимальные изменения
моторно-эвакуаторных функций зарегистрировано при
ОКХ (табл. 4).
Таблица 4. Манометрические
показатели функционального состояния сфинктера
Одди у пациентов с ЖКБ, ПХЭС по сравнению с нормой
Отдел ЖКТ
|
Показатель |
Норма
(n=20)
|
ЖКБ
(n=107)
|
пхэс
(n=37)
|
р (жкб/
пхэс) |
| ДПК |
Среднее давление, мм вод. ст. |
7,9
5,5/8,7
[1,1-10,0] |
22,9 *
8,1/42,9
[3,3-101,8] |
9,0-
6,8/20,1
[0,5-45,0] |
0,005 |
| Холедох |
Среднее давление, мм вод. ст. |
16,4
12,7/20,0
[5-23] |
35,0 *
19,9/70,1
[4,7-134] |
20,3 *
17,2/34,0
[8,2-56] |
0,012 |
| Сфинктер Одди |
Среднее давление, мм вод. ст. |
28,4
25,5/32,5
[14,3-37,8] |
46,4 *
28,7/71,2
[14,6-169,9] |
48,5 *
31,1/59,9
[7,3-88,0] |
>0,05
0,392 |
Средняя амплитуда
сокращений,
мм вод. ст |
62,5
43,1/87,5
[30,2-109,8] |
75,6 *
46,3/125,6
[33,3-272,3] |
72,1
56,1/81,8
[9,3-95,1] |
>0,05
0,145 |
Результаты представлены в
виде медианы (первая строка), 25%/75%
квартилей (вторая строка) 95% –
доверительного интервала (третья строка).
* – достоверное отличие от нормы при p<0,05
(критерий Манна-Уитни). |
Таким образом, наибольший дисбаланс
манометрических показателей был у пациентов с ЖКБ
на 1-е сутки исследования. Однако полученные
данные говорят о том, что выполненная в среднем 14
лет назад холецистэктомия не нормализовала
физиологические показатели давления в сфинктере
Одди и в холедохе, патологический процесс
билиарного дерева у пациентов с ПХЭС продолжает
развиваться длительное время, хотя и в меньшей
степени, чем при обострении холецистита.
Наличие конкрементов в желчном пузыре и
связанный с этим отек и воспалительные явления
рефлекторно повышали давление в сфинктере Одди,
общем желчном протоке и даже в ДПК. Последнее
может быть связано со свойственным пациентам с ЖКБ
лишним весом, что увеличивает не только
внутрибрюшное давление, но и давление в кишечнике.
Гипертония СО, холедоха и ДПК является
неотъемлемой частью нарушения желчеоттока и
сопровождается болевым синдромом и диспептическими
явлениями.
Анализ манометрических показателей у пациентов
с острым и хроническим калькулезным холециститом
установил, что наибольшее изменения были при ОКХ,
при котором было зарегистрированы максимальные
цифры давления и амплитуды сокращений холедоха,
сфинктера Одди и наибольшая амплитуда сокращений
ДПК на фоне повышенного давления в ДПК. Это
связано с наибольшей выраженностью отека и
воспалительных явлений при ОКХ. На втором месте по
степени изменения манометрических показателей были
пациенты с ХКХ. Однако такие показатели как
среднее давление в сфинктере Одди, амплитуда
сокращений сфинктера, а также среднее давление и
амплитуда сокращений ДПК, были сопоставимы с
данными пациентов с ОКХ; статистически значимое
отличие состояло в более высоких показателях
среднего давления и амплитуды сокращений в
холедохе (на 59% и 42% соответственно), а также
показателя диапазона амплитуды сокращений
сфинктера Одди (на 39%) у пациентов с ОКХ по
сравнению с пациентами с ХКХ. Полученные
существенные различия желчеоттока у пациентов с
острым и хроническим холециститом могут служить
основанием для тактики дальнейшего лечения.
Несмотря на то, что степень изменения
показателей манометрии у пациентов с ПХЭС была
наименьшей, такие показатели как среднее и
базальное давление в сфинктере Одди, минимальная
амплитуда сокращения сфинктера у пациентов с
хроническим холециститом и ПХЭС не отличались
(рис. 5).
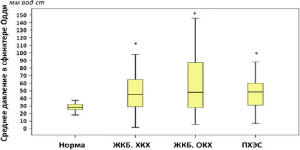
Рис. 5. Среднее давление в сфинктере Одди у
пациентов разных групп (* – достоверное отличие от
нормы при p<0,05; критерий Манна-Уитни)
Анализ показателей манометрии у пациентов с
ПХЭС, предъявляющих жалобы на постоянный и
периодически болевой синдром и диспепсические
явления, показал, что постоянный болевой синдром и
диспепсия у пациентов с ПХЭС сопровождается
повышением давления в сфинктере Одди, холедохе и
ДПК, а также повышением амплитуды сокращения
сфинктера Одди, что говорит о постоянных
функциональных расстройствах сфинктера, приводящих
к стабильному и пролонгированному нарушенному
пищеварению. Периодически возникающая клиническая
картина ПХЭС в большинстве случаев не
сопровождалась изменением давления в путях тока
желчи (рис. 6-7).
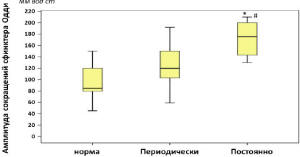
Рис. 6. Амплитуда сокращений в сфинктере
Одди у пациентов с ПХЭС, предъявляющих жалобы на
постоянные и периодические боли (* – достоверное
отличие от нормы при p<0,05; # – межгрупповое
различие при p<0,05 групп пациентов с ПХЭС;
критерий Манна-Уитни)
Анализ манометрических показателей,
определяемых при госпитализации и при выписке
пациентов с ЖКБ, осуществляемой на 9-16 сутки
(12,2±2,3 сут) показал, что включившиеся механизмы
адаптации нормализовали давление в сфинктере Одди,
улучшился уровень давления в холедохе в
большинстве случаев, хотя и полностью не
нормализовался. Впрочем, это трудно было бы
ожидать, принимая во внимание исчезновение
накопительной функции желчного пузыря у
оперированных пациентов. У не оперированных
больных при купировании острого приступа также
наступало улучшение показателей, однако это
улучшение было хуже, чем после ХЭ.
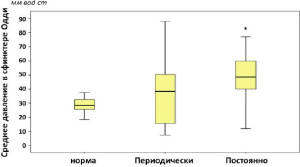
Рис. 7. Среднее давление в сфинктере Одди у
пациентов с ПХЭС, предъявляющих жалобы на
постоянные и периодические боли (* – достоверное
отличие от нормы при p<0,05; критерий Манна-Уитни)
Это свидетельствует об
приспособительно-компенсаторных изменениях ЖКТ к
ЖКБ, и связанных с этим изменениями пищеварения,
которые не всегда могут быть ликвидированы в
короткие сроки после операции или после
нивелирования приступа обострения болезни.
Оценка динамики показателей эндоскопической
манометрии показала, что давление и амплитуда
сокращений сфинктера Одди, холедоха и ДПК
нормализовались через год после ХЭ и сохранялись
на относительно стабильном уровне в течении 10
лет.
Спустя 10 и более лет после исчезновения
резервуарно-накопительной функции желчного пузыря
декомпенсировалась адаптативная функция сфинктера
Одди, нарастала его дисфункция и гипертензия
сфинктера Одди, холедоха и ДПК (табл. 5),
коррелируя с развитием патологии ЖКТ в отдаленном
периоде.
Таблица 5. Динамика
манометрических показателей
Отдел ЖКТ
|
Показатель
|
ЖКБ
1 сут
|
ЖКБ
при выписке
|
ЖКБ
через год
|
ПХЭС
2-10 лет
|
ПХЭС
11-45 лет |
| ДПК |
Среднее давление, мм вод. ст. |
29,3 *
12,3/55,7 |
15,5 *
7,0/60,5
# |
8,2
5,8/9,3
# |
7,5
6,9/9,1
# |
16,4 *
5,1/34,2
# |
| |
Амплитуда сокращений, мм вод. ст. |
28,4 *
11,0/47,3 |
36,9 *
15,7/80,9 |
14,4
10,9/17,3
# |
13,2
11,2/14,5
# |
20,4
4,7/25,1 |
| Холедох |
Среднее давление, мм вод. ст. |
35,0 *
19,9/70,1 |
33,3 *
20,5/59,2 |
17,1
15,1/20,5
# |
16,5
15,9/19,1
# |
30,2 *
22,9/40,1 |
| |
Амплитуда сокращений, мм вод. ст. |
59,9 *
24,3/85,7 |
44,4 *
24,9/75,8 |
25,8
20,4/29,1
# |
22,3
21,1/27,4
# |
35,3 *
28,9/46,3
# |
Сфинктер
Одди |
Среднее давление, мм вод. ст. |
46,4 *
28,7/71,2 |
40,1
34,5/90,2 |
38,9
25,9/51,4 |
42,2
38,2/50,3 |
49,1 *
24,1/77,3 |
| |
Амплитуда сокращений, мм вод. ст. |
75,6 *
46,3/125,6 |
86,2 *
40,1/137,5 |
65,1
43,9/89,4 |
60,4
56,2/81,8 |
79,1
60,5/87,1 |
| * – отличие показателя от
нормы при р<0,05; # – отличие от показателя
при ЖКБ на 1 сутки при р<0,05. |
Таким образом, несмотря на наличие позитивной
тенденции в динамике манометрических показателей,
выписываются пациенты с ЖКБ с выраженной
дисфункцией сфинктера Одди и со значимой
гипертонией исследуемых нами отделов ЖКТ.
Нормализация амплитуды сокращений и давления в ДПК,
холедоха и сфинктере Одди наступила через год
после холецистэк-томии и сохранялась до 10 лет (у
пациентов с ПХЭС). Дисфункция, гипертензия
сфинктера Одди, в большинстве случаев
характеризующая стеноз и спазм сфинктера,
формировалась у трети больных, перенесших ХЭ, при
этом ее формирование происходит в отдаленном
периоде, что говорит о смене адаптативных
механизмов на декампенсаторные в отдаленном
периоде.
Несмотря на проведенные профилактические меры,
развились осложнения манометрии, проводимой при
первой госпитализации. Панкреатит развился у 3,0%,
гиперамилаземия – у 7,6% человек. Осложнения были
успешно устранены консервативным путем в течении
2-7 дней.
Анализ жалоб, лабораторных и инструментальных
исследований позволил разделить пациентов по типу
дисфункции сфинктера Одди на билиарный и
панкреатический типы. К билиарному типу мы отнесли
пациентов, имеющих типичные билиарные боли,
локализованные в правом подреберье с/без
иррадиацией в эпигастрий, у которых повышены АлАт,
АсАт, а также пациентов с расширенным желчным
протоком. К панкреатическому типу были отнесены
больные с рецидивирующим панкреатитом, жалующиеся
на боль опоясывающего или диффузного характера, в
т.ч. с иррадиацией в спину, а также имеющие
повышенный уровень амилазы крови. Отсутствие
жалоб, органической патологии, повышения ферментов
печени и амилазы при отсутствии изменений
манометрических и других инструментальных данных
свидетельствовало об отсутствии дисфункции
сфинктера Одди после ХЭ. Установлено, что в 78,4%
диагностирована ДСО. Биллиарный тип дисфункции
зарегистрирован у 34,7% пациентов, панкреатический
– у 43,7%.
Заключение
Проведенное исследование продемонстрировало
актуальную эпидемиологическую ситуацию ПХЭС и
дисфункции сфинктера Одди, приводящую к патологии
ЖКТ, нарастающей в отдаленном послеоперационном
периоде. Поэтому целесообразно проводить
пристальное диспансерное наблюдение за пациентами
с ЖКБ в течении первого года после операции и
после консервативного купирования обострения
калькулезного холецистита, а также за пациентами с
ПХЭС. Вследствие высокого процента функциональной
и органической патологии ЖКБ в отдаленном периоде
после ХЭ, следует внимательно относиться к
показаниям к оперативному лечению пациентов без
клинической картины ЖКБ, у которых камни в желчном
пузыре найдены случайно.
Учитывая максимальную диагностическую ценность
эндоскопической манометрии относительно
функционирования путей желчеооттока и дисфункции
сфинктера Одди, манометрию необходимо проводить
совместно с дуоденоскопией в динамике всем
пациентам с ПХЭС (при отсутствии
противопоказаний), в том числе, для оценки
динамики течения, эффективности лечения и
прогноза.
При выявлении функциональных расстройств
сфинктера Одди, сопровождающихся клинической
картиной ПХЭС, особенно постоянным болевым
синдромом и симптомами нарушенного пищеварения,
целесообразна плановая госпитализация с целью
комплексного обследования и своевременного лечения
пациентов, перенесших ХЭ. При этом необходимо
выполнять не только стандартные методы диагностики
(УЗИ органов брюшной полости, общий и
биохимический анализ крови), но и дуоденоскопию в
сочетании с манометрией, а также другие методы
диагностики, соответствующие клинической картине
(например, колоноскопию пациентам с нарушением
стула для своевременного выявления и лечения рака
ободочной кишки, развивающегося вследствие ДСО и
бесконтрольного тока желчи, являющейся агрессивной
средой для толстого кишечника при отсутствии
поступающих с пищей жирных кислот; ЭГДС с целью
своевременного выявления и лечения рака желудка,
развивающегося на фоне ДСО и связанного с этим
рефлюкс гастритом).
Список литературы
- Басарболиева Ж.В., Ступин В.А., Кобесов
Н.В. Оптимизация лечебно-диагностического
алгоритма у больных с постхолецистэктомическим
синдромом. Справочник врача общей практики.
2015. № 2. С. 22-30.
- Винник Ю.С., Серова Е.В. Значение
холецистокинина октапептида в развитии
дисфункции сфинктера Одди неорганической
этиологии после холецистэктомии у пациентов,
оперированных по поводу калькулёзного
холецистита. Пермский медицинский журнал,
2013. Т. 30. №5. С. 78-85.
- Дорофеенков М.Е. Факторы риска,
особенности клинического течения и
распространенность желчнокаменной болезни у
лиц пожилого и старческого возраста в Москве.
Клиническая геронтология. 2013. Т. 19, № 3-4.
С. 30-35.
- Звягинцева Т.А., Гриднева С.В. Механизмы
развития и подходы к лечению дисфункции
сфинктера Одди после холецистэктомии.
Гастроэнтерология. 2014. Т. 52. № 2. С. 77-81.
- Кучерявый Ю.А. Состояние после
холецистэктомии: взгляд гастроэнтеролога.
Медицинский совет. 2013. № 6. С. 39-44.
- Левин М.Д., Мендельсон Г., Коршун З.
Сфинктер Одди и его роль в патогенезе
заболеваний желчно-панкреатической зоны.
Новости хирургии. 2011. Т. 19. № 6. С.
139-145.
- Леонтьев А.С., Короткевич А.Г., Репникова
Р.В. и др. Оценка влияния оперативного доступа
на структуру и частоту отдаленных осложнений
холецистэктомии. Медицина в Кузбассе. 2014. №
1. С. 32-36.
- Панцырев Ю.М., Шаповальянц С.Г.,
Чернякевич С.А. Функциональные расстройства
сфинктера Одди после холецистэктомии.
Российский журнал гастроэнтерологии,
гепатологии, колопроктологии. 2011. Т. 21. №
3. С. 28-34.
- Тонких Ю.Л., Бронникова Е.П., Цуканов В.В.
Распространенность и факторы риска заболеваний
желчевыводящих путей у коренных жителей Тывы.
Здравоохранение Российской Федерации. 2014. Т.
58. № 5. С. 42-45.
- Чарышкин А.Л., Бадеян В.А., Бикбаева К.И.
Результаты холецистэктомии в отдаленном
послеоперационном периоде. Сибирский
медицинский журнал. – Иркутск. 2011. Т. 107. №
8. С. 32-34.
- Elmi F., Silverman W.B. Biliary sphincter
of Oddi dysfunction type I versus occult
biliary microlithiasis in postcholecystectomy
patients: are they both part of the same
clinical entity? Dig Dis Sci. 2010. №55(3). Рр.
842-846.
- Everhart JE, Khare M, Hill M, et al.
Prevalence and ethnic differences in
gallbladder disease in the United States.
Gastroenterology, 1999; 117(3): 632-9.
- Glasgow R.E., Mulvihill S.J. Treatment of
gallstone disease. In: Feldman M, Friedman LS,
Brandt LJ, eds. Sleisenger & Fordtran’s
gastrointestinal and liver diseases, 8th edn.
Philadelphia, PA: Saunders. 2006. Рр.
1419-1437.
- Jessri M., Rashidkhani B. Dietary Patterns
and Risk of Gallbladder Disease: A
Hospital-based Case-Control Study in Adult
Women. J Health Popul Nutr. 2015. №33(1). Рр.
39-49.
- Luman W., Adams W.H., Nixon S.N. et al.
Incidence of persistent symptoms after
laparoscopic cholecystectomy: a prospective
study. Gut. 1996. №39(6). Рр. 863-866.
- Madacsy L., Fejes R., Kurucsai G., et al.
Characterization of functional biliary pain
and dyspeptic symptoms in patients with
sphincter of Oddi dysfunction: effect of
papillotomy. World J Gastroenterol. 2006. №12.
Рр. 6850-6856.
Статья опубликована на сайте
http://www.gastroscan.ru
Если вы заметили орфографическую, стилистическую или другую ошибку на этой странице, просто выделите ошибку мышью и нажмите Ctrl+Enter. Выделенный текст будет немедленно отослан редактору
|
|
|
|

