Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Выбор фармакологической терапии при спастическом мышечном
гипертонусе
А. А. Королев, кандидат медицинских наук
ФГБУ «Всероссийский центр экстренной и радиационной медицины им. А. М.
Никифорова» МЧС России, Санкт-Петербург
Основными препаратами, используемыми для снижения мышечного тонуса, являются
миорелаксанты. По механизму действия различают миорелаксанты центрального
действия (влияют на синаптическую передачу возбуждения в центральной нервной
системе) и периферического действия (угнетают прямую возбудимость
поперечно-полосатых мышц). При применении миорелаксантов могут возникать
достаточно значимые побочные действия, которые при выборе препарата надо
тщательно оценивать [1, 2].
При выборе антиспастических препаратов учитывают в основном их способность
тормозить полисинаптические рефлексы (уменьшение спастики), оказывая при этом
наименьшее влияние на моносинаптические рефлексы (сила мышц). Антиспастический
препарат должен уменьшать мышечную спастичность при минимальном снижении
мышечной силы [3, 4].
Медикаментозная терапия основана на использовании таблетированных и
инъекционных форм. Применяемые внутрь антиспастические средства, уменьшая
мышечный тонус, могут улучшить двигательные функции, облегчить уход за
обездвиженным пациентом, снять болезненные мышечные спазмы, усилить действие
лечебной физкультуры, предупредить развитие контрактур [5]. При легкой степени
спастичности применение миорелаксантов может привести к значительному
положительному эффекту, однако при выраженной спастичности могут потребоваться
большие дозы миорелаксантов, применение которых нередко вызывает нежелательные
побочные эффекты. Лечение миорелаксантами начинают с минимальной дозы, затем ее
медленно повышают для достижения эффекта [6].
К миoрелаксантам центрального действия, наиболее часто используемым в России
для лечения спастического мышечного гипертонуса, относятся баклофен, тизанидин,
толперизон, диазепам [7, 8].
Баклофен (Баклосан, Лиорезал) оказывает антиспастическое действие
преимущественно на спинальном уровне. Препарат представляет аналог
гамма-аминомасляной кислоты (ГАМК), который связывается с пресинаптическими
ГАМК-рецепторами, приводя к уменьшению выделения возбуждающих аминокислот (глутамата,
аспартата) и подавлению моно- и полисинаптической активности на спинальном
уровне, что и вызывает снижение спастичности. Препарат проявляет также умеренное
центральное анальгезирующее действие. Баклофен используется при спинальном и
церебральном спастическом мышечном гипертонусе различного генеза. Начальная доза
составляет 5–15 мг/сут (в один или три приема), затем дозу увеличивают на 5 мг
каждый день до получения желаемого эффекта. Препарат принимают во время еды.
Максимальная доза баклофена для взрослых составляет 60–75 мг/сут. Побочные
эффекты чаще проявляются седацией, сонливостью, снижением концентрации внимания,
головокружением и часто ослабевают в процессе лечения. Возможно возникновение
тошноты, запоров и диареи, артериальной гипертонии, усиление атаксии, появление
парестезий. Требуется осторожность при лечении больных пожилого возраста,
пациентов, перенесших инсульт, пациентов с язвенной болезнью желудка и
двенадцатиперстной кишки. Баклофен противопоказан при эпилепсии, наличии судорог
в анамнезе [9, 10].
При выраженной спастичности, когда обычное пероральное применение
антиспастических препаратов не эффективно, показано интратекальное введение
баклофена, которое впервые было предложено в 1984 г. R. Penn. Для достижения
необходимой концентрации препарата в спинномозговой жидкости необходимо
принимать довольно значительные дозы баклофена, что может привести к нарушениям
сознания, сонливости, слабости. В связи с этим были разработаны системы, при
помощи которых баклофен доставляется непосредственно в подоболочечное
пространство спинного мозга при помощи подоболочечной баклофеновой насосной
системы. При этом клинического эффекта добиваются гораздо меньшими дозами
баклофена, чем при использовании таблетированных форм [11, 12].
Данная система состоит из резервуара, где содержится баклофен или аналогичный
препарат, насоса (помпы), при помощи которого препарат дозированно подается в
подоболочечное пространство спинного мозга через люмбальный катетер и блока
питания. Из резервуара баклофен поступает непосредственно в спинномозговую
жидкость, а его дозировка контролируется специальным радиотелеметрическим
устройством. Количество поступающего в спинномозговую жидкость лекарственного
препарата можно изменять в зависимости от клинической картины. Добавление
баклофена в резервуар производится через 2–3 месяца при помощи чрезкожной
пункции [13].
Использование баклофеновой помпы улучшает скорость и качество ходьбы больных
с нефиксированными рефлекторными контрактурами, обусловленными высокой
спастичностью мышц-синергистов и дисбалансом мышц-антагонистов. Имеющийся
15-летний клинический опыт применения баклофена интратекально у больных,
перенесших инсульт, свидетельствует о высокой эффективности этого метода в
уменьшении не только степени спастичности, но и болевых синдромов и
дистонических расстройств. Отмечено положительное влияние баклофеновой помпы на
качество жизни больных, перенесших инсульт [14].
Тизанидин (Сирдалуд) — миорелаксант центрального действия, агонист
альфа-2-адренергических рецепторов. Препарат снижает спастичность вследствие
подавления полисинаптических рефлексов на уровне спинного мозга, что может быть
вызвано угнетением высвобождения возбуждающих аминокислот L-глутамата и
L-аспартата и активацией глицина, снижающего возбудимость интернейронов спинного
мозга. Тизанидин обладает также умеренным центральным анальгетическим действием.
Препарат эффективен при церебральной и спинальной спастичности, а также при
болезненных мышечных спазмах. Начальная доза препарата составляет 2–6 мг/сут в
один или три приема, при индивидуальном подборе увеличение дозы происходит на
3–4 день на 2 мг. При пероральном приеме действие препарата проявляется через
30–45 минут, максимальный эффект наступает в течение 1–2 часов. Средняя
терапевтическая доза составляет 12–24 мг/сут, максимальная доза — 36 мг/сут. В
качестве побочных эффектов могут возникнуть сонливость, сухость во рту,
головокружение и снижение артериального давления, что ограничивает использование
препарата при постинсультной спастичности. Антиспастический эффект тизанидина
сопоставим с эффектом баклофена, однако тизанидин при адекватном подборе
дозировки лучше переносится, т. к. не вызывает общей мышечной слабости и не
усиливает мышечную слабость в парализованной конечности [15, 16].
Толперизон (Мидокалм) — антиспастический препарат центрального действия,
угнетает каудальную часть ретикулярной формации и обладает Н-холинолитическими
свойствами. Толперизон снижает активность спинальных нейронов, участвующих в
формировании спастичности, путем ограничения потока натрия через мембрану
нервных клеток. Наиболее часто используется по 300–450 мг/сут в два или три
приема. Снижение мышечного тонуса при назначении толперизона иногда
сопровождается сосудорасширяющим действием, что следует учитывать при назначении
больным с тенденцией к артериальной гипотонии. Также препарат может вызывать или
усиливать у больных недержание мочи [17].
Основным побочным эффектом баклофена, тизанидина и толперизона является
быстрое наступление мышечной слабости, причем в каждом случае врач должен
находить баланс между снижением тонуса и усилением слабости. Кривая баланса
между снижением спастического тонуса и усилением мышечной слабости у больных на
фоне увеличения дозы Мидокалма, Сирдалуда или Баклофена показывает, что наиболее
быстрое усиление слабости происходит при приеме Баклофена, а самый мягкий
препарат, позволяющий эффективно подобрать индивидуальную дозировку, — Мидокалм.
Во всех случаях, учитывая наличие узкого терапевтического окна, курс лечения
начинают с небольшой дозы препарата, постепенно наращивая ее до достижения
отчетливого антиспастического эффекта, но не до появления слабости [18, 19].
Диазепам (Реаланиум, Релиум, Сибазон) является миорелаксантом, поскольку
обладает способностью стимулировать уменьшенное пресинаптическое торможение на
спинальном уровне. Он не имеет прямых ГАМК-ергических свойств, увеличивает
концентрацию ацетилхолина в мозге и тормозит обратный захват норадреналина и
дофамина в синапсах. Это приводит к усилению пресинаптического торможения и
проявляется снижением сопротивляемости растяжению, увеличением диапазона
движений. Диазепам также обладает способностью уменьшать болевой синдром,
вызываемый спазмом мышц. Наряду со снижением мышечного тонуса, развиваются
заторможенность, головокружение, нарушение внимания и координации ввиду
токсического действия на центральную нервную систему. Это значительно
ограничивает применение диазепама в качестве миорелаксанта. Используется он, в
основном, для лечения спастичности спинального происхождения при необходимости
кратковременного снижения мышечного тонуса. Для лечения спастичности назначают
в дозе 5 мг однократно или по 2 мг 2 раза в день. Максимальная суточная доза
может составлять 60 мг. При больших дозах могут отмечаться расстройства
сознания, преходящая дисфункция печени и изменения крови. Продолжительность
лечения ограничена из-за возможного развития лекарственной зависимости [20].
Клоназепам является производным бензодиазепина. Клоназепам оказывает
успокаивающее, центральное миорелаксирующее, анксиолитическое действие.
Миорелаксирующий эффект достигается за счет усиления ингибирующего действия ГАМК
на передачу нервных импульсов, стимуляции бензодиазепиновых рецепторов,
расположенных в аллостерическом центре постсинаптических ГАМК-рецепторов
восходящей активирующей ретикулярной формации ствола головного мозга и
вставочных нейронов боковых рогов спинного мозга, а также уменьшения
возбудимости подкорковых структур головного мозга и торможения полисинаптических
спинальных рефлексов.
Быстрое наступление сонливости, головокружения и привыкания ограничивает
применение этого препарата. Для снижения проявления возможных побочных реакций,
достигать терапевтической дозы необходимо путем медленного титрования в течение
двух недель. Для приема внутрь взрослым рекомендуется начальная доза не более 1
мг/сут. Поддерживающая доза — 4–8 мг/сут. Возможно назначение небольших доз в
сочетании с другими миорелаксантами. Клоназепам эффективен при пароксизмальных
повышениях мышечного тонуса. Противопоказан при острых заболеваниях печени,
почек, миастении [21].
Дикалия клоразепат (Транксен) — аналог бензодиазепина, трансформируется в
главный метаболит диазепама, обладает большей активностью и длительностью
антиспастического действия, чем диазепам. Отмечен его хороший эффект при лечении
в виде уменьшения фазических рефлексов на растяжение, обладает незначительным
седативным эффектом. Первоначальная доза составляет 5 мг 4 раза в сутки, затем
уменьшается до 5 мг 2 раза в сутки [22].
Дантролен — производное имидазолина, действует вне центральной нервной
системы, преимущественно на уровне мышечных волокон. Механизм действия
дантролена — блокирование высвобождения кальция из саркоплазматического
ретикулума, что ведет к снижению степени сократимости скелетных мышц, редукции
мышечного тонуса и фазических рефлексов, увеличению диапазона пассивных
движений. Важным преимуществом дантролена по отношению к другим миорелаксантам
является его доказанная эффективность в отношении спастичности не только
спинального, но и церебрального генеза. Начальная доза — 25 мг/сут, при
переносимости дозу увеличивают в течение 4 недель до 400 мг/сут. Побочные
эффекты — сонливость, головокружение, тошнота, диарея, снижение скорости
клубочковой фильтрации. Серьезную опасность, особенно у пожилых пациентов в дозе
более 200 мг/сут, представляет гепатотоксическое действие, поэтому в период
лечения надо регулярно следить за функцией печени. Элиминация дантролена на 50%
осуществляется за счет печеночного метаболизма, в связи с этим он противопоказан
при заболеваниях печени. Осторожность следует соблюдать и при тяжелых сердечных
или легочных заболеваниях.
Катапресан — применяется в основном при спинальных повреждениях, действует на
альфа-2-агонисты головного мозга, обладает пресинаптическим торможением. Из
побочных эффектов отмечаются снижение артериального давления и депрессия.
Первоночальная доза — 0,05 мг 2 раза в день, максимальная — 0,1 мг 4 раза в
день.
Темазепам — взаимодействует с бензодиазепиновыми рецепторами аллостерического
центра постсинаптических ГАМК-рецепторов, расположенных в лимбической системе,
восходящей активирующей ретикулярной формации, гиппокампе, вставочных нейронах
боковых рогов спинного мозга. В результате открываются каналы для входящих токов
ионов хлора и таким образом потенцируется действие эндогенного тормозного
медиатора — ГАМК. Рекомендуемая доза — 10 мг 3 раза в день. Эффективно его
сочетание с баклофеном [23, 24].
Основные лекарственные средства, используемые для лечения спастического
мышечного гипертонуса, представлены в табл.
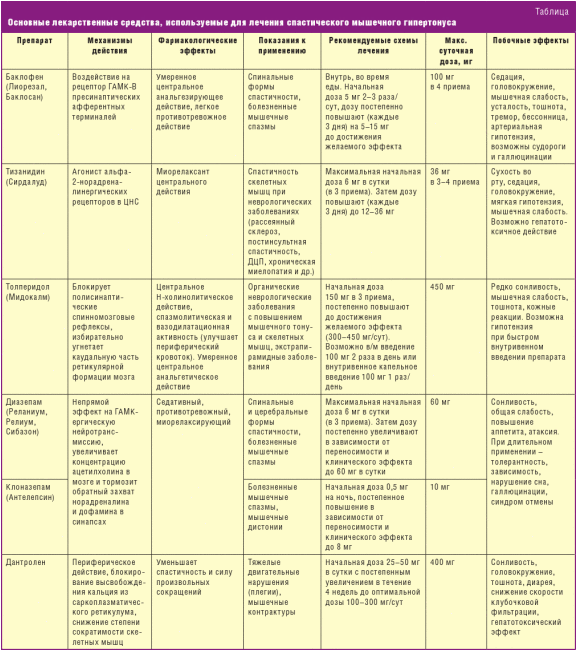
Таким образом, выбор препарата определяется основным заболеванием,
выраженностью мышечной спастичности, а также побочными эффектами и особенностями
действия конкретного препарата.
Так, например, тизанидин и баклофен в большей степени действуют на тонус
мышц-разгибателей, поэтому в случаях наличия значительного гипертонуса
мышц-сгибателей руки, легкой спастичности мышц ноги их прием не показан,
поскольку легкое повышение тонуса мышц-разгибателей ноги компенсирует мышечную
слабость в ноге и стабилизирует походку больного. В таком случае средством
выбора являются методы физического воздействия на мышцы верхней конечности.
При лечении церебральной спастичности наиболее часто применяют Сирдалуд, а
при спинальной спастичности — Сирдалуд и Баклофен. Важным преимуществом перед
другими миорелаксантами обладает Мидокалм, который не оказывает седативного
эффекта и имеет благоприятный спектр переносимости, поэтому является препаратом
выбора для лечения в амбулаторных условиях и для лечения пожилого контингента
пациентов.
Допустима комбинация нескольких средств, что позволяет эффективно снижать
тонус на меньших дозах каждого из препаратов. Сочетание препаратов с разными
точками приложения, начиная от центров в головном мозге и до мышц, может
привести к суммированию терапевтического эффекта.
Эффективность пероральных антиспастических препаратов снижается при их
длительном использовании, часто возникает необходимость возрастающего повышения
дозировок для поддержания начального клинического эффекта, что сопровождается
увеличением частоты и тяжести побочных реакций [25–27].
В ситуации, когда спастичность носит локальный характер и системный эффект
пероральных миорелаксантов нежелателен, предпочтительны локальные методы
воздействия, одним из которых является локальное введение ботулотоксина [28,
29].
Литература
- Скоромец А. А., Амелин А. В., Пчелинцев М. В. и др. Рецептурный
справочник врача-невролога. СПб: Политехника. 2000. 342 с.
- Шток В. Н. Фармакотерапия в неврологии: Практическое руководство.
4?е изд., перераб. и доп. М.: ООО «Медицинское информационное агентство»,
2006. 480 с.
- Методические рекомендации по организации неврологической помощи больным с
инсультами в Санкт-Петербурге / Под ред. В. А. Сорокоумова. СПб:
Санкт-Петербург, 2009. 88 с.
- Леманн-Хорн Ф., Лудольф А. Лечение заболеваний нервной системы.
М.: МЕДпресс-информ. 2005. 528 с.
- O’Dwyer N., Ada L., Neilson P. Spasticity and muscle contractur
in stroke // Brain. 2006. Vol. 119. P. 1737–1749.
- Дамулин И. В. Синдром спастичности и основные направления его
лечения // Журнал неврологии и психиатрии им. С. С. Корсакова. 2003. № 12. С.
4–9.
- Завалишин И. А., Бархатова В. П., Шитикова И. Е. Спастический парез // В
кн. Рассеянный склероз. Избранные вопросы теории и практики. Под ред. И. А.
Завалишина, В. И. Головкина. ООО «Эльф ИПР». 2000. С. 436–455.
- Левин О. С. Основные лекарственные средства, применяемые в
неврологии: Справочник. М.: МЕДпресс-информ, 2007. 336 с.
- Бойко А. Н., Лащ Н. Ю., Батышева Т. Т. Повышение мышечного
тонуса: этиология, патогенез, коррекция // Справочник поликлинического врача.
2004. Т. 4. № 1. С. 28–30.
- Дамулин И. В. Синдром спастичности и основные направления его
лечения // Журнал неврологии и психиатрии им. С. С. Корсакова. 2003. № 12. С.
4–9.
- Избранные лекции по неврологии: под ред. В. Л. Голубева. М.: ЭйдосМедиа,
2006. 624 с.
- Parziale J., Akelman E., Herz D. Spasticity: pathophysiology and
management // Orthopaedics. 2003. Vol. 16. P. 801–811.
- Katz R., Rymer Z. Spastic hypertonia: mechanisms and measurement
// Arch. Phys. Med. Rehab. 2009. Vol. 70. P. 144–155.
- Barnes M. An overview of the clinical management of spasticity //
In: Upper motor neuron syndrome and spasticity. Cambridge University Press.
2001. P. 5–11.
- Парфенов В. А. Патогенез и лечение спастичности // Русский
медицинский журнал. 2011. Т. 9. № 25. С. 16–18.
- Кадыков А. С., Шахпаранова Н. В. Медикаментозная реабилитация
больных со спастическими парезами. В кн.: Синдром верхнего мотонейрона. Под
ред. И. А. Завалишина, А. И. Осадчих, Я. В. Власова. Самара: Самарское отд.
Литфонда, 2005. С. 304–315.
- Кадыков А. С., Черникова Л. А., Сашина М. Б. Реабилитация больных
с центральным постинсультным болевым синдромом // Реабилитология. Сборник
научных трудов (ежегодное издание), № 1. М.: Изд-во РГМУ, 2003. С. 357–359.
- Сашина М. Б., Кадыков А. С., Черникова Л. А. Постинсультные
болевые синдромы // Атмосфера. Нервные болезни. 2004. № 3. С. 25–27.
- Камчатнов П. Р. Спастичность — современные подходы к терапии //
Русский медицинский журнал. 2004. Т. 12. № 14. С. 849–854.
- Гусев Е. И., Скворцова В. И., Платинова И. А. Терапия
ишемического инсульта // Consilium medicum. 2003, спец. выпуск. С. 18–25.
- Кадыков А. С., Черникова Л. А., Сашина М. Б. Постинсультные
болевые синдромы // Неврологический журнал. 2003. № 3. С. 34–37.
- Мусаева Л. С., Завалишин И. А. Лечение спастичности при
рассеянном склерозе // Материалы 9 симпозиума «Рассеянный склероз: лечение и
оздоровление». СПб: Лики России. 2000. С. 59–60.
- Инсульт. Принципы диагностики, лечения и профилактики / Под ред. Н. В.
Верещагина, М. А. Пирадова, З. А. Суслиной. М.: Интермедика, 2002. 208 с.
- Sommerfeld D. K., Eek E. U.-B., Svensson A.-K. et al. Spasticity
after stroke: its occurrence and association with motor impairments and
activity limitations // Stroke. 2004. Vol. 35. P. 134–140.
- Bakheit A., Zakine B., Maisonobe P. The profile of patients and
current practice of treatment of upper limb muscle spasticity with botulinum
toxin type A // Int. J. Rehabil. Res. 2010. Vol. 33. P. 199–204.
- Малахов В. А. Мышечная спастичность при органических заболеваниях
нервной системы и ее коррекция // Международный неврологический журнал. 2010.
№ 5. С. 67–70.
- Davis T., Brodsky M., Carter V. Consensus statement on the use of
botulinum neurotoxin to treat spasticity in adults // Pharmacy and
Therapeutics. 2006. Vol. 31. P. 666–682.
- Childers M., Brashear A., Jozefczyk P. Dose-dependent response to
intra-muscular botulinum toxin type A for upper limb spasticity after stroke
// Arch. Phys. Med. Rehab. 2004. Vol. 85. P. 1063–1069.
- Кадыков А. С. Миорелаксанты при реабилитации больных с
постинсультными двигательными нарушениями // Журнал неврологии и психиатрии
им. С. С. Корсакова. 1997. № 9. С. 53–55.
Статья опубликована в журнале
Лечащий Врач

