Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
«Золотой стандарт» в лечении ювенильного идиопатического
артрита
Ф. В. Рохлина
Г. А. Новик, доктор медицинских наук, профессор
ГБОУ ВПО СПбГМПУ МЗ РФ, Санкт-Петербург
Ювенильный идиопатический артрит (ЮИА) это наиболее распространенное
ревматическое заболевание среди детей. В классификации Международной лиги
ревматологических ассоциаций (League of Associations for Rheumatology, ILAR) (Durban,
1997 г.) выделяют следующие типы артрита. Системный вариант — это артрит,
сопровождающийся лихорадкой в сочетании с летучей эритематозной сыпью, и/или
серозитом, и/или генерализованной лимфаденопатией, и/или гепатомегалией, и/или
спленомегалией. Олигоартикулярный вариант — это артрит с поражением от 1 до 4
суставов в течение первых 6 месяцев болезни, эта форма артрита является типичной
для детей и не наблюдается у взрослых. Выделяется два подтипа олигоартрита:
персистирующий олигоартрит — поражается от 1 до 4 суставов за весь период
болезни и прогрессирующий олигоартрит — поражается 5 суставов и более после 6
месяцев болезни. Полиартикулярный вариант (негативный/позитивный по
ревматоидному фактору) — это артрит с поражением 5 суставов или более в течение
первых 6 месяцев болезни, ревматоидный фактор отрицательный/положительный
соответственно. Псориатический артрит — поражение, проявляющееся артритом и
псориазом или артритом и двумя из следующих симптомов: дактилитом/изменением
ногтей/семейным псориазом, подтвержденным дерматологом у лиц 1-й степени
родства. Энтезитный артрит — основными клиническими проявлениями являются артрит
и энтезит или артрит, либо энтезит с двумя из следующих признаков:
чувствительность сакроилеальных сочленений и/или боль в спине
(воспаление)/обнаружение HLA-B27 в крови/семейный анамнез
(HLA-B27-ассоциированные болезни у лиц 1-й или 2-й степени родства). Другие
артриты — это артриты, причина возникновения которых неизвестна, персистирующие
в течение 6 недель, не укладывающиеся в характеристику какой-либо категории или
отвечающие критериям более чем одной категории. Группа неопределенных артритов
включает пациентов, которые не удовлетворяют критериям включения в любую из
категорий или которые отвечают критериям более чем одной категории [1].
У больных ЮИА часто встречается устойчивость к терапии различными
препаратами, в том числе нестероидными противовоспалительными средствами (НПВС),
а также к внутрисуставным инъекциям и физиотерапии [2]. Для лечения ЮИА
используется несколько групп препаратов: НПВС, глюкокортикоиды (ГК),
иммуносупрессивные препараты и биологически-активные вещества, полученные
генно-инженерным путем. Применение НПВС и ГК оказывает обезболивающий и
противовоспалительный эффекты, но не способствует предотвращению деструкции
суставов и инвалидизации больных.
Известно, что иммуносупрессивная и биологическая терапии зачастую
приостанавливают развитие системных проявлений и прогрессирование деструкции
суставов. Иммуносупрессивная терапия должна быть дифференцированной, длительной
и непрерывной, начинаться сразу после верификации диагноза в течение первых 3–6
месяцев болезни [3].
«Золотым стандартом» в терапии ЮИА можно считать метотрексат (МТХ) [2] —
цитостатический препарат из группы антиметаболитов, антагонистов фолиевой
кислоты.
МТХ оказывает выраженное иммуносупрессивное действие даже в относительно
низких дозах, не характеризующихся заметной гематологической токсичностью.
Несмотря на это, при приеме МТХ рекомендовано проводить клинико-лабораторный
мониторинг, который необходим для предупреждения побочных эффектов [4]. По
данным различных авторов около 70% пациентов, получающих терапию МТХ, входят в
ремиссию по заболеванию.
В 1988 г. МТХ был разрешен Управлением по надзору за качеством пищевых
продуктов и лекарственных средств США (Food and Drugs Administration of the
United States, FDA) для лечения ревматоидного артрита [4]. В настоящее время МТХ
является основным препаратом в лечении ЮИА [2]. Популярные терапевтические
рекомендации по назначению МТХ основаны на рандомизированном двойном слепом
плацебо-контролируемом исследовании, проведенном в 1992 г. В ходе исследования
сравнивались группы пациентов с устойчивым к терапии артритом: получающие низкую
дозу МТХ (10 мг/м2/нед), получающие очень низкую дозу МТХ (5 мг/м2/нед)
и получающие плацебо. Результатом исследования стало повышение дозы МТХ у «плохоотвечающих»
на терапию пациентов, так как уже появился длительный опыт применения МТХ.
Отчеты еще одного исследования поддерживают использование высоких доз МТХ (25–30
мг/м2 или 0,8–1 мг/кг) у пациентов ЮИА, не отвечающих на стандартную
дозу (10–15 мг/м2 или 0,3–0,5 мг/кг) [5]. Однако только одно
исследование применения МТХ у детей сравнило эффективность высоких доз (30 мг/м2)
МТХ со средней дозой МТХ (15 мг/м2) [6]. Никакой разницы в
эффективности и токсичности терапии замечено не было. Более того, это
исследование включило только детей с ЮИА, которые до исследования уже имели опыт
терапии стандартной дозой МТХ без эффекта. Современные тенденции раннего и
агрессивного лечения артритов сопровождаются практическим использованием высоких
начальных доз МТХ как попыткой предотвратить поздние осложнения и
нетрудоспособность, несмотря на отсутствие объективных клинических исследований,
сравнивающих токсичность и эффективность при начальной высокой дозе и
стандартной дозе МТХ для поддержки такой практики. По этой причине ученые не
могут прийти к единому мнению, с какой дозы стоит начинать терапию МТХ у детей с
ЮИА [7].
Ретроспективные данные о терапии метотрексатом у детей и подростков впервые
были опубликованы в 1986 г. В метаанализе Giannini и соавт. сравнили МТХ (5–10
мг/м2/нед) с пенициламином, гидроксихлорокином и ауранофином. Только
при применении МТХ в дозе 10 мг/м2/нед была отмечена положительная
динамика по сравнению с плацебо. Эффективность терапии МТХ у детей была оценена
в контролируемом исследовании, которое показало, что МТХ несколько эффективнее
лефлуномида. В ходе исследования дети, в том числе подростки, в возрасте 3–17
лет, получали лефлуномид или МТХ в течение 16 недель. Группа, получающая МТХ,
дала лучший ответ на терапию [2].
В 2011 г. Американской коллегией ревматологии (American College of
Rheumatology, ACR) были выпущены рекомендации по лечению ювенильного
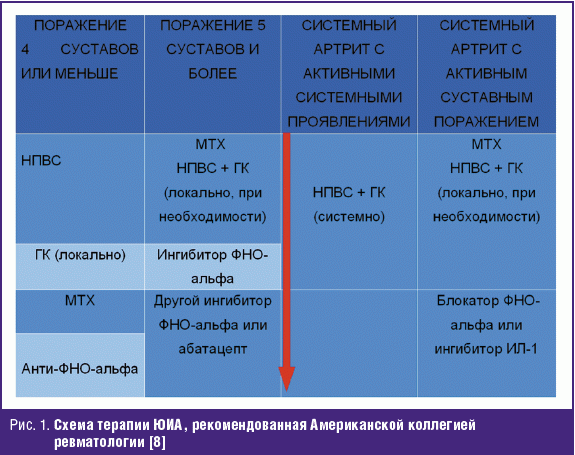
идиопатического артрита. Авторами были рассмотрены 4 схемы терапии [8].
Первая схема относится к больным с поражением до 4 суставов. При отсутствии
высокой активности рекомендуется начинать с монотерапии НПВС, в случае
неэффективности и прогрессирования рекомендовано переходить к внутрисуставному
введению ГК, в дальнейшем предусматривалось назначение МТХ. МТХ может быть
заменен на сульфасалазин, у больных с энтезитассоциированной формой ЮИА. В
случае высокой активности или быстрого прогрессирования рекомендовано начинать с
внутрисуставных введений ГК или назначения в/м МТХ. При неэффективности этих
схем или прогрессирования заболевания назначаются блокаторы фактора некроза
опухоли альфа (ФНО-альфа).
Вторая схема предназначена для больных с поражением 5 суставов и более, таким
пациентам рекомендовано назначение МТХ (или лефлуномида), а также возможно
назначение НПВС и ГК (локально). Через 3–6 месяцев при отсутствии положительной
динамики или сохранении активности рекомендуется назначать ингибиторы ФНО-альфа.
В случае, если в течение 4 месяцев положительная динамика не получена, авторы
предлагают назначение другого препарата анти-ФНО-альфа или абатацепта.
Для лечения детей с системным вариантом ЮИА используются две вышеописанные
схемы. Третья схема предусматривает терапию пациентов с активными системными
проявлениями, таким детям рекомендовано назначение системных ГК, в случае
невысокой активности можно начинать с курса НПВС. В дальнейшем рекомендован
переход на ингибитор интерлейкина-1 (ИЛ-1) (анакинру). В тяжелых случаях
заболевания ингибитор ИЛ-1 предлагается как препарат выбора для начального
лечения. В четвертой схеме описывается терапия пациентов с системным ЮИА, в
настоящий момент имеющих активный артрит. Таким больным рекомендовано начинать
терапию с МТХ в сочетании с НПВС и ГК (локально), затем через 3 месяца решать
вопрос о назначении блокаторов ФНО-альфа или ингибитора ИЛ-1 (рис. 1).
По рекомендациям Американской коллегии ревматологии по лечению ЮИА 2011 г.,
больным, получающим терапию МТХ, необходимо проводить клинический анализ крови,
определять уровни аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ) и
креатинина в сыворотке крови перед назначением терапии, а также через 1 месяц
после первого введения препарата. При повышении дозы МТХ необходимо
контролировать показатели крови через 1–2 месяца после изменения дозировки. При
нормальном течении заболевания и стабильной дозе МТХ рекомендовано повторять
анализ крови 1 раз в 3–4 месяца [8].
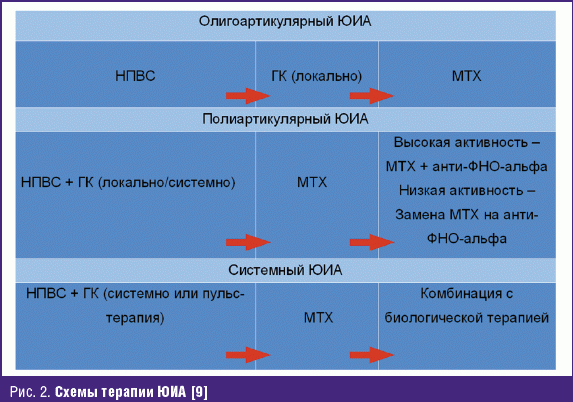
В 2012 г. в журнале «Клиническая иммунология» были опубликованы немецкие
рекомендации по лечению ЮИА [9]. При олигоартрикулярном варианте рекомендовано
начинать терапию с НПВС, затем применяются внутрисуставные введения ГК, при
неэффективности такой терапии назначается МТХ. Пациентам с полиартикулярной
формой ЮИА в дебюте, кроме НПВС, рекомендовано назначать ГК как локально, так и
системно. На втором этапе назначается МТХ. При сохранении активности добавляется
терапия анти-ФНО-альфа, а при невысокой активности и недостаточном эффекте МТХ
рекомендуется заменить его на препараты анти-ФНО-альфа. У больных с системным
вариантом ЮИА, кроме НПВС, в дебюте назначаются ГК в виде пульс-терапии, на
следующем этапе назначается МТХ, который в дальнейшем рекомендовано
комбинировать с биологической терапией (рис. 2).
Ruperto и соавт. [10] провели исследование по применению более высоких доз
для парентерального введения метотрексата (средняя доза 15 мг/м2/нед
и высокая доза 30 мг/м2/нед). Результатом исследования стало, что
больные, получившие высокие (30 мг/м2/нед) дозы МТХ, не дали большего
терапевтического ответа, чем те пациенты, кто получил в средней дозе по 15 мг/м2.
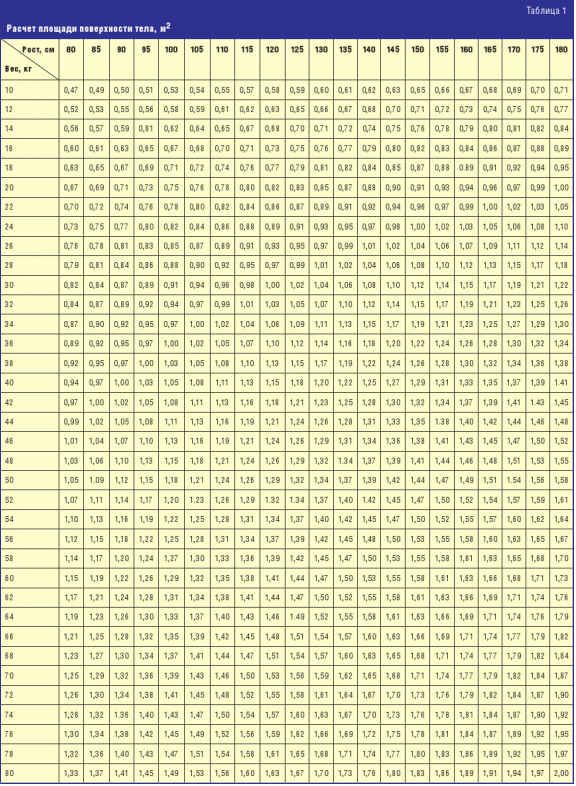
Для корректного назначения МТХ необходимо рассчитать площадь поверхности тела
(ППТ), для этого можно использовать формулу — ППТ = (рост × вес/3600), где ППТ —
это площадь поверхности тела (м2), рост — рост (см), вес — масса тела
(кг), кроме того, для определения ППТ можно использовать специальные таблицы
(табл. 1).
Для достижения лучшего эффекта от терапии метотрексатом рекомендуется
комбинирование с НПВС, а также с биологическими препаратами [2]. В 2011 г. в
Финляндии K. J. Aaltonen и соавт. было проведено большое исследование по
применению анти-ФНО-препаратов у детей с различными формами ЮИА. Результатом
этого исследования стал вывод, что при комбинации препаратов анти-ФНО с МТХ
эффективность значительно выше, чем после применения этих препаратов по
отдельности [11].
В клинических рекомендациях для педиатров по детской ревматологии под
редакцией А. А. Баранова и Е. И. Алексеевой изложены общепринятые схемы лечения
ювенильного артрита и дозирования основных препаратов. Согласно этим
рекомендациям у больных с олигоартритом МТХ применяется в дозе 10–15 мг/м2/нед,
при полиартритическом варианте в дозе 15–25 мг/м2/нед, а при
системном варианте рекомендовано назначать МТХ в дозе 20–25 мг/м2/нед
(в случае неэффективности у больных с системным артритом назначается
пульс-терапия с МТХ в дозе 50 мг/м2/нед, в течение 8 недель) [12].
Нами было проведено исследование, целью которого стала попытка определения
эффективной концентрации МТХ в сыворотке крови у больных с ЮИА.
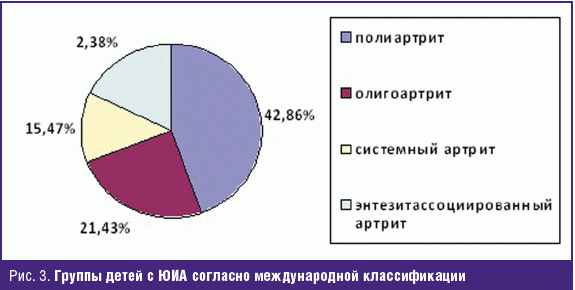
Было обследовано 103 ребенка больных ЮИА, среди которых — 65 (63,11%) девочек
и 38 (36,89%) мальчиков с различными формами ювенильного идиопатического
артрита. Детей с полиартритом — 46 (44,66%), с олигоартритической формой ЮИА —
25 детей (24,27%), системный вариант артрита диагностирован у 14 детей (13,59%),
энтезитассоциированный артрит встречался у 18 больных (17,48%) (рис. 3).
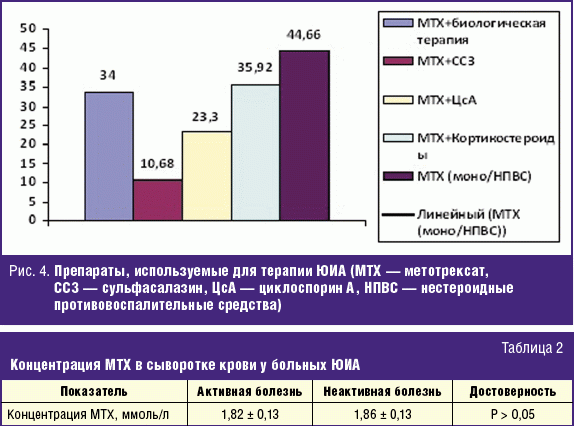
Все дети, включенные в исследование, получали базисную терапию метотрексатом
в дозе 15 мг/м2 в течение трех месяцев и более. У 35 пациентов (34%) к терапии
МТХ добавлена биологически активная терапия (тоцилизимуб, этанерцепт,
инфликсимаб, голимумаб, абатацепт), 11 пациентов (10,68%) получают в дополнение
к терапии МТХ сульфасалазин (ССЗ), 24 ребенка (23,3%) — циклоспорин А (ЦсА), 37
детей (35,92%) — получают преднизолон или метилпреднизолон (в таблетках или в
виде пульс-терапии). Обращает внимание, что у 46 (44,66%) пациентов наблюдается
положительный эффект от монотерапии МТХ, не требующий назначения дополнительных
препаратов (рис. 4).
С. A. Wallace и соавт. разработали критерии «неактивной» болезни.
«Неактивная» болезнь — это отсутствие суставов с активным артритом, отсутствие
лихорадки, сыпи, серозита, спленомегалии или генерализованной лимфоаденопатии,
связанной с ЮИА, отсутствие обострения увеита, нормальные значения скорости
оседания эритроцитов (СОЭ) или уровня С-реактивного белка и объективный осмотр,
подтверждающий отсутствие активной болезни [13]. Все больные были разделены нами
на две группы: с активной и неактивной болезнью. Концентрация МТХ в сыворотке
крови в этих группах никак не отличалась (табл. 2).
По полученным нами данным, концентрация МТХ в сыворотке крови находилась в
диапозоне от 0,76 ммоль/л до 3,96 ммоль/л. Достоверных различий в зависимости от
активности заболевания, вида артрита, длительности терапии МТХ получено не было.
Таким образом, определение концентрации МТХ в сыворотке крови у больных ЮИА не
позволяет прогнозировать эффективность проводимой терапии.
МТХ обладает хорошим профилем безопасности. Для снижения риска развития
побочных эффектов больным назначают фолиевую кислоту (в дозе 1–5 мг) в те дни,
когда МТХ не используется, так как при одновременном приеме фолиевая кислота
может снижать эффективность МТХ [12]. Важной особенностью применения этого
препарата является использование 1 раз в неделю.
Использование цитостатической терапии (МТХ) является препаратом выбора во
всех странах при терапии различных форм ЮИА и является «золотым стандартом»
лечения пациентов с этим заболеванием.
Литература
- Ravelli A., Martini A. Juvenile idiopathic arthritis // Lancet.
2007. 369, 767–778.
- Niehues T., Lankisch P. Recommendations for the Use of
Methotrexate in Juvenile Idiopathic Arthritis // Pediatric Drugs. 2006. P.
347–356.
- Алексеева Е. И., Бзарова Т. М. Ювенильный артрит: возможности
медикаментозного и немедикаментозного лечения на современном этапе // Лечащий
Врач. 2011. № 8.
- Khan Z. A., Tripathi R., Mishra B. Methotrexate: a detailed
review on drug delivery and clinical aspects // Expert Opin. Drug Deliv. 2012.
Vol. 9 (2). P. 151–169.
- Wallace C. A., Sherry D. D. Preliminary report of higher dose
methotrexate treatment in juvenile rheumatoid arthritis // J Rheumatol. 1992.
Vol. 19. P. 1604–1607.
- Ruperto N., Murray K. J., Gerloni V. et al. A randomized trial of
parenteral methotrexate comparing an intermediate dose with a higher dose in
children with juvenile idiopathic arthritis who failed to respond to standard
doses of methotrexate // Arthritis Rheum. 2004. Vol. 50. P. 2191–2201.
- Becker M. L., Rose C., Cron R. et al. Effectiveness and Toxicity
of Methotrexate in Juvenile Idiopathic Arthritis: Comparison of 2 Initial
Dosing Regimens // J Rheumatol. 2010. P. 870–875.
- Beukelman T., Patkar N., Saag K. et al. 2011 American College of
Rheumatology Recommendations for the Treatment of Juvenile Idiopathic
Arthritis: Initiation and Safety Monitoring of Therapeutic Agents for the
Treatment of Arthritis and Systemic Features // Arthritis Care & Research.
2011. P. 465–482.
- Dueckers G., Guellac N., Arbogast M. Evidence and consensus based
GKJR guidelines for the treatment of juvenile idiopathic arthritis // Clinical
Immunology. 2012. 142. P. 176–193.
- Kahn P. Juvenile Idiopathic Arthritis Current and Future
Therapies // Bulletin of the NYU Hospital for Joint Diseases. 2009, 67 (3). P.
291–302.
- Aaltonen K., Virkki L., Malmivaara A. et al. Systematic Review
and Meta-Analysis of the Efficacy and Safety of Existing TNF Blocking Agents
in Treatment of Rheumatoid Arthritis // Plos ONE. 2012. Vol. 7, Issue 1. P.
1–14.
- Клинические рекомендации для педиатров: детская ревматология.
Лекарственные средства, применяемые для лечения ревматических болезней у
детей. Баранов А. А., Алексеева Е. И. 2011, с. 206–207.
- Wallace C. A. Current management of juvenile idiopathic arthritis
// Best Practice & Research Clinical Rheumatology. 2006. P. 279–300.
Статья опубликована в журнале
Лечащий Врач

