Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Ночные апноэ: 30-ти летний период исследований и открытий
С. Л. Бабак
НИИ Пульмонологии
В 1997 году исполнилось 30 лет с того самого времени, когда
Jung и Kuhl [27] впервые выделили из синдрома
Пиквика самостоятельно существующий патологический симптомокомплекс, основным
проявлением которого являлись регулярные эпизоды ночных асфиксических состояний
- ночные апноэ. Они установили, что состояния апноэ сопровождаются
выраженной гипоксией, гиперкапнией, и изменениями электрической активности
мозга, приводящие к частым ночным пробуждениям. Руководствуясь представлениями
Burwell [7] о синдроме Пиквика и рекомендациями
Rechtschaffen и Kales [45] о
проведении ночной множественной регистрации биологических сигналов с
человеческого тела (“ночной полисомнографии”), они впервые зарегистрировали
указанные состояния, предложили объяснение найденному феномену, и осуществили
попытку его коррекции с помощью трахеотомии [30].
Найденный феномен послужил толчком к появлению нового направления в медицине
- “медицине сна” [1], которое во всем мире в настоящее
время переживает свое бурное развитие. Одним из важнейших аспектов этого
направления является диагностика и разработка методов коррекции дыхательных
расстройств у пациентов в ночное время [20]. Это
определило усиленный интерес врачей-пульмонологов к данной проблеме.
Результатами многочисленных работ, проведенных исследователями, явилось
окончательное формирование к 1976 году представления о симптомокомплексе
патологических ночных остановок дыхания [20], названного
“синдромом обструктивного апноэ-гипопноэ сна” (СОАГС).
Синдром обструктивного апноэ-гипопноэ сна - это серьезное, потенциально
угрожающее жизни пациента, состояние, характеризующееся развитием остановок
дыхания длительностью более 10 секунд с частотой развития более
15 в час.
Guilleminault С.[20]
Наиболее характерными и часто наблюдаемыми проявлениями этого
симптомокомплекса являются: коллапс глоточного отдела верхних дыхательных путей,
повышенное сопротивление воздушному потоку дыхания на уровне глоточного отдела,
гиповентиляционные дыхательные расстройства той или иной степени выраженности
[17].
Эпизоды остановок дыхания во время человеческого сна относят к виду ночных
дыхательных расстройств со снижением вентиляции легких [13].
Чаще всего они характеризуются повторяющимися коллапсами в области
верхних дыхательных путей, приводящих к полной остановке дыхания
[20]. У подавляющего большинства пациентов (86%) их развитие
сопровождается громким ночным храпом [19], а также
частыми неосознанными ночными пробуждениями [17].
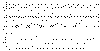
Рисунок 1. Эпизод громкого ночного храпа, фиксируемый у
пациента во время проведения полисомнографического исследования. Хорошо видно,
что при сохраненных грудных (THO) и брюшных
(ABD) дыхательных усилиях он приводит к значительному “урезанию”
ротоносового дыхательного потока (FLOW), что закономерно
приводит к низким показателям насыщения (SAO2)
артериальной крови кислородом. Условные сокращения на
представленном 30 секундном отрезке полисомнографической записи (полисомнографической
эпохе): LITE - показатель освещенности;
C4A1,O2A1 - каналы энцефалографической записи, регистрируемой при
центральном и затылочном расположении электродов; LEOG, REOG -
окулограмма с левого и правого глаза; CHIN -
миограмма с подбородочной области; ECG -
электрокардиограмма; RR - частота сердечного ритма;
MICRO - звуковой канал регистрации храпа;
BODY - позиция тела во время сна (RS - правая
сторона); gSAO2 - графическое представление данных по
насыщению артериальной крови кислородом. Регистрация полисомнографической записи
осуществлена на оборудовании “Alice3” компании
HealthDyne, USA.
Существует два основных вида ночных дыхательных расстройств
[43]. Апноэ - прекращение или снижение на величину более 40%
амплитуды регистрируемого воздушного дыхательного потока (ВДП) с
сохраненными (обструктивный тип) или не сохраненными
(центральный тип) грудными дыхательными усилиями (ГДУ) и брюшными дыхательными
усилиями (БДУ) [45]. Гипопноэ - снижение амплитуды
регистрируемого ВДП на величину от 20% до 40% при сохраненных (обструктивный
тип) или не сохраненных (центральный тип) ГДУ и БДУ
[45, 51].
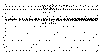
Рисунок 2. Эпизод ночного обструктивного апноэ, фиксируемый у пациента
во время проведения полисомнографического исследования. Хорошо видно, что при
сохраненных грудных (THO) дыхательных усилиях он
закономерно приводит к низким показателям насыщения (SAO2)
артериальной крови кислородом. Эпизод апноэ оканчивается
резким изменением волновой активности на энцефалографических каналах -
“неосознанным пробуждением” (arousal) и двигательной
активностью конечностей (LLEG). Условные сокращения на
представленном 30 секундном отрезке полисомнографической записи (полисомнографической
эпохе): LITE - показатель освещенности;
C4A1,O2A1 - каналы энцефалографической записи, регистрируемой при
центральном и затылочном расположении электродов; LEOG, REOG -
окулограмма с левого и правого глаза; CHIN -
миограмма с подбородочной области; ECG -
электрокардиограмма; FLOW - воздушный ротоносовой
дыхательный поток; ABD - брюшное дыхательное усилие;
BODY - позиция тела во время сна (RS -
правая сторона); gSAO2 - графическое представление данных
по насыщению артериальной крови кислородом. Регистрация
полисомнографической записи осуществлена на оборудовании “Alice3”
компании HealthDyne, USA.
Первые эпидемиологические исследования распространенности СОАГС в популяции
были предприняты в 1983 году группой французских ученых под руководством
Lavie P. [31]. Они провели открытое рандоминизированное
исследование среди 1502 рабочих занятых в машиностроительном производстве.
Результатом их работы явилось определение процентной распространенности СОАГС в
людской популяции, которая составила 4,5 %. Аналогичные данные были позже
получены группой бельгийских и шведских исследователей [6].
В более поздних исследованиях английских эпидемиологов под руководством
Yong T, [59] частота встречаемости СОАГС среди взрослого
населения Великобритании в средневозрастной группе составила среди женщин -
2-4%, а среди мужчин - 4-6%, Это оказалось сопоставимо с распространенностью
бронхиальной астмы, которая в средневозрастной группе достигает 4,5%
[40].
Обнаружение высокой распространенности СОАГС в популяции явилось причиной
пристального внимания ученых разных стран к этой проблеме и привело к бурному
развитию медицины сна и созданию целой сети исследовательских “лабораторий сна”
по всему миру. Наиболее показательным в этом отношении является опыт
американских коллег. Так, в США в 1988 насчитывалось 120 лабораторий сна, а уже
к 1990 году - более 870 [2]. Это явилось причиной для
создания специальной Национальной Комиссии США по исследованию нарушений сна и
Американской Ассоциации Сонных Расстройств [3].
Результатами их совместной работы явились опубликованные в 1994 году данные о
распространенности “расстройств сна” и наносимом ими ущербе для экономики США
[40].
По данным национальной комиссии сша за 1994 год:
11.845.000 американцев в возрасте от 30 до 60 лет страдают синдромом
обструктивного апноэ-гиппопноэ сна; 3.029.000 из них страдают средним или
тяжелым СОАГС;
Из 31.000.000 американцев в возрасте свыше 65 лет СОАГС страдают 7.440.000
человек, из которых 46% имеют среднюю или тяжелую форму;
Последствия СОАГС снижают продуктивность работы и учебы в 20 раз, качество
семейной и общественной жизни в 15 раз, повышают заболеваемость и смертность в
12,5 раза.
87% водителей, перевозящих грузы на дальние расстояния, страдают СОАГС: из
них 46% имеют среднюю или тяжелую форму.
38.000 человек ежегодно погибает из-за проблем, связанных с СОАГС.
В 2,5 раза автомобильные катастрофы со смертельным исходом выше среди
пациентов СОАГС.
Несмотря на широкое распространение СОАГС, большинство случаев остаются не
диагностированными и не леченными. Наносимый американскому обществу ущерб от
различных проявлений расстройств сна составляет 150 миллиардов долларов
ежегодно.
Пациенты с высоким риском развития СОАГС чаще всего страдают громким
хроническим храпом. Если такового выявить не удается, вероятность остановок
дыхания во время сна не велика [33]. С другой стороны,
часто наблюдаемые явления “перехватывания” ночного дыхания и “дыхательной
заслонки” могут служить предрасполагающими факторами в дальнейшем развитии СОАГС.
В этих случаях является необходимым опрос близких родственников и супруга
пациента для наиболее точного и полного сбора информации о состоянии храпа и
периодах кратковременных ночных остановок дыхания. [32].
Избыточный вес тела, в особенности ожирение высокой степени, является
фактором риска и достоверно утяжеляет симптоматику и течение СОАГС
[39]. Большинство пациентов СОАГС имеют ожирение
различной степени, причем наиболее часто повышение веса составляет более 120 %
от “идеального веса тела”. Очень небольшое количество страдающих СОАГС могут
быть охарактеризованы как лица с “Синдромом Пиквика”. Основными критериями
синдрома являются: дневная гиперкапния и гипоксемия, артериальная гипертензия,
полицитемия, и легочное сердце [44]. Рассматривая
ожирение как фактор риска СОАГС, можно отметить, что оно приводит к нарушению
дыхательной функции, выраженной дневной гипоксемии и гиповентиляции легких
и характерным ночным дыхательным расстройствам [34].
Различают следующие основные виды проявления СОАГС у пациентов с
ожирением различной степени:
“Тяжелый храп” без изменения дыхательного
рисунка имеют часть пациентов при начальных проявлениях СОАГС. Эти пациенты, о
которых принято говорить, что они имеют ПСВДП и избыточную дневную сонливость
[16].
“Гипоксемия без изменения дыхательного рисунка” - является характерным
проявлением у большинства пациентов СОАГС с избыточным весом тела. Ее
существование объясняется уменьшением легочных объемов в положении “на спине”.
У одних пациентов наблюдается стабильная SaO2 в пределах от 90% до
94% во время NREM, со значительными снижениями показателя во время REM. У
других имеют место выраженные периоды гиповентиляции [24]. Отсутствие у таких
пациентов свершившихся остановок дыхания может, является нормальным ответом
дыхательных драйверов, при отсутствии обструкции верхних дыхательных путей
[5]. В отличие от варианта циклической гипоксемии, описанной ниже, некоторые
пациенты с проявлениями OHS могут иметь постоянную выраженную гипоксемию без
аномалий дыхательного рисунка. Принято считать, что причиной гипоксемии в этом
случае является гиповентиляция, при которой PaCO2 превышает 100 mm.
Hg [9].
“Периодическая гипоксемия без остановок дыхания”. Колебания SaO2
могут присутствовать без явлений явных остановок дыхания. Иногда это связано с
периодическими изменениями вентиляции, или с не совершившимися явлениями
окклюзии верхних дыхательных путей - синдромом сонного гипопноэ. Эти пациенты
имеют точно такие же последствия, как и пациенты с СОАГС: часто встречающиеся
AR (arousal), циклическая гипоксемия, сонливость и правожелудочковая
недостаточность [14]. Таких пациентов расценивают как “промежуточных”,
поскольку они находятся в переходном состоянии между нормальным сном и СОАГС
[22].
“Остановки дыхания во время сна - “сонное апноэ”. Бесспорно, что пациенты,
имеющие ожирение, предрасположены к остановкам дыхания во время сна. Однако
следует помнить и то, что есть среди них исключения из правил [22]. Как
таковой избыточный вес тела не является абсолютной причиной сонного апноэ.
Скорее всего, лишь сочетание ожирения с анатомической обструкцией верхних
дыхательных путей и есть ключевой элемент в генезе сонного апноэ. Необходимо и
наличие увеличения податливости стенок верхних дыхательных путей, делающей их
легко коллапсируемыми [23]. Пациенты избыточного веса с явлениями сонного
апноэ отчетливо представлены двумя группами: те, кто имеет явления
гиповентиляции во время бодрствования и сниженные химические дыхательные
драйверы, и пациенты без явлений дневной гиповентиляции. Пациенты с сонным
апноэ и OHS были широко популяризированы в литературе как страдающие
“Синдромом Пиквика” [7]. Они имеют более выраженные проявления полицитемии и
легочного сердца, чем пациенты с избыточным весом без явлений гиповентиляции
во время бодрствования. Как показывает практика, гиповентиляция во время
бодрствования обнаруживается лишь у 10% сонливых, пациентов с избыточным весом
тела [12]. До сих пор остается не выясненным, как дыхание во время сна
пациентов СОАГС отличается от такового у пациентов с ожирением и сонным апноэ
без явлений гиповентиляции во время бодрствования, хотя очевидно, что пациенты
OHS чаще демонстрируют лишь постоянную гиповентиляцию во время сна, без
периодов сонного апноэ [36].
Увеличение размера охвата шеи, как у мужчин, так и у женщин в сочетании с
храпом может служить высоким предрасполагающим фактором развития сонного апноэ.
В проводимых исследованиях, мужчины с охватом шеи і 43 см, а женщины с охватом
шеи і 40 см достоверно имели самый высокий риск развития остановок дыхания во
время сна [8].
Другими маркерами заболевания, помогающими идентифицировать пациентов с
риском развития СОАГС, являются артериальная гипертензия, избыточная хроническая
дневная сонливость, автодорожные происшествия и несчастные случаи на
производстве, а также трудно объяснимая легочная гипертензия и легочное сердце
[35] (таблица 1). В случае жалоб пациента на избыточную
дневную сонливость, при отсутствии других симптомов-маркеров, указывающих на
остановки дыхания во время сна, подсказкой могут служить: особенности течения
самого сна, его продолжительность, недавно наступившие изменения паттерна сна,
приведшие к ухудшению качества жизни [2].
Таблица 1. Симптомы и маркеры СОАГС
|
Симптомы |
Маркеры |
| 1 Громкий хронический ночной храп.
2 Периоды перехватывания дыхания или “дыхательной заслонки” во время сна
3 Выраженная избыточная дневная сонливость (особенно у лиц управляющих
транспортным средством). |
· Повышение веса тела, в особенности его значительное
увеличение (і 120% от идеального веса тела).
· Охват шеи (размер воротничка):
мужчины 43 см,
женщины 40 см. |
| 1 Несчастные случаи на производстве или автодорожные
происшествия, причиной которых служила дневная сонливость или дневная
усталость. |
· Системная гипертензия.
· Назофаренгиальные сужения.
· Легочная гипертензия (редкий маркер).
· Легочное сердце (редкий маркер). |
| · Индивидуальные изменения характера пациента
на фоне утомления или дневной усталости. |
Пациент может просто нуждаться в выяснении причин, приводящих к увеличению
бодрствования во время сна. Если сон пациента достаточный, необходимо
рассматривать другие состояния, такие как нарколепсия или депрессия
[37].
В большинстве случаев пациенты СОАГС испытывают различной силы явления
вялости, усталости, сонливости, расстройства памяти, раздражительность,
трудность концентрации внимания, изменения личности, о которых они сообщают
своим лечащим врачам [48]. Для них характерно развитие
непреодолимой сонливости в самые неподходящие моменты, высокая частота
совершения автодорожных происшествий, несчастных случаев на производстве
[10]. Сердечно-сосудистая система также быстро вовлекается в
патологический процесс у таких пациентов СОАГС [55]. Так,
системная гипертензия регистрируется более чем у 50% пациентов
[11]; частота утренней гипертензии линейно возрастает с ростом числа
остановок дыхания в ночное время, причем данные имеют высокую достоверность как
для людей с избыточным весом, так и у лиц без его увеличения. Ночные аритмии так
же тесно взаимосвязаны с явлениями апноэ сна. Часто наблюдаемые брадиаритмии,
различного типа желудочковые тахикардии являются последствием тяжелой гипоксии.
Явления сонных апноэ вносят свой вклад в развитие ишемических изменений
миокарда, ведут к развитию инфаркта миокарда у пациентов с аортокоронарной
несостоятельностью [52].
Наиболее пристальное внимание ученых разных стран уделяется изучению
патогенетических механизмов развития СОАГС. Несмотря на это, четких
представлений, объясняющих все стороны этого феномена, не существует до
сегодняшнего дня. Менее всего оспариваемыми являются представления о процессах,
лежащих в основе развития окклюзии верхних дыхательных путей у пациентов СОАГС
[42].
Фарингиальный коллапс считается основной проблемой у пациентов СОАГС.
Особенностью коллапса является его развитие во время NREM
сна. Несмотря на то, что дыхательное усилие обычно постоянно, незначительная
обструкция глоточного отдела воздухоносных путей прекращает эффективную
вентиляцию во время каждого периода апноэ или гипопноэ. В обоих случаях гипоксия
и гиперкапния быстро приводят к вынужденному “неосознанному пробуждению” -
arousal (AR) - для восстановления воздухоносной функции и
нормальной вентиляции [42]. Локализация такой
воздухоносной обструкции фактически всегда располагается между хоанами и
эпиглоттисом, большей частью как позади небной занавески и мягкого неба (велофарингс),
так и позади языка (орофарингс) или в различных комбинациях первых двух. Реже
наблюдается коллапс воздухоносных путей, обнаруживаемый на уровне эпиглоттиса,
но это не является характерным для пациентов с обструкцией [49].
Аномалии строения глотки и ее функциональные нарушения являются второй
причиной коллапса верхних дыхательных путей (ДП)
во время сна [58]. Наиболее уязвимый воздухоносный
сегмент между хоанами и эпиглоттисом у человеческого организма имеет
недостаточную костную и жесткостную поддержку, в особенности передней и
латеральной глоточной стенок. Вот почему функциональные возможности этого
воздухоносного сегмента во многом зависят от активности различных глоточных
мышц-дилататоров. До тех пор, пока эти мышцы имеют достаточный тонус,
осуществляется поддержание воздухо-проводящей функции. Как правило, потеря
мышечной активности некоторыми или всеми указанными мышцами может уменьшать
размер воздухоносных путей или приводить к полному их коллапсу. Таким образом, в
человеческом организме существуют важные взаимоотношения между анатомией
глоточных воздухоносных путей и их размерами, подконтрольными мышцам-дилятаторам
[49].
Исследования по изучению различных проекций глоточного отдела дыхательных
путей показали, что пациенты с СОАГС как во время бодрствования, так и во время
сна имеют анатомически малый глоточный размер. Одинаковый результат был получен
при исследовании ДП с помощью компьютерной томографии [21],
ультразвуковой диагностики [46], и измерений
повышенного сопротивления верхних дыхательных путей (ПСВДП) воздушному
дыхательному потоку [54]: пациенты СОАГС имеют структурно
узкие воздухоносные пути. В одних случаях это происходило из-за отложения
“жировых подушек” в области шеи, что взаимосвязано с проблемой ожирения у таких
пациентов. В других случаях причиной являлись малые размеры нижней челюсти (микрогнатия),
приводящие к уменьшению воздухоносного размера. В третьих случаях,
гипертрофированные миндалины являются основной причиной глоточной узости. Таким
образом, обширные вариации различных причинных факторов у пациентов СОАГС,
объективно приводят к структурной узости и малым размерам воздухо-проводящего
глоточного пространства.
Кроме того, у пациентов СОАГС происходит выраженное падение мышечной
активности с наступлением сна, что отражает не только аномальный мышечный ответ
на наступление сна, но и утрату нейромышечной компенсации, существующей во время
бодрствования. Уменьшение мышечной активности у пациентов
СОАГС компрометирует воздухоносную потенцию, что приводит к началу периодов
апноэ или гипопноэ. Индуцируемое сном снижение мышечной активности у пациентов
СОАГС является производным от: а) утраты нейромышечной компенсации всех
фазических мышц; б) нормальным снижением активности тонической мускулатуры.
Такая комбинация эффектов сна приводит к недостаточной мышечной активности,
изменяющей воздухоносные возможности ДП [41].
Таким образом, можно сказать, что СОАГС является серьезной проблемой,
отрицательно влияющей на качество жизни пациента. Преобладание СОАГС в
средневозрастной группе у мужчин определяется такими факторами риска как
метаболические, обменные и алиментарные нарушения нормального веса тела, более
высокая подверженность стрессовым ситуациям и нагрузкам, табакокурение и
употребление алкоголя [59]. Основными маркерами болезни,
кроме избыточной дневной сонливости, можно считать стойкую артериальную
гипертензию, сочетающуюся с легочным сердцем, ишемической болезнью сердца и
сосудистой патологией. Вовлечение в процесс сердечно-сосудистой системы приводит
к возможности развития инсульта и инфаркта миокарда, приводящих к летальному
исходу [11]. Поэтому принято считать СОАГС состоянием,
резко уменьшающим длительность жизни пациентов [40].
Лечение соагс постоянным положительным давлением в дыхательных путях
было предложено Sullivan C.E. at al. в 1981 году [57].
В настоящее время данный вид лечения назначается приблизительно 80% всех
пациентов с диагностированным СОАГС обструктивного генеза. В англоязычной
литературе указанный метод получил название CPAP-терапия (Continuous Positive
Airway Pressure - постоянное положительное давление в воздухоносных путях).
Основным преимуществом использования СРАР-терапии является быстрый клинический
эффект при лечении СОАГС. Кроме этого данный метод может использоваться в виде
“пробного” лечения, которое можно отменить в случае непереносимости, в отличие
от хирургических вмешательств. Это особенно важно при легких формах СОАГС или в
том случае, когда сложно оценить влияние СОАГС на клиническую симптоматику у
пациента. Прибор для проведения CPAP-терапии представляет собой компрессор,
подающий в дыхательные пути через воздуховод и носовую маску постоянный поток
воздуха под давлением 2-30 см водн. ст. в течение ночного сна.
Современные CPAP-машины компактные (1,2- 2,0 кг), малошумные, позволяют
профильтровывать, увлажнять и обогревать доставляемый воздух, обеспечивают
точное дозирование давления и компенсацию возможных утечек. Кроме того, в
большинстве приборов предусмотрена функция постепенного повышения давления до
рабочего уровня в течение 5-45 минут, что облегчает процесс засыпания пациента.
Кратко показания к назначению CPAP можно сформулировать следующим образом
[3]: 1) CPAP-терапия эффективна у пациентов с клинически
значимым СОАГС; 2) СРАР-терапия может оказывать положительный эффект у пациентов
с клинически значимым дыханием Чейн-Стокса и апноэ во время сна центрального
генеза; 3) CPAP-терапия обычно не назначается лицам с “обычным” храпом без апноэ
во время сна или клинической симптоматики. В данных показаниях обращает на себя
внимание то обстоятельство, что для назначения лечения важен не только факт
наличия СОАГС как такового, но и клиническая значимость данных нарушений. В
настоящее время имеется тенденция назначать лечение больным СОАГС на основании
только клинической симптоматики, без учета величины
индекса AHI. С учетом того, что повышенная дневная
сонливость при СОАГС сопряжена со снижением работоспособности, значительным
увеличением частоты автомобильных катастроф [10] и
производственного травматизма, ряд авторов такой подход считают правомерным. В
последние несколько лет появились сообщения о пациентах с ПСВДП, у которых кроме
выраженной симптоматики отмечаются частые микро пробуждения. Когда не удается
выявить других причин микро пробуждений, представляется правомерным проведение
диагностического исследования с использованием аппарата CPAP, при котором
подбирается такое ДДП, которое приводит к исчезновению признаков ПСВДП и
нормализует сон пациента [18]. Если диагностическое
исследование оказывается успешным, рекомендуется проведение амбулаторного
лечения CPAP в течение 2-3 недель с последующей оценкой клинической
симптоматики. Продолжение лечения показано в случае исчезновения или
существенного уменьшения дневной сонливости и других сопутствующих симптомов
[17]. Таким образом, если при полисомнографическом
исследовании выявляется СОАГС, то следует предпринять попытку лечения с помощью
СРАР-терапии [3]. Лечение должно быть продолжено, если
отмечается четкая положительная динамика в отношении дневной сонливости и
нарушенных физиологических параметров (легочное сердце, опасные аритмии, ночная
стенокардия, артериальная гипертензия). В противоположность этому у пациентов с
незначительной клинической симптоматикой или “бессимптомных пациентов” показания
к длительному применению СРАР-терапии не определены.
Рациональный подход в настоящее время заключается в назначении СРАР-терапии,
последующей оценке ее эффективности и решения вопроса о необходимости
дальнейшего аппаратного лечения [25].
Не имеется абсолютных противопоказаний к использованию СРАР-терапии
[3]. Относительными противопоказаниями к CPAP-терапии
являются: буллезная эмфизема легких, пневмоторакс или пневмомедиастинум в
анамнезе, рецидивирующие синуситы и глазные инфекции [3].
Следует соблюдать осторожность при назначении CPAP чувствительным пациентам с
утечками спинномозговой жидкости, патологией крибриформной пластинки, травмой
головы или пневмоцефалией в анамнезе [28]. Наиболее
частыми осложнениями СРАР-терапии являются: локальное раздражение кожных
покровов, сухость слизистых носа и глотки (около 50%), заложенность носа/ринорея
(около 25%), раздражение глаз (около 25%) [50]. Реже
сообщается о аэрофагии (около 3%) [47]. Серьезные
осложнения наблюдались в единичных случаях. Имеются описания клинических случаев
конъюнктивита [53], пневмоцефалии [26],
бактериального менингита [4], массивного носового
кровотечения [56], наджелудочковой аритмии [38],
связанных с использованием CPAP-терапии. Не имеется ни одного сообщения о
пневмотораксе. Использование увлажнителей и подогревателей воздуха в дыхательном
контуре CPAP приборов может существенно уменьшить частоту осложнений со стороны
слизистой носоглотки. Применение более современных масок или носовых канюль
снижает вероятность раздражения глаз, обусловленного утечками из дыхательного
контура. Использование носовых канюль также позволяет избегать раздражения
кожных покровов [3]. У пациентов с нарушением носового
дыхания, обусловленным полипами, гипертрофией слизистой оболочки или
искривлением носовой перегородки требуется соответствующее хирургическое
вмешательство [15]. Сухость слизистой можно устранить
ингаляциями солевого раствора. При заложенности носа местно применяются мезатон
или беклометазон, при риноррее пер орально назначается эфедрин.
В идеале прибор CPAP следует использовать ежедневно в течение всего времени
сна. Однако каждый пациент имеет различную индивидуальную норму в отношении
длительности сна. В связи с этим крайне трудно определить среднюю должную
ежедневную длительность лечения. Krieger J.(1988) с соавт.
предлагали считать соблюдением режима лечения использование CPAP не менее 3
часов в сутки [29]. Другие авторы считали приемлемым
использование CPAP не менее 4 часов в сутки и не менее 70% от всех дней лечения
[28]. В дальнейшем были разработаны более объективные
методы оценки соблюдения режима лечения. При оценке времени работы аппарата
следует различать общее время работы, и эффективное лечебное время. Общее время
работы определяется количеством часов, в течение которых прибор был включен.
Эффективное лечебное время характеризуется количеством часов, в течение которых
через маску подавалось установленное лечебное давление. С целью определения
эффективного лечебного времени в дыхательный контур аппарата CPAP включается
датчик, который регистрирует параметры давления в процессе работы аппарата. Если
при включенном аппарате маска оказывается снята или возникают значительные
утечки, это приводит к существенному падению давления в дыхательном контуре,
что, соответственно, снижает общее время эффективного лечебного давления.
Соблюдение режима лечения коррелирует с тяжестью СОАГС [47].
Больные с тяжелыми расстройствами дыхания, во-первых, имеют более выраженную
клиническую симптоматику, в частности значительную дневную сонливость;
во-вторых, отмечают существенное улучшение состояния на фоне лечения. Таким
образом, их мотивация к постоянному лечению существенно выше чем у пациентов с
легким и среднетяжелым течением СОАГС, у которых дискомфорт, связанный с
лечением, может субъективно превосходить эффект самого лечения
[50].
Обычно, к концу первого месяца лечения у пациентов вырабатывается стереотип
использования аппарата [28]. Через 3 месяца от начала
лечения желательно провести повторную оценку и коррекцию. Если эффективность
терапии низка, следует рассмотреть альтернативные формы лечения. Важно отметить
тот факт, что если, несмотря на соблюдение режима лечения, у пациента
сохраняется дневная сонливость или другая клиническая симптоматика, необходимо
выполнить контрольное полисомнографическое исследование с коррекцией
управляемого режима давления в дыхательных путях (ДДП) для оценки адекватности
подобранного лечебного давления [29].
Список литературы:
- Вейн А.М. Медицина сна. // Терапевтический архив,
1991 - Т.4. - с.143-156.
- AARC-APT Clinical Practice Guideline: Polysomnography. // Respir. Care. -
1995. - V.40 (12). - P.1336-1343.
- American Thoracic Society. Indications and standards for use of nasal
continuous positive airway pressure (CPAP) in sleep apnea syndromes. // Am. J.
Respir. Care Med.- 1994.- V.150.- P. 1738-1745.
- Bamford C.R., Quan S.F. Bacterial meningitis. A possible complication of
nasal continuous positive airway pressure therapy in a patient with
obstructive sleep apnea syndrome and a mucocele. // Sleep. - 1993.- V.16.- P.
31-32.
- Bedell GN, Wilson WR, Seebohm PM. Pulmonary function in obese persons. //
J. Clin. Invest. - 1958. - V.37. - P.1049-1061.
- Berry DT, Webb WB, Block AJ, Switzer DA. Sleep-disordered breathing and
its comcomitants in a subclinical population. // Sleep. - 1986. -V.9. -
P.478-83.
- Burwell CS, Robin ED, Whaley RD. Extreme obesity associated with alveolar
hypoventilation and pickwickian syndrome. // Am. J. Med. - 1956. - V.21. -
P.811-818.
- Davies RJO, Stradling JR. The relationship between neck circumference,
radiographic pharyngeal anatomy, and the obstructive sleep apneoa syndrome. //
Eur. Respir. J. - 1990. - V.3. -P.509-14.
- Dempsey JA, Reddan W, Balke B. Work capacity determinants and physiologic
cost of weight supported breathing in obesity. // J. Appl. Physiol. - 1966. -
V.21. - P.1815-1820.
- Findley LJ, Unverzagt ME, Suratt PM. Automobile accidents involving
patients with obstructive sleep apnea. // Am. Rev. Pespir. Dis. - 1988. -
V.138. - P.337-40.
- Fletcher EC, DeBehnke RD, Lovoi MS, Gorin AB. Undiagnosed sleep apnea in
patients with essential hypertension. // Ann. Intern. Med. - 1985. - V.103. -
P.190-5.
- Fritts HW, Filler J, Fishman AP. The efficiency of ventilation during
voluntary hyperpnea: Studies in normal subjects and in dyspneic patients with
either chronic pulmonary emphysema or obesity. // J. Clin. Invest. - 1959. -
V.38. - P.1339-1348.
- Gastaut H, Tassinari CA, Duron B. Polygraphic study of the episodic
diurnal and nocturnal (hypnic and respiratory) manifestations of the Pickwick
syndrome. // Brain. Res. - 1965. - V.2. - P.167-186.
- Gould G, Whyte KF, Rhind GB. The sleep hypopnea syndrome. // Am. Rev.
Respir. Dis. - 1988. - V.137. - P.895-898.
- Grunstein R.R., Dodd M.J., Costas L., Sullivan C.E. Home nasal CPAP for
sleep apnea-acceptance of home therapy and its usefulness. // Aust. NZ. J. Med.-
1986- V.16.- P. 635.
- Guilleminault C, Stoohs R, Duncan S. Snoring (I): Daytime sleepiness in
regular heavy snorers. // Chest. - 1991. - V.99. - P.40-48.
- Guilleminault C., Stoohs R., Clerk A., Cetel M., Maistros P. A cause of
excessive daytime sleepiness. The upper airway resistance syndrome. // Chest.-
1993.- V.104.- P. 781-787.
- Guilleminault C., Stoohs R., Clerk A., Simmons J., Labanowski M. From
obstructive sleep apnea syndrome to upper airway resistance syndrome:
consistency of daytime sleepiness. // Sleep.- 1992.- V.15.- P.13-16.
- Guilleminault C., Stoohs R., Duncan S. Snoring: daytime sleepiness in
regular heavy snorers. // Chest.- 1991.- V.99.- P. 40-48.
- Guilleminault C., Tilkian A., Dement W.C. The sleep apnea syndromes. //
Ann. Rev. Med. - 1976. - V.27.-P.465-84.
- Haponik E, Smith P, Bohlman M, Allan R, Goldman S, Bleecher E.
Computerized tomography in obstructive sleep apnea: correlation of airway size
with physiology during sleep and wakefulness. // Am. Rev. Resp. Dis. - 1983. -
V.127. - P.221.
- Harman E, Wynne JW, Block AJ. Sleep disordered breathing and desaturation
in obesity bypass patients (abstract). // Am. Rev. Respir. Dis. - 1979. -
V.119. - P.125.
- Hoffstein V, Brown I, Zamel N. Changes in pharyngeal size with recumbency
and the application of continuous positive airway pressure in patients with
obstructive sleep apnea. // Am. Rev. Respir. Dis. - 1986. - V.133. - P.147.
- Holley HS, Milic-Emili J, Becklake MR. Regional distribution of pulmonary
ventilation and perfusion in obesity. // J. Clin. Invest. - 1967. - V.46. -
P.475-481.
- Issa F.G., Costas L.J.V., Berthon-Jones M., McCauley V.J., Bruderer J.,
Sullivan C.E. Nasal CPAP treatment for obstructive sleep apnea (OSA): long
term experience with 117 patients // Am. Rev. Respir. Dis.- 1985.- V.131.-
P.108.
- Jarjour N.N., Wilson P. Pneumocephalus associated with nasal continuous
positive airway pressure in a patient with sleep apnea syndrome // Chest.-
1989.- V.96.- P.1425-1426.
- Jung R, Kuhlo W. Neurophysiological studies of abnormal night sleep and
the Pickwickian syndrome.// Progr. Brain. Res. - 1967. - V.18. - P.141-159.
- Kribbs N.B., Pack A.I., Kline L.R., Smith P.L., Schwartz A.R., Schubert
N.M. Objective measurement of patterns of nasal CPAP use by patients with
obstructive sleep apnea // Am. Rev. Respir. Dis.- 1993.- V.147.- P. 887-895.
- Krieger J., Kurtz D. Objective measurement of compliance with nasal CPAP
treatment for obstructive sleep apnoea syndrome // Eur. Respir. J.- 1988.-
V.1.- P. 436-438.
- Kuhlo W. Sleep attacks with apnoe.The Abnormalities of Sleep. // Men.Proc.
15th Eur. Meet. Electroencephalogr., Bologna. - 1967. - P.205-207.
- Lavie P. Incidence of sleep apnea in a presumably healthy working
population. // Sleep. - 1983. - V.6. - P.312-8.
- Liistro G., Stanescu D.C., Veriter C., Rodenstein D.O., Aubert-Tulkens G.
Pattern of snoring in obstructive sleep apnea patients and in heavy snorers //
Sleep.- 1991.- V.14.- P.517-525.
- Loube DI, Loube AA, Mitler MM. Weight loss for obstructive sleep apnea:
optimal therapy for obese patients.// J. Am. Diet. Assoc.-
1994.-V.194.-P.1291-5.
- Lourenco RV. Diaphragm activity in obesity. // J. Clin. Invest. - 1969. -
V.48. - P.1609-1614.
- Luce JM. Respiratory complications of obesity. // Chest. - 1980. - V.78. -
P.4.
- Lyons HH, Huang CT. Therapeutic use of progesterone in alveolar
hypoventilation associated with obesity. // Am. J. Med. - 1968. - V.44. -
P.881-888.
- Martikainen K, Hasan J, Urponen H, Vuori I, Partinen M. Daytime sleepness:
a risk factor in community life. // Acta. Neurol. Scand. - 1992.-V.86. -
P.337-41.
- Meurice J.C., Mergy J., Rostykus C., Dore P., Paquerreau J., Patte F.
Atrial arrhythmia as a complication of nalal CPAP // Chest.- 1992.- V.102.- P.
640-642.
- Millman RP, Carlisle CC, McGarvey ST, Eveloff SE, Levinson PD. Body fat
distribution and sleep apnea severity in women. // Chest.-
1995.-V.107.-P.362-6.
- National Heart, Lung, and Blood Institute.Fact Book: Fiscal Year 1993. //
U.S. Department of Health Servicees, U.S. Public Health Service, National
Institutes of Health. - February 1994.
- Onal E, Lopata M. Periodic breathing and the pathogenesis of occlusive
sleep apneas. // Am. Rev. Resp. Dis. - 1982. - V.126. - P.676-680.
- Phillipson EA and Sullivan CE. Arousal: The forgotten responce to
respiratory stimuli. // Ann. Rev. Resp. Dis. - 1978. - V.118. - P.807-809.
- Rapoport D.M. Treatment of sleep apnea syndrome // Mt. Sinai J. Med.-
1994.- V.61.- P. 123-130.
- Rapoport DM, Garay SM, Epstein H, Goldring RM. Hypercapnia in the
obstructive sleep apnea syndrome. A reevaluation of the “Pickwickian syndrome”.
// Chest. - 1986. - V.89. - P.627-34.
- Rechtschaffen A, Kales A. A manual of standardized terminology, techniques
and scoring system for sleep stages of human subjects. // Los Angeles: Brain
Information Service/Brain Research Institute, University of California at Los
Angeles. - 1968.
- Rivlin J, Hoffstein V, Klabfleish J, McNicholas W, Zamel N, Bryan A. Upper
airway morphology in patients with idiopatic obstructive sleep apnea. // Am.
Rev. Resp. Dis. - 1984. - V.129.- P.335.
- Rolfe I.L., Olson L.G., Saunders N.A. Long-term acceptance of continuous
positive airway pressure on obstructive sleep apnea // Am. Rev. Respir. Dis.
1991.- V.144.- P.1130-1133.
- Roth T, Rochrs TA, Conway WA. Behavioral morbidity of apnea. // Sem.
Respir. Med. - 1988. - V.9. - P.554-9.
- Rubinstein I, Slutsky AS, Zamel N, and Hoffstein V. Paradoxical glottic
narrowing in patients with severe obstructive sleep apnea. // J. Clin. Invest.
- 1988. - V.81. - P.1051-1055.
- Sanders M.H., Gruendl C.A., Rogers R.M. Patient compliance with nasal CPAP
therapy for sleep apnea // Chest. - 1986. - V.90. - P.330-333.
- Scharf SM, Garshick E, Brown R. Screening for subclinical sleep-disordered
breathing. // Sleep. - 1990. - V.13. - P.344-353.
- Shepard JW Jr, Garrison MW, Grither DA, Dolan GF. Relationship of
ventricular ectopy to oxyhemoglobin desaturation in patients with obstructive
sleep apnea. // Chest. - 1985. - V.88. - P.335-40.
- Stauffer J.L., Fayter N.A., MacLurg B.J. Conjunctivitis from nasal CPAP
apparatus // Chest.- 1984.- V.86.- P. 802.
- Stauffer JL, Zwillich CW, Cadieux RJ, Bixler ED, Kales A, Varano LA, White
DP. Pharyngeal size and resistance in obstructive sleep apnea. // Am. Rev.
Resp. Dis. - 1987. - V.136. - P.623-627.
- Strohl KP, Novak RD, Singer W. Insulin levels, blood pressure and sleep
apnea. // Sleep. - 1994. - V.17. - P.614-8.
- Strumpf D.A., Harrop P., Dobbin J., Millman R.P. Massive epistaxis from
nasal CPAP therapy // Chest. - 1989. - V.95 - P.141.
- SuIlivan, C. E., Issa F.G., Berthon-Jones M., Eves L. Reversal of
obstructive steep apnoea by continuous positive airways pressure applied
through the nares. // Lancet.- 1981.- V.1.- P.862-865.
- Von Lunteran E and Strohl KP. The muscles of upper airways. // Clin. Chest.
Med. - 1986. - V.7 - P.171.
- Yong T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurence of
sleep disordered breathing among middle-aged adults. // N. Engl. J. Med. -
1993. - V.328 - P.1230-5.
Если вы заметили орфографическую, стилистическую или другую ошибку на этой странице, просто выделите ошибку мышью и нажмите Ctrl+Enter. Выделенный текст будет немедленно отослан редактору
|
|
|
|

