Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Влияние комбинированного препарата (лизиноприл и
гидрохлортиазид)на состояние сосудистого русла у женщин с эстрогенодефицитом
М. М. Хабибулина, кандидат медицинских наук
ГБОУ ВПО УГМА МЗ РФ, Екатеринбург
Артериальная гипертензия (АГ) — одно из
наиболее распространенных заболеваний, характеризующееся высокой частотой
развития сердечно-сосудистых осложнений, нередко имеющих фатальные последствия.
В настоящее время в Российской Федерации продолжается рост сердечно-сосудистой
заболеваемости. В структуре общей смертности и инвалидизации населения более 50%
приходится на долю болезней сердечно-сосудистой системы, что дает основания
рассматривать сложившуюся ситуацию как угрожающую для национальной безопасности
России (Чазов Е. И. и соавт., 2005).
Ряд исследований, проведенных в последние годы, подтвердили прогностическую
ценность исследования жесткости артерий в разных когортах больных. Спектр
сосудистых нарушений при АГ шире и включает в себя неатероматозную перестройку
артерий, сопровождающуюся нарушением их демпфирующей функции с изменением
постнагрузки левого желудочка (ЛЖ) и коронарной перфузии. В настоящее время
рассматривается концепция о дисфункции эндотелия, регулирующего равновесие таких
процессов, как поддержание тонуса и проницаемости сосудов, гемостаза и местного
воспаления, в том числе и при АГ [1, 2]. По-видимому, эндотелиальная дисфункция,
в совокупности с имеющимися факторами риска сердечно-сосудистой патологии,
способствует ее развитию и прогрессированию. Кроме того, ряд исследователей
полагают, что снижение функции эндотелия выступает в качестве предиктора
неблагоприятного исхода кардиоваскулярной патологии [3–6]. Сердечно-сосудистые
осложнения являются не только результатом различных взаимосвязанных процессов,
именуемых атеросклерозом и артериосклерозом, эндотелиальной дисфункцией, но и,
как показали многочисленные исследования, структурно-функциональной перестройкой
отделов сердца, также способной ухудшить прогноз течения основного заболевания и
повысить риск развития сердечно-сосудистых осложнений [7–10]. Мужчины и женщины
имеют много общих факторов риска сердечно-сосудистых осложнений. Вместе с тем у
женщин имеется дополнительный фактор риска — угасание функции яичников и
развитие дефицита женских половых гормонов, прежде всего, эстрогенов, в
постменопаузе [11–13]. Целым рядом исследований установлен факт увеличения
частоты таких заболеваний, как ишемическая болезнь сердца (ИБС) и АГ в этом
периоде [14–18]. Несмотря на то, что в настоящее время достигнуты определенные
успехи в изучении сердечно-сосудистой системы при ряде патологических состояний,
исследования этих процессов у женщин, страдающих АГ в различные периоды их
«гормональной» жизни, малочисленны и носят крайне фрагментарный и нередко
противоречивый характер. Вместе с тем изучение этих вопросов имеет несомненный
научный и практический интерес, так как позволяет разработать рекомендации,
направленные на повышение качества обследования женщин с АГ в периоде
пременопаузы, с целью предупреждения развития сердечно-сосудистых осложнений в
последующие периоды жизни женщины — менопаузе и постменопаузе.
Антигипертензивная терапия существенно снижает риск заболеваемости и
смертности от сердечно-сосудистых причин [19, 20]. Однако большинство работ,
касающихся проблем гипертонической болезни (ГБ) у женщин среднего и старшего
возраста, охватывают в основном постменопаузальный период [21, 22], уделяя
значительно меньше внимания доклимактерическому периоду. Крайне мало данных,
позволяющих выработать стандарты в отношении диагностики и лечения ГБ у женщин в
этом периоде. Имеющиеся в литературе сведения о течении АГ в перименопаузальном
и постменопаузальном периодах не однозначны в вопросах взаимосвязи с уровнем
половых гормонов крови, в то время как существует единое мнение об усилении
проявлений АГ у женщин в этом возрасте.
В настоящее время в распоряжении врача имеется большое количество
фармакологических средств, вызывающих при длительном лечении снижение
показателей артериального давления (АД), обратное развитие гипертрофии ЛЖ,
ишемии миокарда, эндотелиальной дисфункции периферических артерий [23–27]. Нам
представляется обоснованной попытка применения препарата Ко-Диротон,
оказывающего влияние на уровень АД, процесс ремоделирования сосудистого русла и
левых камер сердца, дисфункцию эндотелия, в связи с чем улучшение состояния
пациента под влиянием терапии рассматривается как компонент, способствующий
регрессии АГ. Целью нашего исследования явилось изучение показателей
структурно-функционального состояния сосудистого русла у женщин с АГ в позднем
фертильном периоде (ПФП) со сниженным уровнем эстрадиола и влияние Ко-Диротона
на эти параметры.
Материалы и методы исследования
В исследование на условиях добровольного информированного согласия, в
соответствии с принятыми этическими нормами были включены 112 женщин с АГ II
стадии в ПФП (возраст 35–45 лет, сохранение ритма и характера менструаций,
снижение уровня эстрадиола (среднее значение 0,34 ± 0,04 пкг/мл) и повышение
уровня фолликулостимулирующего гормона (ФСГ) в сыворотке крови (среднее значение
17,84 ± 1,15 МЕ/мл)), средний возраст 38,7 ± 3,3 года. Длительность заболевания
АГ составила в среднем 3,8 ± 1,8 года. Средний уровень систолического
артериального давления 148,37 ± 7,91 мм рт. ст. и средний уровень
диастолического АД 98,2 ± 5,75 мм рт. ст. В исследование не вошли пациентки с
ИБС, хронической сердечной недостаточностью (ХСН), дислипидемией, сахарным
диабетом, реноваскулярной патологией. У всех женщин собирался полный анамнез,
проводилось обязательное обследование, включающее маммографию, УЗИ органов
малого таза, взятие мазков, в том числе и на онкоцитологию. Контроль за
состоянием больных, измерение АД по методу Короткова в положении сидя трижды,
фиксируя в протоколе средние показания; частота сердечных сокращений (ЧСС) —
аналогичным образом по пульсу и аускультативно (дополнительно женщины вели
дневники по АД, в которых фиксировали значения АД и ЧСС утром и вечером),
регистрация электрокардиограммы (ЭКГ) проводились до лечения, во время лечения и
через 6 месяцев лечения.
Пациенткам отменялась предшествующая антигипертензивная терапия (только для
пациенток, регулярно принимающих гипотензивные препараты). Через 3–5 дней
«чистого фона» больные начинали лечение Ко-Диротоном (лизиноприл в дозе 10 мг и
гидрохлортиазид 12,5 мг в сутки однократно). За критерий эффективности
антигипертензивной терапии по АД клиническому принимали снижение диастолического
артериального давления (ДАД) клинического на 10% или на 10 мм рт. ст. и
систолического артериального давления (САД) клинического на 15 мм рт. ст. от
исходного уровня. Целевым уровнем АД клинического на фоне терапии считалось
достижение уровня менее 140/90 мм рт. ст.
Для оценки структурно-функционального состояния сосудистого русла у пациенток
с АГ в период пременопаузы в зависимости от статуса половых гормонов всем
пациенткам, включенным в исследование, до и после лечения выполнялось дуплексное
сканирование общих сонных артерий (ОСА) на аппарате «Acuson 128 XP/10» (фирма
Acuson, США). При сканировании ОСА измеряли толщину комплекса интима-медиа на
расстоянии 1 см проксимальнее бифуркации по задней стенке. АД на плечевой
артерии (ПА) измеряли дважды по стандартной методике, в расчет принимали среднее
САД и ДАД и пульсовое давление (ПД) по двум измерениям. В М-режиме с синхронной
записью ЭКГ измеряли просвет ОСА в систолу и диастолу. Для сравнения между
группами использовали среднее значение, равное половине суммы систолического и
диастолического диаметров. Для оценки эластичности ОСА использовали коэффициент
растяжимости (КР) и индекс жесткости (ИЖ). КР рассчитывали по формуле КР = 2 ×
ΔД/ ΔПД/Д (10-3/кПа), где Д — диаметр артерии, ΔД — изменение
диаметра артерии в течение сердечного цикла, ΔПД — пульсовое артериальное
давление. ИЖ рассчитывали по формуле ИЖ = log (САД/ДАД)/(ΔД/Д), где Д — диаметр
артерии, ΔД изменение диаметра артерии в течение сердечного цикла. Из
гемодинамических параметров внутрисосудистого кровотока анализировали
максимальную систолическую скорость кровотока (см/с), индекс резистентности
(ИР).
Статистическая и математическая обработка результатов проводилась на
персональном компьютере с помощью пакета прикладных программ Statistica 6.0.
Данные представлены в виде средних арифметических величин и стандартного
отклонения. Различия считались достоверными при р < 0,05.
Результаты
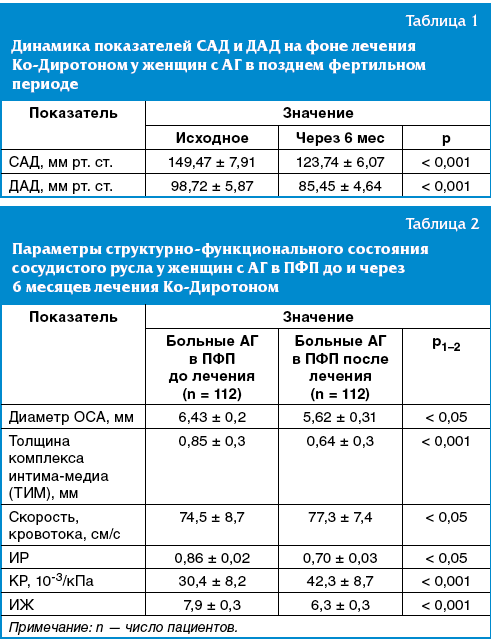
У всех пациенток с АГ в ПФП использование Ко-Диротона позволило получить
хороший антигипертензивный эффект через 2 недели, который удерживался на
протяжении 6 месяцев (р < 0,001) (табл. 1).
Сравнительный анализ параметров структурно-функционального состояния
сосудистого русла у женщин с АГ в ПФП до и после лечения представлен в табл. 2.
При сравнительном анализе диаметра сонных артерий в исследуемой клинической
группе до лечения наблюдалось расширение среднего диаметра сонных артерий у
пациенток с АГ в ПФП (р < 0,05). Скорость кровотока в ОСА также оказалась
достоверно ниже до лечения (р < 0,05). ИР оказался достоверно выше у пациенток с
АГ до лечения (р < 0,001). Эластические свойства стенки сонной артерии
улучшились после лечения, показатель ИЖ оказался достоверно ниже после лечения у
пациенток с АГ в ПФП (р < 0,001). Таким образом, полученные данные убедительно
свидетельствуют о положительном влиянии Ко-Диротона на улучшение эластичности
стенки ОСА и снижении ее жесткости у пациенток с АГ в ПФП со сниженным уровнем
эстрадиола.
Крупные артерии выполняют в организме две основные функции — транспортную и
демпфирующую. Структурно-функциональные изменения стенки, возникающие при АГ,
приводят к нарушению демпфирующей функции сосудов, способствуя увеличению
пульсового давления и постнагрузки сердца [28]. Упругость сосудистой стенки
определяется эластиновыми волокнами межклеточного матрикса, а прочность и
жесткость — коллагеновыми [29, 30]. Повышение давления при АГ у женщин в ПФП с
эстрогенодефицитом вызывает изменение соотношения волокон при росте общей
концентрации в сосудистой стенке. В результате она становится жестче и для ее
нормального функционирования требуется более высокое давление, чем прежде.
Замыкается циклический процесс, потенцирующий дальнейшее прогрессирование
заболевания. Согласно формуле Хагена–Пуазейля, небольшое увеличение радиуса
сосуда приводит к значительному снижению кровотока, что подразумевает уменьшение
скорости кровотока в ней, а небольшая скорость обеспечивает оптимальные условия
доставки прокоагулянтных факторов к заинтересованному участку сосудистой стенки
и способствует развитию межмолекулярного взаимодействия, агрегации и адгезии
форменных элементов, таким образом, прогрессированию атеросклероза [8, 9,
31–33]. В настоящем исследовании наблюдалось расширение просвета ОСА до лечения
и связанное с расширением просвета сосуда снижение скорости кровотока в сонных
артериях прямолинейного хода, без гемодинамически значимых стенозов у пациенток,
страдающих АГ в ПФП с нарушением статуса половых гормонов, что свидетельствует о
более выраженных структурно-функциональных изменениях стенки в виде более
выраженного артериосклероза. Под влиянием Ко-Диротона наблюдалось улучшение
эластичности стенки ОСА и снижение ее жесткости у пациенток с АГ в ПФП с
измененным уровнем гормонов.
Изменение показателей эндотелиальной функции по данным пробы с
постокклюзионной реактивной гиперемией у пациенток с АГ в ПФП на фоне проводимой
терапии
Согласно современным данным, одно из важнейших мест в развитии и
прогрессировании кардиоваскулярной патологии занимает дисфункция эндотелия,
регулирующая равновесие таких процессов, как поддержание тонуса и структуры
сосудов, гемостаза, местного воспаления и проницаемости сосудистой стенки.
Наличие поражения органов мишеней и, прежде всего, сосудистого русла с развитием
артериосклероза позволяют предполагать снижение вазомоторной функции эндотелия у
женщин с АГ в ПФП с измененным гормональным фоном.
Как видно из данных, представленных в табл. 3, при проведении пробы с
постокклюзионной реактивной гиперемией для пациенток, страдающих АГ в ПФП,
характерно увеличение показателей прироста диаметра плечевой артерии после
6-месячной терапии Ко-Диротоном. Процент дилатации плечевой артерии (ПА)
оказался достоверно ниже до лечения (р < 0,001). При этом следует отметить, что
у пациенток с АГ в ПФП и измененным гормональным статусом при проведении пробы
реактивной гиперемии на фоне достоверного снижения вазомоторной функции
эндотелия ПА, в каждом втором случае (в 49,1% случаев) выявлялся инерционный тип
вазомоторной реакции, для которого характерно отсутствие реакции в течение 2
минут от начала пробы, что может свидетельствовать о доклинических (начальных)
признаках атеросклероза. После 6-месячного лечения Ко-Диротоном инерционный тип
вазомотороной реакции выявлялся лишь в каждом четвертом случае (24,7%).

Кроме того, при оценке внутрипросветных диаметров сосудов эластического и
мышечного типов выявлено, что у пациенток с АГ в ПФП сонная артерия расширена
относительно размера ПА (р < 0,001). Складывается впечатление, что артерии с
преобладанием эластиновых структур подвержены воздействию гемодинамических
факторов в большей степени, чем артерии с гладкомышечным и коллагеновыми
волокнами, а выявленная тесная прямая корреляционная связь между уровнем САД и
увеличением диаметра просвета ОСА у пациенток с АГ и гипоэстрогенией (r = 0,56;
р = 0,001) может свидетельствовать о том, что ведущее место в расширении ОСА как
признака ремоделирования и доклинического атеросклеротического поражения
сосудистой стенки занимает уровень САД, по-видимому, обусловленный более
выраженной вариабельностью этого показателя на фоне нарушенного гормонального
фона. Выявленная обратная корреляционная связь между напряжением сдвига на
эндотелии общих сонных артерий и толщиной комплекса интима-медиа у женщин с АГ в
ПФП со сниженным уровнем эстрадиола до лечения (r = –0,74; р = 0,0001), а также
диаметром ОСА в данной клинической группе (r = –0,58; р = 0,0001) может
свидетельствовать о том, что расширение просвета снижает напряжение сдвига на
эндотелии, что может путем влияния на механизмы выработки оксида азота
стимулировать констрикцию мышечных клеток медии, увеличение тонуса и толщины
сосудистой стенки. Кроме того, у пациенток с АГ в позднем фертильном периоде и
дефицитом эстрадиола наблюдался низкий дилатирующий ответ эндотелия при пробе с
реактивной гиперемией, что, по-видимому, связано с более глубокими органическими
изменениями в гладких мышечных клетках сосудистой стенки. Это может быть связано
с увеличением массы гладкомышечных клеток на фоне дефицита эстрогенов, что
увеличивает степень вазоконстрикции в ответ на нейрогормоны, приводит к
повышению периферического сосудистого сопротивления и способствует стабилизации
и усугублению АГ [13]. Утолщение сосудистой стенки, лейкоцитарное пропитывание,
механическое повреждение избыточным давлением крови запускают процесс апоптоза
эндотелиальных клеток и предрасполагают сосуды к развитию и прогрессированию
атеросклероза [1, 7, 28]. Кроме того, при прогрессирующем снижении уровня
эстрадиола возрастает уровень фибриногена, для которого характерно увеличение
вязкости крови, гиперкоагуляция, увеличение агрегации тромбоцитов и повреждение
эритроцитов [9], что также влияет на состояние сосудистого русла и способствует
усугублению атеросклеротических изменений сосудистой стенки.
Наличие поражения органов-мишеней и, прежде всего, сосудистого русла с
развитием артериосклероза, проявления которого были обнаружены нами у женщин с
АГ в ПФП, позволяют предполагать снижение вазомоторной функции эндотелия у
пациенток с АГ с измененным статусом половых гормонов. Согласно современным
данным, одно из важнейших мест в развитии и прогрессировании кардиоваскулярной
патологии занимает дисфункция эндотелия, регулирующая равновесие таких
процессов, как поддержание тонуса и структуры сосудов, гемостаза, местного
воспаления и проницаемости сосудистой стенки.
Ингибиторы ангиотензинпревращающего фермента (иАПФ) способны улучшать функцию
эндотелия и тормозить атерогенез. Клиническое исследование TREND (Trial on
Reversing ENdotelial Dysfunction) подтвердило данные многочисленных
экспериментальных работ о наличии у иАПФ эндотелиймодулирующих и
антиатеросклеротических свойств. При эндотелиальной дисфункции у женщин с АГ в
ПФП ремоделирование сосудистой стенки может наступить из-за дефицита эстрогенов,
который оказывает отрицательное влияние на сосудистую стенку, к тому же
эндотелий сосуда постоянно испытывает нагрузку давлением и повреждается из-за
высокого АД, и NО, который эндотелий секретирует для расширения просвета
сосудов, не выделяется в нужном количестве (развивается дефицит NО),
увеличивается жесткость сосуда, теряется эластичность, вазодилатация снижается,
снижается доставка кислорода, может развиться ишемия.
Таким образом, при проведении обследования женщин с АГ в ПФП необходимо
учитывать нарушение статуса половых гормонов как самостоятельного фактора риска
прогрессирования АГ. Женщин с АГ в ПФП, имеющих нарушение баланса половых
гормонов, необходимо выделять в отдельную группу диспансерного наблюдения.
Характерное для этих пациенток быстрое прогрессирование ремоделирования
сосудистой стенки с развитием артериосклероза и эндотелиальной дисфункции, а
также сочетание таких независимых факторов, как высокие цифры АД, дисбаланс
половых гормонов, определяющих переход адаптивного ремоделирования в
дезадаптивный с развитием нарушений гемодинамики и развитие ХСН, требует
привлечения к наблюдению не только кардиолога, но и гинеколога-эндокринолога для
определения тактики ведения данной категории. Нами отмечено улучшение функции
эндотелия и растяжимости плечевой артерии на фоне длительной терапии
Ко-Диротоном у женщин с АГ в ПФП с дисгормонозом. Представленные в статье данные
важны для практического врача, так как позволяют прогнозировать течение АГ,
изменения в структурно-функциональном состоянии сосудистого русла в данный и
следующий периоды жизни женщины — период менопаузы и постменопаузы.
Выводы
- Ко-Диротон является высокоэффективным средством лечения АГ. У всех
пациенток с АГ в ПФП использование этого препарата позволило получить хороший
антигипертензивный эффект.
- При углубленном дуплексном сканировании ОСА установлено, что у пациенток с
АГ в ПФП с дефицитом эстрадиола имеет место расширение просвета ОСА, снижение
скорости кровотока в сонных артериях прямолинейного хода, без гемодинамически
значимых стенозов, что свидетельствует о выраженных структурно-функциональных
изменениях сосудистой стенки в виде артериосклероза.
- У пациенток с АГ в позднем фертильном периоде и нарушенным гормональным
фоном при проведении пробы с реактивной гиперемией на фоне достоверного
снижения вазомоторной функции эндотелия практически в каждом втором случае
(49,1% случаев) выявляется инерционный тип вазомоторной реакции, что
свидетельствует о существенной роли дисгормоноза в прогрессировании АГ и,
прежде всего, за счет увеличения жесткости сосудистой стенки и развития
эндотелиальной дисфункции.
- Ко-Диротон улучшает структурно-функциональные изменения сосудистой стенки
ОСА, положительно влияет на функцию эндотелия, снижает жесткость сосудистой
стенки артерий.
Литература
- Козлова М. В. Особенности нарушений микроциркуляции у женщин
постменопаузального периода с артериальной гипертонией: автореферат дис. …
канд. мед. наук. Иваново, 2008. 20 с.
- Майчук Е. Ю., Воеводина И. В., Пиляева Н. Г. и др. Состояние
сосудов у женщин перименопаузального периода / Материалы конгресса ЧиЛ. С.
23–27.
- Баталова А. А., Ховаева Я. Б., Берг М. Д. Этапность нарушения
эндотелиальной функции при развитии гипертонической болезни и атеросклероза //
Кардиоваскулярная терапия и профилактика: мат. Рос. нац. конгр. кардиологов.
2008. № 7 (6). С. 44: Прил. 1.
- Иванова О. В., Балахонова Т. В., Соболева Г. Н. и др. Состояние
эндотелийзависимой вазодилатации плечевой артерии у больных гипертонической
болезнью, оцениваемое с помощью ультразвука высокого разряжения //
Кардиология. 1997. № 7. С. 41–46.
- Нелидова А. В., Бунова С. С., Остапенко В. А. Диагностические
особенности раннего выявления дисфункции эндотелия у больных гипертонической
болезнью // Кардиоваскулярная терапия и профилактика: мат. Рос. национ. конгр.
кардиологов. 2008. № 7 (6). С. 262–263: прил. 1.
- Lusher T. F., Barton M. Endothelins and endothelin receptor
antagonists. Theraupetic concentrations for novel class of cardiovascular
drugs // Circulation. 2000. Vol. 102. P. 2324–2332.
- Диагностика и коррекция нарушений липидного обмена с целью профилактики и
лечения атеросклероза / Российские рекомендации, IV пересмотр. М., 2009. С.
20–22.
- Кудряшова О. Ю., Затейщиков Д. А., Сидоренко Б. А. Возможная роль
эстрогенов в профилактике и лечении атеросклероза у женщин после наступления
менопаузы // Кардиология. 1998. № 4. С. 51–58.
- Маколкин В. И., Подзолков В. И., Павлов В. И. Состояние
микроциркуляции при гипертонической болезни // Кардиология. 2002. № 7. С.
36–40.
- Panza J. A., Quyyumi A. A., Brush J. E. Abnormal endothelium–dependent
vascular relaxation in patients with essential hypertension // N Engl J Med.
1990. Vol. 323. P. 22–27.
- Руководство по климактерию / Под ред. В. П. Сметник, В. И. Кулакова. М.:
Медицинское информационное агентство, 2001. 685. 62 с.
- Шардин, С. А., Барац С. С., Бенедиктов И. И. Сердечно-сосудистая
патология у женщин. Изд-во Уральского университета, 1997. С. 187.
- Mendelsone M. E., Karas R. The protective effects of estrogen on
cardiovascular system // N. Engl. J. Med. 1999. Vol. 340. P. 1801–1811.
- Кательницкая Л. И., Хаишева Л. А. Гендерные особенности
клинического течения больных с гипертонической болезнью: фокус на сосуды //
Кардиоваскулярная терапия и профилактика: мат. Рос. национ. конгр.
кардиологов. 2008. № 7 (6). С. 173: прил. 1.
- Подзолкова Н. М., Подзолков В. И., Можарова Л. Г. Гормональный
континуум женского здоровья: эволюция сердечно-сосудистого риска от менархе до
менопаузы // Сердце. 2005. № 6. С. 276–279.
- Сметник В. П. Защитное влияние эстрогенов на сердечно-сосудистую
систему // Сonsilium medicum. 2002. Экстравыпуск. С. 3–6.
- Mendelsone M. E. Genomic and nongenomic effects of estrogen in
the vasculature // Am. J. Cardiol. 2002. Vol. 9. P. 3–6.
- Pechere-Bertschi A., Burnier M. Female sex hormones, salt, and
blood pressure regulation // Am J Hypertens. 2004. № 17. Р. 994?10?01.
- Глезер М. Г. Результаты Российского исследования эффективности и
безопасности лизиноприла при АГ под контролем суточного мониторирования АД //
Проблемы женского здоровья. 2007. № 1. Т. 2. С. 1–8.
- Карпов Ю. А. Ингибиторы АПФ: от снижения АД до профилактики
осложнений и улучшения прогноза // Сердце. 2002. № 4. С. 192–194.
- Моисеев В. С., Кобалава Ж. Д. АРГУС. АГ у лиц старших возрастных
групп. Монография. М.: ООО «МИА», 2002; 448.
- Кисляк О. А. Ингибитор АПФ лизиноприл в лечении пожилых пациентов
с систоло-диастолической АГ // Лечебное дело. 2007. № 2. С. 2–7.
- Постникова С. Л. иАПФ в кардиологической практике // Русский мед.
журнал. 2004. № 12 (7). С. 496–500.
- Дядык А. И., Багрий А. Э., Яровая Н. Ф., Щукина Е. В. Влияние
ингибиторов ангиотензинпревращающего фермента на гипертрофию левого желудочка
сердца у больных артериальными гипертониями // Тер. арх. 1995. № 8. С. 65–67.
- Майчук Е. Ю., Юренева С. В., Воеводина И. В. и др. Использование
лизиноприла для лечения АГ у женщин после овариэктомии при климактерическом
синдроме/Человек и лекарство: тезисы докладов Х Российского национального
конгресса. М., 2003. С. 256.
- Беленков Ю. Н., Мареев В. Ю., Агеев Ф. Т. Ингибиторы АПФ в
лечении сердечно-сосудистых заболеваний. М., 2002. 86 с.
- Татаренко О. К., Носенко Е. М., Алехин М. Н. и др. Влияние
ингибитора ангиотензинпревращающего фермента моэксиприла на центральную и
периферическую гемодинамику у женщин с умеренной АГ в период менопаузы //
Кардиология. 1999. Т. 39, № 1. С. 48–53.
- Ишманова А. Р., Закирова А. Н., Карамова И. М. и др.
Функциональное состояние сосудистого эндотелия и липидные сдвиги у женщин с
артериальной гипертензией и метаболическим синдромом // Кардиоваскулярная
терапия и профилактика: мат. Рос. национ. конгр. кардиологов. 2008. № 7 (6).
С. 158–15: прил. 1.
- Осипова Е. В., Мельникова Л. В., Бартош Л. Ф. Эластические
свойства стенки общих сонных артерий при артериальной гипертензии в
зависимости от группы сердечно-сосудстого риска // Кардиоваскулярная терапия и
профилактика: мат. Рос. национ. конгр. кардиологов. 2008. № 7 (6). С. 273–274:
прил. 1.
- Протасов К. В., Синкевич Д. А., Дзизинский А. А. и др. Оценка
взаимосвязей параметров морфофункционального состояния общей сонной артерии
при различных вариантах артериальной гипертонии // Кардиоваскулярная терапия и
профилактика: мат. Рос. национ. конгр. кардиологов. 2008. № 7 (6). С. 303:
прил. 1.
- Рабинович Р. М. Анализ факторов, влияющих на состояние кровотока
в бассейне внутренней сонной артерии при артериальной гипертонии //
Терапевтический архив. 2008. Т. 80. № 9. С. 18–21.
- Рябиков А. Н., Малютина С. К., Иванов С. В. Жесткость
артериальной стенки и отражение пульсовой волны: связь с установленными и
обсуждаемыми детерминантами сердечно-сосудистых заболеваний / Материалы
конгресса ЧиЛ. 2007. М., 2007. С. 11–14.
- Ховаева Я. Б., Сыромятникова Т. Н., Головской Б. В. и др.
Состояние интима-медианного комплекса артерий разного типа в зависимости от
уровня артериального давления // Материалы XI Всероссийского
научно-образовательного форума. Кардиология. М., 2009. С. 304–305.
Статья опубликована в журнале
Лечащий Врач

