Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Тилорон как средство выбора для профилактики и лечения острых
респираторных вирусных инфекций
О. В. Калюжин, доктор медицинских наук, профессор
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Тяжело переоценить медико-социальную значимость острых респираторных вирусных
инфекций (ОРВИ), которые не только лидируют в структуре заболеваемости
населения, но и провоцируют возникновение вторичных бактериальных инфекций
(пневмонии, отита и др.) и обострения хронических легочных заболеваний (астмы,
хронической обструктивной болезни легких и др.) [1–4]. Вместе с тем только для
вирусов гриппа из более чем двухсот возбудителей ОРВИ разработаны и широко
используются профилактические вакцины. По данным последних системных обзоров и
метаанализов, эффективность специфической иммунопрофилактики гриппа существенно
варьирует от сезона к сезону вплоть до полного отсутствия, что связанно с
высокой антигенной изменчивостью вирусов [5, 6]. Единственной группой
противовирусных химиопрепаратов, применение которых с учетом чувствительности к
ним циркулирующих в последние годы возбудителей гриппа признано рациональным
ведущими экспертами мира, являются ингибиторы нейраминидазы. Однако степень их
действенности остается предметом дискуссии, особенно в отношении развития
осложнений этого заболевания [7–9]. Кроме того, широкое использование
осельтавимира и занамивира неизбежно ведет к селекции и экспансии резистентных
штаммов вирусов гриппа, в том числе номенклатурно идентифицируемых как A
(H1N1)pdm2009, которые уже выявляются среди пациентов [10]. В отношении
множества других ОРВИ, в частности респираторно-синцитиальной, рино-, корона- и
метапневмовирусных инфекций, а также парагриппа, даже в наиболее развитых
странах мира эффективных вакцин и противовирусных химиопрепаратов, внедренных в
клиническую практику, пока нет. Основные неотвеченные вызовы, стоящие пред
практическими врачами и разработчиками средств специфической профилактики и
лечения вирусных инфекций дыхательных путей, были предметом недавнего детального
рассмотрения [11]. Недостижимость эффективного контроля сезонной заболеваемости
ОРВИ с помощью вакцинации и этиотропной химиотерапии говорит о необходимости
применения препаратов, воздействующих на наиболее универсальные врожденные
механизмы противовирусной защиты, на этапах сезонной/экстренной профилактики и
лечения этих заболеваний [12].
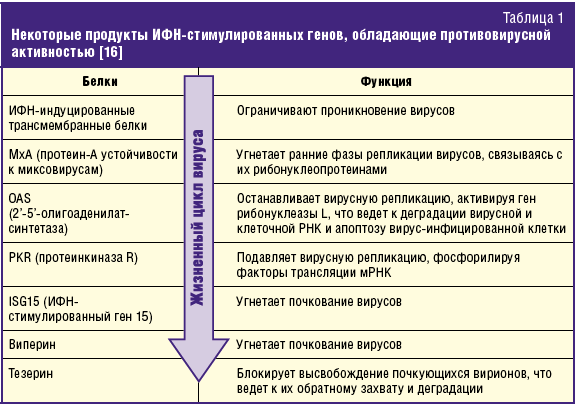
Центральным звеном противовирусного иммунного ответа на инвазию возбудителей
ОРВИ являются интерфероны (ИФН). Если ИФН II типа (ИФН-γ) главным образом
активирует адаптивные клеточные реакции в отношении вирус-инфицированных клеток,
то ИФН I (ИФН-α/β и др.) и III типов (ИФН-λ) обеспечивают врожденный
противовирусный ответ, индуцируя экспрессию более чем 300 так называемых
ИФН-стимулированных генов (interferon stimulated genes, ISG), многие из
продуктов которых обладают прямой или опосредованной противовирусной активностью
[13–15]. Важно то, что эти продукты блокируют все ключевые этапы жизненного
цикла респираторных вирусов, начиная от их проникновения в клетку и заканчивая
почкованием/высвобождением дочерних вирионов (табл. 1). Кроме того, ИФН I типа
потенцируют адаптивные клеточные противовирусные реакции [13].
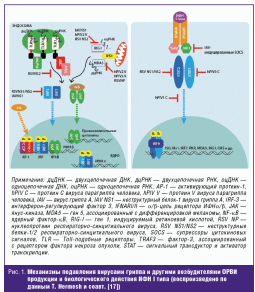
В ходе эволюционной гонки вооружений с совершенствующимися механизмами
противоинфекционного ответа многие возбудители ОРВИ приобрели способность
подавлять врожденные защитные механизмы, в том числе выработку и биологическую
функцию ИФН I типа. Ключевые молекулярные механизмы иммуносупрессивного действия
вирусов гриппа, парагриппа, респираторно-синцитиального вируса и некоторых
других патогенов дыхательных путей раскрыты (рис. 1).
Вышесказанное говорит о необходимости коррекции вызванных респираторными
вирусами расстройств врожденной защиты, в частности, дефектов системы ИФН.
Однако роль ИФН I и III типов при ОРВИ неоднозначна, и функция этих цитокинов
не ограничивается противовирусной защитой [11]. Доказано, что избыточная
продукция ИФН I и III типов является одним из основных факторов развития
вторичных бактериальных инфекций, в том числе пневмококковой пневмонии [3], и
вирус-индуцированных обострений астмы [18]. По этой причине задачи
иммунокорригирующей терапии на разных этапах вирусной инфекции дыхательных путей
существенно различаются.
При внедрении вируса в организм и в первые часы клинических проявлений ОРВИ
рациональной стратегией представляется восполнение недостаточной/подавленной
продукции ИФН I типа за счет экзогенного введения этих цитокинов или стимуляции
их выработки. Напротив, на пике воспалительных проявлений и на поздних этапах
вирусной инфекции, когда, несмотря на иммуносупрессивные свойства патогенов,
высокий уровень продукции ИФН и некоторых других провоспалительных цитокинов
становится фактором повреждения и развития осложнений, целью иммуномодуляции
является подавление выработки этих эндогенных флогогенных медиаторов.
Целесообразность временной супрессии избыточной продукции эндогенных
медиаторов повреждения макроорганизма в острую фазу заболеваний неоднократно
подчеркивалась нами [19–22] и сейчас уже не вызывает дискуссии.
Возможность использования тилорона (2,7-бис-[2-(диэтиламино)этокси]флуорен-9-она)
дигидрохлорида — первого в мире и, пожалуй, наиболее изученного перорального
синтетического индуктора ИФН [23] — как универсального иммунокорректора, который
в зависимости от режима введения, исходного состояния макроорганизма, стадии
инфекционного процесса оказывает разнонаправленные эффекты на продукцию ИФН и
других провоспалительных цитокинов, обсуждалась ранее [11]. Эти свойства
позволяют тилорону смещать баланс повреждения и интенсивности иммунного ответа в
благоприятную для организма зону, в которой вероятность развития тяжелых форм
ОРВИ и их осложнений минимизируется или, по крайней мере, существенно снижается
(рис. 2).
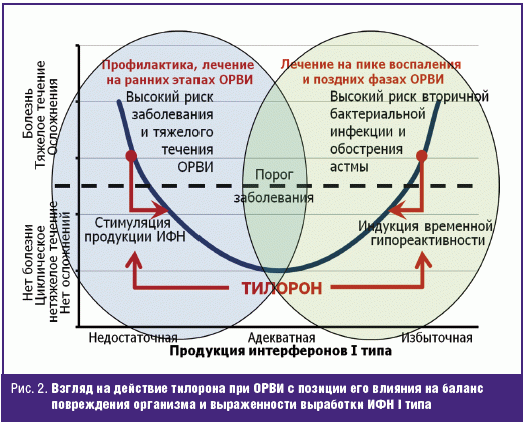
В этой связи описанная еще в 1970-е гг. способность тилорона при ежедневных
повторных введениях вызывать обратимое состояние гипореактивности, при котором
дальнейшая стимуляция продукции цитокинов не происходит, является отнюдь не
отрицательным качеством, как считали некоторые специалисты 30–40 лет назад [24],
а, наоборот, весьма полезным свойством при использовании этого препарата на пике
воспалительных проявлений ОРВИ.
Очевидно, именно с временным снижением избыточной выработки ИФН и других
провоспалительных веществ в значительной степени связана эффективность тилорона
у взрослых и детей как средства лечения гриппа и других ОРВИ, подтвержденная в
целой серии клинических исследований. Важно то, что этот иммуномодулятор при
терапевтическом использовании не только уменьшал продолжительность и
выраженность основных симптомов вирусных инфекций дыхательных путей, но и снижал
частоту и тяжесть осложнений этих заболеваний [25].
Не менее выражена способность тилорона предотвращать возникновение ОРВИ при
профилактическом приеме. В этом случае действие препарата обусловлено его
классификационным свойством индуцировать выработку ИФН I и II типов и ряда
других цитокинов, обеспечивающих врожденную противовирусную защиту и
стимулирующих клеточные адаптивные иммунные реакции в отношении
вирус-инфицированных клеток.
Описана высокая профилактическая эффективность Лавомакса, включающего в
качестве активного ингредиента тилорона дигидрохлорид, у работников крупного
лечебно-профилактического учреждения (Московского научно-исследовательского
онкологического института имени П. А. Герцена), входящих в группу повышенного
риска ОРВИ, в период высокой сезонной заболеваемости. Применение Лавомакса по
125 мг per os 1 раз в неделю на протяжении 6 недель приводило к четырехкратному
снижению заболеваемости и пятикратному сокращению средней продолжительности ОРВИ
в течение периода приема препарата и двух недель дополнительного наблюдения в
сравнении с такой же по численности и сопоставимой по другим признакам
контрольной группой (табл. 2). Среди заболевших обеих групп преобладающими
возбудителями были вирусы парагриппа и аденовирусы, а в этот период по городу
Москве, кроме указанных патогенов, частой находкой при ОРВИ был
респираторно-синцитиальный вирус (данные Роспотребнадзора), который выявлен и у
одного участника испытания. Эти данные говорят о широком спектре
профилактического действия тилорона в отношении респираторных вирусов. В ходе
исследования зарегистрировано два случая нежелательных явлений. В одном случае
на каждый прием препарата у испытуемого отмечался жидкий стул 2–3 раза в течение
первых суток. Эти проявления не требовали отмены индуктора ИФН. В другом случае
у участника исследования выявлены зудящие кожные высыпания, которые усилились
после второго приема Лавомакса и стали причиной прекращения приема препарата
[26].

С декабря 2006 г. по май 2007 г. на базе Областной клинической больницы
города Тулы и Городской поликлиники города Новомосковска изучен профилактический
эффект Лавомакса в сравнении с действием субъединичных противогриппозных вакцин
(Гриппол, Инфлювак). За участниками исследования наблюдали в течение 6 недель
применения препарата по вышеуказанной схеме и еще 12 дополнительных недель.
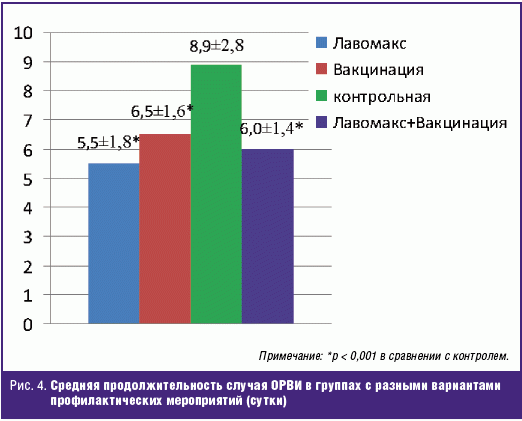
Прием тилорона здоровыми добровольцами (n = 340) приводил к восьмикратному
снижению заболеваемости ОРВИ (рис. 3) и сокращению более чем на одну треть
средней продолжительности случая респираторной инфекции (рис. 4) в сравнении с
контрольной группой (n = 260), участники которой не получали специфических и
неспецифических превентивных средств. При этом профилактическая действенность
индуктора ИФН в отношении гриппоподобных заболеваний с лабораторно не
верифицированным возбудителем была сопоставима с таковой, зарегистрированной в
группе добровольцев (n = 340), которые за 2 недели — 9 месяцев до включения в
исследование были подвержены противогриппозной иммунизации. Использование
Лавомакса в ограниченной группе участников исследования (n = 40), прошедших
вакцинацию Грипполом или Инфлюваком, не выявило синергизма этих средств
специфической и неспецифической иммунопрофилактики в снижении заболеваемости и
средней длительности ОРВИ, что отчасти можно объяснить небольшой численностью
этой группы.
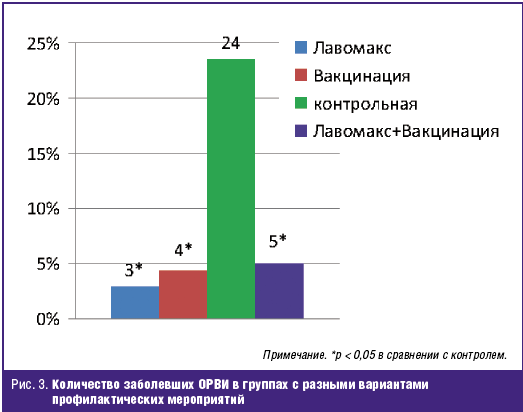
В ходе данного опыта применения Лавомакса не зарегистрировано ни одного
нежелательного явления.
В этой работе верификацию респираторных патогенов не проводили. Однако с
учетом того, что среди участников выявлена высокая эффективность
противогриппозных вакцин, можно предположить, что заболеваемость ОРВИ у лиц,
включенных в исследование, в период наблюдения была в значительной степени
связана с вирусами гриппа. Это можно рассматривать как аргумент в поддержку
тезиса о способности Лавомакса предотвращать грипп.
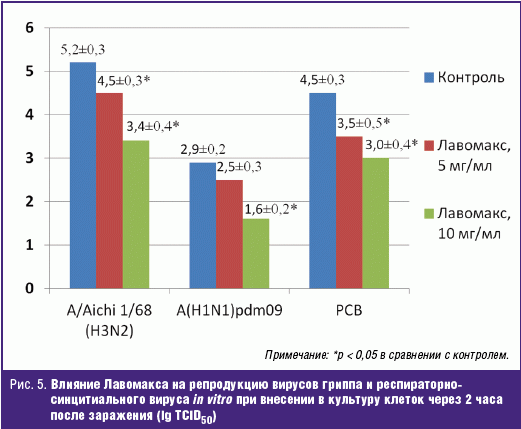
Проведенное в НИИ вирусологии им. Д. И. Ивановского изучение влияния
Лавомакса на репродукцию возбудителей гриппа типа А (А/Aichi 1/68 (H3N2) и A(H1N1)pdm09)
и респираторно-синцитиального вируса в культурах чувствительных к этим патогенам
клеток (соответственно клеток почки собаки MDCK и эпителиоидных клеток человека
HEp-2) выявило прямое противовирусное действие препарата. Детальное описание
методики этого исследования и его результатов станет предметом отдельной
публикации; в рамках настоящего сообщения приведены только данные, касающиеся
подавления репродукции вирусов при внесении Лавомакса в культуру клеток в
«лечебном» режиме (через 2 часа после заражения). Степень угнетения репликации
двух штаммов возбудителей гриппа, относящихся к двум наиболее актуальным
сероподтипам, и респираторно-синцитиального вируса, оцениваемая по снижению их
инфекционного титра, была умеренной и колебалась в пределах 1,5–1,8 Δlg TCID50
(рис. 5). При этом концентрации, в которой тилорон проявлял виростатическое
действие (5 и 10 мкг/мл), не только не оказывают цитопатического действия на
зараженные клетки, но и являются вполне достижимыми в плазме крови и тканях
человека при пероральном приеме препарата в терапевтической дозировке. Эти
данные коррелировали с результатами определения противовирусной активности
Лавомакса в условиях тех же моделей in vitro с помощью иммуноферментного
анализа: подавление репродукции А/Aichi 1/68 (H3N2), A(H1N1)pdm09 и
респираторно-синцитиального вируса при «лечебном» использовании препарата (10
мкг/мл) составляло 48,2 ± 5,3, 28,6 ± 6,0 и 45,3 ± 5,7% соответственно.
Вклад выявленной умеренной виростатической активности тилорона в его
терапевтическое действие при ОРВИ еще предстоит выяснить.
Вместе с тем представленные данные заслуживают пристального внимания, так как
они не только укрепляют убежденность в целесообразности использования этого
индуктора ИФН при ОРВИ, но и раскрывают возможности для увеличения его
клинической эффективности путем совершенствования и персонализации режима
применения с учетом вновь обнаруженного противовирусного действия. Еще одной
отправной точкой для оптимизации тактических схем назначения и более широкого
использования тилорона в клинической практике может стать новый взгляд на
механизмы его фармакологических эффектов с позиций модуляции баланса повреждения
организма и выраженности врожденного иммунного ответа.
Таким образом, тилорон сегодня может быть признан средством выбора для
профилактики и лечения ОРВИ, в том числе гриппа, а рассмотренные в настоящем
сообщении свойства препарата говорят о перспективах расширения сферы его
клинического применения в условиях дефицита эффективных противовирусных
химиопрепаратов и вакцин.
Литература
- Seto W. H., Conly J. M., Pessoa-Silva C. L. et al. Infection
prevention and control measures for acute respiratory infections in healthcare
settings: an update // East Mediterr Health J. 2013; 19 (Suppl. 1): S39–47.
- Rudan I., O’Brien K. L., Nair H. et al. Epidemiology and etiology
of childhood pneumonia in 2010: estimates of incidence, severe morbidity,
mortality, underlying risk factors and causative pathogens for 192 countries
// J Glob Health. 2013; 3 (1): 10401. doi: 10.7189/jogh.03.010401.
- Bosch A. A. T. M., Biesbroek G., Trzcinski K. et al. Viral and
bacterial interactions in the upper respiratory tract // PLoS Pathog. 2013; 9
(1): e1003057. doi: 10.1371/journal.ppat.1003057.
- Gavala M., Bertics P. J., Gern J. E. Rhinoviruses, allergic
inflammation, and asthma // Immunol Rev. 2011; 242 (1): 69–90. doi:
10.1111/j.1600–065 X.2011.01031.x.
- Manzoli L., Ioannidis J. P. A., Flacco M. E. et al. Effectiveness
and harms of seasonal and pandemic influenza vaccines in children, adults and
elderly: a critical review and re-analysis of 15 meta-analyses // Hum Vaccin
Immunother. 2012; 8 (7): 851–862. doi:10.4161/hv.19917.
- Osterholm M. T., Kelley N. S., Sommer A., Belongia E. A. Efficacy
and effectiveness of influenza vaccines: a systematic review and meta-analysis
// Lancet Infect Dis. 2012; 12 (1): 36–44. doi: 10.1016/S1473–3099
(11.70295-X.
- Hsu J., Santesso N., Mustafa R. et al. Antivirals for treatment
of influenza: a systematic review and meta-analysis of observational studies
// Ann Intern Med. 2012; 156: 512–524.
- Jefferson T., Jones M. A., Doshi P. et al. Neuraminidase
inhibitors for preventing and treating influenza in healthy adults and
children // Cochrane Database Syst Rev. 2012; 1: CD008965. doi:
10.1002/14651858.CD008965.pub3.
- Michiels B., Van Puyenbroeck K., Verhoeven V. et al. The value of
neuraminidase inhibitors for the prevention and treatment of seasonal
influenza: a systematic review of systematic reviews // PLoS ONE. 2013, 8 (4):
e60348. doi: 10.1371/journal.pone.0060348.
- Dixit R., Khandaker G., Ilgoutz S. Emergence of oseltamivir
resistance // Infectious Disorders — Drug Targets. 2013; 13 (1): 35–45.
- Калюжин О. В. Острые респираторные вирусные инфекции: современные
вызовы, новый взгляд на место индукторов интерферонов в профилактике и терапии
// Лечащий Врач. 2013. 9: 78–84.
- Караулов А. В., Калюжин О. В. Иммунотропные препараты: принципы
применения и клиническая эффективность. М.: МЦФЭР; 2007.
- Fensterl V., Sen G. C. Interferons and viral infections //
Biofactors. 2009; 35 (1): 14–20. doi: 10.1002/biof.6.
- Караулов А. В., Калюжин О. В. Цитокины: биологическое действие и
клиническое применение. В кн.: Успехи клинической иммунологии и аллергологии /
Под ред. А. В. Караулова. Т. 1. М.: РАЕН, 2000: 193–205.
- Levy D. E., Marie I. J., Durbin J. E. Induction and function of
type I and III interferon in response to viral infection // Curr Opin Virol.
2011; 1 (6): 476–486. doi: 10.1016/j.coviro.2011.11.001.
- Van de Sandt C. E., Kreijtz J. H. C. M., Rimmelzwaan G. F.
Evasion of influenza A viruses from innate and adaptive immune responses //
Viruses. 2012; 4 (9): 1438–1476. doi: 10.3390/v4091438.
- Hermesh T., Moltedo B., Lopez C. B., Moran T. M. Buying time-the
immune system determinants of the incubation period to respiratory viruses //
Viruses. 2010; 2 (11): 2541–2558. doi: 10.3390/v2112541.
- Miller E. K., Hernandez J. Z., Wimmenauer V. et al. A mechanistic
role for type III IFN-λ1 in asthma exacerbations mediated by human
rhinoviruses // Am J Respir Crit Care Med. 2012; 185 (5): 508–516.
- Абидов М. Т., Баштаненко А. Ф., Нелюбов М. В. и др. Регуляция
иммунных реакций в лечении хронических и острых воспалительных заболеваний //
Якутский медицинский журнал. 2004; № 3 (7): 58–60.
- Абидов М. Т., Калюжин О. В., Нелюбов М. В. Иммунотерапия острых и
хронических воспалительных заболеваний // Tera Medica Nova. 2001; № 2: 3–7.
- Караулов А. В., Калюжин О. В., Ликов В. Ф. Подходы к
иммунотерапии воспалительных заболеваний // Кремлевская медицина. Клинический
вестник. 2002; № 1: 62–64.
- Караулов А. В., Сокуренко С. И., Калюжин О. В., Евсегнеева И. В.
Направленная регуляция иммунных реакций в профилактике и лечении заболеваний
человека // Иммунопатология, аллергология, инфектология. 2000; 1: 7–13.
- Krueger R. F., Mayer G. D. Tilorone hydrochloride: an orally
active antiviral agent // Science. 1970; 169: 1213–1214.
- Stringfellow D. A. Production of the interferon protein:
hyporesponsiveness // Tex Rep Biol Med. 1977; 35: 126–131.
- Максимов М. Л. Рациональный выбор индуктора интерферонов для
лечения и профилактики острых вирусных инфекций // Справочник поликлинического
врача. 2012; № 7: 9–12.
- Лыткина И. Н., Гренкова Т. А. Профилактическая эффективность
препарата Лавомакс при гриппе и ОРВИ // Врач. 2010; № 4: 64–67.
Статья опубликована в журнале
Лечащий Врач

