Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Комплексная
клинико-функциональная оценка тонкой кишки при
метаболическом синдроме
Я.М. Вахрушев,
М.В. Ляпина
ГБОУ ВПО «Ижевская государственная медицинская
академия», кафедра пропедевтики внутренних
болезней, г. Ижевск.
Резюме
Цель исследования: комплексное изучение
функционального состояния тонкой кишки (ТК) при
метаболическом синдроме (МС).
Материалы и методы. Обследовано 120
больных с МС. В подтверждении МС использованы
критерии диагностики, предложенные Всероссийским
научным обществом кардиологов в 2009 году. При
обследовании ТК, помимо клинических данных,
использованы результаты исследования моторной,
пищеварительной и всасывательной функций. Изучены
особенности изменений гормонального, вегетативного
статуса и липидного обмена у больных с МС.
Результаты. У большинства (82,9 %)
больных МС отмечены клинические местные и общие
признаки поражения ТК. При изучении
функционального состояния ТК отмечены нарушения на
всех этапах гидролизно-резорбционного конвейера на
фоне гипомоторной дискинезии в постпрандиальном
периоде и гиперсимпатикотонии у больных с МС.
Выявлены патогенетические закономерности,
касающиеся роли гормонов в нарушении
пищеварительной, всасывательной и двигательной
функций кишечника при МС.
Заключение. Результаты наших
исследований позволяют полагать, что изменения
функционального состояния ТК, выявленные при МС,
являются важным звеном сложного патогенетического
круга метаболического синдрома.
Ключевые слова: метаболический синдром;
функциональное состояние тонкой кишки; гормоны;
вегетативный статус.
ДГР — дуодено-гастральный рефлюкс, ДПК —
двенадцатиперстная кишка, ЖКТ — желудочно-кишечный
тракт, ИМТ — индекс массы тела, КА — коэффициент
атерогенности, ЛПВП — липопротеины высокой
плотности, МС — метаболический синдром, ОТ —
окружность талии, ПЭГЭГ — периферическая
электрогастроэнтерография, Тг — триглицериды, ТК —
тонкая кишка, ТТГ — тиреотропный гормон, Хс —
общий холестерин
Метаболический синдром (МС) представляет собой
комплекс глубоких обменных нарушений,
сопровождающихся абдоминальным ожирением,
артериальной гипертензией, дислипидемией, сахарным
диабетом 2-го типа или нарушением толерантности к
глюкозе и сопряжённой с ними
инсулинорезистентностью [3, 12, 22, 24, 26, 27,
28]. Основные составляющие каскада нарушений при
МС тесно связаны с функциональным состоянием
пищеварительной системы. Органы пищеварения могут
играть триггерную роль в патогенезе основных
кластеров МС, нередко и сами они становятся
органами-мишенями и конечными этапами проявлений
дислипидемии [4, 5, 11]. Пищеварительный тракт
можно рассматривать как главную «репетиционную
сцену» МС, где уже на ранних стадиях формируются
основные патогенетические механизмы данного
синдрома [2].
В последнее время большой интерес вызывает
изучение роли тонкой кишки (ТК) в развитии МС,
являющейся одним из центральных органов в
регуляции обмена веществ [6, 7, 15]. Тем не менее,
у пациентов с МС функциональное состояние ТК
изучено недостаточно. Это связано с трудоёмкостью
и инвазивностью методик исследования ТК.
Задачами нашей работы являлись, во-первых,
характеристика клинического течения энтерального
поражения при МС, во-вторых, комплексное
исследование функционального состояния ТК,
в-третьих, изучение роли нейро-гормональных
факторов в нарушении функций ТК, и, наконец,
выяснение сопряжённости нарушений функций ТК и
липидного обмена.
Материалы и методы
Обследовано 120 больных с МС, который
подтверждался с помощью критериев диагностики,
предложенных Всероссийским научным обществом
кардиологов в 2009 г [10]. Больные были в возрасте
от 32 до 75 лет. Женщин было 66 (55,0 %), мужчин —
54 (45,0 %). Средний возраст у мужчин составил
49,45±1,55 лет, у женщин — 58,61±1,8 лет. В
результате комплексных исследований нами выявлены
патологические изменения пищевода у 57 % больных с
МС, заболевания печени и билиарного тракта — у 41
%, патологические изменения со стороны желудка и
двенадцатиперстной кишки — у 63 %, заболевания
поджелудочной железы — у 89 %.
Основные методы обследования для выявления
ожирения включали антропометрию — измерение веса,
роста, окружности талии (ОТ), расчет индекса массы
тела ( ИМТ). ИМТ (индекс Кетле) определяли по
формуле: ИМТ = вес (кг)/рост (м)2.
Состояние вегетативного тонуса у больных с МС
оценивали по индексу Кердо, который рассчитывали
по формуле: (1 — диастолическое артериальное
давление/ пульс) × 100. Величину индекса Кердо
оценивали по номограмме, значения выше +5
расценивали как преобладание симпатического
тонуса, ниже - 5 — преобладание парасимпатического
тонуса [28].
Состояние углеводного обмена оценивали с
помощью перорального глюкозотолерантного теста
путем исследования содержания глюкозы в
капиллярной крови натощак и через 1 и 2 часа после
перорального приема 75 г глюкозы, растворённой в
200 мл воды.
Оценка липидного обмена проводилась по
содержанию в плазме крови общего холестерина (Хс),
Хc липопротеинов высокой плотности (ЛПВП),
триглицеридов (Тг ). У р о в е н ь Хс, ХсЛПВП, Тг
определяли на анализаторе F P - 9 0 1 ( M ) фирмы
« L a b s y s t e m s » ( F i n l a n d ) ,
полученные результаты выражали в ммоль/л. В
соответствии с полученными данными определяли
коэффициент атерогенности (КА) по формуле
КА = (Хс-ХсЛПВП)/ХсЛПВП,
при этом КА от 3 до 4 соответствовал умеренному
риску, КА ≥ 4 — высокому риску развития
сердечно-сосудистых осложнений.
Изучение базального уровня гормонов в
периферической крови (инсулина, кортизола,
гастрина, тиреотропного гормона — ТТГ, свободного
тироксина — Т4) проводилось методом
электрохемилюминесцентного иммуноанализа с помощью
анализатора IMMULITE фирмы «Siemens». Исходя из
концентрации иммунореактивного инсулина и глюкозы,
рассчитывался индекс инсулинорезистентности HOMA–IR
по формуле:
HOMA–IR =
инсулин натощак (мкМЕ/мл) × глюкоза натощак (ммоль/л)
: 22,5
Для изолированного исследования резорбтивных
процессов использованы вещества, не подвергающиеся
ферментативной обработке в кишке: глюкоза,
D-ксилоза. Концентрацию глюкозы в крови натощак и
прирост её в течение двух часов после нагрузки
углеводами определяли глюкооксидантным
энзиматическим методом. Содержание D-ксилозы в
моче определяли методом, предложенным Roe и Rice,
после приёма её внутрь в количестве 5 г в
пятичасовой порции мочи. Состояние пристеночного
пищеварения оценивалось по результатам усвоения в
тонкой кишке дисахарида сахарозы. Для
характеристики полостного пищеварения в тонкой
кишке использована проба с растворимым крахмалом.
У всех обследованных проводили изучение
копрограммы и определение эластазы-1 в кале.
В изучении моторно-эвакуаторной функции ТК
применялась периферическая
электрогастроэнтерография (ПЭГЭГ) с использованием
приборов ЭГГ-4М, модифицированного нами частотным
фильтром для измерения биопотенциалов ТК, и «Гастроскан-ГЭМ»
(НПП «Исток-Система» г. Фрязино). Исследование
проводили в два этапа: 1 этап — утром натощак — 40
минут; 2 этап — после стандартного завтрака (200
мл тёплого чая, 4 г сахара, 100г белого хлеба) —
40 минут. Проведение 2-х этапов исследования
позволяет оценивать функциональную и органическую
патологию ЖКТ, особенно его верхних отделов —
желудка, двенадцатиперстной кишки (ДПК) и тощей
кишки [19, 20]. При этом учитывали числовые
значения, характеризующие энергию (суммарную (Pi)
и по частотным спектрам (Ps)), процентное
отношение вклада каждого отдела ЖКТ в суммарную
мощность (Pi/Ps)), ритмичность сокращений каждого
отдела ЖКТ (Kritm), а также коэффициент
соотношения (Pi/P(i+1)), представляющий собой
отношение электрической активности вышележащего
отдела к нижележащему (последний характеризует
эвакуаторную функцию). На основе анализа ритма,
частоты сокращений и амплитуды зубцов определялся
тип двигательной активности ТК.
Результаты специальных
лабораторно-инструментальных исследований
сравнивали с показателями контрольной группы,
которую составили 45 практически здоровых лиц.
Результаты исследования представлены в
международных единицах СИ и подвергнуты
статистической обработке, которая включала
традиционные методики вычисления относительных (Р)
и средних величин (М) с определением их ошибки
(±m). Оценка достоверности различий показателей и
средних величин осуществлялась с использованием
параметрических (критерий Стьюдента (t),
достоверными считались различия при p<0,05)
критериев. Для определения наличия связи между
признаками использовался коэффициент парной
корреляции Пирсона (r).
Результаты и обсуждение
Обязательный критерий МС — центральный тип
ожирения (ОТ более 94 см у мужчин, более 80 см у
женщин), наблюдался у всех (100 %) исследуемых
больных. При этом избыточную массу тела (ИМТ = 25
— 29,9 кг/м2) имели 23 пациента (18,9 %), ожирение
I степени (ИМТ = 30 — 34,9 кг/м2) — 63
(52,8 %), ожирение II степени (ИМТ = 35 — 39,9
кг/м2) — 23 (18,9 %), ожирение III
степени (ИМТ 40 кг/м2 и более) — 11(9,4
%).
Нарушения углеводного обмена носили различный
характер: нарушенная гликемия натощак была
выявлена у 21 больного (17,5 %), у остальных
больных (82,5 %) наблюдалось нарушение
толерантности к глюкозе. Повышение показателя
индекса НОМА выявлено у всех больных, включенных в
исследование. Средний уровень индекса НОМА
соответствовал 4,22+0,8 и был выше среднего
показателя контрольной группы — 2,05±0,00, p<0,05.
При этом превышение этого показателя более чем в 2
раза отмечалось у 50 % пациентов, что
свидетельствует о наличии выраженной
инсулинорезистентности.
Основными клиническими симптомами поражения
кишечника при МС были вздутие живота (82,9 %),
чувство тяжести в животе после еды (43 %) и
нарушение стула (63 %) в виде запора (29 %),
полифекалии (47 %), диареи (32 %), чередования
запоров и поносов (18 %). В 66,5 % случаев отмечен
болевой синдром в околопупочной области,
характерный для поражения тонкой кишки.
При физикальном обследовании выявлены симптомы
полигиповитаминоза и качественных расстройств
трофики, как проявления общего энтерального
поражения (ломкость ногтей, выпадение волос,
сухость кожи, фолликулярный кератоз, ангулярный
стоматит, кровоточивость дёсен, глоссит) у 48 %
больных. Обложенность языка желтовато-белым
налётом выявлена в 96,7 % случаев, болезненность в
точке Поргеса и околопупочной области — в 62 %,
болезненность при пальпации отделов толстой кишки
— в 35,0 % случаев.
У больных с МС наблюдается нарушение
мембранного и полостного этапов пищеварения. Так,
при проведении нагрузочной пробы с сахарозой
прирост уровня глюкозы в течение 30 минут в
сравнении с контролем (2,5±0,14 ммоль/л)
существенно не отличался (2,6±0,22 ммоль/л, р >
0,05), а через 60 минут был достоверно ниже
(1,36±0,26 ммоль/л и 2,7±0,38 ммоль/л,
соответственно, р < 0,05). Изменение усвоения
сахарозы может быть связано не только с
подавлением собственно кишечного пищеварения, но и
с нарушением адсорбции ферментов (главным образом
панкреатических), принимающих участие в мембранном
пищеварении. Деятельность этих двух систем тесно
связана [16, 21].
Несмотря на более высокий уровень гликемии
натощак, прирост после приёма крахмала, в
сравнении с контролем, у больных был достоверно
ниже как через 30 минут (0,4±0,02 ммоль/л и
1,54±0,31 ммоль/л, соответственно, р < 0,01), так
и через 60 минут (0,36±0,06 ммоль/л и 1,65±0,41
ммоль/л, соответственно, р < 0,01), что указывает
на нарушение полостного пищеварения в ТК при МС. У
больных с МС в среднем содержание эластазы-1 в
кале составило 196,1±12,28 мкг/г, что было
существенно ниже в сравнении с контролем —
500,33±28,51 мкг/г (p<0,01). Содержание
нейтрального жира в кале выявлено у 40 %
пациентов, синдром креатореи, характеризующийся
преимущественно наличием мышечных волокон без
исчерченности — у 76 %, амилорея выявлена у 55 %
пациентов.
При исследовании резорбционной функции ТК с
помощью нагрузочной пробы с глюкозой в течение 30
минут прирост гликемии был сопоставим с
контрольной группой (2,68±0,12 ммоль/л и 2,71±0,21
ммоль/л, р > 0,05), а через 60 мин был более
выраженным, чем в группе здоровых лиц (3,09±0,15
ммоль/л и 2,87±0,44 ммоль/л, р > 0,05).
Однонаправленные изменения всасывательной функции
тонкой кишки установлены при использовании теста с
D-ксилозой. У больных с МС отмечено повышение
резорбции D-ксилозы в ТК в сравнении с контрольной
группой — 2,05±0,05 г/л и 1,82±0,08 г/л
соответственно, р < 0,05.
В изменении этапов пищеварительного процесса в
тонкой кишке у больных при патологии
желудочно-кишечного тракта участвуют механизмы
компенсации и перераспределения нарушенных функций
[14, 17]. С этим согласуются результаты наших
корреляционных исследований, когда между приростом
гликемии после нагрузки сахарозой и концентрацией
D-ксилозы в моче наблюдается средней силы обратная
связь (r = -0,47; p<0,05), то есть при угнетении
пристеночного пищеварения активность резорбционной
функции возрастает. Между приростом гликемии после
нагрузки крахмалом и показателями экскреции
D-ксилозы также отмечена умеренная обратная связь
(r = -0,53; p<0,05).
При проведении электроэнтерографии с помощью
ЭГГ-4М натощак у 42 % больных с МС наблюдался
нормотонический и нормокинетический тип сокращений
ТК, у 33 % — гиперкинетическая дискинезия, у 25 %
— гипокинетическая дискинезия ТК (табл. 1).
Таблица 1. Показатели
двигательной функции тонкой кишки у больных с
метаболическим синдромом
|
Показатели
|
Исследование натощак (n = 48) |
Исследование через 1 час после пищевой
нагрузки (n = 48) |
Нормо-
моторика
(n = 20) |
Гипо-
моторика
(n = 12) |
Гипер-
моторика
(n = 16) |
Нормо-
моторика
(n = 9) |
Гипо-
моторика
(n = 34) |
Гипер-
моторика
(n = 5) |
| Частота, цикл/мин (больные с МС) |
6,3±0,43
|
3,14±0,12*
|
9,38±0,69*
|
9,4±1,05
|
5,04±0,74*
|
14,2±0,81*
|
| Частота, цикл/мин (контрольная группа)
|
6,02±0,24 |
8,9±0,68 |
| Амплитуда, мВ (больные с МС) |
0,08±0,012
|
0,03±0,001*
|
0,39±0,07*
|
0,24±0,03
|
0,05±0,003*
|
0,48±0,02*
|
| Амплитуда, мВ (контрольная группа) |
0,09±0,002 |
0,21±0,003 |
Примечание: * — достоверные изменения по
отношению к контролю (р<0,05), n — число
наблюдений.
Через 1 час после стандартного завтрака у
большинства больных (81 %) имело место нарушение
моторной функции ТК. При этом значительно
преобладала гипотоническая дискинезия ТК на фоне
снижения частоты сокращений в минуту (у 71,5 %
больных). У 9,5 % исследуемых наблюдалась
гипертоническая тахикинезия. Лишь в 19 % случаев
биоэлектрическая активность ТК была сопоставима с
данными контрольной группы.
По результатам гастроэнтеромониторинга на
ГЭМ-01 «Гастроскан-ГЭМ» у большинства больных с МС
(70 %) электрическая активность ДПК, тощей и
подвздошной кишок натощак повышена по сравнению с
контрольной группой. В пищевую фазу электрическая
активность тощей и подвздошной кишок сопоставима с
контролем. Электрическая активность ДПК в
постпрандиальном периоде у 70 % больных низкая,
что свидетельствует о недостаточном ответе ДПК на
пищевую стимуляцию при МС (рис. 1).
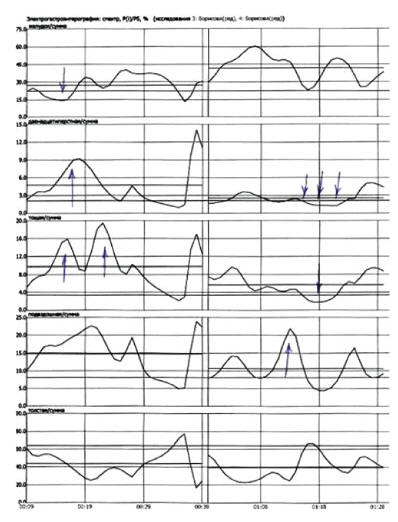
Рис. 1. Электрогастроэнтерография: спектр,
Pi/Ps, %. Тощаковая фаза (слева) — электрическая
активность желудка снижена, электрическая
активность ДПК и тощей кишки повышена, пищевая
фаза (справа) — электрическая активность желудка
повышается, электрическая активность ДПК и тощей
кишки снижена
Дискоординация моторики между желудком и ДПК
усугубляется в постпрандиальном периоде, при этом
у 40 % больных появляется дуодено-гастральный
рефлюкс (ДГР), который не наблюдался в тощаковую
фазу исследования. Несмотря на то, что коэффициент
соотношения ДПК/тощая кишка натощак у большинства
больных (70 %) не изменён, в пищевую фазу у 60 %
имеет низкие значения, что свидетельствует о
снижении эвакуации из ДПК в тощую в
постпрандиальном периоде. Между подвздошной и
толстой кишками наблюдается дискоординация
моторики, усугубляющаяся после пищевой стимуляции
(рис. 2).
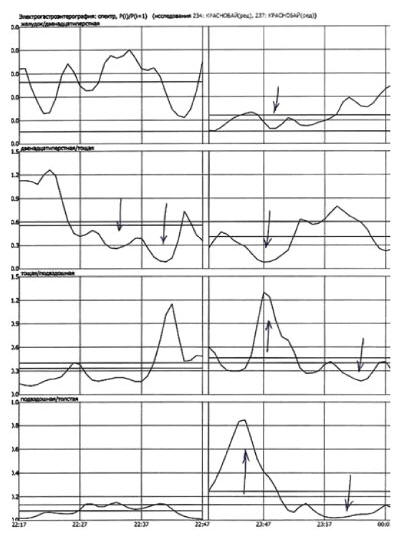
Рис. 2. Электрогастроэнтерография: спектр,
Pi/P(i+1). Тощаковая фаза (слева) — коэффициент
соотношения ДПК/тощая кишка снижен, пищевая фаза
(справа) — коэффициенты соотношения желудок/ ДПК,
ДПК/тощая кишка снижены, дискоординация моторики
подвздошной и толстой кишок
Коэффициент ритмичности ДПК у 40 % больных
снижен в обе фазы исследования, у 50 % — не
изменён и лишь в 10 % случаев повышен.
Значительное снижение ритмичности сокращений
наблюдается на частотах тощей, подвздошной и
толстой кишок как натощак, так и в
постпрандиальном периоде, что указывает на
ослабление пропульсивных сокращений кишечника у
больных с МС.
Функционирование пищеварительной системы,
включающее сопряжение моторики, секреции и
всасывания регулируются сложной системой нервных и
гормональных механизмов [8]. Однако исследований
зависимости гидролизно-резобционной и
моторно-эвакуаторной функций кишечника от гормонов
в крови у больных с МС мы не встретили.
У больных с МС нами отмечено повышение
базального уровня гастрина, инсулина, кортизола и
ТТГ, снижение уровня свободного Т4 в крови (табл.
2).
Таблица 2. Данные
исследования базального уровня гормонов у больных
с МС
|
Обследуемые группы |
Гастрин
(пг/мл) |
Кортизол
(нмоль/л) |
Инсулин
(мкМЕ/л) |
ТТГ
(мкМЕ/л) |
Т4(св)
(пмоль/л) |
| Больные с МС |
180,9±23,0**
n=25 |
547,9±49,6
**
n=25 |
15,4±1,86 *
n=25 |
3,01±0,14*
n=29 |
16,1± ,21*
n=29 |
| Контрольная группа |
66,14±2,44
n=20 |
419,4±12,81
n=20 |
10,46±0,66
n=20 |
2,09 ±0,08
n=20 |
18,9 ±0,27
n=20 |
Примечание: n — число наблюдений; * —
достоверность по отношению к группе контроля, p<0,05;
** — достоверность по отношению к группе контроля,
p<0,01.
Для выяснения роли гормональных факторов в
нарушениях гидролиза и резорбции в ТК у больных с
МС, проведены корреляционные исследования между
гормонами и показателями функционального состояния
ТК. Так, выявлена обратная связь между полостным
пищеварением и уровнями кортизола и инсулина, то
есть на фоне повышения уровня кортизола и инсулина
наблюдается угнетение процессов полостного
пищеварения в кишечнике. Выявлена прямая связь
между мембранным пищеварением и уровнем инсулина
крови, то есть отмечено однонаправленное повышение
мембранного пищеварения и уровня инсулина. Связь
между резорбцией глюкозы и D-ксилозы и уровнем
кортизола отсутствовала. Между уровнем инсулина и
показателями всасывания глюкозы и D-ксилозы
выявлена умеренная прямая зависимость (табл. 3).
Таблица 3. Показатели
корреляции между уровнями гормонов и некоторыми
показателями функционального состояния тонкой
кишки
|
Функциональные пробы |
Гастрин
|
Инсулин
|
Кортизол
|
ТТГ
|
Т4
|
| Прирост гликемии после нагрузки глюкозой
|
- 0,74
p<0,01 |
+ 0,58
p<0,05 |
- 0,18
p>0,05 |
- 0,64
p<0,01 |
+ 0,25
p>0,05 |
| Прирост гликемии после нагрузки
сахарозой |
+ 0,13
p>0,05 |
+ 0,49
p<0,05 |
+ 0,49
p<0,05 |
- 0,21
p>0,05 |
+ 0,61
p>0,01 |
| Прирост гликемии после нагрузки
крахмалом |
- 0,39
p<0,05 |
- 0,26
p>0,05 |
- 0,38
p<0,05 |
+ 0,05
p>0,05 |
+ 0,42
p<0,05 |
Примечание: р — достоверность показателя.
Проведённый корреляционный анализ показал
умеренную отрицательную связь между уровнем
гастрина и электрической активностью (Pi/Ps)
желудка и ДПК, между уровнем гастрина и
коэффициентом соотношения (Pi/P(i+1)) желудка к
ДПК, в итоге приводящие к замедлению эвакуации
химуса из желудка и ДПК и возникновению ДГР (табл.
4).
Таблица 4. Показатели
корреляции между уровнями гормонов и некоторыми
показателями МЭФ желудка и двенадцатиперстной
кишки у больных с МС
| Гормоны
|
Электрическая
активность (Pi/Ps)
желудка |
Электрическая
активность (Pi/Ps)
ДПК |
Коэффициент
соотношения (Pi/P(i+1))
желудок/ДПК |
Коэффициент
соотношения (Pi/P(i+1))
ДПК/тощая кишка |
| Гастрин |
- 0,44
р<0,05 |
- 0,13
р>0,05 |
- 0,42
р<0,05 |
- 0,57
р<0,05 |
| Инсулин |
+ 0,22
р>0,05 |
- 0,06
р>0,05 |
- 0,04
р>0,05 |
- 0,36
р<0,05 |
| Кортизол |
- 0,42
р<0,05 |
- 0,33
р<0,05 |
- 0,14
р>0,05 |
- 0,44
р<0,05 |
| ТТГ |
- 0,12
р>0,05 |
- 0,13
р>0,05 |
- 0,05
р>0,05 |
- 0,17
р>0,05 |
| Т4 |
+ 0,32
р<0,05 |
+ 0,04
р>0,05 |
+ 0,01
р>0,05 |
+ 0,16
р>0,05 |
Примечание: р — достоверность показателя.
При повышении уровня кортизола наблюдается
снижение скорости эвакуации из ДПК и уменьшение
электрической активности ТК. Полученные нами
данные согласуются с ранее проведёнными
исследованиями [9, 18], показавшими, что избыток
эндогенных кортикостероидов в организме оказывает
расслабляющее действие на гладкую мускулатуру
органов, вызывая снижение их моторики, амплитуды
сокращений, снижение давления в области
сфинктеров. Зависимость нарушений моторной функции
ЖКТ от уровней инсулина, ТТГ и Т4 была
незначительной. Кроме того, в нарушении моторики
ТК нельзя исключить и роль активизации
симпатической нервной системы [13, 23], являющейся
признаком МС [1, 3, 22]. Проведённый нами анализ
индекса Кердо показал, что у 86 % больных с МС
наблюдается преобладание симпатического тонуса.
Снижение скорости эвакуации пищевого химуса по
ТК у больных с МС способствует нарушению
соотношения питательных веществ в составе потока,
тем самым изменяя темп их переноса из энтеральной
во внутреннюю среду, усугубляя метаболические
нарушения, в том числе обмен липидов. Так ,
уровень общего Хс у больных был выше (6,08±0,16
ммоль/л, р<0,05), чем в группе контроля (4,99±0,32
ммоль/л и 2,28±0,17 ммоль/л, соответственно).
Наряду с этим наблюдалась гипертриглицеридемия
(2,83±0,34 ммоль/л, р<0,05) в сравнении с
контролем (1,48±0,29 ммоль/л) и снижение
содержания ХсΛПВП — 0,86±0,14 ммоль/л (в
контрольной группе — 1,4±0,11 ммоль/л, р<0,05). У
большинства больных с МС (97 %) было выявлено
повышение уровня коэффициента атерогенности (КА) —
5,21±0,28, при этом средний риск (КА от 3 до 4)
наблюдался у 27,6 %, высокий риск (КА > 4) — у
69,4 % больных. При корреляционном анализе
выявлена умеренная отрицательная зависимость между
показателями резорбции D-ксилозы (r=-0,68),
глюкозы (r=-0,42) в ТК и частотой её сокращений,
умеренная отрицательная связь между уровнем
коэффициента атерогенности и частотой и амплитудой
сокращений ТК (r = -0,53, r = -0,48,
соответственно).
Заключение
У всех больных с МС выявлены клинические
симптомы энтерального поражения, которые находятся
в тесной зависимости от характера нарушений
пищеварительной, всасывательной и двигательной
функций тонкой кишки. Комплексное исследование
пищеварительной и всасывательной функции тонкой
кишки позволило уточнить характер нарушений
мальдигестии и мальабсорбции при метаболическом
синдроме.
На фоне угнетения полостного и пристеночного
пищеварения обнаружено повышение резорбции глюкозы
и D-ксилозы, сопряжённое со снижением
электрической активности и замедлением эвакуации
по тонкой кишке в постпрандиальном периоде. При
гипомоторной дискинезии тонкой кишки в
постпрандиальном периоде создаются условия для
более длительной экспозиции питательных веществ в
энтеральной среде. Это, в свою очередь,
способствует повышению уровня липидемии и гликемии
(преимущественно за счёт моносахаридов), что на
фоне инсулинорезистентности усугубляет
формирование абдоминального ожирения у больных с
метаболическим синдромом.
Исследование показателей моторно-эвакуаторной
функции и гидролизно-резорбционного конвейера ТК с
одной стороны и уровней гормонов и
нейро-вегетативного статуса с другой позволило
выявить новые патогенетические закономерности,
касающиеся роли последних в нарушении функций
кишечника у больных с МС. Результаты наших
исследований позволяют утверждать, что поражение
тонкой кишки, выявленное при МС, является важным
звеном в сложном патогенетическом круге
метаболического синдрома. Можно полагать, что с
позиции коррекции функционального состояния ТК
будут разработаны более эффективные способы
лечения МС.
Список литературы
- Алимова И.Л. Метаболический синдром у
детей и подростков. М.:ГЭОТАР- Медиа; 2008.
- Буторова Л.И. Дислипидемия и патология
органов пищеварения. Медицинский Вестник.
2012; 9 (586): 6-10.
- Бутрова С.А. Метаболический синдром:
патогенез, клиника, диагностика, подходы к
лечению. РМЖ. 2001; 2: 56-60.
- Вахрушев Я.М., Волкова А.А.
Дифференцированные подходы к лечению больных
хроническим панкреатитом с сопутствующим
метаболическим синдромом. Эксп. и клин.
гастроэнтерология. 2011; 11: 33-36.
- Вахрушев Я.М., Волкова А.А. Специфическое
динамическое действие пищи у больных
хроническим панкреатитом с сопутствующим
метаболическим синдромом. Тер. архив. 2012; 2:
49-52.
- Вахрушев Я.М., Ляпина М.В.
Клинико-функциональная характеристика тонкой
кишки при метаболическом синдроме. Эксп. и
клин. гастроэнтерология. 2011; 9: 26-29.
- Вахрушев Я.М., Ляпина М.В. Изучение роли
тонкой кишки в развитии метаболического
синдрома. Тер. архив. 2012; 12: 62-65.
- Вахрушев Я.М., Крючкова В.И. Очерки по
нейрогуморальной регуляции дыхательной и
пищеварительной систем. Ижевск; 1993.
- Герман С.В., Степенко А.С., Гурвич Р.Н.
Гиперкортицизм и моторика пищевода. Рос. журн.
Гастроэнтерол., гепатол., колопроктол. 1996;
4: 2.
- Диагностика и лечение метаболического
синдрома. Российские рекомендации (второй
пересмотр). Разработаны Комитетом экспертов
Всероссийского научного общества кардиологов и
Российского медицинского общества по
артериальной гипертонии. Москва 2009.
- Егорова Е.Г., Звенигородская Л.А.,
Лазебник Л.Б. Метаболический синдром с позиции
гастроэнтеролога. РМЖ. 2005; 26: 1706-1712.
- Лазебник Л.Б., Звенигородская Л.А.
Метаболический синдром и органы пищеварения.
М.: Анахарсис; 2009.
- Лычкова А.Э. Серотониновая регуляция
моторной функции тонкой кишки. Эксп. и клин.
гастроэнтерология. 2011; 3: 130 — 135.
- Метельский С.Т. Физиологические механизмы
всасывания в кишечнике. Рос. журн.
гастроэнтерол., гепатол., колопроктол. 2009;
3:51-56.
- Парфёнов А.И. Энтерология. М.: ООО
«Медицинское информационное агенство»; 2009.
- 1Парфёнов А.И. Синдром нарушенного
пищеварения (К 50-летию открытия А.М. Уголевым
мембранного пищеварения). Эксп. и клин.
Гастроэнтерология. 2008; 7: 76-81.
- Петухов А.Б., Лысиков Ю.А., Морозов И.А.
Энзиматический барьер слизистой оболочки
тонкой кишки при патологии. «Санкт-Петербург —
Гастро-2000». 2000; 1-2: 73.
- Положенкова Л.А., Герман С.В. Особенности
клинической симптоматики гастроэзофагеальной
рефлюксной болезни при избытке эндогенных
стероидов в организме. Материалы Десятой
Российской Гастроэнтерологической Недели.
Российск. журн. гастроэнтерол., гепатол.,
колопроктол. 2004; 5: 13.
- Смирнова Г.О., Силуянов С.В.
Периферическая электрогастроэнтерография в
клинической практике. М.: ИД «МЕДПРАКТИКА-М»;
2009.
- Ступин В.А. Функциональная
гастроэнтерология. Инструментальные методы
исследования. Пособие для врачей. М.: ИД «МЕДПРАКТИКА-М»;
2009.
- Уголев А.М. Мембранный гидролиз и
транспорт: новые данные и гипотезы. Л.; 1986.
- Чазова И.Е., Мычка В.Б. Метаболический
синдром. М.: Медиа Медика; 2004.
- Шмидт Р., Тевс Г. Физиология человека.
Т.3. М.: Мир; 1996.
- Avogaro P. Association of hyperlipidemia,
diabetes mellitus and mild obesity. Acta
Diabetol. Lat. 1967; 4: 572-590.
- Angelo J. Diabetes prevention: a review of
current literature. Preventive Medicine. 2005;
5: 250-259.
- Balkau B. Eschwege E. Insulin resistance:
an independent risk factor for cardivascular
disease? Diabetes. Obesity&Metab. 1999; 1:
23-31.
- Codario R. A. Type 2 diabetes,
pre-diabetes, and the metabolic syndrome: the
primary care guide to diagnosis and management.
Humana Press. Inc. 2005.
- Kerdo I. Einaus der Blutzirkulation
kalkulierten Index zur Beurteilung der
vegetativen Tonuslage. Acta neurovegetativa
1966; 29 (2): 250-268.
Статья опубликована на сайте
http://www.gastroscan.ru

