Первичные Т-клеточные кожные лимфомы представляют собой гетерогенную группу
лимфопролиферативных заболеваний, характеризующуюся клональной пролиферацией
Т-лимфоцитов в коже. Они составляют 75–80 % всех кожных лимфом. Разграничение
первичных лимфом кожи и вторичных ее поражений при других лимфомах требует
тщательного анализа клинической картины, патологических, иммунологических и
молекулярно-генетических данных. Первичные лимфомы кожи отличаются от
нодальных лимфом характером течения, прогнозом и подходами терапии. Это
обстоятельство вызвало необходимость создания подробной классификации,
отражающей весь спектр первичных кожных лимфом. В 2005 г. на основе
классификации ВОЗ для опухолей гемопоэтической и лимфоидной тканей [1] и
классификации лимфом кожи Европейской организации по исследованию и лечению
рака (EORTC) [2] создана ВОЗ/EORTC-классификация кожных лимфом, наиболее полно
охватывающая весь спектр этих заболеваний [3].
Т- и NK-клеточные лимфомы кожи
- Грибовидный микоз (ГМ):
— фолликулотропный ГМ;
— педжетоидный ретикулез;
— синдром гранулематозной вялой кожи.
- Синдром Сезари.
- Первичные кожные CD30+-лимфопролиферативные заболевания:
— первичная анапластическая крупноклеточная лимфома кожи;
— лимфоматоидный папулез.
- Подкожная панникулитоподобная Т-клеточная лимфома.
- Экстранодальная NK/Т-клеточная лимфома, назальный тип.
- Первичная кожная периферическая Т-клеточная лимфома, неуточненная.
- Первичная кожная агрессивная эпидермотропная CD8+ Т-клеточная
лимфома.
- Кожная γ/δ-Т-клеточная лимфома.
- Первичная кожная CD4+ плеоморфная Т-клеточная лимфома из
клеток малых и средних размеров.
Самыми распространенными подтипами являются: ГМ, синдром Сезари, первичная
анапластическая крупноклеточная лимфома кожи и лимфоматоидный папулез. Они
составляют приблизительно 95 % всех Т-клеточных кожных лимфом.
ГМ — первичная эпидермотропная Т-клеточная лимфома кожи, отличительной
чертой которой является пролиферация Т-лимфоцитов малых и средних размеров с
церебриформными ядрами. Термин «грибовидный микоз» в настоящее время принято
использовать только для классического варианта микоза Алибера–Базена,
характеризующегося поэтапной эволюцией пятен, бляшек и узлов, или для
вариантов со схожим клиническим течением.
Это наиболее часто встречающаяся Т-клеточная опухоль кожи, составляющая 1 %
всех неходжкинских лимфом и 50% Т-клеточных кожных лимфом. Средний возраст
заболевших — 57 лет, соотношение мужчин и женщин — 2 : 1 [4]. ГМ, особенно на
ранних стадиях, может протекать «под маской» различных доброкачественных
кожных процессов, таких как хроническая экзема, аллергический контактный
дерматит или псориаз. Для начальных кожных проявлений характерна локализация
на ягодицах и других защищенных от солнца областях. Заболевание обычно течет
благоприятно, медленно прогрессируя в течение нескольких лет или даже
десятилетий. Кожные морфологические элементы постепенно эволюционируют от
пятен или бляшек до опухолевых узлов с признаками изъязвления. На поздних
стадиях заболевания в патологический процесс могут вовлекаться лимфатические
узлы и внутренние органы.
Гистологическая картина на ранних стадиях ГМ неспецифична и может быть
схожа с таковой при доброкачественном воспалительном дерматозе: отмечаются
периваскулярные инфильтраты в сочетании с псориазоформной гиперплазией
эпидермиса [5]. Для бляшечной стадии характерен плотный полосовидный
инфильтрат в верхней части дермы, содержащий высокий процент церебриформных
лимфоцитов с выраженным эпидермотропизмом. Внутриэпидермальные скопления
атипичных лимфоцитов (микроабсцессы Потрие) являются характерной чертой этой
стадии, но встречаются лишь в 10 % случаев [6]. С прогрессированием в
опухолевую стадию эпидермотропизм исчезает, а инфильтрат, состоящий из
церебриформных лимфоцитов малых, средних и крупных размеров, становится
диффузным и может проникать в подкожную жировую клетчатку.
Опухолевые клетки при ГМ имеют фенотип зрелых Т-лимфоцитов памяти (CD3+,
CD4+, CD45RO+, CD8-). Редко может наблюдаться
фенотип CD4-, CD8+. Клиническое течение и прогноз в
таких случаях не отличаются от классического варианта, и, следовательно, их не
следует рассматривать отдельно. О наличии аберрантного фенотипа при ГМ говорит
утрата пан-Т-клеточных антигенов CD2, CD3, CD5, CD7, что во многих случаях
является важным дополнением к диагнозу [7].
Прогноз при ГМ напрямую зависит от стадии заболевания, характера и
распространенности кожного процесса, а также наличия внекожных поражений.
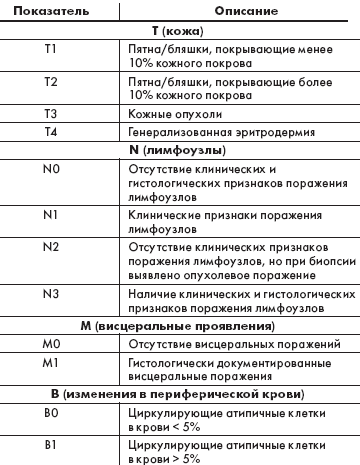
Таблица 1. TNMB классификация грибовидного микоза
В 1978 г. Национальным институтом рака США была предложена TNMB (tumor,
node, metastasis, blood) — классификация кожных Т-клеточных лимфом, которая
применима для определения стадий ГМ (табл. 1, 2) [8]. Данные о пятилетней
выживаемости при грибовидном микозе/синдроме Сезари (ГМ/СС) в зависимости от
стадии заболевания следующие: IA — 96 %, IB / IIA — 73 %, IIB / III — 44 %, IV
— 27 %.
Кроме классической формы ГМ, имеется несколько вариантов этого заболевания
с необычными клиническими и/или гистологическими характеристиками. Из них в
классификации ВОЗ/EORTC выделены три клинико-патологических варианта:
фолликулотропный ГМ, педжетоидный ретикулез и синдром гранулематозной «вялой»
кожи [3].
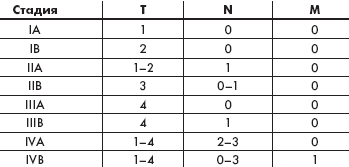
Таблица 2. Стадии грибовидного микоза по классификации
TNMB (США, 1978)
Фолликулотропный ГМ характеризуется наличием фолликулотропного и часто
неэпидермотропного инфильтрата. Клинически заболевание может проявляться
фолликулярными папулами, бляшками и иногда опухолями, локализующимися чаще
всего на голове и шее и сопровождающимися алопецией. Гистологически выявляется
плотный периаднексальный (перифолликулярный) инфильтрат, состоящий из малых и
средних лимфоидных клеток с церебриформными ядрами. Эпидермотропизм может
отсутствовать. Волосяные фолликулы часто кистозно расширены, возможна
муцинозная дегенерация фолликулярного эпителия.
Педжетоидный ретикулез (моноочаговая форма Ворингера–Колоппа) является
благоприятно протекающей формой ГМ и характеризуется наличием одного очага в
виде псориазоформной бляшки, локализующейся на нижних конечностях.
Гистологическая картина характеризуется акантотическим эпидермисом, содержащим
«спонгиоформный» инфильтрат из средних и крупных лимфоидных клеток с
вакуолизированной цитоплазмой, расположенных поодиночке или скоплениями.
К одним из самых редко встречающихся вариантов ГМ относится синдром
гранулематозной «вялой» кожи, характеризующийся клональной пролиферацией
Т-лимфоцитов и дегенерацией эластических волокон в дерме. Заболевание
клинически проявляется развитием в крупных складках своеобразных изменений
кожи в виде появления складчатых, инфильтрированных и лишенных эластичности
образований. Гистологическая картина характеризуется наличием плотного
диффузного инфильтрата, состоящего из малых и средних лимфоидных клеток без
выраженной атипии ядер, и отсутствием эластических волокон в сосочковой и
сетчатой частях дермы. Специфическим гистологическим признаком данного
заболевания считается наличие в инфильтрате многоядерных гигантских клеток,
имеющих от 20 до 30 концентрически расположенных ядер. В их цитоплазме могут
находиться лимфоциты, а также остатки эластических волокон.
Синдром Сезари характеризуется триадой признаков: эритродермия,
лимфаденопатия и наличие опухолевых Т-лимфоцитов (клеток Сезари) в коже и
периферической крови [9].
Клинически синдром Сезари характеризуется развитием эритродермии с
генерализованным зудом кожного покрова, увеличением периферических
лимфатических узлов, наличием ладонно-подошвенного гиперкератоза и
ониходистрофии. Интернациональным обществом по кожным лимфомам были предложены
следующие критерии для диагностики синдрома Сезари: абсолютное количество
клеток Сезари в периферической крови не меньше 1000 в мм3,
увеличение соотношения CD4/CD8 лимфоцитов более чем в 10 раз и потеря
Т-клеточных антигенов (CD2, CD3, CD4, CD5), подтверждение Т-клеточной
клональности в периферической крови молекулярными или цитогенетическими
исследованиями [10].
Гистологические изменения при синдроме Сезари сходны с таковыми при ГМ,
однако эпидермотропизм может быть менее выражен.
Терапия ГМ/СС также зависит от стадии заболевания. На ранних стадиях, при
локальных изменениях кожи, эффективна РUVA-терапия, которая позволяет получить
полную ремиссию в подавляющем большинстве случаев [11–13]. При I и II стадиях
PUVA-терапия может быть использована в комбинации с интерфероном α [14–16].
Применение агрессивных методов лечения (химио- и лучевая терапия) на ранних
стадиях не меняет прогноз и, следовательно, неоправдано [17]. При
распространенном поражении локальная лучевая терапия, тотальное облучение кожи
(ТОК), экстракорпоральный фотоферез позволяют контролировать течение болезни,
но имеют ограниченную доступность [18–21]. Когда заболевание становится
резистентным к указанным методам лечения, используется комбинированная
химиотерапия, однако вне зависимости от ее варианта продолжительность эффекта
обычно не превышает 1 года [22–26]. В последнее время в лечении ГМ/СС все
большее распространение получает применение биологических препаратов, механизм
действия которых основан на специфическом связывании с различными антигенами
на мембране опухолевых клеток. К ним относятся интегрированный протеин — Ontak
и анти-CD52-моноклональное антитело — алемтузумаб (Кэмпас). Ontak является
конъюгатом токсина дифтерии с интерлейкином-2, который после связывания с
рецептором к интерлейкину-2 (СD25) подвергается эндоцитозу с последующим
высвобождением внутри клетки дифтерийного токсина. Результатом этого процесса
является нарушение синтеза белка и в конечном итоге апоптоз Т-лимфоцитов [27].
Кэмпас представляет собой гуманизированное IgG1-моноклональное антитело,
специфически связывающееся с CD52-антигеном. Эффекторный механизм Кэмпаса
изучен не до конца, он, вероятно, основан на антителозависимой клеточной
цитотоксичности [28, 29], комплемент-обусловленном клеточном лизисе [30, 31] и
апоптозе [32]. Опухолевые Т-лимфоциты экспрессируют на своей поверхности
большое количество молекул CD52 (около 500 000 молекул на лимфоцит), и
интенсивность экспрессии CD52 напрямую коррелирует с клиническим эффектом [33,
34]. Основанием для использования Кэмпаса при ГМ является его успешное
применение при других Т-клеточных опухолях, например, при Т-клеточном
пролимфоцитарном лейкозе [35]. По данным одного из наиболее крупных
исследований по использованию Кэмпаса в терапии ГМ/СС, в которое было включено
22 больных со II–IV стадиями заболевания, ранее получавших другие виды
лечения, общий ответ на терапию составил 55 %, полная ремиссия достигнута в 32
% случаев. Если предшествующее лечение включало в себя не более двух режимов
терапии, общий ответ составлял 80 %. Медиана выживаемости без прогрессии для
12 больных, ответивших на лечение, составила 12 мес [36]. Клиническая картина
до и после терапии ГМ препаратом Кэмпас представлена на рис. 1–4.
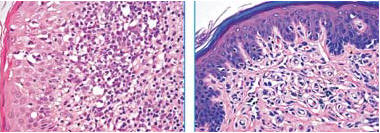
Рис. 1. Разрушение зоны эпидермально-дермального стыка.
Распространение инфильтрата в эпидермис с образованием абсцессов Потрие.
Рис. 2. Единичные лимфоидные клетки среди эпителиоцитов базального слоя
эпидермиса (после терапии алемтузумабом)
Первичные CD30+-лимфопропролиферативные заболевания кожи
занимают второе место по частоте возникновения среди всех Т-клеточных лимфом
кожи. Они включают анапластическую крупноклеточную лимфому кожи и
лимфоматоидный папулез. Их объединяющим признаком является экспрессия
опухолевыми клетками CD30 — рецептора, принадлежащего к группе рецепторов
фактора некроза опухолей.
Первичная анапластическая лимфома кожи чаще развивается у лиц мужского
пола, в основном в возрасте старше 60 лет. Клинически определяются обычно один
или несколько узлов (в том числе подкожных), имеющих тенденцию к изъязвлению.
Наиболее частая локализация высыпаний — верхние и нижние конечности.
Гистологическая картина представлена диффузными инфильтратами в дерме и
подкожно-жировой клетчатке, состоящими из клеток с анапластической или
иммунобластной морфологией. Эпидермотропизм не характерен. Опухолевые клетки
экспрессируют CD30, а также один или несколько пан-Т-клеточных антигенов (CD2,
CD3, CD4, CD5). Экспрессия антигена эпителиальных мембран (EMA) и ALK-протеина
обнаруживается крайне редко, что отличает первичную кожную анапластическую
лимфому от нодальной анапластической лимфомы с поражением кожи [37].
Первичная анапластическая лимфома кожи имеет, как правило,
доброкачественное течение. Пятилетняя выживаемость составляет около 90 %.
Лучевая терапия или хирургическое удаление применяются в случае единичных
очагов. У больных с множественными высыпаниями проводится лечение малыми
дозами метотрексата (5–20 мг в неделю) или лучевая терапия. Только
быстропрогрессирующее течение заболевания с внекожным распространением требует
назначения полихимиотерапии.
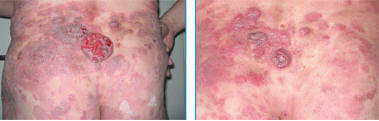
Рис. 3. Множественные пятна, бляшки и опухолевые
образования с элементами изъязвления на коже (до начала лечения).
Рис. 4. Вид после терапии алемтузумабом
Лимфоматоидный папулез — хроническое лимфопролиферативное заболевание кожи,
характеризующееся рецидивирующим течением с повторными высыпаниями
самопроизвольно разрешающихся папулезных элементов с гистологическими
признаками CD30+-лимфомы. Выделяют три гистологических варианта
заболевания: тип А, тип В и тип С.
Тип А характеризуется кожным инфильтратом состоящим из крупных атипичных
клеток, напоминающих клетки Рида–Штернберга.
Тип В гистологически напоминает картину ГМ. Анапластические клетки
встречаются в малом количестве или отсутствуют.
Тип С характеризуется мономорфным инфильтратом или наличием крупных
кластеров CD30+ Т-лимфоцитов. Наиболее эффективным методом лечения
является назначение малых доз метотрексата, особенно в случае распространенных
высыпаний и частых обострений [3].
Таким образом, диагностика и лечение первичных Т-клеточных кожных лимфом
требуют учета многих факторов и использования широкого спектра современных
методов обследования (гистологических, иммунологических,
молекулярно-генетических), позволяющих правильно определить прогноз и
оптимизировать терапию.