Опыт использования полуэлементной смеси у пациентов в
критических состояниях
Ю. В. Ерпулёва, доктор медицинских наук
ДГКБ № 9 им. Г. Н. Сперанского, 2-й ФГУ педиатрии и детской хирургии Росздрава,
Москва
В последние десятилетия методика раннего применения энтерального
питания у детей в критических состояниях стала одной из основных составляющих
интенсивного лечения реанимационных больных [1–5]. Основные показания для
использования энтерального питания в педиатрической практике — тяжелая
сочетанная или ожоговая травма с отсутствием сознания и актов глотания, часто —
ранний восстановительный послеоперационный период, когда доставка питательных
веществ обычным путем затруднительна и (или) противопоказана [6, 7, 8]. Острый
дефицит питательных веществ и энергии, наблюдающийся у данной категории больных
детей в этом периоде, приводит к утяжелению состояния, делает чувствительным
организм ребенка к развитию инфекционных осложнений, что в конечном итоге
приводит к увеличению длительности и стоимости стационарного лечения [1, 6, 10].
С позиций современной медицины преимущество перед стандартными
лечебными диетами получили специализированные продукты питания, достоинства
которых выражаются в полном сбалансированном соответствии с потребностями детей,
обогащенных витаминами и микроэлементами, высококачественными белками,
незаменимыми жирными кислотами. При критических состояниях часто наблюдается
недостаточность ферментативного гидролиза полимеров в тонкой кишке, для
энтерального питания были разработаны так называемые полуэлементные диеты,
содержащие основные питательные вещества в виде гидролизатов [6, 9, 10, 11].
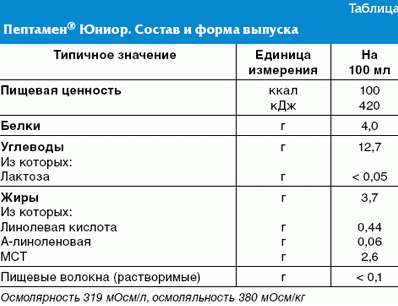
В практике хирургической реанимации ДГКБ № 9 им. Г. Н.
Сперанского проведена оценка клинической эффективности готовой жидкой формы
полуэлементной смеси Пептамен® Юниор — специализированного продукта для
энтерального (зондового) питания c нейтральным вкусом для детей с 1 года до 10
лет.
Белковый компонент смеси Пептамен® Юниор состоит из пептидов (олигопептидов,
полученных при гидролизе сывороточных белков). Известно, что пептиды имеют
основным путем поступления в кишечнике — чресклеточное всасывание через мембраны
ворсинок либо с использованием молекул-переносчиков, либо диффузно через
липидные участки в мембранах [10]. Помимо этого, пептиды обладают способностью
всасываться, минуя ворсинки кишечника (в том числе в точках с дефектами
слизистой). Пептиды оказываются часто предпочтительнее нативного белка и
свободных аминокислот благодаря более высоким [10, 11]:
Говоря о сывороточном белке, следует вспомнить, что этот белок
является высокобиологически ценным продуктом с широким набором аминокислот; у
белка отмечается оптимальный коэффициент белковой эффективности по
серосодержащим аминокислотам/аминокислотам с разветвленной цепью = 3,2; белок
способствует восстановлению двигательной активности желудка и кишечника, что
наиболее актуально у критических больных при нарушениях двигательной функции
желудочно-кишечного тракта (ЖКТ).
Жировой состав представлен среднецепочечными триглицеридами, что
улучшает усвоение смеси в ЖКТ, а также позволяет назначать в ранние сроки после
операций, в том числе на ЖКТ, при ограниченном усвоении жиров у пациентов в
критических состояниях с нарушениями функции пищеварительной системы. Всасывание
среднецепочечных триглицеридов (МСТ) не требует дополнительных ферментативных
усилий, что обеспечивает относительный функциональный покой печени и
поджелудочной железе. В состав жирового компонента входят эссенциальные жирные
кислоты (линолевая и альфа-линоленовая), что позволяет добиться максимального
усвоения смеси при хорошей энергетической обеспеченности. В смесях содержатся
L-карнитин, необходимый для полноценного усвоения жирных кислот, и таурин —
эссенциальная аминокислота для больных, получающих интенсивную терапию.
Углеводный компонент сформирован смесью мальтодекстринов с
различным декстрозным эквивалентом (степенью гидролиза). Соотношение углеводных
компонентов обеспечивает низкую осмолярность (319 мОсм/л) и хорошие
органолептические свойства продукта. Смесь имеет сбалансированный
витаминно-минеральный состав, что делает возможным ее применение в течение
длительного времени.
Цель работы: оценить эффективность раннего энтерального питания
с использованием «готовой» полуэлементной смеси Пептамен® Юниор для энтерального
питания у детей в раннем посттравматическом периоде.
Пациенты и методы: обследовано 26 детей, находившихся в
отделении реанимации и интенсивной терапии (в возрасте от четырех лет до 12 лет
с сочетанной травмой (сочетанная травма, ожоги более 15% поверхности тела).
Эффективность изучаемых смесей проводилась по данным
клинико-лабораторных и функциональных методов исследований. Клиническими
критериями усвоения смесей служили отсутствие застоя, признаков диспепсических
расстройств (тошнота, рвота, метеоризм, диарея).
После разрешения пареза ЖКТ, назначали энтеральное питание с
использованием пектина с Регидроном (5,5 г Пекто ± 100,0 Регидрона), начиная с
30,0–50,0 мл за одно кормление, объемом до 150–500 мл/сутки через зонды
внутреннего диаметра (5–14 мм), установленные назогастрально, что обеспечивало
восстановление моторики кишки и нарушенного водно-электролитного баланса
организма ребенка. Энтеральное зондовое питание смесью Пептамен® Юниор
проводилось через 24 часа после операции при отсутствии выраженных
моторно-эвакуаторных нарушений ЖКТ. Начальный объем составлял 50,0–60,0 мл за
одно кормление, скорость введения составляла 10–20 мл/ч. Скорость введения
увеличивали в зависимости от индивидуальной переносимости больного. Объем
увеличивали на 10,0–20 мл, доведя до 60–100 мл/ч, в дальнейшем, при удержании
смеси, отсутствии застойного содержимого, с четвертых суток — назначение смеси
по 50,0–120,0 мл за одно кормление до 6–7 раз в сутки, увеличивая объем к 5–7
суткам по 120,0–180,0 мл за одно кормление. После перевода в коечное отделение
больные продолжали прием сухой смеси Пептамен® Юниор перорально в виде напитка
объемом до 1000–1200 мл. На фоне проведения питания осложнений со стороны ЖКТ не
отмечено.
При биохимическом обследовании отмечено, что с момента
поступления у наблюдаемых больных отмечались гипопротеинемия (45,6 ± 2,1 г/л),
гипоальбуминемия (30,1 ± 0,9 г/л).
На фоне раннего энтерального питания к 5–7 суткам наблюдается
рост белковых фракций, достигая к 7-м суткам 51,7 ± 1,9 г/л показателя общего
белка, 31,9 ± 2,1 г/л альбумина.
Таким образом, результаты биохимического исследования показали
эффективность назначения энтеральной терапии, позволяющей адекватно
корригировать метаболические нарушения до уровня нормы в относительно короткий
период времени (7 дней) и полноценно обеспечивать возросшие энергетические и
пластические потребности детей в раннем послеоперационном периоде. Все дети,
получившие нутритивную поддержку в ранние сроки от поступления, своевременно
были переведены в коечные отделения в среднем на 7 ± 2,1 дня, без развития
послеоперационных осложнений. Следует отметить, что проведение питания нередко у
детей в критических состояниях осложнялось проведением искусственной вентиляции
легких, парезом ЖКТ, а также нередко наличием стрессовых язв, что предопределяло
выбор полуэлементной смеси в связи с хорошей усвояемостью.
Таким образом, использование специализированной нутритивной
поддержки в раннем посттравматическом периоде у детей является необходимым
важным компонентом в общем комплексе интенсивной терапии, позволяющей улучшить
качество лечения пациентов детской практики.
Литература
-
Вретлинд А., Суджян А. Клиническое питание. Стокгольм-Москва. 1990. 354 с.
-
Guidelines for the Use of Parenteral and Enteral Nutrition in Adult and
Pediatric Patients. A.s.p.e.n. Board of Directors // JPEN. 1993. V. 17. № 4.
P. 27 SA–32 SA.
-
Костюченко А. Л., Костин Э. Д., Курыгин А. А. Энтеральное искусственное
питание в интенсивной медицине. Санкт-Петербург. 1996. 330 с.
-
Лейдерман И. Н. Нутритивная поддержка — важнейший компонент терапии
сопровождения при лечении онкологических больных. М., 2002.
-
Маев И. В., Шабуров Р. И., Хенкина Н. А. Экспериментальная и клиническая
гастроэнтерология, 2003, № 3, с. 101–106.
-
Попова Т. С., Шестопалов А. Е., Тамазашвили Т. Ш., Лейдерман И. Н.
Нутритивная поддержка больных в критических состояниях. М.: Издат. Дом
«М-Вести», 2002, 320 с.
-
Adam S., Batson S. A study of problems associated with delivery of enteral
food in critically ill patients in five ICUs in the UK // Intensive Care Med.
1997. V. 23. P. 261–266.
-
Baker G. P. Scientific base of enteral nutrition support in pediatrics/Selected
Abstracts From the 3 rd Congress of the Parenteral and Enteral Nutrition
Society of Asia (PENSA), October 29–31,1997, Bangkok, Thailand. Nutr. 1999.
V. 15. Р. VIII.
-
Lykhach T. V., Kliusov A. M., Slobodianok M. L. Experience of application of
the mixed enteral preparation Peptamen after performance of radical
operations for malignant gastroduodenal tumor//Klin Khir. 2004, Jul; 7: 5–7.
-
Meredith J. W. et al.//J Trauma. 1990; 30: 825–829.
-
Ziegler F. et al.//Am J Clin Nutr. 1998; 67: 124–128.
Статья опубликована в журнале
Лечащий Врач