Особенности клинического течения желчнокаменной болезни у
детей с ожирением и метаболическим синдромом
Т. А. Бокова, кандидат медицинских наук, доцент
ГБУЗ МОНИКИ им. М. Ф. Владимирского, Москва
Ожирение является одной из наиболее актуальных медицинских и социальных
проблем современного здравоохранения. Практически повсеместно количество детей с
избыточным весом растет и удваивается каждые три десятилетия [3].
Известно, что с увеличением массы тела связано повышение
обменно-воспалительных заболеваний билиарного тракта, заболеваемости ишемической
болезнью сердца (ИБС), гипертонической болезнью (ГБ), сахарным диабетом (СД)
2-го типа, злокачественными новообразованиями. Больные ожирением III–IV степени
живут в среднем на 15 лет меньше [4, 8].
В последние годы все чаще врачам различных специальностей приходится
сталкиваться с таким симптомокомплексом, как метаболический синдром (МС). На
сегодняшний день в МС включены следующие компоненты: инсулинорезистентность (ИР)
с компенсаторной гиперинсулинемией, СД и другие нарушения толерантности к
глюкозе, абдоминальное ожирение, артериальная гипертензия (АГ), атерогенная
дислипидемия, неалкогольная жировая болезнь печени (НАЖБП), нарушения
фибринолитической активности крови, гиперандрогения, гиперурикемия,
микроальбуминурия.
В связи с тем, что клиническая манифестация этих состояний имеет место уже в
детском возрасте, МС начинает признаваться как актуальная педиатрическая
проблема.
Многочисленными исследованиями установлено, что ожирение сопровождается
вторичным поражением печени по типу НАЖБП, включенной в критерии МС. Известно,
что если средняя распространенность НАЖБП составляет 23% и колеблется в
интервале 3–58%, то среди людей с избыточной массой тела она достигает 74–100%,
при этом у 20–47% из них диагностируется неалкогольный стеатогепатит (НАСГ).
Отмечается высокий процент патологии билиарного тракта (от 41,9% до 62,4%) у
больных с ожирением. Так, частота желчнокаменной болезни (ЖКБ) у взрослых с
избыточной массой тела составляет 64,7%, а при выраженном ожирении — до 100%
случаев [1, 4–6].
Омоложение ЖКБ, как и ожирения, обусловлено совокупностью целого ряда
факторов, таких как несбалансированное питание, стрессовые нагрузки,
гиподинамия, ухудшение экологической обстановки. Как и у взрослых, у детей
немаловажную роль играет наследственная предрасположенность. Другими факторами,
способствующими формированию ЖКБ в детском возрасте, являются психосоматические,
дисгормональные и рефлекторные дисфункции билиарного тракта, приводящие к
нарушению желчеоттока.
Все больше данных свидетельствуют о том, что уровень инсулина натощак,
который может быть маркером ИР, является фактором риска ЖКБ.
Как уже упоминалось выше, холестериновые камни формируются при участии
нескольких патогенетических факторов, включая перенасыщенность печеночной желчи
холестерином и нарушение моторики желчного пузыря (ЖП) [2]. Гиперинсулинемия и
ИР могут воздействовать на каждый из этих факторов. Так, гиперинсулинемия
напрямую влияет на метаболизм липидов в печени, увеличивает синтез холестерина,
влияя на активность гидроксилметилглутарил-КоА-редуктазы (ГМГ-КоА-редуктазы),
повышает захват печенью липопротеинов низкой плотности (ЛПНП). Кроме того,
инсулин подавляет базальную и стимулированную холецистокинином моторику ЖП. В
экспериментах на мышах установлено, что у животных с нормальной массой и СД была
снижена сократимость ЖП и в его полости быстро образовывались кристаллы
холестерина, причем сократительная способность ЖП у животных с ожирением
ослабевала по мере повышения уровня глюкозы и инсулина в крови.
Цель исследования. Изучить особенности клинического течения
ЖКБ у детей с ожирением и метаболическим синдромом.
Материалы и методы. Обследован 51 ребенок с ЖКБ. В процессе
исследования выделено две группы: I группа — 25 детей с ЖКБ и ожирением (SDS по
ИМТ (индексу массы тела) более 1,99, средний возраст 12,06 ± 0,37 года,
мальчиков — 9, девочек –16), II группа — 26 детей с ЖКБ, имеющих нормальную
массу тела (SDS по ИМТ ± 0,99, средний возраст 9,68 ± 0,52 года, мальчиков — 11,
девочек — 15).
Всем детям проводился комплекс лабораторно-инструментальных методов
обследования, включающих ультразвуковое исследование (УЗИ) органов
гепатобилиарной системы и поджелудочной железы, эндоскопическое исследование
верхнего отдела ЖКТ, биохимическое исследование сыворотки крови с определением
уровня печеночных ферментов, показателей углеводного и липидного обмена
(глюкозы, инсулина, С-пептида, холестерина и его фракций). Диагностика МС
основывалась на классификации Международной диабетической федерации (International
Diabetes Federation, IDF) (2007), согласно которой о наличии МС у подростков
10–16 лет свидетельствует наличие абдоминального ожирения (окружность талии
более 90 перцентили) в сочетании с не менее двумя из следующих признаков:
- уровень триглицеридов > 1,7 ммоль/л;
- уровень липопротеидов высокой плотности < 1,03 ммоль/л;
- повышение артериального давления > 130/85 мм рт. ст.;
- повышение уровня глюкозы венозной плазмы натощак > 5,6 ммоль/л или
выявленный СД 2-го типа и/или другие нарушения углеводного обмена [9].
Статистическая обработка результатов проведена с использованием
статистического пакета Statistika 5.5. Различия среднеарифметических величин
считали достоверными при р < 0,05.
Результаты и их обсуждение. В результате проведенного
обследования установлено, что признаки экзогенно-конституционального ожирения
имели 15 (60,0%) детей I группы, гипоталамического ожирения — 9 (36,0%), причем
у 5 (55,6%) из них гипоталамический синдром развился на фоне первичного
ожирения. Еще у 1 ребенка (4,0%) диагностировано нейроэндокринное ожирение (микроаденома
гипофиза). У 16 (64,0%) больных определялась I–II степень ожирения, у 11 (44,0%)
— III–IV степень ожирения. В 2/3 случаев (17–68%) жировая клетчатка
распределялась по абдоминальному и смешанному типу, реже — по гиноидному.
Признаки МС выявлены у 16 (64,0%) детей I группы. Все дети с МС были
подросткового возраста, причем половина из них (13–52,0%) — старше 12 лет.
Выявлены характерные межгрупповые возрастные различия (табл. 1).
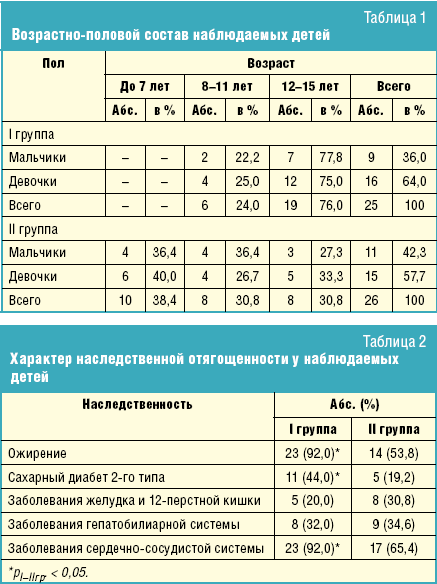
В обеих группах преобладали дети пубертатного возраста, при этом подростки 12
лет и старше в I группе встречались значительно чаще, чем во II группе, —
соответственно 76,0% и 30,8% (р < 0,05). Дети младшего возраста (до 7 лет)
встречались исключительно во II группе (38,4%). Полученные данные
свидетельствуют о высокой частоте диагностики МС и ЖКБ у детей старшего
школьного возраста, что может свидетельствовать о единых механизмах их
патогенеза.
Как в I группе, так и во II группе преобладали девочки (16–64% и 15–57,7%
соответственно). Преобладание лиц женского пола характерно как для ожирения, так
и для ЖКБ, причем как в детском возрасте, так и у взрослых, что согласуется с
данными литературы. Высокая частота заболеваемости ЖКБ среди мальчиков II группы
младшего школьного возраста свидетельствует об особенностях камнеобразования и,
в частности, о высокой частоте пигментного литиаза в этом возрастном периоде.
Абсолютное большинство обследованных детей имели наследственную отягощенность
по различным заболеваниям обменного характера и болезням органов пищеварения
(табл. 2).
Ожирение, СД 2-го типа, а также болезни сердца и сосудов (ГБ, ИБС)
значительно чаще выявлялись у родственников детей I группы (р < 0,05).
Заболевания органов пищеварения регистрировались чаще во II группе, значимых
различий при этом не выявлено.
В обеих группах отмечены общие закономерности. Так, среди родственников,
страдающих заболеваниями гепатобилиарной системы и болезнями обменного генеза,
преобладали лица женского пола, тогда как заболевания ЖКТ чаще выявлялись у
мужчин. Несколько чаще наследственная отягощенность прослеживалась по линии
матери (11–44,0% и 12–46,2% детей I и II группы соответственно), реже — по линии
обоих родителей (соответственно 6–24,0% и 6–23,1% детей).
Основными клиническими проявлениями ЖКБ у большинства детей обеих групп были
болевой и диспепсический синдромы. Боли в животе в анамнезе отмечались у 19
(76,0%) детей I группы и 23 (88,5%) детей II группы. Каждый третий ребенок в
обеих группах предъявлял жалобы на нарушения дефекации: неустойчивый характер
стула отмечался у 8 (32,0%) детей I группы и 7 (26,9%) детей II группы, запоры —
у 4 (16,0%) и 10 (38,5%) детей соответственно.
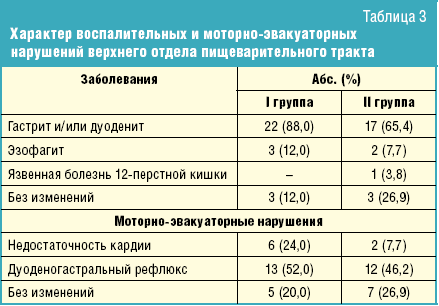
Из сопутствующей патологии со стороны органов пищеварения наиболее часто
диагностировались воспалительные изменения верхнего отдела пищеварительного
тракта (гастриты и/или дуодениты) и моторно-эвакуаторные нарушения (дуоденогастральный
рефлюкс, недостаточность кардии) (табл. 3).
В результате проведенного эндоскопического обследования установлено, что
морфофункциональные изменения слизистой пищевода на фоне нарушения деятельности
верхнего кардиального сфинктера значительно чаще регистрировались у детей I
группы.
Диффузные изменения поджелудочной железы в виде повышения эхогенности
паренхимы, неоднородности структуры и увеличения размеров органа или его
отдельных частей регистрировались у 23 (92,0%) детей I группы и 19 (73,1%) детей
II группы. Увеличение поперечного размера печени при УЗИ достоверно чаще
отмечалось у детей I группы, изменения паренхимы печени в виде повышения
эхогенности, а также диффузной неоднородности, нечеткости сосудистого рисунка и
затухания ультразвукового луча, являющиеся УЗ-признаками НАЖБП, определялись
исключительно у детей I группы (табл. 4).
Различные аномалии развития ЖП регистрировались одинаково часто как у детей I,
так и II группы (48,0% и 46,2% соответственно). Изменения стенки ЖП, характерные
для развития холестероза, диагностировались значительно чаще у детей I группы (р
< 0,05). У 2/3 детей I группы обнаруживались желчные конкременты в полости
пузыря, а у 1/3 — билиарный сладж, тогда как во II группе предкаменная стадия
ЖКБ определялась значительно реже — билиарный сладж в этой группе выявлялся у
11,5% больных (р < 0,05), что может свидетельствовать об отличных механизмах
патогенеза камнеобразования у детей с нарушениями липидного и углеводного
обмена.
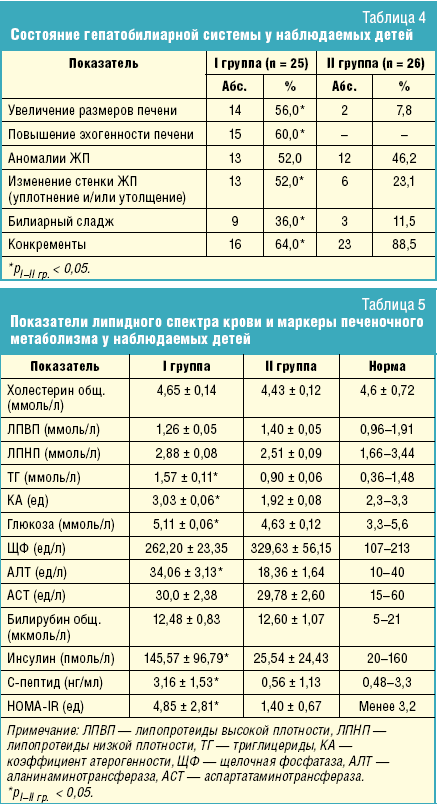
Установлены характерные различия ряда показателей сыворотки крови у
наблюдаемых детей (табл. 5).
У каждого четвертого ребенка I группы (7–28,0%) выявлено повышение показателя
АЛТ, причем у половины из них — в 1,5 и более раз, что может свидетельствовать о
течении ЖКБ на фоне формирования воспалительного процесса в печени в виде НАСГ.
У больных I группы отмечалось повышение уровня общего холестерина и
триглицеридов, причем средние значения этих показателей были выше долженствующих
норм для данного возраста. Значения глюкозы сыворотки крови натощак, инсулина,
С-пептида и индекса ИР (НОМА-IR) были также выше у детей I группы (р < 0,05),
что свидетельствует о выраженных нарушениях липидного и углеводного обмена у
детей с ЖКБ, протекающей на фоне ожирения.
Таким образом, полученные данные свидетельствуют о тесной
этиопатогенетической взаимосвязи холелитиаза с нарушениями углеводного и
липидного обмена в детском возрасте, что требует включения в комплексную терапию
детей с ожирением и тесно ассоциированным с ним МС препаратов, улучшающих
морфофункциональное состояние печени и желчевыводящих путей.
Одним из препаратов выбора в лечении этой категории больных может являться
препараты урсодезоксихолевой кислоты (УДХК), которая обладает доказанным
спектром положительных эффектов. За счет стабилизации физико-химических свойств
желчи, предотвращения осаждения кристаллов в ЖП, компенсации потерь желчных
кислот и слабого холекинетического эффекта препарат способствует восстановлению
моторной функции желчевыводящих путей и снижает риск образования билиарного
сладжа и конкрементов в ЖП. Кроме того, он существенно уменьшает холестаз,
обладает гепатопротективным, умеренным иммуномодулирующим действием, блокирует
пролиферативную фазу фиброгенеза, обладает антиоксидантными свойствами.
Оптимальным и наиболее изученным лекарственным препаратом УДХК является
Урсофальк, который производится в Германии с 1979 г. и применяется в большинстве
стран Евросоюза в трех лекарственных формах — капсулы, таблетки и суспензия.
Другие лекарственные средства, содержащие УДХК, могут иметь различия как по
эффективности действия, так и по побочным реакциям. Урсофальк является
референтным (эталонным) препаратом УДХК в Евросоюзе, т. е. все другие препараты
УДХК для регистрации должны предоставить данные о полной фармакологической и
клинической эквивалентности именно Урсофальку.
Целесообразно и патогенетически обосновано включение в комплексную терапию МС
препаратов на основе пищевых волокон. К ним относится Мукофальк (псиллиум),
содержащий в своем составе пищевые волокна семян подорожника овального (Plantago
ovata). При приеме Мукофалька образующаяся в тонкой кишке гельформирующая
фракция связывает желчные кислоты (ЖК), снижая их реабсорбцию в терминальном
отделе подвздошной кишки и увеличивая их экскрецию с калом. Потеря ЖК
активизирует внутриклеточную 7-альфа-гидроксилазу холестерина, что приводит к
повышенному образованию ЖК из холестерина и уменьшению его запасов внутри
клеток. Как следствие повышается активность рецепторов ЛПНП на поверхности
клеток и увеличивается экстракция холестерина ЛПНП из крови, что приводит к
снижению уровня холестерина в плазме крови. В связи с тем, что сорбируются
желчные кислоты неодинаково (свободные ЖК связываются больше, чем конъюгаты),
снижается индекс литогенности желчи. Растворимые объем-формирующие вещества
расщепляются кишечной микрофлорой на короткоцепочечные жирные кислоты,
ингибирующие ГМГ-КоА-редуктазу, что снижает новый синтез холестерина. Псиллиум
способствует снижению уровня глюкозы крови, замедляя всасывание сахара в тонкой
кишке. Уменьшается и всасывание холестерина из кишечника.
Выводы
- ЖКБ у детей, страдающих ожирением, с высокой частотой сочетается с МС
(64%) и абдоминальным характером распределения жировой ткани (68%).
- Среди детей с ЖКБ, протекающей на фоне ожирения, значительно чаще
выявляются подростки 12 лет и старше (44%, р < 0,05).
- Установлена высокая частота наследственной отягощенности по заболеваниям
сердечно-сосудистой системы, болезням обменного характера у детей с ЖКБ,
протекающей на фоне ожирения, что оказывает определенное влияние на
формирование и течение заболевания у данной категории больных.
- Высокая частота диагностики у детей с ожирением предкаменной стадии ЖКБ
может свидетельствовать об особенностях формирования желчных конкрементов у
этой категории больных.
- У детей с ожирением и МС с высокой частотой ЖКБ сочетается с диффузными
изменениями печени и поджелудочной железы, характерными для развития стеатоза,
воспалительными и моторными нарушениями верхнего отдела ЖКТ.
- Патогенетически обосновано включение в комплексную терапию детей с ЖКБ,
протекающей на фоне ожирения и МС, препаратов УДХК (Урсофальк) и псиллиума (Мукофальк),
оказывающих спектр положительных эффектов на липидный и углеводный обмен,
улучшающих морфофункциональное состояние гепатобилиарной системы, снижающих
литогенность желчи.
Литература
- Бокова Т. А., Урсова Н. И. Патология гепатобилиарной системы у
детей и подростков с ожирением и метаболическим синдромом // Врач. 2011, № 1,
с. 56–58;
- Герок В. Заболевания печени и желчевыделительной системы. М.:
МЕДпресс-информ, 2009. 199 с.
- Дедов И. И., Мельниченко Г. А. Ожирение в подростковом возрасте.
Результаты российского эпидемиологического исследования // Терапевт. архив.
2007. № 10, с. 28–32.
- Лазебник Л. Б., Звенигородская Л. А. Метаболический синдром и
органы пищеварения. М., 2009. 177 с.
- Маев И. В., Дичева Д. Т. Патогенетические механизмы формирования
патологии гепатобилиарной системы у больных с метаболическим синдромом и пути
их коррекции // Consilium medicum. Гастроэнтерология. 2008, № 2, с. 33–36.
- Успенский Ю. П., Балукова Е. В. Метаболический синдром и
неалкогольный стеатогепатит: причинно-следственный континуум // Consilium
medicum. Гастроэнтерология. 2009, № 1, с. 41–45.
- Харитонова Л. А., Запруднов А. М. Обменно-воспалительные
заболевания билиарного тракта у детей (алгоритмы диагностики и лечения). М.,
2010, 36 с.
- Чазова И. Е., Мычка В. Б. Профилактика, диагностика и лечение
метаболического синдрома. М., 2005. 48 с.
- Zimmet P., Alberti G. The metabolic syndrome in children and
adolescents // Lancet. 2007. 369: 2059–2961.
Статья опубликована в журнале
Лечащий Врач