Сравнительное изучение эффективности и переносимости
оригинальных и генерических препаратов периндоприла
А. И. Малыхина*
М. В. Журавлева**, доктор медицинских наук, профессор
А. К. Стародубцев**, доктор медицинских наук, профессор
О. А. Рогачева*
* ГУЗГКБ № 23 им. Медсантруд ДЗ Москвы,
** ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Артериальная гипертензия (АГ) является одной из наиболее важных медицинских и
социальных проблем во всем мире [1–3]. Согласно результатам обследования
российской национальной представительной выборки, стандартизированной по
возрасту, распространенность АГ у мужчин составляет 37,2%, у женщин — 40,4% [4].
АГ является хорошо изученным и доказанным независимым фактором риска развития
инсульта, инфаркта миокарда и других сердечно-сосудистых заболеваний.
Имеющиеся в настоящее время данные доказательной медицины в кардиологии
предоставляют врачу огромные возможности в отношении лечения и профилактики
сердечно-сосудистых заболеваний. В многочисленных контролируемых исследованиях
продемонстрирована способность целого ряда лекарственных препаратов
предупреждать возникновение осложнений сердечно-сосудистых заболеваний и, в
конечном счете, продлевать жизнь больных [5–6], однако не следует забывать о
том, что все результаты этих исследований были получены с использованием
оригинальных препаратов.
На российском рынке сегодня представлены три вида лекарственных препаратов:
оригинальные лекарства, воспроизведенные препараты, или генерики, и
фальсификаты. По официальным источникам соотношение инновационных и
воспроизведенных препаратов в России определяется как 1:4 (Рекомендации по
рациональной фармакотерапии больных сердечно-сосудистыми заболеваниями, 2009).
Единственным недостатком оригинальных препаратов является их высокая
стоимость, ограничивающая их широкое применение [7].
Генерики с доказанной терапевтической эквивалентностью оригинальным
препаратам могут применяться в клинической практике, и только при назначении
таких генериков мы сможем ожидать таких же результатов в отношении
предупреждения риска сердечно-сосудистых осложнений, которые были получены в
контролируемых рандомизированных исследованиях с оригинальными препаратами [8].
Целью нашей работы являлось изучение терапевтической эквивалентности и
переносимости двух препаратов периндоприла и фармакоэкономической
целесообразности их применения у больных мягкой и умеренной АГ.
Материалы и методы исследования
Характеристика материала
В исследование было включено 45 пациентов (19 мужчин и 26 женщин) в возрасте
от 35 до 75 лет (средний возраст — 53 года).
Для исследования были отобраны пациенты с АГ 1–2 степени (140 ≤ систолическое
артериальное давление (САД < 180 мм рт. ст. и/или 90 ≤ диастолическое
артериальное давление (ДАД) < 110 мм рт. ст.).
Из 45 пациентов, включенных в исследование, у 29 (64,4%) была диагностирована
АГ 1-й степени, у 16 (35,6%) — 2-й степени. Длительность АГ составила от 1 года
до 37 лет (в среднем — 7,4 года).
Проведено открытое перекрестное рандомизированное научное исследование по
сравнительному изучению терапевтической эффективности и переносимости
оригинального и воспроизводимого препаратов периндоприла. Исследование проведено
в соответствии с современными требованиями МЗ РФ.
Пациенты, включенные в исследование, прошли обследование с учетом данных
анамнеза. Учитывались следующие показатели: возраст, пол, вес, рост, наличие
факторов риска (ФР) развития сердечно-сосудистых заболеваний (ССЗ), длительность
заболевания, предшествующая терапия, сопутствующие заболевания и сопутствующая
терапия, уровень артериального давления (АД) и частота сердечных сокращений (ЧСС).
Из биохимических показателей контролировался уровень калия, креатинина,
глюкозы, показатели липидного обмена, а также уровни ферментов:
аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), и билирубина.
Все пациенты соответствовали следующим критериям включения:
- наличие письменного информированного согласия пациента на участие в
исследовании;
- мужчины и женщины в возрасте от 35 до 75 лет;
- первичная (эссенциальная) артериальная гипертензия 1–2 степени.
Критериями невключения в исследование были следующие факторы:
- повышенная чувствительность к исследуемым препаратам и его компонентам;
- любые формы вторичной (симптоматической) АГ;
- АГ 3-й степени (САД > 180 мм рт. ст. и/или ДАД > 110 мм рт. ст.);
- нестабильная стенокардия, стенокардия напряжения III–IV функционального
класса, инфаркт миокарда в анамнезе;
- выраженная цереброваскулярная недостаточность, острое нарушение мозгового
кровообращения в анамнезе;
- хроническая сердечная недостаточность III–IV согласно критериям
Нью-Йоркской кардиологической ассоциации (New York Heart Association (NYHA));
- постоянная форма фибрилляции предсердий;
- двусторонний стеноз почечных артерий или стеноз артерии единственной
почки;
- печеночная недостаточность (уровни АЛТ или АСТ или общий билирубин или
щелочная фосфатаза более чем в 3 раза выше верхней границы нормы);
- гиперкалиемия ≥ 5,5 ммоль/л;
- сахарный диабет;
- злоупотребление алкоголем, психотропными, наркотическими веществами.
Протокол исследования
Все 45 пациентов, включенных в исследование, получили по 2 курса
(длительностью по 2 месяца каждый) гипотензивной терапии оригинальным (Престариум
А производства компании Servier, Франция) и воспроизведенным периндоприлом (Парнавел
производства ООО «Озон», Россия).
Последовательность назначения курсов препаратов для каждого больного
определялась путем рандомизации «методом конвертов». Длительность исследования
для каждого пациента составила 4 месяца.
Пациентам с высоким риском развития сердечно-сосудистых осложнений (ССО) по
SCORE (Systematic COronary Risk Evaluation) назначалась комбинированная терапия
(периндоприл + индапамид). Всем пациентам, включенным в исследование,
проводились рутинные лабораторные методы исследования, электрокардиография (ЭКГ),
эхокардиография (ЭХО-КГ), ультразвуковая допплерография бассейна средних
мозговых артерий (УЗДГ СМА), суточное мониторирование артериального давления (СМАД)
и нейропсихологическое тестирование (краткое исследование психического состояния
(Mini-Mental State Examination — MMSE), FAB-шкала (Frontal Assessment Battery),
тест на запоминание 10 слов).
Через 2 месяца лечения проводилось контрольное СМАД с последующей
перекрестной заменой препарата: оригинального на воспроизведенный и наоборот, и
пациент в течение 2 месяцев продолжал курс терапии, по окончании которого вновь
проводилось контрольное СМАД, рутинные лабораторные методы исследования, ЭКГ,
УЗДГ СМА, СМАД, ЭХО-КГ и нейропсихологическое тестирование (MMSE, FAB-шкала,
тест на запоминание 10 слов).
На протяжении всего исследования проводилась оценка общей переносимости,
контроль АД и ЧСС, а также фиксировались возможные побочные действия препарата.
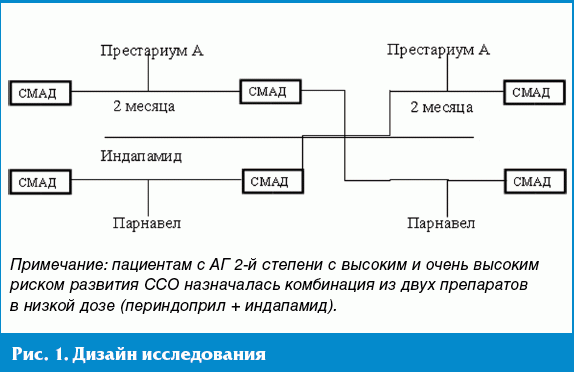
Дизайн исследования представлен на рис. 1. Эффективность препаратов оценивали
по достижению целевых значений АД: САД < 140 мм рт. ст. и ДАД < 90 мм рт. ст.
Статистический анализ
Статистический анализ данных включал элементы описательной статистики
(количество больных, средние и стандартные ошибки и др.).
Была оценена эффективность препаратов и проведена оценка нежелательных
лекарственных явлений на фоне приема препаратов. Достоверность различий
оценивали с использованием парного t-критерия Стьюдента. Различия считали
достоверными при p < 0,05.
Для оценки фармакоэкономической эффективности терапии использовали анализ
минимизации затрат (cost minimization analysis) [9, 10].
Результаты и их обсуждение
Из исследования выбыло 5 человек: 4 из-за нежелательных лекарственных
реакций: 2 мужчин (на фоне приема Парнавела через 1,5 недели и через 2 недели на
фоне приема Престариума А появился сухой кашель) и 2 женщины (на фоне приема
Парнавела появилась тошнота, у одной на 4-й день, у другой на 7-й день). 1
мужчина из I группы Престариума А отказался от дальнейшего участия в
исследовании на втором визите, таким образом, полностью курс лечения
Престариумом А и Парнавелом завершило 40 человек.
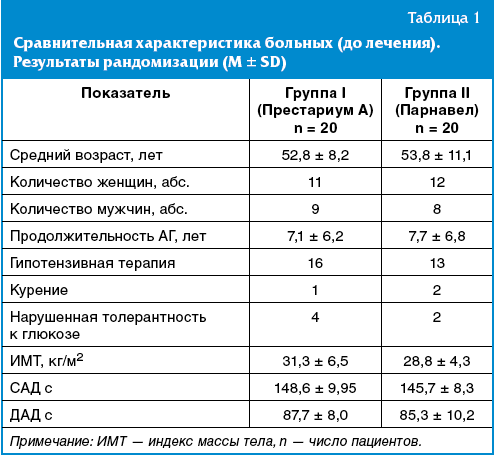
В результате рандомизации были сформированы две группы пациентов, в одной из
которых первым получаемым препаратом был Престариум А, а в другой — Парнавел
(табл. 1). Статистически значимых отличий по основным параметрам
(клинико-демографическая характеристика, показатели СМАД, ЭХО-КГ и УЗДГ, а также
когнитивные функции) на начало исследования между группами выявлено не было,
поэтому результаты анализировались суммарно и без учета последовательности
назначения препарата.

По исходным показателям СМАД статистически значимых различий между группами
выявлено не было (табл. 2).
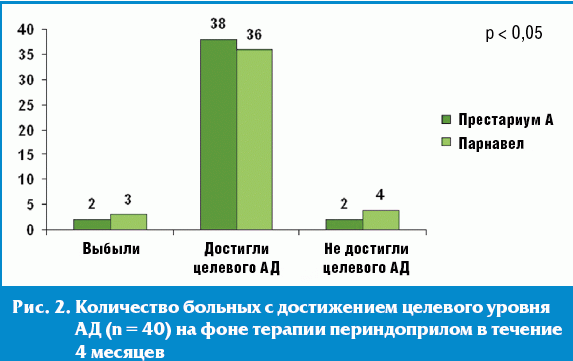
Целевого уровня АД (< 140/90 мм рт. ст.) после 4 месяцев терапии достигли 95%
пациентов в группе Престариума А и 90% пациентов в группе Парнавела (рис. 2).
Динамика АД на фоне регулярного приема Престариума А и Парнавела представлена
в табл. 3.
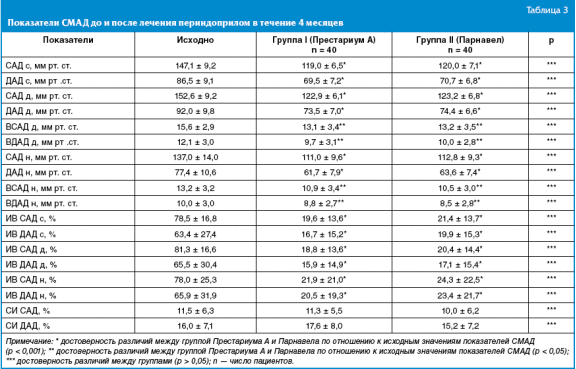
Исходно при анализе результатов СМАД выявлен высокий уровень вариабельности
АД, показателей «нагрузки давлением», что является фактором риска развития
ассоциированных клинических состояний.
По завершении исследования в обеих группах пациентов, получавших Престариум А
или Парнавел, отмечалось достоверное снижение среднесуточных, среднедневных,
средненочных показателей САД и ДАД, а также статистически значимое уменьшение
времени нагрузки давлением на протяжении суток для САД и ДАД, в обоих случаях р
< 0,001 за исключением суточного индекса (СИ) САД и СИ ДАД (p > 0,05). Различия
между группами были недостоверными. Вариабельность САД и ДАД достигла
достоверных значений как в дневной, так и в ночной периоды (р < 0,05).
При проведении индивидуального анализа полного контроля АД достигли 25
пациентов (65,8%), принимавших Престариум А, и 21 пациент (58,3%), принимавший
Парнавел, таким образом, 13 пациентов (34,2%) и 15 пациентов (41,7%) достигли
частичного контроля АД в группах Престариума А и Парнавела соответственно.
Анализируя показатели ЭХО-КГ, представленные в табл. 4, отмечается
достоверное уменьшение толщины задней стенки левого желудочка (ТЗСЛЖ) и толщины
межжелудочковой перегородки (ТМЖП). Отмечается тенденция к увеличению фракции
выброса (ФВ), однако она не является статистически достоверной.
Что касается переносимости препаратов и их побочного действия, то следует
отметить, что во время исследования только у 4 пациентов были зарегистрированы
нежелательные лекарственные реакции (НЛР), которые послужили причиной исключения
пациентов из исследования. НЛР не носили характера серьезных, но потребовали
отмены препарата.
Зарегистрированные во время исследования побочные реакции перечислены в табл.
5.
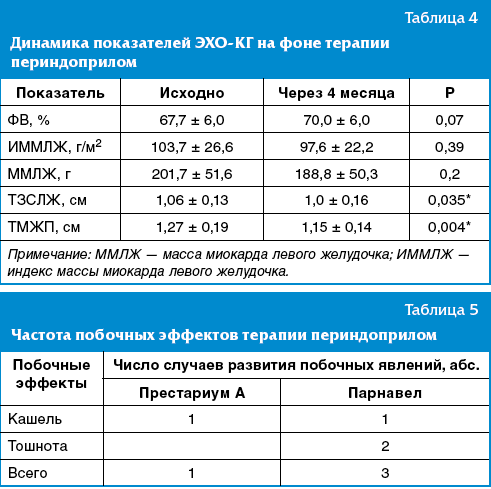
Зарегистрированные побочные эффекты были типичными для этого класса препарата
и были неоднократно описаны другими исследователями [11].
В данном исследовании подтверждены терапевтическая эффективность и
безопасность использования генерического препарата периндоприла Парнавела в
сравнении с оригинальным препаратом.
Достижение целевого уровня АД у 90–95% больных (при приеме как Парнавела, так
и Престариума А) свидетельствует о выраженной гипотензивной активности
сравниваемых препаратов при лечении больных АГ 1–2 степени.
Монотерапия оказалась эффективна лишь у 25% больных, включенных в
исследование.
Полученные данные свидетельствуют о сопоставимом гипотензивном эффекте двух
препаратов периндоприла: Парнавела и Престариума А у пациентов с артериальной
гипертензией 1–2 степени. При проведении статистического анализа с
использованием стандартных методов описательной статистики оказалось, что по
основным показателям СМАД: по снижению среднесуточных, среднедневных,
средненочных показателей САД и ДАД, а также индексу времени и вариабельности АД
между препаратами достоверных отличий выявлено не было.
Не было выявлено также значимых отличий в отношении переносимости обоих
препаратов и регистрации побочных явлений в группах, различавшихся по
последовательности назначавшихся препаратов.
Таким образом, можно считать, что препарат Парнавел по основному критерию
эффективности, в первую очередь, по способности добиваться целевых значений АД,
в целом соответствует оригинальному препарату периндоприла.
Заключение
Отечественный генерический препарат периндоприла Парнавел имеет сходный
оригинальному препарату профиль клинической эффективности и безопасности.
Однако при назначении Парнавела, также как и других гипотензивных препаратов,
следует использовать принципы персонализированной медицины.
Литература
- Бритов А. Н. Профилактика артериальной гипертонии на
популяционном уровне: возможности и актуальные задачи // Рос. мед. журн. 1997.
5 (9). 571–576.
- Оганов Р. Г., Масленникова Г. Я. Смертность от
сердечно-сосудистых и других хронических неинфекционных заболеваний среди
трудоспособного населения России // Кардиоваскулярная терапия и профилактика.
2002. 3. 4–8.
- Шальнова С. А. Проблемы лечения артериальной гипертонии //
Кардиоваскулярная терапия и профилактика. 2003. 2 (3). 17–21.
- Фонякин А. В., Гераскина Л. А., Суслина З. А. Артериальная
гипертензия, цереброваскулярная патология и сосудистые когнитивные
расстройства. Актуальные вопросы. М., 2006. С. 3.
- Оганов Р. Г., Марцевич С. Ю. Лекарственная терапия
сердечно-сосудистых заболеваний: данные доказательной медицины и реальная
клиническая практика // Российский кардиологический журнал. 2001; 4: 8–11.
- Volpe M., Alderman M., Furberg C. et al. Beyond hypertension.
Toward guide-lines for cardiovascular risk reduction // Amer. J. Hypertension.
2004; 17: 1068–1074.
- Марцевич С. Ю., Кутишенко Н. П., Деев А. Д. Оригинальные
препараты и дженерики в кардиологии. Можно ли решить проблему
взаимозаменяемости? // Вестник Росздравнадзора. 2009, № 4.
- Марцевич С. Ю., Кутишенко Н. П., Якусевич В. В. Еще раз о
проблеме взаимозаменяемости лекарств. Взгляд на дженерики с позиций
доказательной медицины // Вести кардиологии. 2010, с. 19.
- Авксентьева М. В., Воробьев П. А., Герасимов И. Б., Горохова С. Г.
Проект отраслевого стандарта «Фармакоэкономические исследования. Общие
положения» // Проблемы стандартизации в здравоохранении. 2000. № 4. С. 42–54.
- Кабина С. А., Семенов В. Ю. Введение в фармакоэкономику // Проблемы
стандартизации в здравоохранении. 1999. № 1. С. 39–48.
- Барбараш О. Л., Полтавцева О. В., Смакотина С. А. Проаритмические
факторы у больных гипертонической болезнью. Эффект периндоприла //
Артериальная гипертензия. 2005, т. 11, № 3.
Статья опубликована в журнале
Лечащий Врач