Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
6.3. Локализация постинсультных ишемических
поражений головного мозга и дальнейшее развитие стресс-индуцированной
сердечно-сосудистой патологии
Для решения вопроса о том, как локализация перенесенного в прошлом
ишемического инсульта, могла влиять на варианты дальнейшего развития и
клинического течения сердечно-сосудистой патологии, было проведено сравнительное
исследование среди больных выделенных нами 1-й и 2-й групп наблюдений с
присутствием ишемического инсульта полушарной локализации в анамнезе.
Среди представителей 1-й группы наблюдений ишемические инсульты
перенесли 24 пациента. При этом правосторонняя локализация коркового
ишемического очага имела место у 15 (62,50%) них, левосторонняя - у 9 (37,50%).
Преимущественно были поражены лобные (n=8;
33,33%), теменные (n=7; 29,17%)
и височные (n=7; 29,17%)
области головного мозга. Ишемический инсульт с локализацией преимущественно в
затылочных долях диагностирован у 2 (8,33%) пациентов.
Во 2-й группе наблюдений, из 13 больных с наличием ишемического
инсульта в анамнезе, зоны постинсультного ишемического церебрального очага были
локализованы справа у 6 (46,15%), слева - у 7 (53,85%) пациентов.
Преимущественно были поражены теменные (n=5;
38,46%) и височные (n=5;
38,46%) области головного мозга. Ишемические очаги в затылочных долях
диагностированы в 3 (23,08%) наблюдениях. Исходя из этих данных, группы по
признаку локализации ишемического очага были сопоставимы. Результаты
представлены в табл. 58 и на рис. 37.
Таблица 58. Варианты сердечно-сосудистой
патологии в зависимости от локализации постинсультного ишемического очага
|
Варианты
сердечно-сосудистой
патологии |
Последствия ишемического инсульта, локализация ишемического
очага (n=37; 100%); |
|
правосторонняя, n=21
(56,76%) |
левосторонняя, n=16
(43,24%) |
|
n |
% |
n |
% |
|
Артериальная гипертония |
21 |
100 |
16 |
100 |
|
ИБС: стенокардия |
21 |
100 |
16 |
100 |
|
I-II ФК |
13 |
61,9 |
3 |
18,75* |
|
III-IV ФК |
8 |
38,1 |
13 |
81,25* |
|
ПИКС |
6 |
28,57 |
10 |
62,5* |
|
Нарушения ритма и проводимости: |
9 |
42,86 |
11 |
68,75* |
|
Фибрилляция предсердий |
5 |
23,81 |
8 |
50* |
|
сложные |
4 |
19,05 |
3 |
18,75 |
|
Облитерирующий атеросклероз артерий нижних конечностей: |
21 |
100 |
16 |
100 |
|
I-II ст. |
8 |
38,1 |
9 |
56,25 |
|
III-IV ст. |
13 |
61,9 |
7 |
43,75 |
Примечание: *- р<0,05.
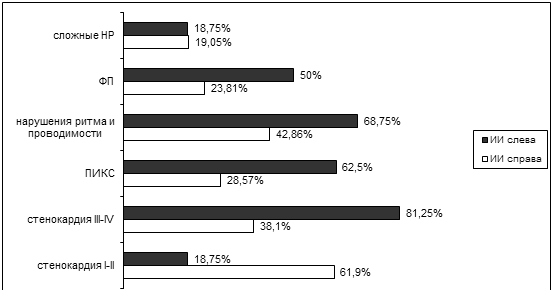
Рис. 37. Зависимость сердечно-сосудистых
расстройств от локализации перенесенного в прошлом ИИ.
Как следует представленных из данных, сторонность перенесенного в
прошлом ишемического инсульта оказала существенное влияние на развитие и тяжесть
такой сердечно-сосудистой патологии, как ИБС. Так, III-IV
ФК стенокардии и ПИКС в анамнезе достоверно (р<0,05) чаще встречались среди
пациентов с левосторонней локализацией церебрального ишемического очага. Также и
фибрилляция предсердий (ФП) была представлена достоверно (р<0,05) чаще именно
при левостороннем постинсультном очаге.
При анализе атеросклеротических изменений, определенных
морфометрически, отличия выявлены как со стороны пре- и церебральных сосудов,
так и коронарных артерий, причем именно при левосторонней локализации
ишемического очага эти изменения достоверно (р<0,05) более выражены (рис. 38).
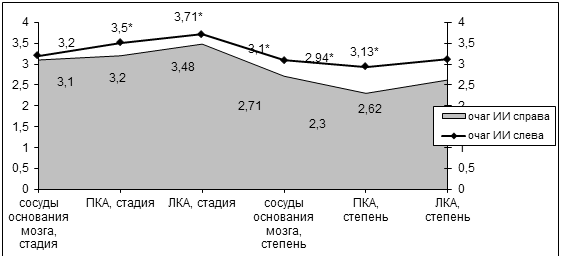
Рис. 38. Зависимость морфометрических изменений
от локализации ишемического очага.
Примечания: * - р<0,05; ПКА – правая коронарная артерия, ЛКА –
левая коронарная артерия.
Следовательно, именно при левосторонней локализации ишемического
церебрального очага, вне зависимости от сосудистого бассейна, отмечаются
наиболее тяжелые кардиальные расстройства. Также морфометрически определяемые
стадия и степень атеросклеротического поражения пре- и церебральных сосудов и
обеих коронарных артерий оказываются более значимыми при той же локализации.
Возможно, это объясняется экспериментальными данными, установившими, что
аритмогенез обусловливается патологической импульсацией из левого полушария
головного мозга, проявляясь преимущественно при поражениях лобной доли, и связан
с патологической активацией парасимпатической нервной системы (Бурцев Е.М.,
1993; Battarbee
B., Harold
D., 1995). Разумеется, с
течением времени, прошедшего после инсульта, прослеживается некоторая
положительная динамика нарушений, регулируемых центральными, надсегментарными
вегетативными образованиями, но полной нормализации все же не происходит. Именно
это позволяет рассматривать нарушения сердечного ритма и проводимости не только
как факторы риска развития ишемических расстройств мозгового кровообращения, но
и как «порочный круг» взаимосвязанной патологии, когда ишемический очаг, в свою
очередь, оказывает опосредованное негативное влияние на биоэлектрическую
активность не только головного мозга, но и пейсмейкерной системы сердца
(Мякотных В.С., Антюфьев В.Ф., 1991; Бейн Б.Н., 1997). Аномальный процесс
усугубляется и прогрессирующим атеросклеротическим поражением коронарных
артерий, в частности, правой коронарной, кровоснабжающей атриовентрикулярный и
синусовый узлы.

