
5.7 Инфекции мочевыводящих путей
Классификация инфекций мочевыводящих путей.
Согласно анатомической классификации, инфекции мочевыводящих путей
(ИМП) подразделяют на инфекции нижних и верхних отделов мочевыводящих путей. К
инфекции нижних мочевыводящих путей относится острый цистит, уретрит. К
инфекциям верхних отделов – острый и хронический пиелонефрит.
Неосложненные ИМП возникают при отсутствии обструкции в почках
и мочевыводящих путях, мочекаменной болезни, поликистоза почек, аномалий
развития и расположения почек, стриктур мочеточника, стриктур уретры,
пузырно-мочеточникового рефлюкса, доброкачественной гиперплазии предстательной
железы с нарушением пассажа мочи и т.д., а также у пациентов без серьезных
сопутствующих заболеваний.
В полной мере к неосложненным инфекциям мочевыводящих путей
относиться только острый цистит и острый пиелонефрит у небеременных женщин, без
стриктурных уропатий и неврологических нарушений.
Осложненные ИМП возникают у пациентов с различными
обструктивными уропатиями, на фоне инструментальных (инвазивных) методов
обследования и лечения, с серьезными сопутствующим заболеванием (сахарный
диабет, нейтропения). Осложненные ИМП могут приводить к развитию тяжелых
гнойно-септических осложнений, бактериурии, сепсиса.
Важность выделения осложненных и неосложненных ИМП определяется
разными подходами к лечению.
Острый цистит у взрослых
Острый цистит относится к наиболее распространенным заболеваниям,
при оказании медицинской помощи в амбулаторно-поликлиническом звене.
Встречаемость острого цистита у женщин составляет 0,5-0,7 эпизодов заболевания
на 1 женщину в год. Распространенность острого цистита в России, по расчетным
данным, составляет 26-36 миллионов случаев в год. Заболеваемость острым циститом
у взрослых мужчин крайне низка и составляет 6-8 эпизодов в год на 10000 мужчин в
возрасте 21-50 лет.
Риск развития острого цистита зависит от возраста, пола пациента,
наличия сопутствующих заболеваний и патологии мочевыводящих путей. У женщин риск
ИМП в 30 раз выше, чем у мужчин. Существенным фактором риска острого цистита у
молодых женщин является частота половых актов и характер применяемых
контрацептивов: частота возникновения острого цистита выше при использовании
диафрагм и спермицидов.
Этиологические агенты вызывающие острый цистит.
Наиболее значимым международным проектом по изучению этиологических
агентов вызывающих инфекции нижних мочевыводящих путей является проект
«ECO-SENS-проект». В рамках мультицентрового исследования (ECO-SENS-проект
2000-2002гг.), в котором приняло участие 240 центров в 16 странах Европы, было
обследовано 1960 пациентов с неосложненной инфекцией нижних мочевых путей, от
которых выделено 1463 патогенных штаммов микроорганизмов. Наиболее часто
выделяемым микроорганизмом явилась E.coli выявленная у 77,7 % больных, Proteus
mirabilis - 5,2 %, Klebsiella spp. - 2,8 %, другие Enterobacteriaceae - 3,9%,
Staphylococcus saprophyticus - 4,6 %, другие микроорганизмы - у 5,8 % пациентов.
Проведенное исследование выявило высокий уровень устойчивости в Европе
уропатогенной E.coli к таким антибиотикам как ампициллин и ко-тримоксазол.
Резистентность к фторхинолонам, нитрофуранам и фосфомицину по данным этого
исследования была невысокой. Так же исследование ECO-SENS подтвердило
предположение о существовании значительных географических отличий в уровне и
характере антибиотикорезистентности (таб. 5.20).
Таблица 5.20.
Резистентность штаммов E.coli, выделенных у
взрослых с неосложненными внебольничными ИМП в некоторых странах Европы, данные
исследования ECO-SENS, %
|
Страна |
Ампициллин |
Ко-тримоксазол |
Ципрофлоксацин |
Нитрофурантоин |
Фосфомицин |
|
Бельгия |
30,7 |
14,6 |
2,9 |
0,7 |
0,7 |
|
Франция |
27,6 |
15,1 |
2,0 |
1,0 |
1,0 |
|
Германия |
29 |
21 |
2,2 |
0,7 |
0 |
|
Нидерланды |
28,7 |
10,3 |
2,1 |
1,0 |
0,5 |
|
Норвегия |
23,8 |
11,3 |
0 |
0 |
1,2 |
|
Испания |
53,9 |
25,7 |
14,7 |
4,2 |
0,5 |
|
Великобритания |
37,2 |
12,2 |
0,6 |
0 |
0 |
|
По всем странам в среднем |
29,8 |
14,8 |
2,3 |
1,2 |
0,7 |
В другом трехлетнем международном исследовании по изучению
антибиотикорезистентности возбудителей острого неосложненного цистита (Antimicrobial
Resistance Epidemiological Survey on Cystitis - ARESC study), которое было
инициировано в сентябре 2003 года и закончено в июне 2006-го года (в
исследовании приняли участие 61 медицинский центр из 10 стран, в том числе из
Австрии - 3, Бразилии - 6, Франции - 10, Германии - 7, Венгрии - 4, Италии - 4,
Нидерландов - 2, Польши - 6, Испании - 9 и из России - 10 клиник) также было
определено, что в настоящее время ведущее место среди возбудителей неосложненной
инфекции мочевых путей в разных странах мира занимает E.coli 76,3 %, далее
S.saprophyticus 3,6 %, Klebsiella pneumonia - 3,5 %, Proteus mirabilis 3,1 %,
Enterococcus faecalis 3,0 %, Citrobacter - 1%, Enterobacter - 0,8 %, Pseudomonas
aeruginosa - 0,2 %, другие энтеробактерии - 4,4 %, грамположительные - 3,7 %
(рис. 5.16).
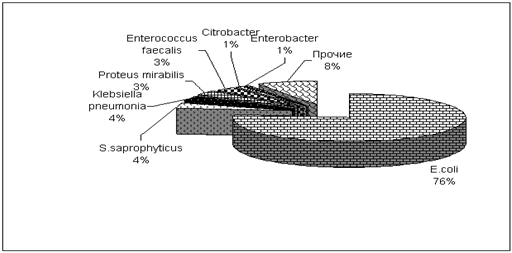
Рис. 5.16 Этиологическая структура возбудителей
цистита по данным исследования ARESC (n=3254),
%
При определении чувствительности к антибактериальным препаратам
были получены сходные данные по уровень резистентных штаммов к ко-тримоксазолу и
ампициллину по всем клиническим центрам (таб. 5.21).
Таблица 5.21.
Резистентность штаммов E. coli, выделенных у
взрослых с неосложненными циститами по результатам исследования ARESC, %
|
Антибактериальный препарат |
% резистентных штаммов страна |
|
Франция (n=331) |
Испания(n=438) |
Россия (n=146) |
|
Ampicillin |
45,2 |
75,9 |
67,1 |
|
Co-trimoxazole |
14,4 |
38,2 |
28,1 |
|
Amoxiсlav |
13,4 |
36,8 |
24 |
|
Cefuroxime ax. |
17,1 |
43,4 |
22,6 |
|
Nalidixic acid |
8,7 |
33 |
16,4 |
|
Ciprofloxacin |
2,3 |
13,6 |
10,3 |
|
Nitrofurantoin |
3 |
9,4 |
4,1 |
|
Fosfomycin |
1 |
0,9 |
1,4 |
Суммарные показатели резистентности E.coli (n=1562) демонстрировали
достаточно высокие уровень резистентных штаммов к налидиксовой кислоте,
амоксиклаву и цефуроксиму от 10 до 20% (рис. 5.17). Низкий уровень (<10%)
резистентных штаммов зафиксирован к препаратам: фосфомицину трометамолу,
нитрофуранам, фторхинолонам (ципрофлоксацину) и мециллинаму (полусинтетический
пенициллин - в России не зарегистрирован). Самый низкий уровень резистентных
штаммов к фосфомицину можно объяснить тем, что этот антибиотик применяется
только для лечения бактериального цистита, в монодозе, т.е. очень коротко и в
пище у животных он не используется, как другие антибиотики. Плазмидная передача
генов резистентности редкая (менее 2%) и нет ко-селекции с ампициллином,
цефалотином, тетрациклином.
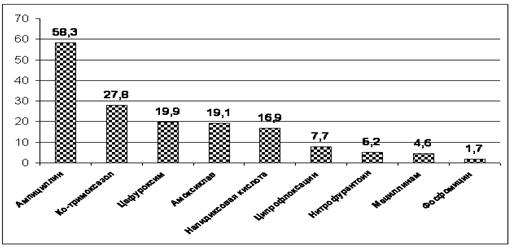
Рис. 5.17 Суммарные показатели резистентности к
АМП штаммов E.coli, выделенных у взрослых с неосложненными циститами по
результатам исследования ARESC (n=1562),
%
Возрастающая резистентность E. coli к фторхинолонам вызывает
серьезную озабоченность. Беспокойство ростом резистентности микроорганизмов к
фторхинолонам заставляет крайне осторожно рекомендовать их для рутинного лечения
неосложненной инфекции мочевых путей. В некоторых странах уровень штаммов E.
coli, резистентных к фторхинолонам, уже превысил 10%. Фосфомицин, мециллинам и
нитрофурантоин сохраняют свою высокую эффективность и могут успешно применяться
для эмпирической терапии неосложненной инфекции нижних мочевых путей.
Необходимо заметить, что т.к. в России уровень резистентных штаммов
возбудителей к пенициллинам и ко-тримоксазолу выше 20% (как по данным
исследования ARESC, так и по данным российских исследований по изучению
резистентности возбудителей неосложненной ИМП - UTIAP), такие препараты, как
сульфаметоксазол/триметоприм, ампициллин, амоксициллин в России для эмпирической
терапии НИМП не рекомендуются.
В связи с существованием региональных отличий в уровне
антибиотикорезистентности, крайне важной задачей является мониторинг
резистентности возбудителей ИМП в России. Данные по этиологии возбудителей
различных форм амбулаторных ИМП и их антибиотикорезистености были получены в
ходе многоцентровых проспективных эпидемиологических исследований,
организованных НИИ антимикробной химиотерапии Смоленской государственной
медицинской академии. По данным Л.С. Страчунского и В.В. Рафальского, 1999г.
(рис. 5.18), наиболее частыми возбудителями при острых циститах являются
грамотрицательные энтеробактерии, главным образом E.coli - 70-95%. Вторым по
частоте выделения является S.saprophyticus 5-20% , который чаще выделяется у
молодых женщин. Значительно реже НИМП вызывают другие грамотрицательные бактерии
(клебсиеллы, протеи, и др). В 1-2% возбудителями являются грамположительные
микроорганизмы (стрептококки, энтерококки).
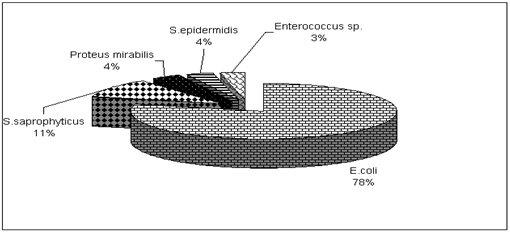
Рис. 5.18 Этиологическая структура возбудителей
острого цистита (n=200) (Л.Страчунский, В.Рафальский, 1999г. )
Исследования по изучению резистентности возбудителей острого
цистита в России показывают, что распространённость уропатогенных штаммов E.coli,
устойчивых к ампициллину и ко-тримоксазолу, является весьма высокой и составляет
33,3% и 18,4%, соответственно, фторхинолоны (ципрофлоксацин и норфлоксацин)
являются наиболее активными препаратами в отношении штаммов E.coli, выделенных
при остром цистите. Резистентность к ним составляет 2,6%. Кроме того,
ципрофлоксацин и норфлоксацин активны в отношении штаммов кишечной палочки,
устойчивых к налидиксовой и пипемидиевой кислотам (рис. 5.19).
Цели антибиотикотерапии.
- Быстрое купирование симптомов заболевания;
- Восстановление трудоспособности и социальной активности;
- Предупреждение осложнений;
- Профилактика рецидивов.
Выбор антимикробных препаратов.
Выбор препарата в подавляющем большинстве случаев проводится
эмпирически, на основе данных о преобладающих возбудителях (преимущественно
E.coli), их резистентности в регионе и тяжести состояния пациента (рис. 5.20).
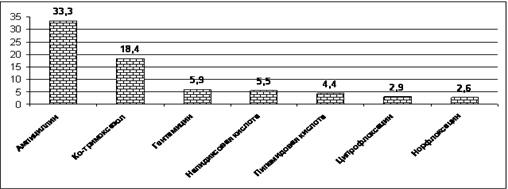
Рис. 5.19 Показатели резистентности к
антимикробным препаратам E. Coli,
выделенной из мочи от больных с острым циститом.
Основным критерием выбора продолжительности антибиотикотерапии
является наличие или отсутствие факторов риска. При отсутствии факторов риска
проводится 3-5 дневный курс, а при выявлении факторов риска рационально
использовать 7-дневный курс терапии.
Основными противопоказаниями к проведению короткого курса
антимикробной терапии являются:
- Беременность;
- Возраст > 65 лет;
- ИМП у мужчин;
- Длительность сохранения симптомов > 7 дней;
- Рецидив инфекции;
- Использование диафрагм и спермицидов;
- Сахарный диабет.
Для лечении острого цистита как осложненного так и не осложненного
используются одни и те же антимикробные препараты, которые отличаются только по
длительности антимикробной терапии.
В соответствии с рекомендациями Европейской и Американской
урологических ассоциации для лечения инфекций нижних отделов мочевыводящих
путей, 2007г.:
Препаратами выбора являются: пероральные фторхинолоны (норфлоксацин,
офлоксацин, ципрофлоксацин).
Альтернативные препараты: амоксициллин/клавуланат, фосфомицина
трометамол, нитрофурантоин, ко-тримоксазол (для регионов, где уровень
резистентности к E.coli составляет менее 10 %).
Ошибки при терапии острого цистита:
- Использование цефалоспоринов I
поколения (цефалексина), является нерациональным в связи с низкой активности в
отношении микроорганизмов вызывающих данный инфекционный процесс;
- Использование ко-тримоксазола является не всегда оправданым в связи с
высоким риском возникновения нежелательных побочных реакций (риск синдромов
Стивенса-Джонсона, Лайелла), а также высоким уровнем резистентности основных
микроорганизмов;
- Использование незащищенных аминопенициллинов (ампициллина и амоксициллина)
является нерациональным в связи с высокими показателями резистентности,
обусловленными продукцией β-лактамаз у грамотрицательных бактерий;
- Использование фторхинолонов (левофлоксацин, пефлоксацин) – приводит к
удорожанию стоимости проводимой фармакотерапии, при сохраняющейся одинаковой
эффективности.
- Использование инъекционных препаратов (цефазолин, гентамицин) в связи с
низкой комплаетностью пациентов к проводимой фармакотерапии и высокими
уровнями резистентности у микроорганизмов;
- Длительные курсы антибиотикотерапии при остром цистите. При отсутствии
факторов риска достаточно 3-5-дневных, а при их наличии – 7-дневных курсов
терапии. Увеличение продолжительности терапии существенно не влияет на
эффективность лечения, но увеличивает риск нежелательных реакций.
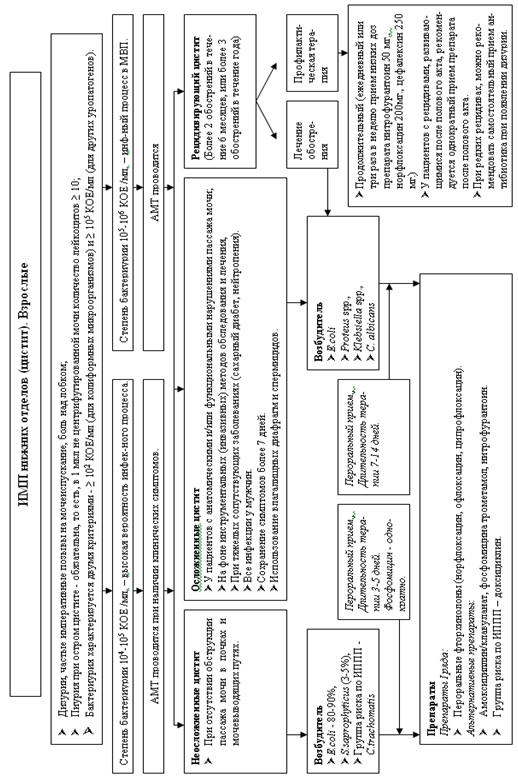
Рис. 5.20 Алгоритм ведения больных с ИМП нижних
отделов (цистит). Взрослые
Пиелонефрит - Неспецифическая бактериальная инфекция
органов мочевой системы с преимущественным вовлечением в бактериальный процесс
тубуло-интерстициальной ткани и чашечно-лоханочной системы почек.
В настоящее время пиелонефрит рассматривается как стадийный
процесс.
1 стадия: Преморбидный этап подавления и накопления в
макроорганизме потенциальных возбудителей инфекции (этап формирования
дисбактериоза или воспалительного очага).
2 стадия: Этап транслокации уропатогенов из исходного биотопа в
почки после преодоления иммунологических барьеров хозяина, прорыва микрофлоры в
лимфорусло и ее гематогенной диссеминации, заканчивающейся инфицированием почки.
3 стадия колонизации: закрепление инфекционных агентов в почечной
ткани путем адгезии на канальцевом и чашечно - лоханочном уроэпителии. Обратимые
этапы при адекватной терапии.
4 стадия альтерации колонизированных тканей: межклеточное и
тканевое взаимодействие возбудителя и хозяина: продукция бактериями
гистоповреждающих субстанций (цитокинов, ферментов, метаболитов), ответная
реакция организма - кульминация патогенеза, обуславливающая латентную,
маломанифестную или ярко выраженную симптоматику заболевания.
5 стадия санации: элиминация уропатогенов из МВП, инволюция
клинической симптоматики. При неадекватной терапии – переход в этап персистенции
с минимальными почечными и клинико - лабораторными проявлениями - хронизация
пиелонефрита.
В настоящее время предложены различные классификации пиелонефритов,
которые определяют подходы к введению больных с данной патологией и определяют
выбор антимикробных препаратов при проведении эмпирической антимикробной
терапии.
Классификация пиелонефрита:
Острый пиелонефрит - острый деструктивный
микробно-воспалительный процесс в тубуло-интерстициальной ткани почек.
Хронический пиелонефрит - деструктивный микробно-воспалительный
процесс в тубуло-интерстициальной ткани почек, имеющий затяжное, рецидивирующее
или латентное течение.
Первичный пиелонефрит - воспалительный процесс в паренхиме без
факторов, способствующих воспалению в тубуло-интерстициальной ткани почек.
Вторичный пиелонефрит - на фоне порока, аномалии,
дизэмбриогенеза почечной ткани, нейрогенной дисфункции мочевого пузыря.
- Вторичный обструктивный пиелонефрит
- микробно - воспалительный
процесс на фоне органических, наследственных, приобретенных или функциональных
нарушений уродинамики.
- Вторичный необструктивный пиелонефрит -
воспаление на фоне обменных
нарушений (дисметаболии, цистинурии), врожденных или приобретенных
иммунодефицитных состояниях, эндокринных дисфункций.
В соответстветствии с МКБ X
предложена следующая классификация пиелонефрита:
- N10 Острый тубулоинтерстициальный нефрит (При необходимости
идентифицировать инфекционный агент используют дополнительный код (B95-B97)).
- N11 Хронический тубулоинтерстициальный нефрит (При необходимости
идентифицировать инфекционный возбудитель используют дополнительный код
(B95-B97)).
- N11.0 Необструктивный хронический пиелонефрит, связанный с рефлюксом.
- N11.1 Хронический обструктивный пиелонефрит неуточненный.
Этиологические агенты вызывающие пиелонефрит.
Наиболее частым возбудителем пиелонефрита является кишечная
палочка. Серотипы эшерихии коли, поражающие мочевую систему, имеют определенный
набор факторов вирулентности, облегчающих проникновение и фиксацию ее в мочевых
путях с выработкой эндотоксина. К наиболее часто встречающимся факторам
вирулентности относят:
- О-антиген - входит в клеточную стенку бактерии и является эндотоксином.
- К-антиген - капсулярный антиген, способствующий развитию резистентности
к фагоцитозу.
- Р-фимбрии - обеспечивают взаимодействие бактерии с поверхностью
уроэпителия при помощи белковых нитей – фимбрий.
В зависимости от условий возникновения заболевания отмечаются
этиологические особенности пиелонефрита. У амбулаторных больных при остром и
хроническом пиелонефрите в этиологии заболевания преобладает
E. coli,
значение других микроорганизмов существенно меньше. При пиелонефрите возникшем в
стационаре, значительно увеличивается спектр возбудителей заболевания причем
возрастает значение и грамм положительных микроорганизмов - энтерококков,
стафилококков (в основном S.saprophyticus). У больных находящихся на лечении в
отделениях интенсивной терапии, особенно при наличии постоянного мочевого
катетера, увеличивается этиологическое значение синегнойной палочки и других
неферментирующих грамотрицательных бактерий, а также энтерококков и грибов (рис.
5.21).
Отличительной особенностью пиелонефритов, в отличие от циститов,
является высокий удельный вес микробных ассоциаций, что необходимо учитывать при
планировании антибиотикотерапии.
При анализе суммарных уровней резистентности к антимикробным
препаратам E.
coli, выделенной из мочи амбулаторных
больных, обращает внимание высокий уровень резистентности к аминопенциллинам и
ко-тримоксазолу. Представленные данные не значительно отличаются от общемировых
тенденций резистентности E.
coli полученные в
многоцентровых исследованиях (рис. 5.22).
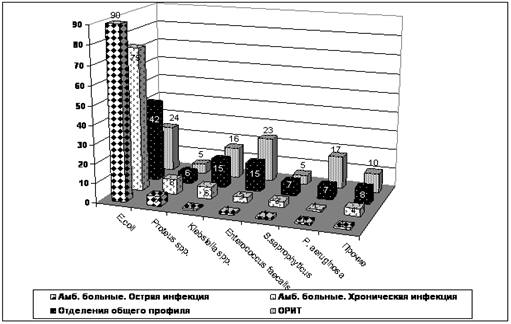
Рис. 5.21 Этиологическая структура пиелонефрита,
%
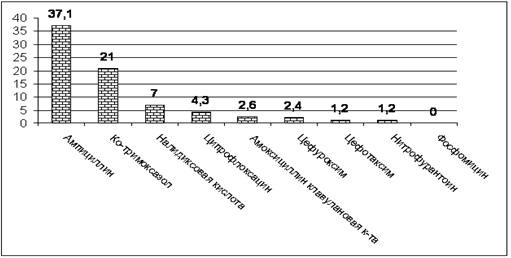
Рис. 5.22 Резистентность E. coli, выделенной у
пациентов с амбулаторными ИМП в России, к пероральным антибиотикам, % (Рафальский
В.В., 2005)
По нашим данным E.
coli выделенная из мочи
амбулаторных больных с пиелонефритом, демонстрировала высокие уровни
резистентности к фторированным хинолонам, аминогликозидам. Низкие показатели
резистентности отмечались к амоксициллину/клавулановой кислоте (рис. 5.23).
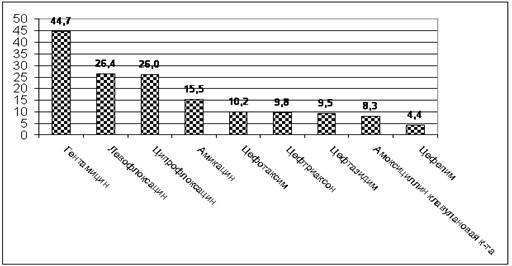
Рис. 5.23 Резистентность к антимикробным
препаратам E. coli, выделенной от амбулаторных больных с пиелонефритом (n=104),
%
Лечение пиелонефритов должно быть комплексным включающим в себя
обязательные мероприятия:
- Устранение причин, вызывающих нарушение пассажа мочи! Без устранения
нарушений пассажа мочи антибактериальная терапия почти всегда лишена смысла;
- Антибактериальную терапию (эмпирическую и этиотропную);
- Лечение нарушений коагуляции;
- Симптоматическую терапию;
- Профилактику рецидивов и обострений.
Выбор антимикробных препаратов.
Пациенты с легким и среднетяжелым течением острого пиелонефрита, а
также легким и среднетяжелым обострением хронического пиелонефрита обычно
лечатся в амбулаторных условиях, и госпитализация не требуется. При тяжелом
течении пиелонефрита, наличии выраженных симптомов интоксикации необходима
госпитализация пациента (рис. 5.24, таб. 5.23).
Добиться эрадикации возбудителя при поражении паренхимы почек
сложнее, чем при поверхностном поражении слизистой оболочки. Поэтому при лечении
пиелонефритов антимикробные препараты назначаются более длительно, чем при
циститах. При легком и среднетяжелом течении острого и хронического пиелонефрита,
без выраженных симптомов интоксикации, антибиотики назначаются перорально не
менее 10-14 дней, и определяются клинико-лабораторной картиной. При
неэффективности 14-дневного курса используют более длительное назначение
антибиотиков – в течение 4-6 недель.
При тяжелом течении пиелонефрита, наличии выраженных симптомов
интоксикации необходимо парентеральное введение антибиотиков до исчезновения
лихорадки. Затем возможен переход на пероральный прием антибиотика в течение
10-14 дней. При развитии рецидивов применяют противорецидивное лечение в течение
6-12 месяцев.
Выбор антимикробных препаратов в подавляющем большинстве случаев
проводится эмпирически, на основе данных о преобладающих возбудителях
(преимущественно E.coli), их резистентности в регионе и тяжести состояния
пациента. Так же при выборе перорального антимикробного препарата необходимо
учитывать фармакокинетику антибиотика и использовать препараты, позволяющие
обеспечить высокие (выше МПК возбудителя) концентрации в моче при приеме 1-2
раза в сутки. Антибиотики с длительным периодом полувыведения могут назначаются
1-2 раза в сутки, что повышает комплаентность пациентов.
С учетом вышеуказанных особенностей (антибиотикорезистентности
основных уропатогенов, фармакокинетики и безопасности антимикробных препаратов)
на амбулаторном этапе препаратами выбора при легком и средне тяжелом остром
пиелонефрите и легком и средне тяжелом обострении хронического пиелонефрита
у взрослых являются:
- Препараты первого ряда:
пероральные фторхинолоны (ципрофлоксацин,
левофлоксацин, офлоксацин), амоксициллин/клавуланат.
- Альтернативные препараты:
пероральные цефалоспорины II-III поколения
(цефуроксим аксетил, цефиксим, цефтибутен), ко-тримоксазол.
При лечении тяжелых и осложненных форм пиелонефрита необходима
госпитализация. Антимикробные препараты используемые для стартовой
антибактериальной терапии всегда вводятся парентерально до исчезновения
лихорадки, затем переход на пероральное применение антибиотиков, как при
пиелонефрите легкой и средней степени тяжести.
- Препаратами выбора являются
: парентеральные фторхинолоны (левофлоксацин,
офлоксацин, ципрофлоксацин), амоксициллин/клавуланат, ампициллин/сульбактам.
- Альтернативные препараты
: парентеральные цефалоспорины II-IV поколения
(цефуроксим, цефотаксим, цефтриаксон, цефепим), цефоперазон/сульбактам,
тикарциллин/клавуланат, ампициллин + аминогликозиды (гентамицин, нетилмицин,
амикацин), карбапенемы (имипенем, меропенем).
При неэффективности эмпирической терапии коррекцию
антибактериальных препаратов следует проводить с учетом данных
микробиологических исследований и резистентности выделенных возбудителей (этиотропной
терапии), а также всегда исключать - нарушение уродинамики – (осмотр уролога).
Профилактическое применение антимикробных препаратов.
При частых рецидивах (более 2 в течение 6 мес.) следует рассмотреть
возможность проведения профилактической терапии: продолжительный прием низких
доз АМП один раз в сутки на ночь (таб. 5.22). Предварительно желательно провести
бактериологическое исследование мочи с определением чувствительности микрофлоры
к антибиотикам. У пациентов с рецидивами, развивающимися после полового акта,
рекомендуется однократный прием препарата после полового акта. При таком режиме
профилактики снижается доза препарата, число нежелательных реакций и риск
селекции резистентных штаммов.
Таблица 5.22.
Профилактическое применение антимикробных
препаратов
|
Препарат |
Профилактическая ( 1 раз в сутки внутрь, на ночь) |
|
Цефалексин |
0,25 г |
|
Цефаклор |
0,25 г |
|
Норфлоксацин |
0,2 г |
|
Офлоксацин |
0,1 г |
|
Ципрофлоксацин |
0,1 г |
|
Нитрофурантоин |
0,05 г |
К профилактическому применению антимикробных препаратов при частых
обострениях пиелонефрита следует относится с осторожностью. В настоящее время
нет достоверных данных, свидетельствующих об эффективности и целесообразности
профилактических курсов антибактериальных препаратов при пиелонефрите, кроме
того возможна селекция устойчивых штаммов микроорганизмов.
По-видимому более целесообразным является проведение
немедикаментозных методов профилактики – фитотерапии. Хотя эффективность
фитотерапии не доказана. Благоприятное влияние лекарственных растений на
почечную систему связано с:
- Мочегонном действием – зависит от содержания эфирных масел и сапонинов
(можжевельник, петрушка, листья березы);
- Противовоспалительным действием – обусловлено танином и арбутином (листья
брусники, толокнянки);
- Антисептическим действием – обусловлено фитонцидами (лук, чеснок, ромашка,
зверобой).
Оценка эффективности лечения.
Назначение антимикробных препаратов, как правило приводит к
быстрому улучшению на 2-3 сутки терапии. Полного исчезновения симптомов
заболевания удается достичь к 4-5 дню терапии. Однако нормализация субъективных
и объективных показателей не должна быть причиной сокращения продолжительности
курса антибактериальной терапии.
Критерии излеченности:
- Исчезновение клинических симптомов;
- Нормализация анализа мочи;
- Бактериурия менее 104 КОЕ /мл .
При персистировании возбудителя в моче после окончания курса
антибактериальной терапии целесообразно продолжить прием антибиотика (с учетом
чувствительности) в течении 1-2 недель.
Ошибки при терапии пиелонефрита у взрослых:
- Цефалоспорины I поколения - недостаточно высокая активность в отношении
грамотрицательной флоры. Назначение оправдано только при кортикальном
абсцессе, имеющем преимущественно стафилококковую этиологию.
- Назначение при пиелонефрите нитрофурантоина, нитроксолина, налидиксовой и
пипемидиевой кислот - препараты не создают терапевтических концентраций в
паренхиме почек.
- Использование норфлоксацина – препарат не создает высоких концентраций в
паренхиме почек, в этой связи целесообразным является использования препарата
при нижних инфекциях мочевыводящих путей.
- Гентамицин в/м при нетяжелом пиелонефрите - эффективны пероральные АМП (фторхинолоны,
амоксициллин/клавуланат).
- Использование аминогликозидов однократно –официально не зарегистрирован, и
является проведением клинических испытаний на людях.
- Парентеральное введение АМП в амбулаторных условиях - современные
пероральные антибиотики, например, фторхинолоны, не уступают по эффективности
парентеральным препаратам.

Рис. 5.24 Алгоритм ведения взрослых больных
пиелонефритом.
Таблица 5.23.
Дозы антимикробных препаратов для лечения инфекций
МВП у взрослых
|
Препарат |
Доза |
|
Терапевтическая |
Профилакти-ческая
(1 раз в сутки внутрь,
на ночь) |
|
Внутрь |
Парентерально |
|
Амоксициллин |
0,25-0,5 г каждые 8 ч |
|
|
|
Ампициллин |
|
0,5-1,0 г каждые 6 ч |
|
|
Оксациллин |
|
1,0-2,0 г каждые 6 ч |
|
|
Амоксициллин/ клавуланат |
0,375-0,625 г каждые 8ч |
1,2 г каждые 6-8 ч |
|
|
Ампициллин/ сульбактам |
|
1,5-3,0 г каждые 6 ч |
|
|
Тикарциллин/ клавуланат |
|
3,1 г каждые 6-8 ч |
|
|
Цефалексин |
0,5 г каждые 6 ч |
|
0,25 г |
|
Цефаклор |
0,25-0,5 г каждые 8 ч |
|
0,25 г |
|
Цефуроксим |
|
0,75-1,5 г каждые 8 ч |
|
|
Цефуроксим аксетил |
0,25-0,5 г каждые 12 ч |
|
|
|
Цефиксим |
0,2-0,4 г каждые 12-24 ч |
|
|
|
Цефтибутен |
0,4 г каждые 24 ч |
|
|
|
Цефоперазон |
|
2 г каждые 6-8 ч |
|
|
Цефтриаксон |
|
1,0-2,0 г каждые 24 ч |
|
|
Цефепим |
|
1,0-2,0 г каждые 12 ч |
|
|
Цефеперазон/ сульбактам |
|
2,0-4,0 г каждые 12 ч |
|
|
Амикацин |
|
15 мг/кг/сут за 1 введение |
|
|
Имипенем |
|
0,5 г каждые 6-8 ч |
|
|
Меропенем |
|
0,5 г каждые 6-8 ч |
|
|
Норфлоксацин |
0,4 г каждые 12 ч |
|
0,2 г |
|
Офлоксацин |
0,2-0,4 г каждые 12 ч |
0,2-0,4 г каждые 12 ч |
0,1 г |
|
Левофлоксацин |
0,25 г каждые 24 ч |
0,25-0,5 г каждые 24 ч |
|
|
Пефлоксацин |
0,4 г каждые 12 ч |
0,4 г каждые 12 ч |
0,2 г |
|
Ципрофлоксацин |
0,25-0,5 г каждые 12 ч |
0,2-0,4 г каждые 12 ч |
0,1 г |
|
Ванкомицин |
|
15 мг/кг каждые 12 ч |
|
|
Ко-тримоксазол |
0,96 г каждые 12 ч |
0,96 г каждые 6-8 ч |
0,24 г |
|
Нитрофурантоин |
0,1 г каждые 6 ч |
|
0,05 г |
|
Фосфомицина трометамол |
3,0 г однократно |
|
|
Острый цистит у детей
Острый цистит развивается у 1-5% детей и нередко протекают
бессимптомно. В возрасте до 1 года цистит чаще развиваются у мальчиков, что
связано с наличием врожденных аномалий мочевыводящей системы. В возрасте от 2 до
15 лет преобладают девочки в соотношении 6:1.
Этиологические агенты вызывающие острый цистит.
Спектр возбудителей у детей не отличается от такового у взрослых.
Ведущим возбудителем является E.coli и другие представители семейства
Enterobacteriacеae. При осложненном цистите частота выделения Е.сoli
снижается до 35-40%, чаще встречаются другие возбудители – Proteus spp.,
Pseudomonas spp., Klebsiella spp., грибы преимущественно С.albicans.
По данным исследования АРМИД (2000-2001гг.,
n=330) в России (Санкт-Петербург,
Смоленск, Казань, Оренбург, Иркутск, Нижний Новгород) отмечается высокая частота
резистентности внебольничных штаммов Е.coli, выделенных у детей, к ампициллину
51,5 % и ко-тримоксазолу 35,5 %. Резистентность к нитрофурантоину, налидиксовой
кислоте и цефуроксиму относительно невысока и составляет от 1 % до 6 % (рис.
5.25).
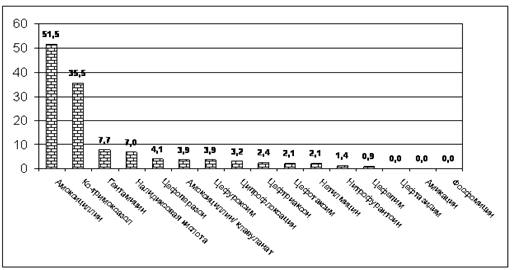
Рис 5.25 Показатели резистентности к
антимикробным препаратам E. Coli,
выделенной из мочи от больных детей с острым циститом (АРМИД-2000,
Л.С. Страчунский, А.Н. Шевелев, 2000г.,)
Цели антибиотикотерапии.
- Быстрое купирование симптомов заболевания;
- Восстановление трудоспособности и социальной активности;
- Предупреждение осложнений;
- Профилактика рецидивов.
Выбор антимикробных препаратов.
Антибиотики назначают в подавляющем большинстве случаев
эмпирически, основываясь на локальных данных чувствительности уропатогенов.
Препараты выбора: амоксициллин/клавуланат, ампициллин/сульбактам,
пероральные цефалоспорины II-III поколения (цефуроксим аксетил, цефаклор,
цефиксим, цефтибутен).
Альтернативные препараты: фосфомицина трометамол (старше 5 лет),
ко-тримоксазол (в регионах с низким уровнем резистентности основных уропатогенов),
нитрофурантоин.
Путь введения антимикробных препаратов пероральный, длительность
фармакотерапии составляет как правило 7 дней. Терапия коротким курсом у детей не
рекомендуется ввиду частого развития рецидивов.
Пациентам с рецидивами инфекций нижних мочевыводящих назначается
нитрофурантоин в дозе 1-2 мг/кг/сут в течение 3 – 6 месяцев. Если в течение
периода профилактики эпизоды инфекции не возникают, то лечение прекращается. В
противном случае, оно возобновляется вновь.
Ошибки при терапии острого цистита у детей:
- Фторхинолоны вследствие риска развития хондропатии у детей не применяются.
- В/м введение гентамицина при остром цистите при наличии эффективных
пероральных антибиотиков (амоксициллин/клавуланат).
- Парентеральное введение антибиотиков в амбулаторных условиях.
- Недопустимо использование у детей терапии одной дозой.
Пиелонефрит у детей.
Этиологические агенты.
В настоящее время установлено, что пиелонефрит у детей наиболее
часто вызывается кишечной палочкой, клебсиеллой, а также протеем, цитробактером
и другими микробами. Значительно реже он вызывается стафилококком и
стрептококком. Таким образом спектр возбудителей у детей не отличается от
такового у взрослых. Ведущими возбудителями являются E.coli и другие
представители семейства Enterobacteriacеae.
Цели антибиотикотерапии: основной задачей при лечении детей,
больных пиелонефритом, является ликвидация или уменьшение
микробно-воспалительного процесса в почечной ткани и мочевыводящих путях.
Лечение больных детей с пиелонефритами.
Низкая эффективность терапии при лечении пиелонефрита у детей,
особенно у мальчиков, обусловлена в ряде случаев наличием аномалий развития,
нарушениями уродинамики, решающим фактором, определяющим эффективность терапии,
является хирургическая вмешательство.
При легком и среднетяжелом течении острого и обострения
хронического пиелонефрита у детей старше 2-х лет, оправдано амбулаторное лечение
с организацией "стационара на дому". При тяжелом течении, а также у детей до 2-х
лет рекомендуется госпитализация.
Для достижения адекватного эффекта при проведении антибактериальной
терапии необходимо учитывать следующие рекомендации:
- Как можно раньше провести идентификацию возбудителя и подобрать антибиотик
с учетом чувствительности к нему микробной флоры;
- Выбрать антибиотик для конкретного больного с учетом сопутствующей
патологии;
- Использовать оптимальные дозы и пути введения антибиотика;
- Чаще использовать "ступенчатую" терапию, учитывая ее преимущества;
- Учитывать особенности взаимодействия антибиотиков с другими препаратами и
пищевыми продуктами, а также уровнем рН мочи.
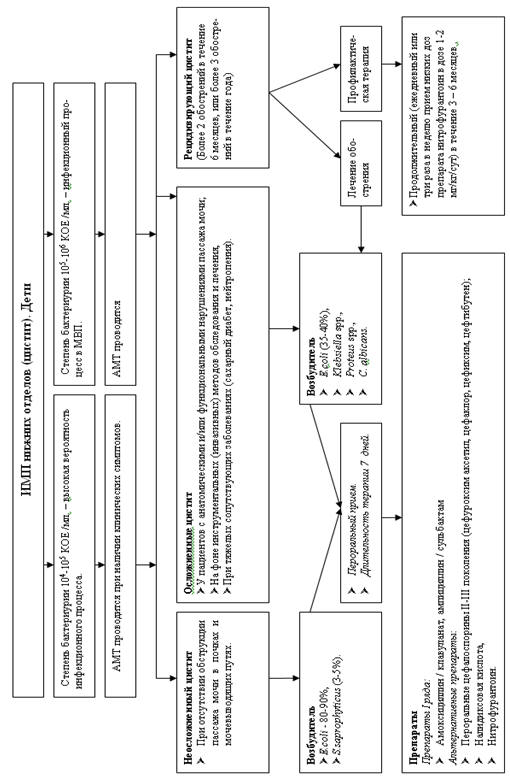
Рис. 5.26 Алгоритм ведения детей с ИМП нижних
отделов (цистит).
При использовании антимикробных препаратов в детской практике, дозы
антибиотиков принято рассчитывать препараты на кг. массы тела. Это обусловлено
рядом анатомо-физиологических особенностей: дети имеют более низкий клиренс,
эффективный почечный кровоток, "незрелый" тубулярный отдел нефрона, сниженную
активность ряда ферментных систем печени, что может приводить к замедлению
выведения некоторых лекарственных веществ и кумуляции в организме.
При лечении пиелонефритов большая роль отводиться ступенчатой
терапии, которая предусматривает использование при максимальной активности
воспалительного процесса в течение 3-5 дней парентерального введения препаратов
(внутривенно или внутримышечно) с последующей заменой на пероральный путь. При
этом возможно применение препаратов одной группы, например, цефуроксим в/в или
в/м на цефуроксима аксетил per os; амоксициллин/клавулановая кислота в/в на per
os; ампициллин/сульбактам в/м на амоксициллин/клавулановая кислота per os.
Ступенчатая терапия имеет значительные клинические и экономические преимущества.
При переходе на пероральный прием препарата ребенок может быть выписан домой для
амбулаторного долечивания.
Комбинированная антибактериальная терапия при пиелонефрите у детей
используется по следующим показаниям:
- Тяжелое септическое течение с целью повышения синергизма действия
антибактериальных препаратов;
- Тяжелое течение инфекции мочевой системы, обусловленное микробными
ассоциациями;
- Для преодоления полирезистентности микроорганизмов к антибиотикам
(особенно при терапии "проблемных" инфекций, вызванных протеем, синегнойной
палочкой, клебсиеллой и др.);
- Для воздействия на внутриклеточно расположенные микроорганизмы (хламидии,
микоплазмы, уреаплазмы).
Путь введения антибиотиков.
При легком и среднетяжелом течении пиелонефрита может быть
использован только пероральный путь введения антибиотика в виде специальных
детских форм (сироп, суспензия), которые отличаются хорошей всасываемостью из
желудочно-кишечного тракта, приятными вкусовыми качествами.
При тяжелом течении лечение необходимо начинать с парентерального
введения и затем, по мере улучшения состояния переходить на пероральный прием
(ступенчатая терапия).
Длительность терапии при остром пиелонефрите и обострении
хронического пиелонефрита должна составлять не менее 14 дней.
Выбор антимикробных препаратов.
У большинства больных с пиелонефритом до выделения возбудителя
"стартовая" антибактериальная терапия назначается эмпирически, то есть
основывается на знаниях этиологической характеристики наиболее вероятных
возбудителей и их потенциальной чувствительности к данному препарату, поскольку
посев мочи и определение чувствительности требуют времени, а начало терапии
откладывать недопустимо (рис. 5.27, таб. 5.24).
Выбор стартового препарата для эмпирической терапии, что при остром
пиелонефрите, что при обострении хронического пиелонефрита будет практически
одинаковым, а отличия антибактериальной терапии будут обусловлены тяжестью
течения (путь введения), длительностью курса терапии, а также данными анамнеза –
какие антимикробные препараты больной получал в предшествующие три месяца.
Препараты выбора: амоксициллин/клавуланат, ампициллин/сульбактам,
цефалоспорины II-IV поколения (цефуроксим, цефотаксим, цефтриаксон, цефиксим,
цефепим).
Альтернативные препараты: ампициллин + аминогликозиды (гентамицин,
нетилмицин, амикацин), ко-тримоксазол ( в территориях с низким уровнем
резистентности менее 10%).
В случае успешной антибактериальной терапии больным в условиях
поликлиники под наблюдением нефролога и участкового педиатра после курса
непрерывной антибактериальной терапии проводится противорецидивное лечение в
течение 4-6 недель в зависимости от характера пиелонефрита (обструктивный,
необструктивный).
Рекомендуются следующие варианты противорецидивной терапии:
- Фуразидин (фурагин) из расчета 5-7 мг/кг массы (полная доза) в течение 2-3
недель; далее при нормализации анализов мочи и крови переходят на 1/2-1/3 от
максимальной лечебной дозы в течение 2-4-6 недель.
- Детям старше 5 лет: фосфомицина трометамол 2 г один раз в 10 дней в
течение 1-2 месяцев в возрастных дозировках.
Оценка эффективности лечения.
Назначение антимикробных препаратов, как правило, приводит к
быстрому улучшению на 2-3 сутки терапии. Полного исчезновения симптомов
заболевания удается достичь к 4-5 дню терапии. Однако нормализация субъективных
и объективных показателей не должна быть причиной сокращения продолжительности
курса антибактериальной терапии.
Критерии излеченности:
- Исчезновение клинических симптомов;
- Нормализация анализа мочи;
- Бактериурия менее 104 КОЕ /мл .
Ошибки при терапии пиелонефрита у детей:
- При острых пиелонефритах не следует назначать цефалоспорины I поколения,
так как они имеют недостаточно высокую активность в отношении
грамотрицательной флоры.
- Назначение при пиелонефрите нитрофурантоина, нитроксолина, пипемидиевой
кислоты нецелесообразно в связи с тем, что препараты не создают
терапевтических концентраций в паренхиме почек.
- Ампициллин не может быть рекомендованы для лечения инфекций МВП из-за
высокой резистентности к нему E.coli, а ко-тримоксазол - из-за высокого риска
развития тяжелых нежелательных побочных реакций (синдромы Стивенсона-Джонсона
и Лайелла).
- При введении нефротоксичных антибиотиков может разиться острый
тубулоинтерстициальный нефрит, проявляющийся острой почечной недостаточностью.
Нефротоксичность антибиотиков возникает чаще всего при применении больших доз
препарата в случае функциональном несостоятельности мочевой системы. Возможно
поражение почек вследствие идиосинкразических реакций, то есть
гиперчувствительности организма к определенному препарату, что не зависит от
дозы препарата и длительности терапии. Эти реакции проявляются чаще в виде
клиническою синдрома некротического васкулита и вызываются в основном
пенициллинами и тетрациклинами.
- В/м введение парентеральных антимикробных препаратов (аминогликозидов,
цефалоспоринов) при нетяжелом пиелонефрите при наличии эффективных пероральных
антибиотиков (амоксициллин/клавуланат); парентеральное введение антибиотиков в
амбулаторных условиях;
- Детям до 2 мес. противопоказано использование цефепима и ко-тримоксазола,
меропенема - до 3 мес.
- Детям и подросткам противопоказано назначение фторхинолонов из-за высокого
риска необратимых нежелательных побочных эффектов со стороны костно-мышечной
системы, а также развитие фотодерматоза связаного с фотодеградацией молекулы
фторхинолонов под действием ультрафиолетовых лучей с последующим образованием
в коже токсичных свободных радикалов, повреждающих кожные структуры
- Использование фитопрепаратов с лечебной и профилактической целью при ИМП у
детей в контролируемых клинических исследованиях не доказано.
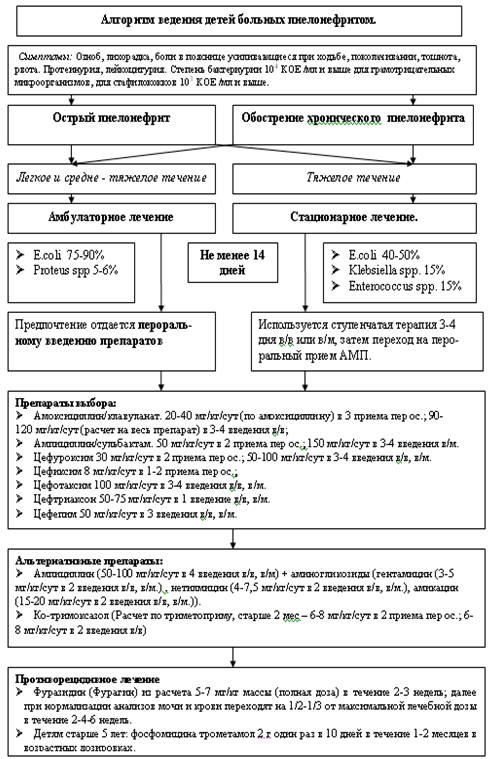
Рис. 5.27 Алгоритм ведения детей больных
пиелонефритом.
Таблица 5.24.
Режим дозирования антибактериальных препаратов для
лечения ИМП у детей
|
Препарат |
Доза |
|
Внутрь |
Парентерально |
|
Амоксициллин |
30-60 мг/кг/сут в 3 приема |
– |
|
Ампициллин |
|
Старше 1 мес – 50-100 мг/кг/сут в 4 введения |
|
Амоксициллин / клавуланат
|
3 мес-12 лет – 20-40 мг/кг/сут (по амоксициллину) в 3 приема |
3 мес-12 лет – 90-120 мг/кг/сут (расчет на весь препарат) в
3-4 введения |
|
Старше 12 лет – 375-625 мг 3 раза в сутки |
Старше 12 лет – 1,2 г х 3-4 раза в сутки |
|
Ампициллин/ сульбактам |
50 мг/кг/сут в 2 приема |
150 мг/кг/сут в 3-4 введения |
|
Цефаклор |
20-40 мг/кг/сут в 2-3 приема |
– |
|
Цефуроксим натрия |
– |
50-100 мг/кг/сут в 3-4 введения |
|
Цефуроксим |
30 мг/кг/сут в 2 приема |
– |
|
Цефотаксим |
– |
Старше 1 мес – 50-100 мг/кг/сут в 2-3 введения |
|
Цефтибутен |
9 мг/кг/сут в 1-2 приема |
– |
|
Цефтриаксон |
– |
Старше 1 мес –20-75 мг/кг/сут в 1 введение |
|
Цефепим |
– |
Старше 2 мес – 50 мг/кг/сут в 3 введения |
|
Гентамицин |
– |
3-5 мг/кг/сут в 2 введения |
|
Нетилмицин |
– |
4-7,5 мг/кг/сут в 2 введения |
|
Амикацин |
– |
15-20 мг/кг/сут в 2 введения |
|
Имипенем |
– |
Старше 1 мес – 60-100 мг/кг/сут в 3-4 введения |
|
Меропенем |
– |
Старше 3 мес – 10-12 мг/кг/сут в 3 введения |
|
Ко-тримоксазол |
Старше 2 мес – 6-8 мг/кг/сут в 2 приема |
Старше 2 мес – 6-8 мг/кг/сут в 2 введения |
|
Нитрофурантоин |
Старше 1 мес – 5-7 мг/кг/сут в 4 приема |
– |
Инфекции мочевыводящих путей при беременности
Инфекции мочевыводящих путей - это основная
экстрогенитальная причина, по которой возникают осложнения у беременных женщин:
анемия, гипертензия, преждевременные роды, преждевременное излитие околоплодных
вод, рождение детей с низкой массой тела (<2500 г), что в свою очередь приводит
к повышению перинатальной смертности в 3 раза. В то же время осложненные
инфекции мочевыводящих путей могут являться показанием к прерыванию беременности
независимо от срока: прогрессирующая почечная недостаточность (увеличение
креатинина более 265 мкмоль/л (3 мг%), клубочковая фильтрация ниже 30 мл/мин),
нарастание тяжести гипертензии, особенно при злокачественных формах ее течения.
Высокая распространенность инфекций мочевых путей у беременных
объясняется следующими факторами:
- Короткой широкой уретрой.
- Близостью ее к естественным резервуарам инфекции (влагалище, анус).
- Механическим сдавлением мочеточников маткой.
- Снижением тонуса мочевых путей.
- Глюкозурией.
- Иммуносупрессией.
- Изменением рН мочи.
Наличие предрасполагающих факторов приводит к тому, что 10%
беременных женщин на протяжении беременности страдают той или иной формой
инфекции мочевыводящих путей, и это очень значительная и
социально-экономическая, и медицинская проблема.
Инфекции мочевых путей у беременных могут проявляться в виде
инфекций нижних отделов мочевыводящих путей (бессимптомная бактериурия, уретрит,
острый цистит, рецидивирующий цистит) и инфекций верхних отделов мочевыводящих
путей (острый и хронический пиелонефрит, абсцесс и карбункул почек).
В настоящее время инфекционные заболевания мочеполовой системы у
женщин отличаются полиэтиологичностью, стертой клинической картиной, высокой
частотой микст-инфекции и склонностью к рецидивированию, что требует
комплексного подхода к диагностике и лечению.
Этиология инфекции мочевыводящих путей у беременных.
Чаще всего этиологическим фактором развитием инфекций мочевых путей
у беременных является кишечная палочка. В своей работе А.П. Никонов представляет
E. coli как основного возбудителя инфекций мочевых путей во время беременности
на долю которого приходится до 80%.
В то же время в многоцентровом исследовании АРИМБ – посвященном
изучению чувствительности возбудителей острого цистита и бессимптомной
бактериурии у беременных в лечебных центрах г.Санкт-Петербурга, Москвы,
Смоленска, Волгограда в 2002г. были отмечены тенденции к некоторому снижению
количества кишечной палочки и ее этиологической роли – уровень её составил 63%.
Наблюдается увеличение других представителей микроорганизмов как
грамотрицательных, так и грамположительных (рис. 5.28).
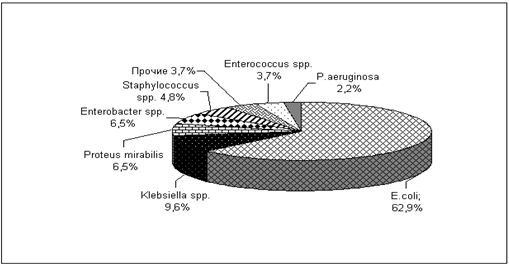
Рис. 5.28 Этиология инфекций мочевых путей у
беременных по данным многоцентрового исследования АРИМБ, 2003 (n=117).
Это следует учитывать, потому что, по истечении некоторого времени
мы будем все чащи и чаще сталкиваться с проблемами антибактериальной терапии,
связанной с меньшей чувствительностью этих микроорганизмов к тем стратегическим
антибактериальным программам, к которым мы привыкли.

Рис. 5.29 Резистентность к антимикробным
препаратам штаммов E. coli выделенных при инфекций мочевых путей у беременных по
данным многоцентрового исследования АРИМБ, 2003.
Многоцентровое исследование АРИМБ выявило высокий уровень
резистентности E. coli к ампицилину 32%, ко-тримоксазолу 14,5%, ципрофлоксацину
6%. В то же время низкие уровни резистентности отмечены к нитрофурантоину 4,3%,
амоксициллин/клавулановой кислотой, цефуроксиму, цефотаксиму в пределах
3,4-1,7%. И только у фосфомицина в России не выделено резистентных штаммов (рис.
5.29).
Общие принципы использования антимикробных препаратов при инфекциях
мочевыводящих путей у беременных женщин.
В выборе антимикробного препарата для лечения инфекций
мочевыводящих путей у беременных кроме микробиологической активности, уровня
резистентности, фармакокинетического профиля, доказанной эффективности
препарата, необходимо учитывать его безопасность и переносимость.
Во время беременности предполагает выполнение следующих условий:
- Использование лекарственных средств только с установленной безопасностью
при беременности, с известными путями метаболизма (критерии FDA);
- При назначении препаратов учитывается срок беременности: ранний или
поздний. Поскольку срок окончательного завершения эмбриогенеза установить
невозможно, то необходимо особенно тщательно подходить к назначению
антимикробного препарата до 5 месяцев беременности;
- В процессе лечения необходим тщательный контроль за состоянием матери и
плода.
Во всем мире широко пользуются следующими категориями риска
применения ЛС при беременности, разработанными Американской администрацией по
контролю за лекарствами и пищевыми продуктами - FDA (Food and Drug
Administration):
А - в результате адекватных строго контролируемых исследований не
выявлено риска неблагоприятного действия на плод в I триместре беременности (и
нет данных, свидетельствующих о подобном риске в последующих триместрах). К
сожалению, этих препаратов практически нет.
B - изучение репродукции на животных не выявило риска
неблагоприятного действия на плод, а адекватных и строго контролируемых
исследований у беременных женщин не проведено.
C - изучение репродукции на животных выявило неблагоприятное
действие на плод, а адекватных и строго контролируемых исследований у беременных
женщин не проведено, однако потенциальная польза, связанная с применением ЛС у
беременных, может оправдывать его использование, несмотря на возможный риск. Но
препараты категории С могут назначаться беременным с учетом пользы и риска.
D - имеются доказательства риска неблагоприятного действия ЛС на
плод человека, полученные при проведении исследований или на практике, однако
потенциальная польза, связанная с применением ЛС у беременных, может оправдывать
его использование несмотря на возможный риск.
В категорию Х входят 30 препаратов, которые вызывают необратимые и
тяжелые аномалии развития плода. Эти препараты противопоказаны беременным, или
женщинам, которые могут забеременеть.
Основная проблема с которой сталкиваются врачи, состоит в том, что
подавляющее большинство лекарственных препаратов, которые применяются в
урологии, невозможны для применения во время беременности:
- Сульфаниламиды - ядерная желтуха, гемолитическая анемия у новорожденных;
- Нитрофураны - гемолитическая анемия у детей с дефицитом
глюкозо-6-фосфатдегидрогеназы при назначении препаратов в III триместре
беременности;
- Аминогликозиды - нефротоксическое, ототоксическое действие;
- Хинолоны и фторхинолоны – артропатии, повреждение сухожилий, фотодерматиты,
риск аритмий;
- Нитроксолин - периферические полиневриты, атрофия зрительного нерва. В
подавляющем большинстве стран он просто запрещен.
- Тетрациклин - один из самых токсичных антибиотиков. При использовании у
беременных он вызывает нарушение кальцификации зубов у трети новорожденных,
задержку роста, аномалии костей. Этот антибиотик опасен не только ребенку, но
и матери: тетрациклин может вызвать у беременной острый гепатит, панкреатит,
острую почечную недостаточность.
На основании классификации возможности использования антимикробных
препаратов при беременности, данных резистентности основных патогенов,
Европейская и Американская урологические ассоциации в 2007г., для лечения
инфекций мочевыводящих путей рекомендуют использовать аминопенициллины,
цефалоспорины I-II-III- поколения, фосфомицина трометамол.
Бессимптомная бактериурия.
Распространенность бессимптомной бактериурии в популяции беременных
женщин в среднем составляет 6% (1,9-9,5%).
Бессимптомная бактериурия беременных - это микробиологический
диагноз, который основывается на исследовании мочи, собранной с максимальным
соблюдением стерильности и доставленной в лабораторию в предельно короткие
сроки, что позволяет в наибольшей степени ограничить рост бактерий.
Диагноз бессимптомной бактериурии ставится если:
- Бактериурия ≥ 105 КОЕ/мл.
- Микроорганизм принадлежит к одному и тому же виду в двух пробах, как
минимум, произведенным с интервалом более 24 часов.
- Отсутствуют клинические признаки инфекции.
- Пиурия +/-.
Учитывая высокую вероятность развития восходящей инфекции мочевых
путей у беременных с бессимптомной бактериурией, возможность развития осложнений
во время беременности с риском летального исхода для матери и плода, всем
пациенткам показано проведение скринингового обследования и лечения
бессимптомной бактериурии беременных. Лечение бессимптомной бактериурии на
ранних сроках беременности позволяет снизить риск развития острого пиелонефрита
на поздних сроках с 28% до уровня менее 3%.
Острый цистит.
Острый цистит встречаются несколько реже у беременных женщин в
1-2,5%.
Диагноз острого цистита устанавливается на основании:
- Дизурии, частые императивные позывы на мочеиспускание, боль над лобком;
- Пиурия при остром цистите - обязательна, то есть, в 1 мкл
нецентрифугированной мочи количество лейкоцитов ≥ 10;
- Бактериурия характеризуется двумя критериями - ≥ 102 КОЕ/мл
(для колиформных микроорганизмов) и ≥ 105 КОЕ/мл (для других
уропатогенов).
- Согласно методическим рекомендациям Европейской ассоциации урологов от
2001 содкржанием ≥ 103 КОЕ/мл патогенных микроорганизмов в средней
порции мочи при остром неосложненном цистите у женщин.
Лечение бессимптомной бактериурии и острого цистита.
Задачей лечения неосложненных инфекций мочевых путей является
быстрая элиминация возбудителя, что одновременно предупреждает прогрессирование
бактериальной инвазии.
В последнее время появилось достаточно много публикаций, в которых
говорится о том, что можно уменьшить длительность антибактериальной терапии до
3-5 дней. Учитывая, что беременность является фактором риска развития
осложненных инфекций, применение коротких курсов антимикробной терапии для
лечения бессимптомной бактериурии и острого цистита является неэффективным. При
таком лечении наблюдается наименьший процент микробиологической эрадикации и
наибольший процент рецидивирования заболевания, в этой связи во всех
международных стандартах длительность терапии остается прежней - 7 дней.
Единственный препарат, который назначается однократно - это фосфомицина
трометамол.
При постановке диагноза бессимптомной бактериурии или острого
цистита назначается семидневный курс терапии (цефуроксима аксетила 500мг.х 2-3
раза в сутки, защищенных аминопенициллинов - амоксициллина клавуланата 375-625
мг. х 2-3 раза в сутки, цефтибутена 400мг. х 1 раз в сутки, нитрофурантоина
100мг. х 4 раза в сутки) или терапия одной
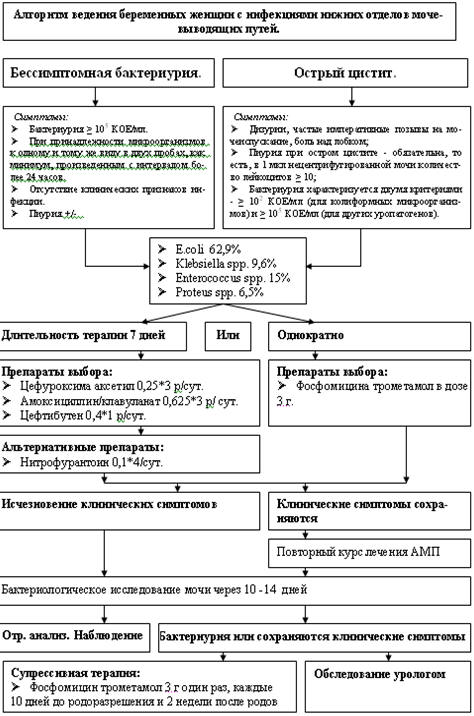
Рис. 5.30 Схема ведения
беременных с инфекцией нижних отделов МВП
дозой фосфомицина трометамолом - 3 г. Затем проводится контрольное
культуральное исследование мочи через 7-14 дней. В случае удачи - терапия
заканчивается. При неудаче необходим повтор курса терапии с последующим
бактериологическим контролем. Если повторный курс удачен, то пациентке
рекомендуется бактериологический контроль мочи ежемесячно, вплоть до родов. Если
и повторный курс терапии неудачен, есть два стратегических подхода. Это
супрессивная терапия до родов и 2 недели после родов с ежемесячным
бактериологическим контролем (фосфомицин трометамол 3 г один раз, каждые 10 дней
до родоразрешения и 2 недели после родов) (рис. 5.30).
И второй момент - это исключение осложненных формы инфекции
мочевыводящих путей, рекомендуется осмотр уролога.
Пиелонефрит.
Острый пиелонефрит встречаются у беременных женщин в 1-2,5%
случаев. У 20-40% беременных с бессимптомной бактериурией во II и III триместре
развивается острый пиелонефрит, а в III триместре в 60-75% случаев. При остром
пиелонефрите в подавляющем большинстве случаев (75%) поражается правая почка, в
10-15% случаев - левая почка или наблюдается двухсторонний процесс. Примерно у
1/3 больных, страдающих хроническим пиелонефритом, во время беременности
развивается обострение.
При этом заболевании наблюдается яркая клиническая симптоматика:
- Клинические симптомы: лихорадка (температура более 38°С), озноб, тошнота,
рвота, боли в поясничной области, дизурия;
- Выраженная пиурия, ≥ 10 лейкоцитов в 1 мкл нецентрифугированной мочи;
- Выраженная бактериурия, ≥ 104 КОЕ/мл. в средней порции мочи.
Антибактериальная терапия острого пиелонефрита у беременных.
В этом случае всегда необходима госпитализация. При остром
пиелонефрите назначается антибактериальные препараты - парентерально: защищенные
аминопенициллины, цефуроксим, цефтриаксон или цефотаксим.
Длительность терапии продолжается в течение двух недель.
Алгоритмы ведения беременных с острым пиелонефритом:
- Госпитализация;
- Бактериологическое исследование крови и мочи;
- Контроль выделительной функции почек;
- Мониторинг жизненно-важных функций - респираторный дистресс,
- Парентеральное назначение антибиотиков.
Антибактериальная терапия проводится только парентерально с
последующим контролем эффективности лечения через 48-72 часа. Впоследствии
коррекция антибактериальной терапии осуществляется по результатам
бактериологического исследования. Длительность терапии серозной стадии
воспаления - 14 дней: 5 дней - парентерально, далее - переход на пероральный
режим. К препаратам, разрешенным к применению у беременных для лечения острого
пиелонефрита, относятся:
- Амоксициллин/клавуланат 1,2 г в/в 3-4 р/сут;
- Цефуроксим натрия 0,75-1,5 г в/в 3 р/сут;
- Цефтриаксон 1-2 г в/в 1 р/сут;
- Цефотаксим 1-2 г в/в 3-4 р/сут.
В случае отсутствие улучшения в течение 48-72 часов, есть два
решения.
Первое, если это резистентность микроорганизмов, то
необходима смена антибиотиков под постоянным бактериологическим контролем. И,
наконец, это супрессивная терапия до окончания беременности и две недели после
родов. При выявлении атипичных возбудителей (уреа-, микоплазменной инфекции,
хламидийной инфекции) у больных с часто рецидивирующим инфекционным процессом,
показано применение макролидов (джозамицина, азитромицина в стандартных
дозировках).
Второе связано с обструкцией мочевых путей. В этом случае
используется хирургическое лечение, т.е. катетеризация мочеточников или
оперативное лечение мочекаменной болезни. Краеугольным камнем лечения больных
гестационным пиелонефритом является решение вопроса о необходимости дренирования
мочевых путей и выборе метода дренирования. Показанием к дренированию мочевых
путей во время беременности является наличие у больной острого пиелонефрита на
фоне нарушенной уродинамики.
Выбор метода дренирования мочевых путей во время беременности
зависит от: причин нарушения уродинамики (МКБ, снижение тонуса мочевых путей,
сдавление маткой, рефлюкс); сроков беременности; стадии пиелонефрита (серозный,
гнойный).
|