
1.3. Коэффициенты активности соляной кислоты в
желудочном соке
Еще в 1931г. Hollander F. обнаружил, что при высоких концентрациях
ионов водорода (рН от 0,91 до 1,14) коэффициенты активности соляной кислоты в
желудочном соке практически равнозначны коэффициентам активности соляной кислоты
в водном растворе.
Авторами работы [Moore E., Scarlata R., 1965г.] впервые были
определены коэффициенты активности соляной кислоты в желудочном соке (рис.1). По
их мнению, подавление активности водородных ионов в желудочном соке обусловлено
наличием других ионов, находящихся в желудочном соке, главным образом ионов
натрия и калия. Они также считали, что ниже ~ 3 рН желудочная кислотность по
своим физико-химическим свойствам идентична чистым растворам соляной кислоты.
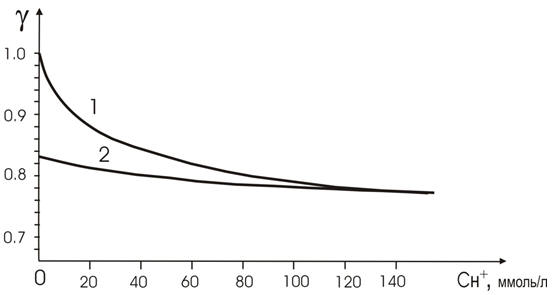
Рис.1 Коэффициенты активности ионов водорода в
растворах НСl (1) и желудочного сока (2) при различных концентрациях ионов
водорода CH+ [Moore E., Scarlata R., 1965].
Следует отметить, что кривая 2 на рис.1 представляет собой
расчетную линию из средних значений 7 исследуемых образцов желудочного сока,
содержащих в среднем 0,05 моль/л натрия и калия. В первоначально взятых образцах
желудочного сока концентрация ионов водорода находилась в интервале от 0,0024 до
0,0746 моль/л. При проведении исследований к первичным образцам желудочного сока
последовательно добавляли соляную кислоту небольшими дозами (по 0,1 ÷ 0,2 мл).
Окончательные величины концентраций ионов водорода в образцах составляли от
0,0973 до 0,1506 моль/л.
Для оценки влияния различия в величинах коэффициентов активности
ионов водорода в желудочном соке и водном HСl растворе мы рассчитали величины
активности и рН по данным [Moore E., Scarlata R., 1965г.]. Из данных таблицы 3
видно, что снижение коэффициента активности HСl желудочного сока
по сравнению с коэффициентом активности HСl водного раствора HСl на 0,030÷0,175
вызывает рост величины рН желудочного сока по сравнению с Н2О-HСl
раствором не более чем на 0,02÷0,08.
Таблица 3. Зависимость коэффициентов активности
ионов водорода и величин рН от молярной весовой концентрации (m) соляной кислоты
в водном HСl растворе и от молярной объемной концентрации (М) в желудочном соке
при 25°C.
|
Молярная
концентрация |
Растворы HСl в Н2О |
Желудочный сок |
|
γ |
aН+
(моль/1000г Н2О) |
рН |
γ |
aН+
(моль/л) |
рН |
|
0,000001 |
1 |
1·10–6 |
6,00 |
~0,825 |
0,825·10–6 |
6,08 |
|
0,0002 |
1 |
2·10–4 |
3,70 |
~0,825 |
1,65·10–4 |
3,78 |
|
0,002 |
0,9521 |
1,90·10–3 |
2,72 |
~0,825 |
1,65·10–3 |
2,78 |
|
0,005 |
0,9285 |
4,64·10–3 |
2,33 |
0,82 |
4,10·10–3 |
2,39 |
|
0,01 |
0,9048 |
9,05·10–3 |
2,04 |
0,82 |
8,2·10–3 |
2,09 |
|
0,02 |
0,8755 |
1,75·10–2 |
1,76 |
0,81 |
1,62·10–2 |
1,79 |
|
0,05 |
0,8304 |
4,15·10–2 |
1,38 |
0,80 |
4,0·10–2 |
1,4 |
|
0,10 |
0,7960 |
7,96·10–2 |
1,10 |
0,80 |
8,0·10–2 |
1,1 |
При концентрации HСl в желудочном соке около 0,1 моль/л
коэффициенты активности ионов водорода в желудочном соке, смешанном водном
растворе HСl-NaCl (или KCl) и водном растворе HСl достаточно близки, а
следовательно, в них практически равны активности ионов водорода и величины рН.
При более низких концентрациях HСl, несмотря на некоторое различие в
коэффициентах активности HСl в желудочном соке и водном растворе HСl (таблица
3), величины рН в последних отличаются незначительно (<0,1 ед. рН) даже при
нейтральном и слабокислых рН.
Поэтому для определения общей истинной кислотности [H+]общ.
желудочного сока по величине активной концентрации ионов водорода, полученной
путем преобразования рН, следует использовать коэффициенты активности
желудочного сока, приведенные на рисунке 1 и в таблице 3. Величина этих
коэффициентов составляет ~0,8 при высокой концентрации (0,05÷0,1 моль/л) HСl в
желудочном соке и 0,82÷0,83 при более низкой концентрации HСl.
Мыш В.Г. в 1987г. установил, что в среднем коэффициент активности
ионов водорода в желудочном соке равен 0,80±0,028. В отличие от чистых водных
растворов соляной кислоты коэффициенты активности ионов водорода в желудочном
соке со снижением концентрации ионов водорода в желудочном соке не увеличиваются
до единицы.
Moore E., Scarlata R. еще в 1965 году сделали вывод, что
определение кислотности с помощью рН-метрии это наиболее точный и практичный
метод определения истинной концентрации ионов водорода в желудочном соке, не
претерпевшем никаких изменений. По их мнению, титрационный метод определения
кислотности желудочного сока приводит к погрешностям, зависящим от концентрации
ионов водорода (CH+) в образце и наличия в нем первоначально
недиссоциированного водорода.
Поэтому более целесообразно для определения кислотности отсосанного
содержимого желудка применять рН-метрию, важным преимуществом которой является
быстрота измерения. Кроме того, недостатком аспирационно-титрационного и
аспирационно-рН-метрического методов является невозможность раздельной оценки
работы кислотообразующих и ощелачивающих желез желудка и двенадцатиперстной
кишки.
Это обусловлено тем, что желудочное содержимое, полученное путем
отсасывания через конец зонда из антрального отдела желудка, является смесью
секрета фундальных желез тела и дна желудка, секрета пилорических желез и
дуоденального содержимого. Очевидно, что определить данными методами, например,
кислотообразующую функцию желудка, то есть базальный рН в теле желудка,
достоверно нельзя.
Например, величины базального рН в теле желудка больных ЯБДК,
определенные с помощью рН-радиокапсулы и аспирационно-рН-метрическим методом,
составляли соответственно 1,14±0,05 и 1,53±0,07 [Коростовцев С.Б., Ивашкин В.Т.,
1971г.]. То есть аспирационно-рН-метрический метод завышает рН.
Кроме того активное отсасывание желудочного сока в полости желудка
провоцирует заброс дуоденального содержимого в желудок, что сопровождается
ощелачиванием аспирата и способствует диагностике гипоацидных и анацидных
состояний [Дубинская Т.К., с соавторами, 2004 г.].
Поэтому только метод внутрижелудочной рН-метрии может обеспечивать
возможность изучать с большой точностью кислотность одновременно в
кислотообразующей и ощелачивающей зонах желудка, пищеводе и двенадцатиперстной
кишке. Для исследования внутрижелудочной рН-метрии применяли различные типы
рН-датчиков [Белоусов А.С., Ястреб И.И, 1972 г., Линар Е.Ю., 1968 г., Лея Ю.Я.,
1976 г., Яковлев Г.А., 1995 г., 2007 г. и др.].
|