
ЗАКЛЮЧЕНИЕ
Представленные в настоящем издании материалы, основанные на данных
литературы и результатах многолетний собственных исследований, вновь возвращают
читателя к проблеме так называемой стресс-индуцированной патологии. И это вполне
закономерно, так как в течение последних десятилетий количество неблагоприятных
воздействий на организм человека продолжает нарастать, и причин этому много -
природные и техногенные катастрофы, террористические акты, социальные
потрясения, финансово-экономические кризисы, боевые действия в различных
регионах планеты. В перечисленные события оказывается вовлеченным множество
людей, для которых эти события и их последствия становятся факторами тяжелого
стресса, оставляющего определенный след в функционировании человеческого
организма на многие годы, часто на всю оставшуюся жизнь. Сложные системы,
способные защитить организм от ближайших и отдаленных последствий стрессовых
воздействий, в какой-то момент сами становятся «мишенью» этих же стрессовых
воздействий, и их надежное функционирование начинает давать сбои. Так по
существу формируется известное ПТСР – многолетний, хронически протекающий
патологический процесс, приводящий, в свою очередь, к множеству хронических
патологических расстройств соматического, психосоматического, нейросоматического
круга.
Наиболее клинически и патогенетически «яркой» моделью развития
описанной цепи постстрессовых событий являются последствия боевого стресса,
полученного в условиях ведения боевых действий. Именно последствия данного
варианта стресса наблюдались авторами предлагаемого издания а течение многих
лет, а результаты этих наблюдений представлены в множестве публикаций. Но только
в последние годы стали достаточно очерченными вопросы взаимосвязи последствий
стрессового воздействия и факторов времени, таких как постоянно увеличивающийся
в процессе естественного старения возраст пострадавших и период, прошедший после
воздействия крайне неблагоприятных ситуаций на организм человека. Появилось
понимание того, что последствия стрессового воздействия не являются статическим
состоянием, а постоянно меняют свою патогенетическую, патоморфологическую,
клиническую структуру, «обрастая» все новыми и новыми патологическими
составляющими в процессе старения и отдаления от момента воздействия
стресс-факторов. Оказалось, что возрастные аспекты оказывают отчетливое влияние
не только на известные взаимоотношения типа «стресс – организм» в ближайшие от
стрессового воздействия периоды, но и на весь цикл последующих изменений.
Удалось даже проследить динамику ряда стресс-индуцированных состояний в течение
многих десятилетий и сопоставить варианты прижизненных патологических изменений
с результатами, полученными в процессе посмертных патологоанатомических,
патогистологических, морфометрических исследований. Это позволило детально и
последовательно определить основные звенья клинико-патогенетических изменений,
происходящих в организме человека, подвергшегося тяжелому стрессовому
воздействию, фактически на протяжении всей его жизни – с момента получении
стресс до летального исхода в результате различных заболеваний, в основе своей
стресс-индуцированных.
Последствия стрессового воздействия не ограничивается психическими
изменениями. Перенесенный тяжелый, в частности боевой стресс является одним из
основных триггерных механизмов при развитии многих заболеваний (Мякотных В.С.,
Торгашов М.Н., 2015; Hooper
T.I.,
DeBakey
S.F.,
Nagaraj
B.E.
et al., 2008; Sledjeski
E.M.,
Speisman В.,
Dierker L.C.,
2008; Avdibegovic
E., Delic
A.,
Hadzibeganovic K.,
Selimbasic
Z., 2010). Изменения, происходящие при
воздействии стресс-факторов в ЦНС, заключаются в снижении адаптационных
возможностей головного мозга с формированием устойчивой стресс-индуцируемой
системы, прежде всего в лимбико-ретикулярном комплексе, с нарушением
нейроэндокринной составляющей стресс-реализующей системы (Novack
D. H.,
Cameron О.,
Epel Е. et
al., 2007;
McEwen B.S.,
2007; 2009). Характерной особенностью наиболее тяжелого, а именно боевого ПТСР
является отставленная во времени манифестация симптоматики данного
патологического процесса (Александров Е.О., 2005). Это, в свою очередь, приводит
к позднему выявлению причинных и патогенетических факторов развития соматических
заболеваний у лиц, подвергшихся воздействию факторов стресса, к преимущественно
симптоматическому, а не этиопатогенетическому их лечению и к возможному
формированию хронических болевых синдромов. Так, нашими исследованиями показано,
что при поступлении в специализированный стационар госпиталя для ветеранов войн
болевые синдромы разного характера и разной локализации испытывали 97,5%
пациентов, а ПТСР различной степени выраженности диагностировано у 91,3%, и
практически все они страдали «сопутствующей» соматической патологией.
Хроническую боль можно считать совершенно специфическим клиническим
проявлением последствий тяжелого стресса и составляющей ПТСР, и данный вариант
боли можно рассматривать в качестве дизрегуляционной патологии нервной системы.
При формировании хронической боли происходит нарушение не только баланса
ноцицептивной и антиноцицептивной систем, но в результате нейропластических
изменений формируется патологическая алгическая система, способная к
самоподдерживающему состоянию (Данилов А.Б., Давыдов О.С., 2007; Гусев Е.И.,
Крыжановский Г.Н., 2009; Мякотных В.С., Торгашов М.Н., 2015;
Niddam
D.M.,
Hsieh
J.-C.,
2009; Apkarian
A.V.,
Hashmi
J.A.,
Baliki
M.N.,
2011). Накопленные современной наукой данные о хронической боли позволяют
говорить об этом патологическом состоянии, как о самостоятельном заболевании или
расстройстве с первичным процессом в соматической сфере и вторичной дисфункцией
в ЦНС и периферической нервной системе при участии личностно-психологических
механизмов, где невозможно выделить отдельные психологические и физические
компоненты (Данилов А.Б., 2008; Loeser
J.D.,
Treede
R.-D.,
2008; Lane
R.D.,
Waldstein
S.R.,
Critchley
H.D.
et al.,
2009). Коморбидность хронической боли и ПТСР, большая распространенность
соматической патологии, сложность патогенеза регуляторных нарушений в ЦНС,
полиморфизм клинических проявлений и вытекающих трудностей медицинской
реабилитации и социальной адаптации пострадавших от стрессовых воздействий еще
более подчеркивают актуальность проблемы.
Нашими исследованиями показано, что с увеличением возраста
интенсивность восприятия перенесенных боевых стресс-факторов может усиливаться.
В то же время, у лиц старше 75 лет воспоминание о травматических событиях
зависит от интенсивности перенесенного боевого стресса и возраста, в котором он
был испытан (Мякотных В.С., Торгашов М.Н., 2015, 2016;
Yoshikawa M.,
Tanaka
K., 2004). Кроме того, в пожилом и
старческом возрасте на оценку воздействия выраженных стресс-факторов влияет
когнитивное состояние пациентов, способствующее, в свою очередь, не только
хронизации ПТСР, но и развитию деменции (Сукиасян С.Г., Тадевосян М.Я., 2010).
После 60-летнего возраста ПТСР регистрировалось значительно реже, чем в более
молодом возрасте, а его интенсивность снижалась (Мякотных В.С., Торгашов М.Н.,
2016). Нейродегенеративные изменения ЦНС, сопровождающиеся деменцией, (болезнь
Альцгеймера, деменция, связанная с нарушениями мозгового кровообращения и др.)
могут инициироваться ПТСР (Mittal
D.,
Torres R.,
Abashidze
A., Jimerson
N., 2001;
Charles E.,
Gafand
L., Ducrocq
F.,
Clement J.P.,
2005). В результате изменения нейротрансмиттерной и нейроэндокринной систем при
ПТСР, особенно на фоне перенесенных боевых черепно-мозговых травм, меняют
биологический возраст, а нейродегенеративные изменения приобретают уже
качественно другой характер, связанный с ускоренным старением организма и как
следствие, с выраженными когнитивными нарушениями (Мякотных В.С., 2009; Мякотных
В.С., Торгашов М.Н., 2015; Торгашов М.Н., Мякотных В.С., Боровкова Т.А., 2016;
Yaffe К., 2010).
Среди наблюдавшихся нами пациентов чаще диагностировалось
выраженное (36%) и умеренное (29,2%) ПТСР. Непрошеные воспоминания
травматических событий, часто сопровождающиеся устрашающими сновидениями и
чувством вины выжившего перед погибшими – это наиболее важные симптомы, дающие
право говорить о ПТСР. В нашем исследовании они присутствовали соответственно у
83,0% и 77,6% ветеранов, страдавших выраженным и умеренно выраженным ПТСР. При
незначительно выраженных проявлениях ПТСР (от 50 до 60 баллов по ОТС) у
наблюдавшихся нами ветеранов не было развернутой клинической симптоматики, но
имели место отдельно взятые симптомы, характерные для ПТСР, которые при
определенных неблагоприятных ситуациях могли «развернуться» в более отчетливую
клиническую картину. В первые 5 лет после воздействия факторов стресса
незначительные проявления ПТСР можно расценивать как латентное его течение, а в
более поздний период, после 25 лет, таких пациентов можно считать
реконвалесцентами ПТСР. В период 10-15 лет после получения боевого стресса ПТСР
имеет наибольшую интенсивность и часто сопровождается различными коморбидными
психопатологическими состояниями, что, конечно же, зависит и от интенсивности
самого перенесенного стресса. В качестве коморбидных ПТСР психопатологических
состояний определялись тревожность (42,9%), депрессия (55,9%), агрессивность
(74,5%), алкогольная или наркотическая зависимости. Кроме психопатологических
состояний, клиническая картина ПТСР складывалась из эпизодической головной боли,
нарушений сна, повышенной утомляемости, хронических болевых синдромов. В
качестве стресс-индуцированных заболеваний при ПТСР чаще всего диагностировались
болезни опорно-двигательного аппарата, сердечно-сосудистой системы,
желудочно-кишечного тракта. Но именно возраст, в котором произошло воздействие
стресса на организм, в значительной степени определял органы-мишени, в которых
развивался стресс-индуцированный патологический процесс.
Наиболее ярким и часто встречающимся вариантом
стресс-индуцированной патологии является, на наш взгляд, сердечно-сосудистая, и
именно формированию, развитию и последующей динамике клинических проявлений
указанной патологии в зависимости от возраста и продолжительности
постстрессового периода бы посвящены проводимые нами исследования.
Представляет интерес выявленная этапность формирования и
дальнейшего развития патологии сердечно-сосудистой системы у участников боевых
действий, переживших тяжелое стрессовое воздействие. Общеизвестно, что изменения
гипоталамо-гипофизарно-надпочечниковой и симпатоадреналовой систем, характерные
для ПТСР, приводят в конечном счете к гиперактивности указанной
симпатоадреналовой системы. Более того, U.S.
Bedi,
R. Arora
(2007) показали, что пациенты с ПТСР реагируют на стрессоры более выраженным и
продолжительным увеличением плазменного уровня адреналина. Как следствие, на
начальном этапе формируются функциональные изменения, затрагивающие вегетативную
нервную систему, обменные нарушения в организме. Данный процесс протекает на
фоне латентного или хронического ПТСР с умеренной и выраженной симптоматикой. С
учетом наследственного фактора, социальных условий и образа жизни так называемая
нейроциркуляторная дистония трансформируется в уже типичную артериальную
гипертонию; далее при гиперпродукции катехоламинов, нарушениях липидного обмена
развивается атеросклероз и, как следствие, ишемическая болезнь сердца,
цереброваскулярные заболевания.
Весьма интересными в этом плане явились результаты впервые
проведенных исследований динамики липидного спектра бывших участников боевых
действий, страдавших ПТСР разной степени интенсивности (Торгашов М.Н., Мякотных
В.С., Пальцев А.И., 2013; Мякотных В.С., Торгашов М.Н., 2015). Оказалось, что
изменения липидного обмена имеют неоднозначную природу. Показана обратная
корреляционная связь выявленных значений общего холестерина и интенсивности ПТСР.
По сравнению с лицами, не подвергавшимися стрессовым воздействиям, у ветеранов
боевых действий чаще выявлялась гипертриглицеридемия и гиполипидемия ЛПВП. У тех
же ветеранов, дополнительно перенесших стрессы мирной жизни уже в послевоенном
периоде, чаще выявлялась гиперлипопротеинемия 2а типа (р=0,037) и более высокие
показатели ЛПНП (р=0,023). Вероятно, повторные стрессы у лиц, страдающих ПТСР,
приводят к длительной гормональной нагрузке (McEwen
B.S., 1998; Bedi
U.S.,
Arora
R., 2007), что в свою очередь может
формировать гиперлипидемии. Этот факт объясняется тем, что глюкокортикоиды в
высоких концентрациях понижают количество апопротеин-В-чувствительных
рецепторов, участвующих в захвате и клиренсе ЛПНП плазмы. Повышенные показатели
ЛПНП, триглицеридов и снижение ЛПВП были выявлены, например, у ветеранов
Вьетнамской войны с ПТСР спустя более 30 лет после окончания боевых действий.
Изменения уровня липидов связывались с активацией норадренергической системы,
однако не учитывался возрастной фактор (Kagan
B.L.,
Leskin
G., Haas
B. et
al., 1999). Наше исследование
показало связь нарушений липидного обмена у ветеранов не только с ПТСР, но и с
возрастом. По нашим данным, с течением времени интенсивность ПТСР и его влияние
на организм уменьшаются, и в последующем приобретают более важную роль в
развитии патологии липидного спектра и атеросклероза именно возрастные
изменения. Тем не менее, развитие гиперлипидемий у бывших участников боевых
действий в более раннем возрасте, чем у лиц, не принимавших непосредственного
участия в военных кампаниях, является следствием триггерного механизма ПТСР.
Данное предположение подтверждается также случаями острых нарушений мозгового
кровообращения в среднем возрасте наблюдавшихся нами участников боевых действий
44,0±3,3 лет, а также обнаружением у наших пациентов характерных нарушений
проведения возбуждения в миокарде, что при определенных неблагоприятных факторах
может привести к фатальным исходам.
Патогенетический механизм перенесенного боевого стресса и
следующего за ним ПТСР также затрагивает иммунную систему, и данное состояние
можно характеризовать как вторичный иммунодефицит нейрогенной природы. Данное
положение подтверждается в том числе результатами нашего исследования,
свидетельствующими о том, что у пациентов с Нр инфекцией интенсивность ПТСР была
отчетливо более высокой, чем также у ветеранов боевых действий без признаков Нр
инфекции (F=4,6 р=0,04). Кроме
того, обсемененность Нр изменялась в связи с продолжительностью послевоенного
периода и изменениями же в степени интенсивности ПТСР. Язвенная болезнь желудка
и 12-перстной кишки в основном диагностировалась в первые 10 лет после
воздействий боевых стресс-факторов, что еще раз подтверждает роль стресса и
нарушений процессов адаптации в развития язвенной болезни.
Одно из проведенных нами исследований было построено нетрадиционным
способом. В отличие от классического принципа «обследование - лечение -
результаты - прогноз», мы отталкивались от обратного, то есть от уже
произошедшего летального исхода в связи с известной причиной. Это позволило нам
не только верифицировать диагноз, подтвердив его морфологически, но и получить
принципиально новые данные, касающиеся различных исходов стресс-индуцированной
сочетанной сердечно-сосудистой патологии. В определены клинические и
морфологические аспекты взаимоотношений ряда вариантов сердечно-сосудистой
патологии у лиц, перенесших боевую черепно-мозговую травму, боевой же стресс и
достигших пожилого и старческого возраста. Прослежена связь между клиническими и
морфологическими проявлениями заболеваний в каждом из ведущих органов-«мишеней»
- сердце и головном мозге - и негативной динамикой клинических и
лабораторно-инструментальных параметров, отражающих состояние других органов и
систем.
Установлено, что особенно важная роль в развитии и прогрессировании
мультифокального атеросклеротического процесса принадлежит перенесенным в
течение жизни больного, а особенно в пожилом и старческом возрасте, сосудистым
катастрофам, в первую очередь, инфарктам миокарда и ишемическим инсультам.
Именно характер произошедшей нефатальной сосудистой катастрофы определяет
«слабое звено» и пути формирования дальнейшего течения уже хронического
сосудистого процесса по кардиальному или церебральному типу.
Перенесенные инфаркты миокарда, ПИКС имеют наибольшее значение в
развитии повторных коронарных катастроф, а также в прогрессировании хронической
ишемии мозга, увеличивая степень выраженности церебрального неврологического
дефицита и вероятность развития инсульта, который, в свою очередь, приводит к
расстройствам сердечной деятельности и прогрессированию ишемии миокарда. Данный
клинический феномен обусловлен не только анатомо-физиологическими особенностями
строения сосудистой системы и прогрессированием атеросклеротического процесса в
целом, но и, в первую очередь, дефицитом кровоснабжения регулирующих
церебральных структур.
В формировании и развитии последующей за ишемическим инсультом
сердечно-сосудистой патологии имеет значение локализация постинсультного
ишемического очага в головном мозге. При левосторонней его локализации
кардиальные расстройства являются достоверно более выраженными, а число
перенесенных в постинсультном периоде инфарктов миокарда столь же достоверно
возрастает. Возникающие в постинсультном периоде нарушения в деятельности
неспецифических, вегетативных, регулирующих образований, биоэлектрической
активности головного мозга способствуют расстройствам сердечной деятельности,
нарастанию нарушений сердечного ритма и проводимости, возрастающей ишемизации
миокарда и головного мозга, способствуя истощению компенсаторных возможностей
организма в целом. Последовательное или одновременное возникновение ишемического
инсульта и инфаркта миокарда у одного и того же пациента значительно утяжеляет
клиническую картину сочетанной патологии, приводит к быстротечному развитию
фатальной сосудистой катастрофы и подтверждается наибольшей морфологической
выраженностью стадии и степени атеросклероза при любой локализации
атеросклеротического процесса.
Вариант клинической манифестации стресс-индуцированной
сердечно-сосудистой патологии, конечно же, оказывает влияние на дальнейшее ее
развитие. Но, при любой манифестации сосудистого процесса в течение 10 и более
лет от момента данной манифестации начинает достоверно преобладать церебральный
компонент. В сроки же свыше 20 лет от начала заболевания в связи с
прогрессированием именно церебральных расстройств, большинство пациентов не
может назвать ведущую причину своего плохого самочувствия. Именно тогда в
качестве таковых причин указываются перенесенные травмы, стрессы.
Весьма интересными оказались обнаруженные факты так называемой
«перекрестной резистентности» обусловленной атеросклерозом сердечно-сосудистой
патологии и онкологической. В процессе клинико-морфологических сопоставлений
выяснилось, что онкологический процесс не способствует утяжелению
морфологических проявлений атеросклероза, а наоборот, даже находится в некоторой
степени в «противофазе» к сердечно-сосудистой патологии, и люди, которые по
степени выраженности сосудистых нарушений могли бы прожить еще достаточно долго,
к сожалению, погибают от рака. Но на сегодняшний день это только довольно
интересное предположение, требующее серьезных доказательств и дальнейшего
тщательного изучения.
Удалось систематизировать результаты лабораторных и
инструментальных исследований, проведенных за 2 - 4 суток до летального исхода
при развитии у пациентов фатальных сердечно-сосудистых катастроф или иных
заболеваний, закончившихся смертью.
Установлено, что параметры ПОЛ/АОЗ системы крови, являясь в целом
неспецифическими, в финальных стадиях сердечно-сосудистых заболеваний
приобретают определенные признаки специфичности и могут выступать в роли
диагностических и прогностических критериев. Наиболее выраженные негативные
изменения отмечены у больных, погибших от ишемического инсульта. Особенно
неблагоприятными явились нарушения именно АОЗ крови - повышение показателей ПРЭ
и пероксидазы на 70% и более с одновременным, столь же отчетливым снижением
показателей каталазы от границ референтных значений. Данный факт может
свидетельствовать о наибольшей «агрессивности» развития сосудистого процесса
именно у данной категории пациентов, подтвердить ведущую роль именно
церебрального атеросклероза и служить прогностическим критерием возможности
развития инсульта. Это тем более очевидно, что наличие «старого» постинсультного
ишемического очага в веществе головного мозга не приводит к столь значимым
изменениям состояния ПОЛ/АОЗ. Результаты патоморфологических исследований также
подтверждают значительно большее поражение не только пре- и церебральных
сосудов, но и сосудов прочих локализаций, в первую очередь, коронарных артерий.
Определена роль системы регуляции мозгового кровообращения в
танатогенезе. Гемодинамика пациентов с поздними клиническими стадиями
хронической цереброваскулярной недостаточности в сочетании с различными
клиническими формами ИБС имеет значительные регуляторные сдвиги. Так, на фоне
изменений центральной пульсации значительно снижаются ударный объем и минутный
объем крови, что не может не сказаться не только на коронарном, но и на
церебральном кровотоке. При этом изменения в системе регуляции гемодинамики
носят тотальный характер, свидетельствуя о грубых нарушениях в регулирующих
системах в целом. Полученные результаты позволили выдвинуть положение о том, что
прогрессирование хронических цереброваскулярных расстройств, возникших у лиц,
подвергшихся тяжелому стрессовому воздействие и перенесших боевые травмы мозга,
связано с угнетением системы регуляции инотропной функции сердца, а ИБС, в свою
очередь, вызывает количественные изменения сократимости миокарда,
сопровождающиеся снижением амплитуд пульсации аорты и периферической пульсации.
В свою очередь, дезадаптация мозгового кровообращения способствует
прогрессированию коронарных нарушений, ишемии миокарда через расстройства
надсегментарных вегетативных регуляторных механизмов. Поэтому у больных пожилого
и старческого возраста необходимо, в первую очередь, акцентировать внимание на
изменении показателей цереброваскулярной реактивности. Критическое снижение
индексов цереброваскулярной реактивности более чем на 90% от возрастной нормы
свидетельствует о рассогласовании адаптационных механизмов церебральной и общей
гемодинамики и является прогностически неблагоприятным фактом.
В различные возрастные периоды атеросклеротический процесс
проявляется по-разному. Если у молодых лиц этот процесс развивается более бурно,
агрессивно, с большим числом осложнений, но вместе с тем, с достаточно
«стандартной» клиникой, то у больных пожилого и, особенно, старческого возраста
проявления атеросклероза в различных органах зачастую маскированы, проявляются
атипично, требуя проведения дополнительных методов обследования и
дифференциальной диагностики. Больные относительно молодого возраста, у которых
самыми ранними и выраженными становятся, в первую очередь, коронарные симптомы
либо головная боль, особенно при последствиях черепно-мозговой травмы, раньше
обращаются за медицинской помощью, но они зачастую воспринимаются врачами
преимущественно как пациенты именно с коронарной патологией. Пожилые пациенты с
более поздним дебютом сосудистого процесса зачастую не в полной мере обследуются
ввиду атипичности клинической симптоматики, да и просто в связи с возрастом.
Нередко и сами пожилые пациенты неадекватно реагируют на необходимость
массивного обследования. Поэтому разница в клинической картине и исходах
патологического процесса у больных различного возраста связана не только с
длительностью течения заболевания, характером и сроками дебюта, наличием в
анамнезе сосудистых катастроф. Пожилые и престарелые пациенты дают не всегда
достаточно ясное и подробное описание своих жалоб, делая основной упор на
головные боли, снижение памяти, боли в ногах, а часто - просто на решение
социальных проблем. Это вводит в заблуждение врача, и полное, подробное
обследование этих пациентов отходит на второй план.
Нельзя обойти стороной и многочисленные социальные факторы. Именно
неблагоприятный социальный фон и особенности адаптации пострадавших от тяжелого
стресса в непрерывно меняющемся обществе имеют первостепенное значение в
развитии, хронизации и прогрессировании ряда соматических заболеваний. Кроме
того, что при старении происходит снижение приспособительных возможностей
организма, что вызывает у пожилых и престарелых больных ипохондрические,
фобические, депрессивные настроения, сопровождающиеся падением активности,
снижением эмоционального резонанса, нарастанием интравертированности и
личностной ригидности. Субдепрессивные настроения на фоне социофобий еще более
усугубляются проявлениями цереброваскулярной болезни и изменениями личностных
характеристик при её прогрессировании. Это негативно сказывается на проведении
лечебных мероприятий.
На основании многолетнего динамического наблюдения лиц,
подвергшихся стрессовому воздействию, а именно участников войн и вооруженных
конфликтов, нами представлена общая поэтапная концепция клинико-патогенетической
модели многолетнего развития сочетанной сердечно-сосудистой патологии,
запущенной стрессом, боевой травмой головного мозга и обусловленной
атеросклерозом (рис. 50).
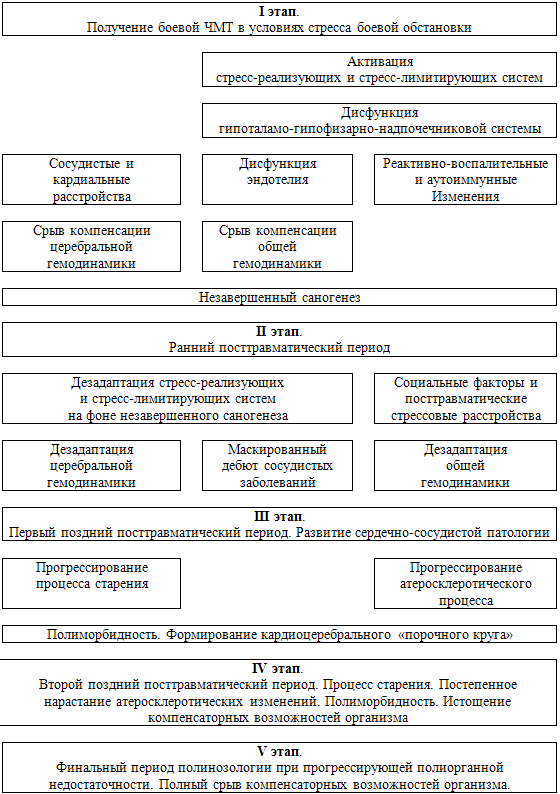
Рис. 50. Поэтапная схема
клинико-патогенетического развития стресс-индуцированной
сосудисто-травматической патологии.
Описательный вариант представленной концепции выглядит следующим
образом.
I этап. Период ведения боевых действий.
Получение боевой травмы мозга в условиях стресса боевой обстановки. При этом в
ответ на травматическое повреждение вне зависимости от характера и тяжести
травмы и рода травматического воздействия развивается билатеральный спазм
сосудов – вазоконстрикция, приводящая к повышению скоростных показателей на фоне
гиперперфузии. Нарушения ликвородинамики и внутричерепная гипертензия с
нарушениями венозного оттока усугубляют сосудистые нарушения. Изменение
деятельности неспецифических, вегетативных, регулирующих образований
способствуют срыву компенсации не только церебральной, но и общей гемодинамики,
ишемизации не только головного мозга, но и миокарда. Дисфункция
гипоталамо-гипофизарно-надпочечниковой системы приводит к усиленному выделению
нейромедиаторов, в первую очередь, серотонина, и это является триггером
ускоренной дисфункции эндотелия и предиктором раннего развития атеросклероза,
чему также способствуют реактивно-воспалительные и аутоиммунные изменения.
Жалобы пациентов на первом этапе имеют преимущественно церебральный
травматический характер.
II этап. Ранний посттравматический период.
Маскированный клинический дебют сосудистого процесса. Нарушения мозгового
кровотока прогрессируют. Незавершенность саногенетических процессов приводит к
ранней клинической манифестации сосудистых заболеваний с истощением
приспособительных механизмов и дезадаптацией функционального состояния не только
головного мозга, но и всего организма. Тем не менее, у пациента сохраняется
уверенность в том, что все его патологические симптомы связаны исключительно с
военными действиями и полученными там травмами; при этом пациентом не
принимаются во внимание и даже отклоняются иные возможные причины головных
болей, головокружений, снижения памяти и прочих субъективных клинических
проявлений, свойственных начальной цереброваскулярной патологии. Даже стабильно
повышенные цифры АД не заставляют больного изменить свое отношение к причине его
страданий. Это связано с определенными социальными и психологическими факторами,
такими, как статус ветерана войны, группа инвалидности, связанная с фронтовыми
ранениями, «ореолом героя». Возможно, данные социальные факторы дополнительно
усугубляют непрерывно прогредиентное течение патологического процесса и позднюю
обращаемость больных. Только значимое изменение привычного характера
церебральных жалоб и/или развитие сердечно-болевого синдрома вызывают
необходимость обращения к врачу и изменение своего отношения к причинам
страданий.
III этап. Первый поздний посттравматический
период. Развитие процесса старения со свойственной ему множественной сочетанной
патологией при накоплении клинических признаков многих заболеваний.
Присоединившаяся и прогрессирующая сопутствующая возрастзависимая патология, в
частности, хронические заболевания легких, желудочно-кишечного тракта,
опорно-двигательного аппарата, онкологические заболевания, определяет развитие
синдрома взаимного отягощения. Присоединяются нехарактерные для травмы, но
облигатные для развития атеросклеротического процесса нарушения липидного обмена
и нарастание процессов ПОЛ. Это, в свою очередь, способствует дальнейшему
прогрессированию эндотелиальной дисфункции. Клинически на первый план вновь
выступают цереброваскулярные расстройства, которые становятся определяющими в
жалобах пациентов вне зависимости от клинического дебюта сосудистого процесса.
Частота предъявляемых цереброваскулярных жалоб не коррелирует с тяжестью
состояния, данными лабораторных, инструментальных исследований и причинами
возможных летальных исходов.
IV этап. Второй поздний посттравматический
период. Быстрое прогрессирование процесса старения, атеросклероза,
полиморбидности. Стремительно прогрессируют клинические проявления хронической
ишемии мозга, развиваются когнитивные нарушения при выраженном и быстром
усугублении психопатологический симптоматики. Одновременно происходит истощение
компенсаторных возможностей организма, подтверждаемое рассогласованностью
механизмов адаптации гемодинамики в целом и выраженными патологическими сдвигами
в системе ПОЛ/АОЗ. Тем не менее, лабораторные и инструментальные показатели по
прежнему носят неспецифический характер.
V этап. Финальный период. Отсутствие
отчетливых клинических признаков травматической болезни головного мозга при
наличии прогрессирующей полиорганной недостаточности. Лабораторные и
инструментальные показатели в финальных стадиях патологического процесса
приобретают черты специфичности и позволяют предположить преобладание
определенной сосудистой или несосудистой патологии, которая может явиться
непосредственной причиной смерти.
Результаты проведенных исследований позволили выработать
полинаправленную концепцию диагностики и оказания медицинской, психологической и
социальной помощи лицам, пострадавших в результате тяжелого стресса и страдающих
стресс-индуцированными расстройствами. Данная концепция поможет более
целенаправленно осуществлять своевременную профилактическую работу,
реабилитационные мероприятия, способствовать улучшению показателей качества
жизни пострадавших.
Наконец, хотелось бы заострить внимание читателя на самом процессе
старения, который также сам по себе может являться определенного рода
стресс-фактором, источником стресса. И это вполне очевидно хотя бы с точки
зрения лавинообразного нарастания количества заболеваний и их тяжести как раз в
переходном периоде от среднего возраста к пожилому. Конечно, данную ситуацию
можно списать на так называемую возрастзависимую патологию, обозначаемую ранее,
как «болезни старости». Но 55 – 60 лет – это еще не старость, хотя, конечно же,
некоторые защитные, адаптивные механизмы в этом возрасте уже начинают давать
сбои. Но с точки зрения возможной физиологической продолжительности жизни
человека к 60-летнему возрасту пройдена лишь половина пути. А с другой стороны,
именно в этом пенсионном и предпенсионном возрасте человек как раз и испытывает
целый ряд социальных, психологических стрессов, связанных с ограничениями в его
профессиональной деятельности, в востребованности его знаний, умений, опыта.
Вполне возможно, что именно эти стресс-факторы являются пусковым механизмом
многих заболеваний и ускоренного старения в целом. И вполне вероятно, что
профилактика старения, основанная на профилактике стресса, станет одним из
отправных пунктов борьбы с процессом старения в целом. Первые шаги в этом
направлении уже сделаны, но необходимы дальнейшие исследования, которые позволят
рассматривать процесс старения человека с точки зрения патологического
стресс-индуцированного состояния, с которым можно и нужно бороться. |