Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Глава № 7. Респираторная поддержка на этапе транспортировки
Как известно, в неонатальной ургентной медицине, в отличие от больных более
старшего возраста, дыхательная недостаточность является одним из основных
синдромов, осложняющих большинство заболеваний и поэтому составляет одну из
основных проблем неонатальной реанимации и интенсивной терапии. Обусловлено это
тем, что любая тяжелая патология приводит к нарушению дыхательных и важнейших
недыхательных функций легких.
В настоящее время дыхание рассматривается не только как легочное дыхание и
газообмен, а как совокупность физиологических процессов, обеспечивающих
поступление кислорода в легкие, доставку его к клеткам и тканям, использование
его в биохимических реакциях и эвакуацию из тканей образовавшегося углекислого
газа.
Поэтому в широком понимании ДН у новорожденных, это ни только расстройство
газообмена в легких, но, прежде всего тканевая гипоксия, приводящая к нарушениям
энергогенеза из-за перехода клетки на анаэробный гликолиз, с образованием
большого количества лактата и малым образованием АТФ.
Установлено, что поступление кислорода в ткани зависит от особенностей
строения капиллярной сети, ее плотности, диффузионых свойств самого кислорода в
конкретных тканях, активности кислородутилизирующих ферментов.
Транспорт кислорода в тканях описан в модели Крога, предложенной в 1919 г.
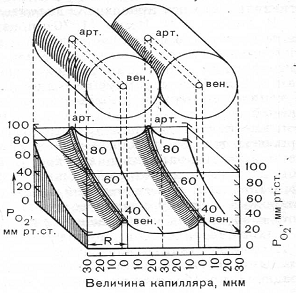
(см. рисунок № 7): "Согласно этой модели, каждый капилляр снабжает
цилиндрический объем ткани. По мере продвижения крови вдоль капилляра происходит
прогрессирующее снижение капиллярного РО2. В результате РО2
в зоне тканей, прилегающих к артериальному концу капилляра, бывает выше чем РО2
в соответствующих участках тканей у его венозного конца. Наименьшее напряжение
кислорода в пределах одного тканевого цилиндра наблюдается в дистальном конце
конце капилляра вблизи венулы. Эту зону иногда называют смертельным углом.
G.Thews (1960) показал, что именно в ней при максимальном снижении РО2
в венозном конце капилляра градиент по кислороду между кровью и тканями может
быть настолько мал, что диффузия кислорода в ткани становится практически
невозможной. В этом и заключается механизм развития тканевой гипоксии. По данным
B.Chance (1959), внутриклеточное РО2 в подобной ситуации может
снижаться до 1 мм.рт.ст., что несовместимо не только с нормальной функцией
клетки но и с ее жизнью" (Рябов Г.А., 1988).
Рисунок № 7. Модель транспорта кислорода в тканях (цилиндр
Крога) (G.Thews 1960).
Хорошо известно, что имеются механизмы, регулирующие доставку кислорода в
ткани, и тонус мышц сосудистых стенок тесно коррелирует с потребностью тканей в
кислороде.
Объем поступающего в ткани кислорода в целом зависит от площади диффузии или
от суммы площадей открытых капилляров, а также от тканевых факторов
(температура, рН и т.д.), определяющих величину градиента РО2 между
кровью и тканями. В связи с этим, даже при разных уровнях РО2
капиллярной крови может быть достигнуто одинаковое обеспечение тканей кислородом
(Шик Л.Л.1966). Возможности подобного пути компенсации достаточно велики,
поскольку в тканях одновременно функционируют в покое 20-35% капилляров. Это
справедливо при одновременном увеличении минутного выброса сердца, т.к.
дополнительные капилляры могут адекватно функционировать лишь при обеспечении их
дополнительным объемом крови. Если не происходит увеличения объемного кровотока,
то капиллярный кровоток замедляется, вследствие чего увеличивается объем
экстракции кислорода из крови. В результате РО2 в венозном конце
капилляра резко снижается.
Таким образом, парциальное напряжение кислорода в венозной крови может
служить критерием соответствия объемного кровотока потребностям тканей в
кислороде. Для такого утверждения есть все основания, поскольку величина
сердечного выброса у человека регулируется согласно кислородным запросам
организма (Шик Л.Л., 1970; Рашмер Р. 1981). Увеличение кровотока по капиллярам
поддерживает тот уровень РО2 в дистальном конце капилляра, который
будет оптимальным для экстракции кислорода из крови тканями и адекватен уровню
метаболизма. Если возможности ССС по увеличению объемного кровотока ограничены и
РО2 в венозной крови становится ниже определенного критического
уровня, то потребление кислорода начинает снижаться, например, при
постгипоксическом отеке-набухании головного мозга. Для ткани мозга у взрослого
человека критический уровень РО2 венозной крови составляет 19-39
мм.рт.ст., для мышц- 20-25 мм.рт.ст., для печени 15-20 мм.рт.ст. Нормальные
показатели газов крови у новорожденных представлены в таблице № 36. Как видно из
таблицы, нормальные показатели газов крови, особенно венозной, у новорожденных
отличаются от взрослых. Связано это с рядом обстоятельств, например наличием
фетального гемоглобина, что определяет сдвиг кривой диссоциации оксигемоглобина
влево и т.д.
В современных представлениях о завершающих фазах патогенеза критических
состояний ведущее место отводится гипоксическим нарушениям метаболизма клетки.
Крайним проявлениям этих расстройств приписывают главную роль в формировании
необратимости некоторых патологических процессов.
Таблица № 36 . Нормальные показатели газов крови у
новорожденного при дыхании воздухом (Гомелла Т.Л., 1995).
| Уровень измерения |
РН |
РСО2 (мм рт.ст.) |
РО2 (мм рт.ст.) |
| Артериальная кровь |
7,35 – 7,45 |
35 – 45 |
55 – 65 |
| Капиллярная кровь |
7,3 – 7,35 |
40 – 45 |
40 – 60 |
| Венозная кровь |
7,25 – 7,30 |
45 – 50 |
30 – 45 |
РО2 в капиллярной крови хорошо коррелирует с артериальным РО2
(обычно капиллярное РО2 меньше на 10 мм.рт.ст.) в том случае, если
участок, из которого берется анализ крови, был предварительно согрет при
температуре 40°С. Кроме того, на степень корреляции РН, РСО2, РО2
в артериальной и капиллярной крови влияют: артериальная гипотензия, снижение
периферического кровотока, полицитемия, РаО2 > 80 мм.рт.ст.,
длительность хранения (пробы крови могут храниться без значительного влияния на
результаты исследования при комнатной температуре 10 – 15 минут, а при Т = 4°С –
1 час). В некоторых случаях при проведении ИВЛ допустимы другие показатели газов
крови.
Таблица № 37. Допустимые показатели газов крови у различных
групп детей (Любименко В.А. и др., 2002, с изменениями).
| Группы детей |
РН |
РаСО2 (мм.рт.ст.) |
РаО2 (мм.рт.ст.) |
| Гестационный возраст менее 28 недель |
≥ 7,25 |
40 – 55 |
45 – 65 |
| Персистирующая легочная гипертензия
новорожденных |
> 7,5 |
< 40 |
80 – 120 |
| Бронхолегочная дисплазия |
> 7,3 |
45 – 80 |
60 - 80 |
В настоящее время большинство исследователей считают, что при некоторых
заболеваниях периода новорожденности можно допускать более низкие величины рН
(около 7,2) и более высокие величины РаСО2 (более 60 – 80 мм.рт.ст.),
чем в норме. Прежде всего, это положение относится к двум группам детей: с
гестационным возрастом менее 28 недель и детям с хроническими неспецифическими
заболеваниями легких (БЛД), находящихся в состоянии клинической компенсации. Это
связано с тем, что возможные отрицательные последствия отдельных видов терапии
(интубации, ИВЛ и т.д.) могут быть больше, чем негативное влияние
компенсированного дыхательного ацидоза.
С другой стороны, высокие значения рСО2 (≥ 60-65 мм.рт.ст) в
острый период любого заболевания у недоношенных крайне опасны, так как в
несколько раз увеличивают частоту развития ВЖК.
Хотелось бы обратить внимание читателей на то, что низкие показатели РаСО2
(менее 20 мм.рт.ст.) не менее опасны, чем высокие, и могут вызвать
выраженный спазм сосудов, в том числе головного мозга, почек и т.д., с развитием
органных нарушений. К сожалению, иногда при проведении кислородотерапии этот
факт, на наш взгляд, недооценивается, а вызванные повреждения связывают с
другими причинами, например, перенесенной гипоксией.
К наиболее распространенным методам респираторной поддержки можно отнести
кислородотерапию.
Кислородотерапия.
Кислородотерапия является одним из основных методов лечения дыхательной
недостаточности у новорожденных. Суть ее состоит в коррекции артериальной
гипоксемии с помощью увеличении концентрации вдыхаемого кислорода. Таким
образом, показанием для ее проведения будет являться снижение РаО2 в
артериальной крови менее 50 мм.рт.ст. при дыхании воздухом (гипоксемия). Как
известно, дотация кислорода новорожденному ребенку может проводиться различными
способами (см. таблицу № 38).
Таблица № 38. Основные системы для дотации О2 (М.В.
Фомичев, 2000, с изменениями).
| Системы для дотации О2 |
Поток О2
%О2 |
Примечания |
Осложнения |
| Носовые канюли |
0.25-2 лмин. 25-50% |
Предпочтительный метод при длительной терапии
стабильного больного. Увлажнение желательно |
При больших потоках О2 возможно
вздутие живота. Сухость и воспаление слизистой носа.
Аллергическая реакция на поливинилхлорид.
При широких канюлях возможно появление PEEP |
| О2 маска |
1-6 лмин 35-55% |
Рекомендуется при коротком курсе
(транспортировка, процедуры). |
Аспирация желудочного содержимого |
| Палатка |
6-12 лмин. Обычно применяется со
смесителем О2воздух
60-80% |
Простой и эффективный способ обеспечения
точной концентрации О2 (если применяется со смесителем). |
Возможен перегрев ребенка При малых потоках
возможно накопление в палатке СО2
Сухость и воспаление слизистой носа при недостаточном увлажнении |
| Инкубатор |
Концентрация зависит от конструкции
инкубатора указывается фирмой-изготовителем |
Обычно применяется у новорожденных с
нестабильной температурой тела Если требуетсяFiO2>40%
предпочтительнее больного поместить в О2 палатку
Быстрое падение FiO2 при открывании кювеза |
Возможен перегрев ребенка Сухость и
воспаление слизистой носа при недостаточном увлажнении
|
Следующим, более инвазивным, методом респираторной терапии является
использование спонтанного дыхания с постоянным положительным давлением в
дыхательных путях (СРАР). Это такой режим дыхательной поддержки, при котором
больной дышит самостоятельно, и заданное положительное давление в дыхательных
путях поддерживается во время вдоха и выдоха. Показания для применения СРАР, по
нашему мнению, можно разделить на абсолютные и относительные. Абсолютные
основаны на лабораторных данных, а относительные – на клинических.
Абсолютным показанием для проведения СРАР является:
Артериальная гипоксемия (РО2 менее 50 мм.рт.ст.) при FiO2
во вдыхаемой смеси более 0,6-0,7 и РСО2 менее 50-55 мм.рт.ст., рН ≥
7,25.
Относительные показания:
- Западение податливых мест грудной клетки, тахипноэ;
- Прекращение ИВЛ.
В клинической практике существуют несколько способов создания СРАР: через
носовые катетеры; назофарингеальные катетеры; с помощью маски; через
интубационную трубку.
Все методы проведения СРАР требуют увлажнения и нагрева дыхательной смеси,
декомпрессии желудка. Величина СРАР зависит от формы патологии и гестационного
возраста и может варьировать от 2 до 10 см.вод.ст. У доношенных детей обычно
начинают проведение СРАР с 4-5 см.вод.ст.
Пошаговая стратегия включает изменение параметров СРАР на 1-2 см.вод.ст. за
15-20 минут. Нижняя граница СРАР составляет 2 см.вод.ст., так как в норме меньше
этой величины СРАР, создаваемое голосовыми связками на выдохе, обычно не
снижается. Пошаговая стратегия включает также изменения FiO2 на 5% за
15-20 минут.
NB: параметры не должны меняться одновременно, так как в конечном итоге
понять, что же “помогло” больному будет невозможно.
Противопоказанием для использования СРАР (Фомичев М.В., 2002, с изменениями)
будут следующие состояния:
Тяжелая сердечно-сосудистая недостаточность;
рН меньше 7,25 и РаСО2 более 55-60 мм.рт.ст.;
Частые эпизоды апноэ (более 2 раз за 3-6 часов), если они сопровождаются
брадикардией и снижением сатурации;
Атрезия хоан, диафрагмальная грыжа, трахеопищеводный свищ;
Как известно, любое терапевтическое воздействие требует контроля и оценки
эффективности, не является исключением и СРАР.
К методам контроля за этим видом респираторной поддержки можно отнести
следующие (Фомичев М.В., 2002, с изменениями):
Показатели КОС в артериальной, капиллярной или венозной крови;
Сатурация или транскутанное определение рО2;
ЧСС и АД;
FiO2 во вдыхаемой кислородно-воздушной смеси;
Температура и влажность кислородно-воздушной смеси;
Цвет кожных покровов;
Аускультативная картина легких;
Рентгенограмму легких в прямой проекции после подбора параметров. В
зависимости от степени пневматизации легких уровень СРАР снижают при
перераздувании или повышают при ателектазировании участков легких. Купол
диафрагмы должен быть расположен между 8 и 9 ребром, но этот уровень может
варьировать у разных больных, что зависит от индивидуальных особенностей
конкретного больного. Например, при БЛД у больного может иметься постоянная
легочная эмфизема.
К оценке эффективности выбранных параметров относятся:
РО2 = 50-70 мм.рт.ст. (сатурация 90-94%) при FiO2 ≤
0,7; РаСО2 ≤ 55-60 мм.рт.ст.; рН ≥ 7,25;
Уменьшение работы дыхания (снижение частоты дыхания на 20-40%, уменьшение
ретракции податливых мест грудной клетки);
Улучшение рентгенологической картины легких (оценить пневматизацию);
Возможные осложнения и побочные эффекты СРАР (М.В.Фомичев, 2002):
Изменение гемодинамического статуса больного будет зависить от величины СРАР,
ОЦК, легочной растяжимости.
Повышение ВЧД;
Снижение диуреза;
Баротравма легких;
Повышение легочного сосудистого сопротивления;
Возможно увеличение шунтирования крови экстрапульмонального и внутрилегочного;
Снижение перфузии мозга;
Повышение работы дыхания;
Повышение объема «мертвого дыхательного» пространства;
Следующий по значимости, но также по агрессивности и инвазивности, метод
респираторной терапии – ИВЛ.
К сожалению, в настоящее время в доступной литературе нам не встретилось
общепринятых абсолютных клинических и лабораторных критериев для перевода
ребенка на ИВЛ. Разные авторы (Любименко В.А., 1995; Фомичев М.В., 2000;
Goldsmith J.P., Karotkin E.H., 1988; Avery G. et al., 2000) указывают
неодинаковые сочетания показателей, которые они используют как показания для
начала проведения ИВЛ. Более однообразное мнение существует по поводу
лабораторных показателей. Вероятно, именно их можно использовать в качестве
абсолютных критериев, как это чаще всего и происходит в клинической практике,
правда, при наличии возможности определения КОС, а в России эта возможность есть
не везде:
- рН менее 7,20 (независимо от формы патологии).
- РСО2 более 55-60 мм.рт.ст., рН ≤ 7,25 при содержании кислорода
во вдыхаемой смеси более 70% и РО2 (арт.) менее 50 мм.рт.ст.
К относительным критериям большинство авторов относят:
-Неэффективность СРАР по поддержанию оксигенации.
-Рецедивирующие апноэ (если консервативные методы не дают эффекта).
- Клиническая картина шока.
Lough M.D. et al. (1979) (цит. по А.П. Зильберу, 1988) указывают, что в
некоторых случаях они использует для определения показаний для начала проведения
ИВЛ следующую таблицу (см.табл. № 39).
Таблица № 39. Показания для проведения ИВЛ (Lough M.D.
et al.,1979 с изменениями).
· - Хотя бы два эпизода апноэ продолжительностью более 45 сек.
Естественно, для проведения ИВЛ необходимым условием является интубация
трахеи. Общепринятым в реаниматологии является проведение рентгенологического
контроля положения интубационной трубки после интубации, так как расстояния в
воздухоносных путях могут значительно различаться. Как известно, они зависят от
массы тела, гестационного возраста, длины тела и т.д. (См. рисунки № 8-9).
На данных рисунках показана зависимость длины верхних дыхательных путей
новорожденного ребенка от длины тела, массы, окружности головы. Вероятно, у
некоторых больных при интубации трахеи целесообразно ориентироваться не только
на массу тела, как обычно принято в России, но и на другие антропометрические
показатели.
В ДГБ № 1 г. Санкт-Петербурга на отделении реанимации принято в отдельном
документе, зафиксированном на аппарате ИВЛ, указывать дату интубации данной
трубкой, ее тип и размеры, глубину стояния у линии губ. (Например, 10.05.02;
Portex; O=4,0; у губ 10,0 см.). На наш взгляд, данная методика позволяет
избежать значимого изменения положения интубационной трубки в процессе ухода за
больным. Как известно, в практической работе необходимо учитывать соответствие
размеров и глубины введения интубационной трубки дыхательным путям ребенка
(см.таблицу № 40).
Рисунок № 8. Зависимость длины верхних дыхательный путей от
длины тела (Coldiran J.S., 1968).
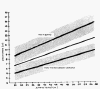
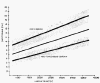
Рисунок № 9. Зависимость длины верхних дыхательных путей от
массы тела (Coldiran J.S., 1968).
При несоблюдении размеров интубационной трубки или катетера для санации
возможно развитие осложнений в виде развитие пролежней трахеи, сброса потока
газа помимо интубационной трубки, значительно затрудняющих подбор параметров ИВЛ.
Если же у больного нарушена глубина постановки ЭТТ, то возможно перераздувание
одного легкого, с риском развития синдромов утечки воздуха и ателектазирование
другого.
Таблица № 40. Рекомендуемые размеры интубационных трубок и глубина введения
от линии губ, размеры катетеров для санации в зависимости от массы тела.
| Масса тела |
Размер ЭТТ (внутренний
диаметр в мм.) |
Глубина введения от линии губ
(см.) |
Размер катетера для санации
(Fr) |
| Менее 1000 гр. |
2,5 |
7 |
5 |
| 1000-2000 гр. |
3,0 |
7-8 |
6,5 |
| 2000-3500 гр. |
3,5 |
8-10 |
6,5 |
| 3500-4000 гр. |
4,0 |
10-11 |
8 |
Хотелось бы обратить внимание, что при проведении ИВЛ по системе Айра, даже
опытным реаниматологом, при отсутствии клапана «безопасности», пиковое давление
на вдохе может достигать 45-50 см.вод.ст. Это может приводить к развитию тяжелой
баротравмы легких. Для обеспечения безопасности больного можно рекомендовать
использование мешков Амбу с установленными клапанами «сброса избыточного
давления на вдохе» или при использовании системы Айра ограничение выставленного
потока газа (см. таблицу № 41).
Таблица № 41. Рекомендуемые «безопасные» потоки газа,
установленные при дыхании по системе Айра (Любименко В.А., 1995).
| Вес ребенка (гр.) |
Поток, устанавливаемый на
системе Айра, лмин. |
Давление (см.вод.ст.)
|
| Менее 1000 |
4-5 (max 6) |
15-20 |
| 1000-2000 |
6 (max 10) |
20-30 |
| 2000-3000 |
8 (max 12) |
25-35 |
| >3000 |
8-10 (max 12) |
30-35 |
Чаще всего в неонатальных респираторах изменяемыми параметрами являются
давление вдоха и выдоха, время вдоха, соотношение вдоха к выдоху, частота
дыхания, процент кислорода во вдыхаемой смеси. Реже используют «объемную»
вентиляцию и регуляцию потока. К сожалению, в настоящее время не существует
общепринятых оптимальных режимов и параметров ИВЛ при различных видах легочной
патологии. Правда, различия касаются прежде всего времени вдоха и соотношения
вдоха к выдоху. Так, например, в зарубежных руководствах (Goldsmith J.P.,
Karotkin E.H., 1988; Гомелла Т.Л., 1998) рекомендуют устанавливать следующие
инициальные параметры ИВЛ: Tвд/Tвыд = 1:1; Tвд до 0,5 сек. В Санкт-Петербурге
чаще всего используют параметры, кратко подытоженные М.В.Фомичевым и
представленные в таблице № 42.
Кроме того, хотелось бы обратить внимание на тот факт, что в некоторых
российских руководствах последних лет по респираторной терапии, например,
Мостового А.В. и др.(2002) имеются неточности, касающаяся рекомендаций раннего
применения высокочастотной вентиляции и сурфактанта. Как показывает клиническая
практика, да и большинство зарубежных рекомендаций, касающихся данного вопроса,
применение высокочастотной вентиляции, как инициальной респираторной терапии в
первые 3 часа жизни или до применения методов традиционной ИВЛ ни только
невозможно, но и не нужно. На наш взгляд, не являются показаниями для применения
ВчИВЛ, как показывает опыт, большинство случаев сепсиса, пневмоний, СДР I типа.
Также, по нашему мнению, профилактическое введение сурфактанта показано не всем
детям, как указывают авторы, а только детям с низкой массой тела, угрожаемым по
развитию СДР I типа.
Таблица № 42. Рекомендуемые параметры ИВЛ при различных заболеваниях (М. В.
Фомичев, 2000, с изменениями).
| Заболевания |
PIP (см. вод. ст.) |
PEEP (см. вод.ст.) |
Tвд (сек) |
Tвд/Tвыд |
ЧД в мин |
| Апноэ Здоровые легкие |
10-12 |
2 |
0.3-0.4 |
Устанавливается индивидуально |
2-10 |
| РДС |
18-30 |
3-5 |
0.3-0.4 |
1:2 |
40-60 |
| ПЛГ |
20-35 |
Менее 2 при легочной патологии PEEP более 2 |
0.2-0.4 |
1:1-1:2 |
60-120 |
| Интерстициальная легочная эмфизема,
пневмоторакс |
Менее 20 |
Менее 2 |
0.2-0.3 |
Устанавливается индивидуально |
60и более |
| Аспирация мекония |
25-30 |
2-5 |
0.3-0.4 |
1:2 – 1:3 |
40-60 |
| БЛД |
Зависит от стадии заболевания |
2-6 |
0.3-0.6 |
Устанавливается индивидуально |
Зависит от стадии заболевания |
Критерием адекватности подобранных параметров может служить уменьшение
клинических проявлений дыхательной недостаточности, возможность поддерживать у
пациента рН свыше 7,25, РаО2 ≥ 50 мм.рт.ст, SatО2 ≥ 88%,
РаСО2 ≤ 55-60 мм.рт.ст., видимое улучшение экскурсий грудной клетки,
отсутствие беспокойства пациента и синхронность дыхания пациента и респиратора.
В случае беспокойства больного необходимо исключить возможные недыхательные
причины, прежде всего болевой синдром, а также вздутие живота, резкий шум, в том
числе и транспортного средства, свет и т.д.
Считаем важным отметить, что оксингенация больного может существенно зависить
от положения тела. Так, хорошо известно, что при положении ребенка на животе
уровень оксигенации выше, чем при положении на спине. Связано это с
физиологическими особенностями гравитационного распределения по зонам легких
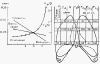
вентиляции и кровотока (см. рисунок № 10).
Рисунок № 10 . Распределение вентиляции и кровотока по зонам
легких (West J.B., 1970).
Следует заметить, что при подборе параметров ИВЛ у больного врач-реаниматолог
РКЦН ориентируется на параметры ИВЛ, к которым ребенок был адаптирован до начала
транспортировки, то есть, существует преемственность в подборе параметров ИВЛ.
Обычно новорожденный синхронизирован с аппаратом ИВЛ при адекватно,
подобранных параметрах. При «травматичных» параметрах или поражении ЦНС может
требоваться дополнительная седатация для синхронизации с аппаратурой ИВЛ. Обычно
используются препараты группы бензодиазепинов (разовая доза 0,2-0,5 мг/кг 0,5%
раствора сибазона или 0,5% раствора реланиума), ГОМК (50-200 мг/кг 20%
раствора), реже группа наркотических анальгетиков в возрастных дозировках (фентанил
микроструйно 0,5-1,0 мкг/кг/час; морфин в дозе 0,1 мг/кг или микроструйно для
недоношенных новорожденных от 2 до 10 мкг/кг/час, а для доношенных – от 5 до 20
мкг/кг/час) (Yaster M. et al., 1997).
Одним из общепринятых критериев тяжести поражения легких при различных
заболеваниях является индекс оксигенации. Кроме того, он косвенно дает
представление о методе дыхательной поддержки, в которой нуждается конкретный
больной. Как известно, он вычисляется по следующей формуле:
Oi=(MAP x FiO2 x 100%) : РаО2, где
Oi-индекс оксигенации
MАР - среднее давление в дыхательных путях
FiO2 - фракция вдыхаемого кислорода
РаО2- парциальное напряжение кислорода в артериальной крови,
измеренной постдуктально.
Существует 3 степени изменения указанного индекса:
Oi-более 12 – свидетельствует о проявлении тяжелой ДН, нуждающейся в
респираторной поддержке.
Oi = 25-35 – у больного имеется дыхательная недостаточность, требующая
экстремальной дыхательной поддержки.
Oi - более 40 - показание для проведения ЭКМО, риск летального исхода
возрастает до 80%.

