 |
|  |
| Медицинская библиотека / Раздел "Книги и руководства" |
|
|
|
| 4.1 Основные причины формирования резистентности к антимикробным препаратам |
|
Медицинская библиотека / Раздел "Книги и руководства" / Фармакоэпидемиологические основы антибактериальной терапии распространенных заболеваний / 4.1 Основные причины формирования резистентности к антимикробным препаратам
Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Cлов в этом тексте - 3593; прочтений - 6121
Размер шрифта:
12px |
16px |
20px
4.1 Основные причины формирования резистентности к
антимикробным препаратам
Считается, что одной из основных причин высокого уровня резистентности
является большой объем потребляемых антибиотиков.
В дальневосточном регионе России в сравнении с результатами отчетов
«Потребление антимикробных средств и антимикробная резистентность наиболее
важных микроорганизмов в Нидерландах» и «Использование антимикробных препаратов
и оценка уровня резистентности микроорганизмов к антибактериальным препаратам
выделенных от животных, продовольствия, пищевых продуктов и людей в Дании»,
показали более высокий уровень потребления АМП, который на 48 % и 63 % превышает
средние показатели в Дании и Нидерландах соответственно (p<0,05), сохраняя во
всех трех сравниваемых анклавах тенденцию к росту потребления АМП в последующие
годы в рамках имитационного прогноза (рис. 4.2).
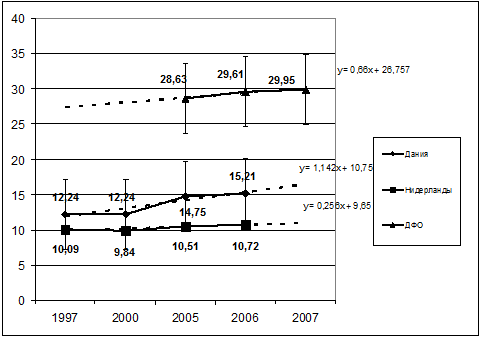
Рис. 4.2 Потребление антибактериальных препаратов
выраженное в DDD на 1000 жителей в день в Дании,
Нидерландах и ДФО РФ.
В то же время в Дальневосточном регионе структура потребления АМП значительно
отличается, от европейских стран (таб. 4.1, 4.2 и рис. 4.3). Так объемы
использования группы J01CA «Пенцициллины с расширенным спектром» в ДФО в 2006г.
составили 4,62 DDD на 1000 жителей в день, а в
Нидерландах 1,87 и Дании 2,95 DDD на 1000 жителей в день
соответственно (рис. 18). В экономически развитых странах Европы более активно
используется группа J01CE «Я-лактамаза чувствительные пенициллины», которые
практически не используются в Дальневосточном регионе. В то же время на востоке
РФ в 20 раз больше используются J01GB «Аминогликозиды», в 5 раз группа J01D «Цефалоспорины»,
в три раза интенсивнее группы J01MA «Фторхинолоны» и J01E «Сульфаниламиды и
триметоприм», чем в Дании и Нидерландах.
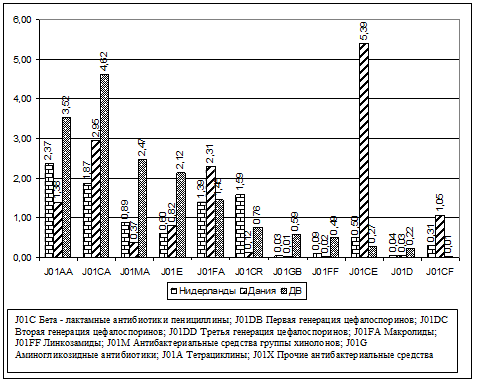
Рис. 4.3. Распределение объемов потребления
антибактериальных препаратов выраженное в DDD на 1000
жителей в день в 2006г.
Таким образом, отличительной особенностью Дальневосточного региона является
широкое использование на амбулаторном этапе «стационарных» АМП, препаратов с
широким спектром активности и высокой стоимостью. Возможно, это связано с
высокими уровнями резистентности основных возбудителей внебольничных инфекций.
В этой связи был проведен анализ резистентности Str. рneumoniaе, как одного
из наиболее частого этиологического агента вызывающего инфекционные заболеваний
на амбулаторно-поликлиническом этапе оказания медицинской помощи.
Таблица 4.1. Сравнительная розничная структура потребления
в DDD/1000жителей/день основных фармакотерапевтических
групп антибактериальных препаратов в Дании в 1997-2006 гг.
| ATC группа |
Терапевтическая группа |
1997 |
1998 |
1999 |
2000 |
2001 |
2002 |
2003 |
2004 |
2005 |
2006 |
| J01AA |
Тетрациклины |
0,98 |
0,98 |
0,93 |
0,98 |
0,99 |
1,04 |
1,07 |
1,17 |
1,27 |
1,38 |
| J01CA |
Пенцициллины с расширенным спектром |
2,39 |
2,39 |
2,29 |
2,3 |
2,47 |
2,51 |
2,52 |
2,63 |
2,78 |
2,95 |
| J01CE |
Я-лактамаза чувствительные пенициллины |
4,57 |
4,81 |
4,48 |
4,7 |
4,91 |
5 |
5,07 |
5,2 |
5,28 |
5,39 |
| J01CF |
Я-лактамаза резистентные пенициллины |
0,34 |
0,4 |
0,48 |
0,52 |
0,65 |
0,77 |
0,85 |
0,92 |
0,97 |
1,05 |
| J01CR |
Пенициллины + ингибитор Я-лактамаз |
0,02 |
0,03 |
0,02 |
0,02 |
0,03 |
0,04 |
0,05 |
0,06 |
0,07 |
0,12 |
| J01DA |
Цефалоспорины |
0,02 |
0,03 |
0,02 |
0,02 |
0,03 |
0,03 |
0,02 |
0,02 |
0,03 |
0,03 |
| J01E |
Сульфаниламиды и триметоприм |
0,79 |
0,77 |
0,73 |
0,73 |
0,75 |
0,75 |
0,77 |
0,77 |
0,79 |
0,82 |
| J01FA |
Макролиды |
2,03 |
2,28 |
2,17 |
2,02 |
2,1 |
2,15 |
2,13 |
2,23 |
2,41 |
2,31 |
| J01FF |
Линкозамиды |
0,01 |
0,01 |
0,01 |
0,01 |
0,01 |
0,01 |
0,01 |
0,01 |
0,01 |
0,02 |
| J01GB |
Аминогликозиды |
0 |
0 |
0 |
0 |
0 |
0,01 |
0,01 |
0,01 |
0,01 |
0,01 |
| J01MA |
Фторхинолоны |
0,22 |
0,23 |
0,2 |
0,15 |
0,17 |
0,18 |
0,25 |
0,28 |
0,32 |
0,37 |
| J01 |
|
12,24 |
12,76 |
12,14 |
12,24 |
12,86 |
13,26 |
13,53 |
14,06 |
14,75 |
15,21 |
Таблица 4.2. Сравнительная розничная структура потребления
в DDD/1000жителей/день основных фармакотерапевтических
групп антибактериальных препаратов в Нидерландах в 1997-2006 гг.
| ATC группа |
Терапевтическая группа |
1997 |
1998 |
1999 |
2000 |
2001 |
2002 |
2003 |
2004 |
2005 |
2006 |
| J01AA |
Тетрациклины |
2,64 |
2,55 |
2,49 |
2,47 |
2,39 |
2,33 |
2,23 |
2,22 |
2,41 |
2,37 |
| J01CA |
Пенцициллины с расширенным спектром |
2,18 |
2,13 |
2,06 |
1,88 |
1,82 |
1,78 |
1,77 |
1,69 |
1,86 |
1,87 |
| J01CE |
Я-лактамаза чувствительные пенициллины |
0,56 |
0,52 |
0,51 |
0,52 |
0,49 |
0,45 |
0,44 |
0,42 |
0,44 |
0,5 |
| J01CF |
Я-лактамаза резистентные пенициллины |
0,23 |
0,22 |
0,23 |
0,24 |
0,25 |
0,25 |
0,27 |
0,28 |
0,29 |
0,31 |
| J01CR |
Пенициллины + ингибитор Я-лактамаз |
0,92 |
0,95 |
1,04 |
1,15 |
1,25 |
1,34 |
1,39 |
1,38 |
1,5 |
1,59 |
| J01DА |
Цефалоспорины |
0,13 |
0,11 |
0,1 |
0,08 |
0,07 |
0,07 |
0,06 |
0,05 |
0,05 |
0,04 |
| J01E |
Сульфаниламиды и триметоприм |
0,76 |
0,75 |
0,76 |
0,71 |
0,7 |
0,67 |
0,66 |
0,65 |
0,63 |
0,6 |
| J01FA |
Макролиды |
1,12 |
1,16 |
1,17 |
1,13 |
1,22 |
1,24 |
1,27 |
1,31 |
1,42 |
1,39 |
| J01FF |
Линкозамиды |
0,03 |
0,03 |
0,03 |
0,04 |
0,05 |
0,06 |
0,06 |
0,07 |
0,08 |
0,09 |
| J01GB |
Аминогликозиды |
0 |
0 |
0 |
0 |
0,01 |
0,01 |
0,02 |
0,02 |
0,02 |
0,03 |
| J01MA |
Фторхинолоны |
0,84 |
0,83 |
0,86 |
0,84 |
0,84 |
0,81 |
0,81 |
0,84 |
0,86 |
0,89 |
| J01 |
|
10,09 |
9,94 |
10 |
9,84 |
9,9 |
9,81 |
9,81 |
9,77 |
10,51 |
10,72 |
Показатели резистентности Str. рneumoniaе к АМП в Нидерландах значительно
отличались от результатов полученных в Дальневосточном регионе. Так, если по
показателю резистентности к пенициллину достоверных отличий не было выявлено, то
по уровню резистентности к макролидным антибиотикам 27,6% и доксициклину 41,3 %
Дальневосточный регион в 3 и 5 раз соответственно превышал показатели в
Нидерландах (рис. 4.4).
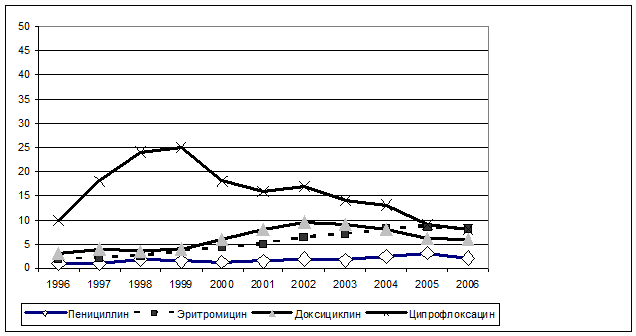
Рис. 4.4. Сравнительные показатели резистентности (%) Str.
рneumoniaе к АМП в Нидерландах (NETHMAP 2007; 2007) и Дальневосточном регионе.
Таким образом, различия в структуре потребления АМП ведут к различным уровням
резистентности основных возбудителей внебольничных инфекционных заболеваний и
как следствие невозможности использования рекомендаций по антибактериальной
терапии Западных стран.
Во многом это объясняется широким применением именно тех препаратов, которые
являются своего рода движущей силой развития лекарственной устойчивости (аминогликозиды,
тетрациклины, хлорамфеникол).
Другая причина роста резистентности — низкий уровень
микробиологической диагностики, связанный с изношенным и несовременным
оборудованием бактериологических лабораторий, а также с подготовкой врачей в
области антимикробной химиотерапии. В настоящее время из всех субъектов ДФО,
только в Республике САХА Якутия имеется современное бактериологическое
оборудование. Во всех других регионах АМП даже у тяжелых больных в стационарах
назначается, как правило, вслепую, бессистемно с хаотической сменой препаратов и
использованием нерациональных комбинаций. Посев микрофлоры у пациента начинают
лишь тогда, когда не дают эффекта 2—3 курса антибиотиков или когда он
декретирован в обязательном порядке (например, при дифтерии). При этом
результаты посевов во многих случаях не удовлетворяют клиническим нуждам.
Неразрывно с низким уровнем микробиологической диагностики связано отсутствие
инфекционного контроля в стационарах России, который обеспечивает профилактику и
предотвращение нозокомиальных инфекций. Эти инфекции в США находятся на 4-м
месте среди причин смертности, от них ежегоднопогибают более 100 тыс. человек.
Одним из способов борьбы с
такими инфекциями является стремление избегать необоснованных госпитализаций,
поскольку стационар и особенно ОРИТ - это место концентрации и циркуляции
устойчивых штаммов микроорганизмов.
Отечественная же традиция состоит в том, чтобы как можно раньше положить
больного в реанимацию, что, по мнению врачей, позволяет обеспечить лучший уход.
При этом возможность инфицирования пациента одним или несколькими возбудителями
тяжелых инфекций во внимание не принимается. Официальная статистика
нозокомиальных инфекций дает картину мнимого благополучия, поскольку число
случаев зарегистрированных нозокомиальных инфекций в России, по данным академика
РАМН В.И. Покровского, занижено в 30—40 раз. Это создает впечатление, что
резистентные штаммы, появившись, быстро и беспрепятственно распространяются по
отделению и всему стационару. Причина данного явления - именно отсутствие
инфекционного контроля и несоблюдение достаточно простых
санитарно-эпидемиологических мероприятий и гигиенических правил.
В России и в Дальневосточном регионе, в отличие от многих стран мира
сохраняется безрецептурная продажа антибиотиков, несмотря на неоднократно
издававшиеся приказы Минздрава России, контрольно-надзорные мероприятия
осуществляемые Росздравнадзора за соблюдением лицензионных требований и условий
аптек (рис. 4.5).
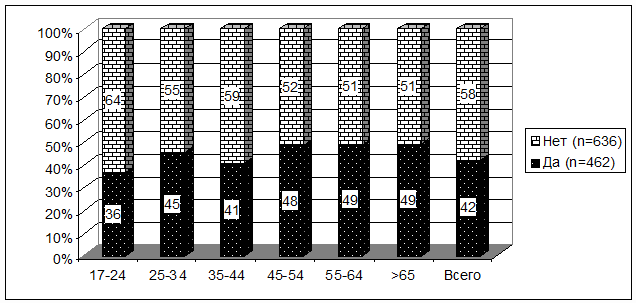
Рис. 4.5.Сведения о выписке рецептов на антибактериальные
препараты при назначении врачом поликлиники в территориях ДФО в 2007-2008 гг.,
%.
В результате более 60% населения ДФО имеет АМП в домашних аптечках, где,
согласно нашим исследованиям, хранится от 1 до 11 антимикробных препаратов. Мы
вынуждены подчеркнуть ещё и тот факт, что в список наиболее «популярных»
препаратов, находившихся у респондентов в домашних аптечках, входят далеко
небезобидные антибактериальные препараты, в частности ко-тримоксазол,
хлорамфеникол и доксициклин (рис. 4.6). В региональной практике при
бесконтрольном использовании вышеуказанных препаратов имеются случаи развития
агранулоцитозов и тяжелых токсико-аллергических реакций: многоформной
экссудативной эритемы, или синдрома Стивенса-Джонсона, токсического
эпидермального некролиза или синдрома Лайела.
По нашим данным более чем у четверти респондентов в домашних
аптечках имеются антибактериальные препараты с истекшим сроком годности.
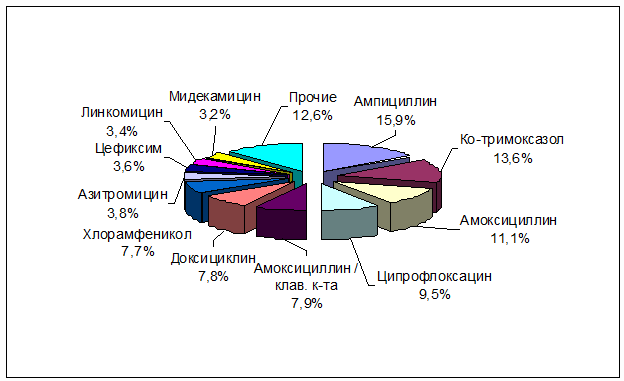
Рис. 4.6 Структура АМП находящихся в домашних аптечках
населения
Большинство из них мотивируют такое «легкомысленное» отношение к домашней
аптечке тем, что имеют информацию о том, что довольно часто срок годности
препаратов в ЛПУ «продляется специальными комиссиями», поэтому применение
просроченных препаратов не является редким явлением. Пациенты не задумываются о
возможных последствиях, хотя известно, что тетрациклины с истекшим сроком
годности приводят к развитию почечной недостаточности.
Не последнюю роль в этом процессе играет реклама в средствах массовой
информации, которой не может противостоять практически отсутствующая
санитарно-просветительная работа. Возможно, что высокий уровень
антибиотикорезистентности в крупных городах, и особенно в Хабаровске, связана в
том числе и с вкладом мигрантов из стран ближнего зарубежья и Китая, где
полностью отсутствует контроль за распространением антибиотиков.
На основании вышеизложенного можно сформировать основные причины
резистентности микроорганизмов к антимикробным препаратам (рис. 4.7)
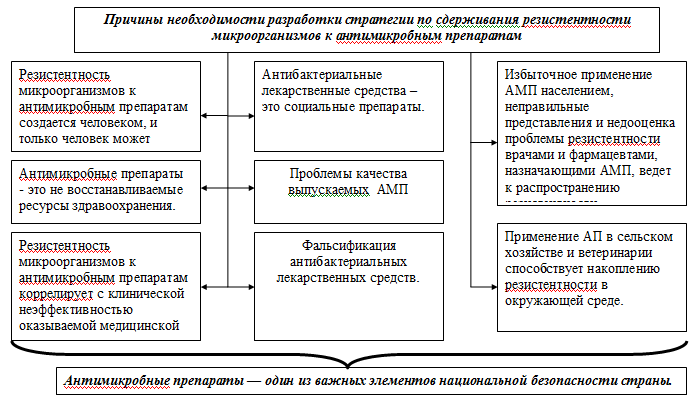
Рис. 4.7 Основные причины резистентности микроорганизмов к
антибактериальным препаратам.
[ Оглавление книги | Главная страница раздела ] |
|
| Поиск по медицинской библиотеке |
|
|
|
|  |
| 
|

