Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Глава 6. СОСУДИСТАЯ ПАТОЛОГИЯ И ЧЕРЕПНО–МОЗГОВАЯ ТРАВМА
Черепно–мозговая травма (ЧМТ) в анамнезе лиц пожилого и старческого возраста
– очень частый факт, и особенно это касается участников Великой Отечественной
войны и других вооруженных конфликтов. Именно на основе перенесенной в прошлом
ЧМТ возникают в последующем сосудистые проблемы, и именно ЧМТ является зачастую
причиной возникновения и формирования нейропсихических расстройств, которые в
дальнейшем рассматриваются как обусловленные сосудистой патологией, хотя на
самом деле имеют сочетанное, травматически–сосудистое происхождение. Именно эти
проблемы заставили нас представить в рамках данного издания представить
взаимоотношения сосудистой патологии и последствий ЧМТ.
6.1. Роль перенесенной травмы головного мозга в возникновении и развитии
сердечно-сосудистой патологии
В соответствии с общепринятой междисциплинарной классификацией (Коновалов
А.М. и др., 1992, 1994) в развитии травматической болезни головного мозга
выделяют следующие основные периоды: острый, промежуточный и отдаленный. Любая
ЧМТ, вне зависимости от ее тяжести, приводит к сложному комплексу деструктивных
и репаративных процессов. Но о клинически значимых последствиях травмы следует
говорить только в том случае, когда у больного развивается устойчивое
патологическое состояние, требующее лечебных мероприятий.
Течение травматической болезни головного мозга определяется не столько
травматическим субстратом, сколько функциональным состоянием головного мозга,
непосредственно обеспечивающего адаптацию организма в новых условиях (Шерман
М.А., 2003). Немаловажное значение играют и дотравматическая неврологическая
патология, возрастные, преморбидные факторы, особенности личности больного,
сопутствующая соматическая патология и т.д.
Исходя из самочувствия лиц, перенесших ЧМТ, выделяется четыре основных типа
развития посттравматического периода:
регрессирующий;
стабильный;
ремиттирующий;
прогредиентный.
Дискуссионным является вопрос о течении посттравматического периода: если
часть авторов считает ЧМТ преимущественно регредиентным процессом, связывая
прогрессирование с дополнительными воздействиями (Levin
H.S., Eisenberg
H.M., 1991), то большинство
исследователей считают обязательным наличие отдаленного периода (Самотокин Б.А.,
1978; Коновалов А.М. и др., 1992, 1994).
В ряде исследований (Педаченко Е.Г. и др., 1993; Ярцев В.В. и др., 1995)
отмечена роль возрастного фактора, при этом указывается на снижение
компенсаторных возможностей головного мозга после 40 лет.
Таким образом, даже отдаленные последствия ЧМТ не являются законченным
состоянием, при этом тип течения и прогноз заболевания определяются частотой
наступления и выраженностью периодов декомпенсации посттравматического процесса.
При этом возможности наступления декомпенсации могут быть зависимы от иной,
нежели травматическая, патологии центральной нервной системы, в частности
сосудистой.
Взаимоотношения травматической и сосудистой патологии представляются
достаточно сложными и неоднозначными. Недостаточно изученными являются
взаимоотношения последствий черепно-мозговой травмы (ЧМТ) и течения
полиорганного, мультифокального атеросклеротического процесса, развития острых
сосудистых церебральных и коронарных катастроф, следующих за перенесенными
травмами головного мозга.
Разумеется, сама ЧМТ способствует нарушению адаптационно-приспособительных
функций организма как в остром, так и в последующих периодах её развития и
течения (Коновалов А.М., Лихтерман Л.Б., 1992; Коновалов А.М. и др., 1994).
Преходящие вегетативные и ангиодистонические расстройства острого периода ЧМТ с
течением времени становятся постоянными структурно очерченными синдромами
сосудистых заболеваний; по мере же удаления сроков ЧМТ и с увеличением возраста
больных, с течением процессов естественного старения организма, вероятность
данных сосудистых заболеваний еще более возрастает (Нестерова М.В., 2002;
Мякотных В.С. и др., 1995, 1996). Поэтому динамика травматической болезни мозга
может быть представлена либо как процесс полной компенсации, завершающийся
восстановлением регуляторных систем, либо как процесс незавершенной компенсации,
которая, постепенно истощаясь, приводит к стойким нарушениям механизмов
регуляции не только в нервной системе, но и в организме в целом.
Особый интерес к провоцирующей роли травмы головного мозга в формировании
сосудистой не только церебральной, но и кардиальной патологии, существенно
возрос в послевоенные годы (Каратыгин В.М. и др., 1948; Мясников А.Л., 1965).
Заболевания внутренних органов развивались не только после тяжелой травмы, но и
после легкой, когда отсутствовали условия для полного выздоровления. Имел важное
значение и повторный боевой травматический эпизод (Гротель Д.М., 1945; Молчанов
Н.С., 1951; Раздольский И.Я., 1951). На фронте значительно увеличилось
распространение АГ и связанных с её кризовым течением сосудистых катастроф -
инфарктов миокарда и острых нарушений мозгового кровообращения (Каратыгин В.М. и
др., 1948; Нагорная Р.А., 1948). Была установлена зависимость развития АГ от
интенсивности боевых действий, так, при наиболее активных действиях Балтийского
флота в апреле - июне 1943 г. больные АГ составили 62,6% от поступивших в
военные госпитали Ленинградского фронта за весь 1943 г. Разумеется, сыграл
важную роль и хронический психоэмоциональный стресс боевой обстановки: среди
участвовавших в боях на Ленинградском фронте на передовой менее одного месяца АГ
развивалась у 10% военнослужащих, от 1 до 6 месяцев – у 27%, более 6 месяцев –
уже у 29,2% (Гротель Д.М., 1945).
Помимо раннего развития АГ и её фатальных осложнений, у участников войны
регистрировались разнообразные нарушения сердечного ритма и проводимости как в
остром, так и в отдаленном периодах ЧМТ - до 11% от всех поступивших больных,
причем лабильность сердечного ритма описывалась Б.П. Кушелевским и Т.Г. Реневой
как «необычайная» (Кушелевский Б.П., 1951). Расстройства нервно-вегетативных
функций непосредственно после получения ЧМТ отмечены в 80-85%, регистрировались
вазомоторные нарушения, изменения ритма сердца в ранние сроки, «спазмы»,
напоминающие стенокардию у молодых лиц. Особо необходимо отметить появление
ранней стенокардии и нарушений ритма сердца у раненых в спинной мозг (Попов
С.П., Данскер В.Л., 1951). Интересным оказался факт зависимости изменений ЭКГ от
локализации травмы мозга, так, менее выраженные изменения ЭКГ отмечены при
ранениях в висок и лоб, а наиболее прогностически неблагоприятные - при ранениях
в теменные и затылочные области. В поздние сроки (через 7 лет после получения
ЧМТ) участились случаи выявления пароксизмальной тахикардии. Напротив, развитие
истинной стенокардии в раннем посткоммоционном периоде диагностировалось не
более чем у 1% пациентов (Кушелевский Б.П., 1951).
В ближайшие послевоенные годы у 9% гипертоников однозначно была установлена
связь с ЧМТ, причем именно после закрытой травмы мозга АГ развивалась
значительно чаще, чем при открытых ранениях черепа (Попов С.П., Данскер В.Л.,
1951). Но специальных наблюдений, касавшихся последующей профилактики
сердечно-сосудистых расстройств, проведено не было.
Сосудистые заболевания нижних конечностей также имели значительное
распространение в годы войны и ближайший послевоенный период. По данным А.П.
Лидского, «спонтанная гангрена» после взрывной травмы, особенно у курящих
военнослужащих, составила не менее 5%. Указывалось, что у 3,7% больных возможно
было связать данную патологию не только с длительным пребыванием в окопах -
«траншейной стопой» - но и с перенесенной ЧМТ. М.С. Иоффе указывал гораздо
большие цифры - до 21% ранних облитерирующих поражений артерий нижних
конечностей именно после ЧМТ. Современные патоморфологические исследования
подтвердили этот факт, так, выявлены выраженные изменения в глубоких слоях дермы
кожи при минно-взрывном поражении: в течение всего посттравматического периода
прогрессировали нарушения микроциркуляции, проявляясь в адгезии и сладже
форменных элементов крови (Бароян К.М., Кялян Г.П., 2004).
Разумеется, основное внимание при травме головного мозга уделялось именно
неврологической симптоматике. В остром периоде взрывной травмы более чем у 85%
пострадавших регистрировались различные дисфункции вегетативной нервной системы,
синкопальные состояния, признаки симпатико-адреналового гипертонуса - головная
боль, повышение АД, тахикардия, ознобоподобные гиперкинезы, повышенная
тревожность (Молчанов Н.С., 1951; Раздольский И.Я., 1951). При взрывной травме
легкой и средней степени тяжести отмечалось множество расстройств
отоневрологического, нейроофтальмического и терапевтического характера.
Логоневротические реакции и сурдомутизм наблюдались у 32,6% пациентов.
Клинические признаки травмы вестибулярного аппарата, системные головокружения с
вегетативной симптоматикой, синдром Меньера, по данным В.И. Воячека и К.А.
Хилова (1951), в период как самой Великой Отечественной войны, так и в ближайшие
послевоенный годы, встречались у 14%, а при дополнительных исследованиях с
применением функциональных нагрузок - у 37% пораженных.
Травматическая энцефалопатия при непроникающих ранениях головы составила не
менее 7%, при проникающих - уже 8,9%. Она развивалась спустя 1-2 года после
ранения и характеризовалась значительным числом пограничных психических
расстройств и снижением интеллектуальных функций (Раздольский И.Я., 1951).
Наблюдавшиеся у ветеранов изменения личности, ослабление познавательных
способностей и преждевременное старение организма в середине XX
века объясняли развитием «метаболического самоотравления», вызывающего
«токсическую энцефалопатию» (Решетников В.А., Резник А.М., 2008). Тем не менее,
тяжелые психические расстройства после закрытой травмы мозга через 7 лет после
окончания войны определяли только у 0,7% больных, а при открытых, проникающих
ЧМТ, через тот же срок не диагностировали вообще (Попов С.П., Данскер В.Л.,
1951). Это сложно объяснить с позиций современных воззрений на травматическую
болезнь мозга; кроме того, факт наличия тяжелой психопатологической симптоматики
при поступлении в госпиталь всего у 1,1% пострадавших заставляет сомневаться в
истинности статистических данных. Травматическая эпилепсия регистрировалась до
8,2% у всех раненых в голову (Раздольский И.Я., 1951), но эти данные также
разноречивы (Morrell F., 59/60,
1985).
Вопрос о роли ЧМТ в генезе сосудистых заболеваний как церебральной, так и
прочих локализаций, решался различно. В исследованиях 60-х гг. прошлого века
отмечалось значительное увеличение случаев обращаемости пациентов, перенесших
ЧМТ в годы войны, по поводу выраженного ухудшения состояния здоровья (Маслиев
А.Т. и др., 1965). Несмотря на длительный, более чем 15-летний срок, прошедший с
момента получения травмы, сами больные связывали негативное самочувствие именно
с ЧМТ. Такая поздняя декомпенсация травматической болезни отличалась от ранней
большей длительностью периода обострения и нарастанием психопатологической
симптоматики (Баронов В.А., 1960, 1966). Предполагалось, что преходящие в момент
получения травмы ангиодистонические расстройства с течением времени становились
постоянными структурно очерченными синдромами сосудистых заболеваний. По мере
удаления сроков ЧМТ вероятность сосудистых заболеваний возрастала, то есть для
того, чтобы неспецифические вегетативные нарушения оформились в сосудистое
заболевание, как самостоятельную нозологическую единицу, было необходимо время
(Мясников А.Л., 1965; Самотокин Б.А. и др., 1965).
Формирование и различные клинические проявления последствий ЧМТ на отдаленных
этапах заболевания в настоящее время объясняются затянувшимися на многие годы
нарушениями мозгового кровотока, впервые возникшими уже в процессе самой травмы
мозга (Хилько В.А., 1988; Помников В.Г., 2002). Вазоспазм обусловливает
изменения мозгового кровообращения, в частности, усиление гиперперфузии и
увеличение линейной скорости кровотока, которые могут затянуться на долгие годы.
Интракраниальные артерии реагируют на механические раздражения сокращением
гладкой мускулатуры, причем травматический спазм является билатеральным и
максимально выраженным в дистальных отделах внутренней сонной артерии,
проксимальных отделах средней и передней мозговых артерий, сосудах основания
мозга (Lynch D.R.,
Dawson T.M.,
1994). Именно спазм является причиной ишемии диэнцефальных структур, во многом
определяющих развитие патологии вегетативной нервной системы, в частности,
нарушений интегративной деятельности лимбико-ретикулярного комплекса (Marmarou
A., 1994; Korpelainen
J.T. et
al., 1999). Одним из главных факторов риска являются
преморбидные аномалии сосудистой сети головного мозга, обусловливающие высокую
частоту развития вторичных ишемических нарушений (Федоров О.О., Горбунов А.В.,
2007).
Патогенез стойких и выраженных головных болей у лиц, перенесших ЧМТ, является
в значительной степени сосудистым, свидетельствующим о наличии раннего
церебрального атеросклеротического процесса, хотя уровень содержания липидов в
сыворотке крови может в течение некоторого времени оставаться нормальным (Боровкова
Т.А., 1999; Мякотных В.С. и др., 2002). Следовательно, в сроки свыше 10 лет
после получения травмы к таким пациентам следует относиться как к лицам с
сочетанной дисциркуляторно-травматической энцефалопатией со всеми вытекающими
отсюда осложнениями процесса (Мякотных В.С. и др., 1995, 1996, 2002).
Спазм сосудов мозга в остром периоде травмы связан и с выделением в ликвор
нейромедиаторов и «гормонов стресса», в первую очередь, серотонина, с
содержанием которого коррелирует тяжесть ЧМТ и ее исходы; доказано увеличение
количества серотонина в ликворе не только в остром, но и в отдаленном периоде
травматической болезни головного мозга (Ерюхин И.А., 1993, 1994;
Jacobs et al.,1995).
Выделение нейромедиаторов провоцирует нарушение функции эндотелия, что может
становиться предиктором последующего развития кардиоваскулярной патологии (Ritter
A.M., Robertson
C.S., 1994; Black P.H.,
Garbutt L.D.,
2002). Эндотелиальная дисфункция существенно возрастает с увеличением возраста
больных, и это, в сочетании с повышением активности симпатической нервной
системы в периферических органах, в первую очередь, в сердце, и нарушением
обмена нейромедиаторов в отдаленном периоде ЧМТ, является дополнительным
фактором риска развития сосудистых заболеваний.
Непосредственно с сосудистым фактором связан и другой патогенетический
механизм формирования последствий ЧМТ - нарушение ликвородинамики, причем
ликвородинамические нарушения кореллируют с гемодинамическими, что также
позволяет нам рассматривать травматическую болезнь мозга как причину развития
сосудистой патологии.
Для отдаленного периода ЧМТ характерна ареактивность вегетативной нервной
системы или парадоксальный тип реагирования (Шогам И.И., 1990;
Stratton M.C.,
Gregory R.J.,
1994). Такие вегетативные расстройства, как лабильность АД и нарушения в
проводящей и пейсмейкерной системах сердца, также способствуют формированию
сердечно-сосудистой патологии (Осетров А.С., 1993; Вейн А.М. и др., 1991;
Мякотных В.С. и др., 1996). Органическая неврологическая симптоматика постепенно
сглаживается, и на первый план нередко выступают вегетативные и
эмоционально-личностные, психопатологические расстройства: астенический,
психопатоподобный, фобический, депрессивно-ипохондрический синдромы (Емельянов
А.Ю., 1995; Ямпольская В.В., 2007; Lipton
M.I., Schaffer
W.R., 1988;
Friedman M.J.
et al., 1994). Нарушения
биоэлектрической активности головного мозга (Жирмунская Е.А., 1997) приводят к
возникновению эпилепсии (Головкин В.И., Глазников А.А., 1991; Шевченко Ю.Л. и
др., 1996; Nuwer M.R.,
1988). Значимым является факт, что психовегетативные и личностные изменения в
отдаленном периоде ЧМТ весьма сходны с таковыми при АГ и ИБС (Боровкова Т.А.,
1999; Linden W. et
al., 2001). При увеличении возраста больного эти
изменения по своей сути не могут считаться исключительно посттравматическими, а
приобретают именно сосудисто-травматический генез (Crump
J.H. et
al., 1988; Soderback
I., Ekholm J.,
1992).
Как сказано выше, последствия ЧМТ отягощают течение сосудистого процесса. С
другой стороны, получены данные о возможности развития в ряде случаев так
называемого феномена «перекрестной резистентности», в силу которого перенесенная
в прошлом травма мозга может способствовать адаптации центральной нервной
системы к произошедшим сосудистым катастрофам как церебрального, так и
коронарного генеза. При этом процесс протекает несколько более благоприятно, и
мобилизованные в результате ишемического инсульта или инфаркта миокарда
механизмы компенсации могут быть направлены не только на ликвидацию их
последствий, но и бывшей травмы мозга (Спектор С.И., Мякотных В.С., 1995;
Мякотных В.С. и др., 2007; Матвеева О.Н., 2008).
Исходя из сказанного, представляется очевидным наличие тесной взаимосвязи
между травматическими и сосудистыми патологическими процессами. Последствия ЧМТ
- это многофакторные состояния, на клинических особенностях и течении которых
сказывается влияние тяжести травмы, локализации первичного очага, соотношение
патологии специфических и неспецифических структур мозга, аутоиммунные,
генетические, социальные и другие факторы. Поэтому последствия ЧМТ необходимо
рассматривать как фон для развития полиорганного, мультифокального
атеросклеротического сосудистого процесса, а не только для атеросклероза
церебрального.
Патоморфологической основой изменений, происходящих в головном мозге при ЧМТ,
являются ультраструктурные нарушения, которые, в зависимости от тяжести травмы,
могут носить как обратимый, так и необратимый характер (Касумова С.Ю., 1994;
Marmarou A.,1994). Наиболее
значимыми и составляющими морфологическую основу формирования клинических
последствий ЧМТ с последующим нарушением интегративной деятельности мозга,
становятся необратимые деструкции митохондрий и других клеточных органелл,
грубоволокнистое перерождение нейропиля и осевых цилиндров, трансформация
гранулярного эндоплазматического ретикулума в «зебровидные тельца» (Alexander
M.P., 1995). Повреждения
выявляются преимущественно в стволовых отделах, корково-подкорковых
образованиях, гипоталамусе, гипофизе, чем и объясняется формирование в
отдаленном периоде нарушений вегетативной, обменной и нейротропной регуляции (Одинак
М.М., 1995; Одинак М.М. и др., 1996). Дисфункция гипоталамуса и базальных ядер
изменяет реализацию функций, регулирующих АД: нарушается обмен серотонина, в
первую очередь, а также эндотелина, вазопрессина, натрийуретического фактора (в
супраоптическом и паравентрикулярных ядрах), что определяет не только раннее
развитие АГ у лиц, перенесших травму мозга, но и столь же раннее развитие
патологии эндотелия как одного их ведущих факторов формирования мультифокального
атеросклеротического процесса (Гайдар Б.В., Парфенов В.Е., 1997). В дальнейшем
небольшие ишемические повреждения после ЧМТ регрессируют, а более крупные
закономерно сменяются рубцово-атрофическим процессом, который также способствует
мозговой и, следовательно, общей сосудистой дисфункции (Morton
M.Y., Wehman
P., 1995).
Морфологические исследования у перенесших ЧМТ выявляют фокальное повреждение
белого вещества головного мозга, значительное снижение числа нейронов в голубом
пятне, аналогичное изменениям, найденным у больных деменцией альцгеймеровского
типа. Характерно правостороннее или двустороннее уменьшение гиппокампа (Bracha
H.S. et
al., 2005). Уменьшение величины гиппокампа кореллирует со
снижением интеллектуального уровня, особенно у лиц пожилого и старческого
возраста (Арушанян Э.Б., Бейер Э.В., 2007), хотя данный факт не может служить
специфичным признаком наличия психических расстройств (Коломеец Н.С., 2007). Это
является морфологическим подтверждением взаимосвязи травматической болезни и
деменции (рис. 7).
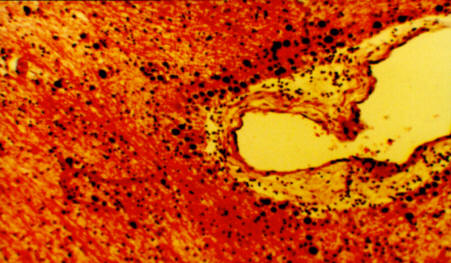
Рис. 7. Криброзность структур, атрофические изменения
вещества головного мозга, дистрофия нейронов у больного, перенесшего ЧМТ.
Морфологические дефекты, выявляемые при нейровизуализационных исследованиях,
подтверждают незавершённость патологических процессов. В оболочках и веществе
мозга прогрессируют нарушения крово- и ликворообращения, приводящие к гипоксии
тканей, частичной атрофии мозгового вещества, нарастающему фиброзу оболочек (Рудас
М.С., Скворцова Т.Ю., 1996). Изменения в отдалённом периоде ЧМТ делятся на
очаговые и диффузные. Очаговые проявляются ограниченными зонами однородного
понижения плотности в коре и в белом веществе мозга без чётких границ, что
свидетельствует о локальном разрежении сосудистой сети, частичной демиелинизации.
Диффузные изменения характеризуются распространённой умеренной атрофией мозга с
незначительным расширением желудочковой системы, субарахноидальных борозд и
щелей (Anderson C.V.,
1995). Тем не менее, эти морфологические находки имеют неспецифический,
смешанный сосудисто-травматический характер, так как могут появляться и в
результате сосудистых, воспалительных поражений, АГ, ИБС, особенно у пожилых
пациентов (Попова Э.Н., 2001; Прохоров А.А. и др., 2002; Егорова И.Ф., Серов
Р.А., 2004). Поэтому, оценивая морфологическую картину головного мозга в
отдалённом периоде ЧМТ, необходимо учитывать анамнестические данные (Труфанова
Г.Е., Фокина В.А., 2007).
Исходя из сказанного, представляется очевидным наличие тесной взаимосвязи
между травматическими и сосудистыми патологическими процессами в центральной
нервной системе. Тем не менее, недостаточно изучен характер такого
взаимодействия в определенных конкретных ситуациях, одной из которых нам
представляется, например, восстановительный период ишемического инсульта у лиц,
в анамнезе которых присутствовала легкая ЧМТ.
На основании многолетнего динамического наблюдения за таким специфическим
контингентом, как участники войн и вооруженных конфликтов, мы предлагаем общую
поэтапную концепцию клинико-патогенетической модели многолетнего развития
сочетанной сердечно-сосудистой патологии, обусловленной атеросклерозом, у лиц,
перенесших боевые черепно-мозговые травмы.
I этап. Период ведения боевых действий. Получение боевой ЧМТ в
условиях стресса боевой обстановки.
В ответ на травматическое повреждение вне зависимости от характера и тяжести
травмы и рода травматического воздействия развивается билатеральный спазм
сосудов – вазоконстрикция, приводящая к повышению скоростных показателей на фоне
гиперперфузии (Коновалов A.M. и др., 1994; Одинак М.М. и др., 1996; Гайдар Б.В.,
Парфенов В.Е., 1997). Нарушения ликвородинамики и внутричерепная гипертензия с
нарушениями венозного оттока усугубляют сосудистые нарушения. Изменение
деятельности неспецифических, вегетативных, регулирующих образований
способствуют срыву компенсации не только церебральной, но и общей гемодинамики -
расстройствам сосудистого тонуса, сердечной деятельности, развитию ранней АГ,
нарушений сердечного ритма и проводимости, ишемизации не только головного мозга,
но и миокарда (Ерюхин И.А., 1994; Емельянов А.Ю., 1995). Замыкается «порочный
круг» полисиндромной, полиорганной, в первую очередь, кардиоцеребральной
патологии.
Возникшая в результате травмы, боевого стресса и связанных с ними сосудистых
расстройств дисфункция гипоталамо-гипофизарно-надпочечниковой системы приводит к
усиленному выделению нейромедиаторов, в первую очередь, серотонина, и это
является триггером ускоренной дисфункции эндотелия и предиктором раннего
развития сердечно-сосудистой патологии, атеросклероза, чему также способствуют
реактивно-воспалительные и аутоиммунные изменения.
Как известно, саногенетическими механизмами, которые обеспечивают
приспособительный эффект и эффект восстановления нарушенных функций, личного и
социального статуса больных, являются реституция (процесс восстановления
деятельности поврежденных структур), регенерация (структурно-функциональное
восстановление целостности поврежденных тканей и органов вследствие роста и
размножения специфических элементов), компенсация (замещение и/или возмещение
утраченных функций) и иммунитет (Белова А.Н., Щепетова О.Н., 2002;
Umphred D.A.,
1990). Но, для полного осуществления саногенеза через названные механизмы
необходимо проведение адекватных лечебно-восстановительных мероприятий
непосредственно с момента травмы. В случаях получения боевой травмы в годы
Великой Отечественной войны ни один из саногенетических механизмов в данных
конкретных условиях не мог реализоваться в полной мере вследствие длительности
войны, необходимости быстрого возвращения в строй при отсутствии адекватных
реабилитационных мероприятий. Таким образом, саногенез в 100% случаев явился
незавершенным при любом характере и тяжести травмы, в отличие от данных
литературы (Мякотных В.С., 1994; Одинак М.М., 1995), где процессы полной
компенсации отмечаются у 30-45% больных, участников уже современных войн.
Жалобы больных на первом этапе имеют преимущественно церебральный
травматический характер.
II этап. Ранний посттравматический период. Клинический дебют
сосудистого процесса.
Нарушения мозгового кровотока, возникшие во время травмы мозга, затягиваются
и прогрессируют. Незавершенность саногенетических процессов приводит к ранней
клинической манифестации сосудистых заболеваний с истощением приспособительных
механизмов и дезадаптацией функционального состояния не только головного мозга,
но и всего организма. Тем не менее, у больного сохраняется уверенность в том,
что все его патологические симптомы связаны исключительно с военными действиями
и полученными там травмами; при этом пациентом не принимаются во внимание и даже
отклоняются иные возможные причины головных болей, головокружений, снижения
памяти и прочих субъективных клинических проявлений, свойственных начальной
цереброваскулярной патологии; даже стабильно повышенные цифры АД не заставляют
больного изменить свое отношение к причине его страданий. Это связано с
определенными социальными и психологическими факторами, такими, как статус
ветерана войны, группа инвалидности, связанная с фронтовыми ранениями, «ореолом
героя». Возможно, данные социальные факторы дополнительно усугубляют непрерывно прогредиентное течение патологического процесса и позднюю обращаемость больных.
Только значимое изменение привычного характера церебральных жалоб и/или развитие
сердечно-болевого синдрома вызывают необходимость обращения к врачу, лечение и
обследование с акцентом на патологию сердца и сосудов.
III этап. Первый поздний посттравматический период. Развитие
процесса старения со свойственной ему множественной сочетанной патологией при
накоплении клинических признаков многих заболеваний.
Возрастные изменения усугубляют течение травматической болезни мозга и, в
особенности, сердечно-сосудистой патологии, «запущенной» травмой и
патогенетически связанной с атеросклерозом, который, с увеличением возраста
пациента, в процессе старения проходит процесс постепенного прогрессирования по
стадиям и степеням при изменении характера жалоб и клинической картины,
характерной для каждой новой стадии и степени выраженности атеросклеротического
процесса.
Присоединившаяся и прогрессирующая сопутствующая возрастзависимая патология,
в частности, хронические заболевания легких, желудочно-кишечного тракта,
опорно-двигательного аппарата, онкологические заболевания, определяет развитие
синдрома взаимного отягощения, обусловленного описанной полиморбидностью.
Уже нарушенные механизмы регуляции церебральной и общей гемодинамики и
гемодинамические сосудистые нарушения в целом усугубляются еще более, что
сопровождается повышением скоростных показателей мозгового кровотока при
значительном снижении реактивности сосудистой стенки и приводит к выраженным
нарушениям перфузии вещества головного мозга и развитию ишемических повреждений.
Присоединяются не характерные для травмы, но облигатные для развития
атеросклеротического процесса нарушения липидного обмена и нарастание процессов
ПОЛ. Процессы ПОЛ, поражая эритроциты, приводят к их гипоксии и усилению
сладж-феномена, редукции части капилляров и тромбообразованию, а это, в свою
очередь, способствует дальнейшему прогрессированию эндотелиальной дисфункции.
Клинически на первый план вновь выступают цереброваскулярные расстройства (до
79,41%), которые становятся определяющими в жалобах пациентов вне зависимости от
клинического дебюта сосудистого процесса. При этом частота предъявляемых
больными цереброваскулярных жалоб не коррелирует с тяжестью состояния, данными
лабораторных, инструментальных исследований и причинами возможных летальных
исходов: смерть от ИБС составляет 67,11%; от ИИ - 32,89%.
IV этап. Второй поздний посттравматический период. Быстрое
прогрессирование процесса старения, мультифокального атеросклероза,
полиморбидности.
Стремительно прогрессируют клинические проявления хронической ишемии мозга,
развиваются когнитивные нарушения при выраженном и быстром усугублении
психопатологический симптоматики до степени деменции. Множественность и
атипичность жалоб больного и объективных клинических проявлений полинозологии,
нарастающая диссоциация субъективных и объективных проявлений комбинированной
патологии создают предпосылки для извращенного восприятия пациентом клинических
характеристик своего заболевания. Больной описывает имеющиеся у него более
простые, «элементарные» расстройства, никак не выделяя основу своих жалоб, а
создавая из них многофакторную смесь, лишенную всяких логических связей.
Одновременно происходит истощение компенсаторных возможностей организма,
подтверждаемое рассогласованностью механизмов адаптации гемодинамики в целом и
выраженными патологическими сдвигами в системе ПОЛ/АОА. Тем не менее,
лабораторные и инструментальные показатели по прежнему носят неспецифический
характер.
V этап. Финальный период полинозологии. Отсутствие отчетливых
клинических признаков травматической болезни головного мозга при наличии
прогрессирующей полиорганной недостаточности.
Лабораторные и инструментальные показатели в финальных стадиях
патологического процесса приобретают черты специфичности и позволяют
предположить преобладание определенной сосудистой или несосудистой патологии,
которая может явиться непосредственной причиной смерти.
6.2. Некоторые клинические особенности восстановительного периода
ишемического инсульта у лиц, перенесших легкую черепно–мозговую травму
В этом разделе в краткой форме представлены результаты исследований,
проведенных в гериатрической клинике Уральской государственной медицинской
академии на базе Свердловского областного клинического психоневрологического
госпиталя для ветеранов войн. Основная направленность исследований – изучение
особенностей восстановительного периода ишемического инсульта у лиц, перенесших
легкие ЧМТ. Полученные результаты подтвердили наши предположения о существовании
определенных различий в течении восстановительного периода ишемического инсульта
у пациентов перенесших и не перенесших ЧМТ в прошлом.
Наиболее частой (80 – 90%) жалобой больных, перенесших ишемический инсульт,
вне зависимости от наличия или отсутствия ЧМТ в анамнезе, является головная
боль. Головные боли имеют смешанный механизм развития, сочетая в себе головные
боли напряжения, сосудистые цефалгии и боли, связанные с нарушением
ликвородинамики. Выделить какой–либо преобладающий характер головной боли в
зависимости от нозологий и их сочетаний не удается, и в этом плане наличие или
отсутствие предшествующей ишемическому инсульту ЧМТ не имеет значения. То же
самое можно сказать и о мнестических нарушениях, встречающихся почти также
часто, как и головные боли. Но преобладание нарушения кратковременной памяти как
при наличии, так и при отсутствии в прошлом ЧМТ что может свидетельствовать в
пользу наличия достаточно выраженных сосудистых расстройств, сопутствующих ЧМТ и
ее последствиям, что подтверждает сказанное выше.
Отчетливые различия в зависимости от наличия или отсутствия ЧМТ в анамнезе
наблюдаются в отношении выраженности и тяжести двигательных расстройств,
практически облигатно связанных с перенесенным инсультом. У больных, перенесших
в самые разные сроки до инсульта легкую ЧМТ, в подавляющем большинстве случаев
отсутствуют наиболее грубые плегические расстройства, тогда как среди пациентов
с неотягощенным травмой мозга анамнезом их частота достигает 50%, и при этом
выраженные двигательные нарушения регрессируют достаточно медленно. Также у
больных с мозговой травмой в прошлом отсутствуют такого рода функциональные
нарушения, как выраженные оптические и вестибуло–атактические, хотя топика
ишемического церебрального очага указывает на высокую вероятность их
присутствия. Подобного рода несоответствие степени выраженности функциональных
нарушений, связанных с инсультом, подтверждается и с помощью шкалы Бартела и не
зависит от степени выраженности морфологического повреждения головного мозга,
определяемого с помощью нейровизуализационных методов. Не исключено, что данный
феномен может объясняться так называемой перекрестной резистентностью, которая
основана на мобилизующих защитные, компенсаторные возможности головного мозга
последствиях ЧМТ, «подготовившей» мозг к защите от любой, в последнем случае
сосудистой, катастрофы (Мякотных В.С. и др., 1995, 1996, 2006). Данное
предположение подтверждается и большей выраженностью депрессивных расстройств у
больных, перенесших только ишемический инсульт, тогда как у травматиков
мотивации к восстановлению оказываются выше.
В значительной степени выше, приблизительно в 2 раза, вероятность
возникновения так называемой симптоматической эпилепсии, формирующейся после
перенесенного инсульта, именно в случаях перенесенной в прошлом ЧМТ, пусть даже
самой легкой. В целом эпилептический процесс у таких больных клинически
протекает более тяжело, с преобладанием судорожных генерализованных
эпилептических припадков, тогда как припадки, обусловленные исключительно
сосудистым церебральным поражением, являются преимущественно парциальными и не
вызывают особого беспокойства как со стороны пациента, так и в плане проведения
соответствующего противоэпилептического лечения.
При проведении нейровизуализационных томографических исследований головного
мозга в случаях присутствия ЧМТ в анамнезе у больных, перенесших ишемические
инсульты, очень часто обнаруживаются небольшие арахноидальные и
интрацеребральные кисты, локализующиеся в различных отделах мозга, рубцово–спаечные,
атрофические изменения, во всех случаях выявляется наружная и внутренняя
заместительная гидроцефалия. У больных, перенесших только ишемический инсульт и
не имеющих указаний на ЧМТ в анамнезе, обнаруживаются исключительно ишемического
характера нейровизуализационные изменения, только по истечение полугода и более
после инсульта они могут сочетаться с «находками», по своему характеру
напоминающими посттравматические, что иногда заставляет задуматься о
перенесенной, но не диагностированной в прошлом ЧМТ.
При проведении исследований биоэлектрической активности головного мозга не
выявляется каких–либо отчетливых различий между ЭЭГ пациентов, имевших или не
имевших указания на ЧМТ в анамнезе. Последнее может свидетельствовать о том, что
характер биоэлектрической активности определяется преимущественно происшедшей
недавно сосудистой катастрофой, и при этом отчетливо пароксизмальные изменения,
характерные для травматической болезни головного мозга, отступают на второй план
и не верифицируются с помощью ЭЭГ. Данное обстоятельство ставит под сомнение
возможности исследования биоэлектрической активности в диагностических целях у
пациентов в восстановительном периоде ишемического инсульта, особенно в плане
поиска отчетливых вариантов изменений данной биоэлектрической активности,
характерных для травматической болезни мозга или даже эпилепсии.
Таким образом, восстановительный период ишемического инсульта у лиц,
перенесших в прошлом легкую ЧМТ, имеет свои, достаточно отчетливые особенности.
Не следует подобного рода больных рассматривать как потенциально более тяжелых,
нежели лица, не имевшие в прошлом ЧМТ. К этим пациентам следует относиться как к
достаточно перспективным в плане восстановления нарушенных в результате инсульта
функций, но с несколько большей вероятностью возникновения эпилептического
характера осложнений. Что касается психических расстройств, то они
представляются скорее сосудистыми, нежели посттравматическими, чего, разумеется,
нельзя сказать о лицах, перенесших в прошлом тяжелые травмы головного мозга с
развитием у них в дальнейшем выраженного психоорганического синдрома,
обусловленного травмой.

