Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Глава 4. КЛИНИКА И ДИНАМИКА ОТДАЛЕННОГО ПЕРИОДА БОЕВОЙ
ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЫ И ПОСЛЕДСТВИЙ ХРОНИЧЕСКОГО ПСИХОЭМОЦИОНАЛЬНОГО СТРЕССА
На основании изложенного в предыдущих главах представляется достаточно
очевидным, что последствия боевой ЧМТ и ХПЭС боевой обстановки, с одной стороны,
являются разными по патогенезу и клиническим проявлениям патологическими
состояниями, с другой, при наличии факта боевого ранения, повреждения головного
мозга эти две патологии практически всегда пересекаются между собой, дополняют
друг друга и создают в определенном смысле единое патологическое состояние. В
данной главе, как и в последующих, на основании наших собственных наблюдений мы
стараемся представить те новые, на наш взгляд, сведения, которые помогли бы
уточнить ряд клинических и патогенетических аспектов рассматриваемой сочетанной
патологии. В связи с этим была поставлена задача проведения сравнительного
анализа клинического течения посттравматической церебральной патологии в
зависимости от характера повреждающего фактора (боевая ЧМТ, ХПЭС, бытовая ЧМТ) и
длительности посттравматического периода.
Наблюдались 197 больных - бывших участников боевых действий в Афганистане в
период 1979-1989 гг. Все больные были разделены на 2 группы. 1-ю составили 132
человека с боевой ЧМТ, подтвержденной документально, 2-ю - 65 больных, в
анамнезе которых отсутствовали указания на перенесенную боевую ЧМТ, но которые,
тем не менее, после воздействия боевого ХПЭС лечились по поводу патологии
центральной нервной системы. Средний возраст больных обеих групп составил
34,25±0,38 лет, срок после возвращения из Афганистана - 12,8±0,35 лет. Группа
сравнения была представлена 50 больными (мужчинами), перенесшими бытовую ЧМТ, и
сопоставимыми с основной группой по возрасту и длительности посттравматического
периода. Критериями исключения из групп наблюдений явились: хроническая
алкогольная зависимость 2-й стадии и выше; наркомании; шизофрения;
злокачественные новообразования или операции по поводу этой патологии в
анамнезе; демиелинизирующие заболевания; для больных с последствиями ХПЭС –
наличие ЧМТ после возвращения из зоны боевых действий.
ЧМТ у всех больных были только закрытыми, легкими и, согласно Единой
Международной классификации ЧМТ (Коновалов А.Н. с соавт., 1985, 1987, 1988;
Самотокин Б.А. с соавт., 1987; Волошин П.В., Шогам И.И., 1990; Штульман Д.Р.,
1999), были представлены сотрясениями головного мозга и ушибами головного мозга
легкой степени тяжести, что удалось уточнить как анамнестически, так и на
основании имевшейся военно-медицинской документации.
Клиническое обследование всех больных проводилось в рамках представленного
исследования дважды: первое - через 4 - 15 лет после перенесенной ЧМТ и выхода
из условий боевой обстановки, и второе – через 10 - 20 лет после перенесенной
травмы и стресса, т.е. в динамике отдаленного периода травматической болезни
головного мозга.
4.1. Особенности неврологической симптоматики и ее динамики
в отдаленном периоде ЧМТ и последствий ХПЭС
Основные жалобы больных на момент первичного обследования, через 4 - 15 лет
после ЧМТ и ХПЭС и их динамика по периодам развития травматической болезни
головного мозга 1 –2, 4 – 15, 10 – 20 лет после ЧМТ или ХПЭС) с учетом
анамнестических сведений представлены в таблицах 4.1 и 4.2.
Таблица 4.1. Основные жалобы больных в отдаленном периоде
ЧМТ и ХПЭС
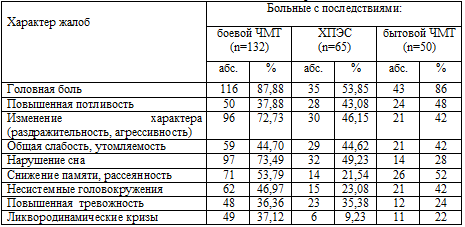
Таблица 4.2. Динамика жалоб по периодам: 1-2, 4-15, 10-20
лет после травмы, ХПЭС
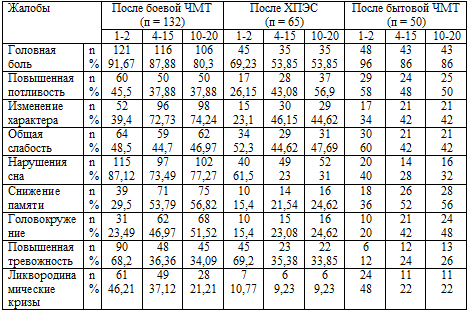
Наиболее частой жалобой, независимо от характера повреждающего фактора, была
головная боль, и об этом наиважнейшем субъективном проявлении, на наш взгляд,
следует поговорить отдельно.
4.1.1. Головные боли
Головные боли, встречающиеся у ветеранов современных боевых действий,
перенесших ЧМТ, ХПЭС, и страдающих целым рядом других заболеваний и последствий
травм, имеют целый ряд особенностей, которые редко наблюдаются у больных иных
контингентов, но весьма характерны для бывших воинов (Мякотных В.С., 1994).
С практической точки зрения, по мнению В. Н. Штока (1987), представляется
необходимым и достаточным называть головной болью любое болезненное ощущение в
области головы. Автор считает, что головная боль является единственным или
ведущим симптомом по меньшей мере при 45 болезнях. По данным N.Н. Raskin, О.
Appenzeller (1980), свыше 60% лиц, страдающих головной болью, находятся в
трудоспособном возрасте. При сопоставлении указанных данных и их применении к
достаточно молодому по календарному возрасту контингенту бывших участников
боевых действий в Афганистане и Чеченской республике, страдающих, как правило,
несколькими заболеваниями, становится понятной высочайшая распространенность
головной боли среди этих пациентов. За более чем 25-летний период наблюдения мы
практически не встречали бывшего «афганца» или «чеченца», который бы не
жаловался на головную боль. Именно поэтому, как с точки зрения патогенетического
принципа классификации клинических разновидностей головной боли, так и в силу
того, что единичное, или единственное заболевание у бывшего «афганца» или
«чеченца» встречается редко, речь идет о полиорганной, полисистемной,
организменной, биосоциальной патологии у этих лиц. Выделить же отдельные
нозологические единицы, выставить несколько правильных диагнозов у одного и того
же больного будет в определенной степени тем проще, чем «более тщательно и
кратко будут описаны определены разные типы и клинические формы головной боли» (Dalessio
О.J., 1981). В то же время В.Н. Шток (1987) указывает на то, что у больных с
разными нозологическими формами механизм головной боли может быть одинаковым, и
патогенетическое лечение головной боли также может быть идентичным. В то же
время автор считает, что только в некоторых случаях мы имеем дело с комбинацией
патогенетических механизмов головной боли, и тогда к четырем основным типам
головной боли (сосудистая, мышечного напряжения, ликвородинамическая,
невралгическая) добавляется и пятый - головная боль смешанного рода.
Еще в монографии 1994 года (Мякотных В.С., 1994) приводились клинические
примеры головных болей, которые можно было расценить в качестве предвестников
эпилептических припадков, дебютировавших в дальнейшем. Подобного рода феномены
наблюдаются нередко. Более того, подобного рода головные боли могут
расцениваться в качестве составной части или даже эквивалента эпилептических
пароксизмов с их последующим переходом в постприпадочное состояние, сон.
Подобное предположение подтверждается фактами облегчения таких головных болей не
только на фоне приема аналъгетиков, но и противоэпилептических средств.
Указанные головные боли, вероятно, можно даже обозначить как эпилептиформные.
Больные эпилепсией с подобного рода клиническими проявлениями, как показал наш
опыт, прогностически неблагоприятны. у них нередко выявляются лобные и височные
эпилептические очаги, быстро нарастают психические расстройства, неуклонно
прогрессирует болезненный процесс, приводящий к тяжелой инвалидизации.
Так называемые психалгии мы очень часто наблюдали у больных с невротическими,
пограничными состояниями, особенно при переходе в фазу невротической депрессии,
во время которой дисфункция центральной антиноцицептивной системы является
ведущей в происхождении головной боли. Такую головную боль, в отличие даже от
головной боли, протекающей по типу эпилептического эквивалента, которую иногда
представляется возможным объективизировать с помощью ЭЭГ, совершенно не удается
объективизировать никакими методиками. Тем не менее, подобного рода головная
боль все же имеет, на наш взгляд, физиологическую основу, но, как считает Б.Д.
Карвасарский (1969, 1980), семиологические особенности такой головной боли
обусловливает главенствующий эмоциональный, а не сенсорный компонент. Головные
боли данного типа не бывают мучительными для больного, хотя возможно их
приступообразное усиление на непродолжительное время. Больные становятся
активными в беседе с врачом и в стремлении возможно более полно рассказать ему о
своих болезненных ощущениях. При сочетании же с головными болями, возникающими в
результате других патофизиологических механизмов, у врача может даже возникнуть
подозрение в агравации, симуляции, особенно если больной социально не устроен,
если идет речь об определении или же усилении группы инвалидности и т. д. Ни в
коем случае нельзя при этом ни словом, ни жестом показывать больному свои
сомнения в правдивости его повествования. В условиях субъективно неразрешимой
психотравмирующей ситуации, на фоне которой формируется синдром невротической
депрессии, это может привести к усилению клинических проявлений последнего.
Необходимость осторожного обращения с больным как личностью понимают и самые
близкие его родственники.
Как уже говорилось, частота и выраженность патологических проявлений, в том
числе и головной боли, в отдаленном периоде ЧМТ не имеет четкой коррелятивной
связи с тяжестью травмы, о каковой мы к тому же можем в подавляющем большинстве
случаев судить лишь анамнестически. Значительную роль в происхождении и развитии
посттравматических головных болей, их выраженности, частоте приступов играют не
только преморбидные особенности личности ряда больных, которые очень легко
переносят острый период травмы, а поэтому не соблюдают обычно предписываемого
режима и лечения (Самотокин Б.А., 1978; Gurdjian Е.S.,
Webster J.Е., 1958, и др.), но и известный феномен боевой экзальтации (Шпиленя
Л.С., 1987), который также способствовал позднему обращению больных за
медицинской помощью, нарушениям в режиме лечения. В дальнейшем даже у больных,
которые, казалось бы, легко перенесли острый период травмы, наступают столь
выраженные морфофункциональные нарушения, что их клинические проявления, в
частности головные боли, превосходят по интенсивности подобные улиц с более
тяжелыми травмами головы. Трудно согласиться с ранее известным мнением Н.G. Wolf
(1963) о том, что посттравматические головные боли обусловлены в основном
мышечным напряжением, которое можно объективизировать с помощью электромиографии
(ЭМГ). Речь идет скоре лишь о патофизиологическом компоненте головной боли
сочетанного, или комбинированного, типа. В отношении бывших воинов «афганцев»
или «чеченцев» можно предположить преобладание сосудистых, либо
ликвородинамических нарушений в происхождении головных болей, а затем уже
феномена мышечного напряжения, который нередко расценивается как синоним
психалгий. Опять же при этом следует помнить о полипатологии, о сочетании
различных нозологических форм у одного и того же больного и различных
этиопатогенетических механизмах их возникновения и развития. Недаром же,
например, N.Н. Raskin, О. Appenzeller (1980) изменения на ЭЭГ, подтверждавшие
нарушения нейродинамики после легкой ЧМТ, выявляли у 55% больных, а по нашим
даннам таковые выявляются практически в 100%. Симптомы вегетативно-сосудистой
дистонии той или иной степени выpaженности определяются также почти у всех
пациентов, перенесших ЧМТ. Пароксизмальность болезненных проявлений, в частности
головных болей, их фенотипическая неоднородность даже в течение суток не
позволяет говорить только о мышечном происхождении болей. Ликвородинамические
нарушения, приводящие к возникновению головных болей, также не являются чем-то
изолированным. Внутричерепное давление зависит и от внутричерепного
кровенаполнения (Шток В.Н., 1987, 1975). Увеличение кровенаполнения
внутричерепных сосудов при снижении их тонуса и затруднении венозного оттока,
локальная церебральная дисциркуляция с вазогенным отеком мозга повышают тканевое
и внутричерепное давление. Вместе с тем процессы, повышающие локальное тканевое
давление, нарушают микроциркуляцию и сосудистую ауторегуляцию (Шток В.Н., 1987).
У ветеранов современных боевых действий, как уже указывалось, имеет место
сочетание многих видов патологии. В плане воздействия на головной мозг эта
патология является не только следствием прямых воздействий на него и его
оболочки фактора травмы. Это еще и факторы общей хронической интоксикации,
аутоинтоксикации, инфекционно-аллергической отягощенности, что приводит к
изменениям иммунного статуса, гомеостаза в целом. Можно предположить поэтому,
что решающую роль в генезе гипертензии, повышения внутричерепного давления в
резидуальном периоде травмы играют не только нарушения ликвороциркуляции и
резорбции, но и нарушения транспорта ионов в жидких средах головного мозга, его
отек и набухание.
Преобладание сочетанного, комбинированного характера головной боли с
различными патофизиологическими механизмами ее возникновения проявляется и в
нетипичности клинической картины ряда симптомов, сопутствующих выраженной
головной боли. Например, у многих наших больных головная боль возникала или
резко усиливалась в вертикальном положении, при попытках движения головой. Часто
можно было увидеть больного, мучающегося головной болью и лежащего с опущенной
по отношению к краю кровати головой, что напоминало симптом «опущенной головы»,
описанный С.Г. Зограбяном (1965). Подобного рода объективные факторы,
сопровождающие головную боль, характерны для ликворной гипотензии (Шток В.Н.,
1987). Тем не менее, по нашим данным, у такого рода больных при проведении им
люмбальной пункции очень часто выявляется высокое ликворное давление, а сама
пункция облегчает состояние больного. Медикаментозное лечение, кроме того,
бывает эффективным при назначении сочетания дегидратирующих, сосудорасширяющих и
седативно-релаксирующих препаратов. Все это свидетельствует о сочетанном
характере головной боли, об участии различных патофизиологических механизмов в
ее возникновении и развитии, хотя клиническая картина, поведение больного в
период приступа могут симулировать совершенно иной генез болевого синдрома.
Нарушения ликвородинамики, ведущие к головным болям, могут быть связаны и с
развитием так называемого посттравматического церебрального арахноидита, хотя
взгляды на правомочность подобного диагноза в течение времени меняются от
значительной частоты до полного неприятия. Этиология арахноидита как
самостоятельной нозологической единицы примерно в 30% связана с бывшей ЧМТ (Пиль
Б.Н., 1977; Маджидов Н.М., 1978). По определению Н.М. Маджидова (1972, 1978),
арахноидит представляет собой хронический продуктивный процесс в паутинной
оболочке головного мозга, в который вовлекаются мягкая оболочка, эпендима и
субэпендимальный слой желудочков, сосудистые сплетения. В.С. Лобзин (1983)
считает, что в развитии арахноидита большую роль играют неспецифические
аутоиммунные и аутоаллергические реакции вовлекаемых в процесс структур. В
результате развивается уплотнение оболочек, их фиброз (аналогично, например,
глиозу мозговой ткани), что в конечном счете приводит к той или иной степени
выраженности кистозно-спаечного или кистозно-слипчивого процесса. Вероятно, у
ветеранов войн подобный механизм возникновения и развития данной патологии
встречается даже чаще, нежели у других групп населения, так как дисбаланс
аутоиммунных и аутоаллергических реакций входит в конечном счете в понятие
иммунопатологического синдрома, столь характерного для лиц, прошедших Афганистан
или другие «горячие точки» за пределами России или даже Советского Союза (Коломоец
Н.М. и др., 1992). Но в то же время нельзя не согласиться с мнением В.А. Карлова
(1990) о том, что церебральный арахноидит как самостоятельный нозологический
феномен встречается крайне редко. Речь скорее идет о лептоменингите, даже о
лептоменингоэнцефалите, так как изолированное воспалительное поражение только
паутинной оболочки представить себе трудно, как и трудно увидеть кистозный
процесс в паутинной, мягкой мозговых оболочках и т. д. в сочетании с абсолютно
неповрежденным веществом головного мозга, особенно на уровне коры и желудочковой
системы.
Фиброз мозговых оболочек, на наш взгляд; всегда сопровождается глиозом с
развитием в атрофический процесс прилежащих слоев мозгового вещества. Отсюда - и
желудочковая гидроцефалия, и признаки атрофии коры головного мозга, выявляемые
при нейровизуализационных обследованиях больных с так называемым церебральным
арахноидитом. И если головные боли, сочетающиеся с несистематизированными
головокружениями, другими вестибулярными расстройствами, тошнотой, нарушениями
сна, можно связать преимущественно с оболочечной патологией, ведущей к
ликвородинамическому дисбалансу, то очаговые неврологические симптомы
определяются как локализацией оболочечных поражений, так и вторичным страданием
(раздражение, сдавление, атрофия, гипоксия) непосредственно мозговых структур.
Именно дислокационные и гипоксические механизмы частичного, но нестойкого
выключения тех или иных церебральных структур могут объяснить в какой-то мере
ремиттирующий характер неврологической симптоматики на фоне относительно
постоянной головной боли сочетанного генеза.
Особо следует сказать о так называемой вертеброгенной головной боли, очень
часто встречающейся среди бывших участников современных войн. Можно было бы
связать подобного рода головную боль с наличием шейного остеохондроза, что и
отмечают многочисленные авторы (Осна А.И., 1973; Попелянский Я Ю., 1981, 1983,
1986; Шток В.Н., 1987 и др.). И.В. Давыдовский (1966), R.У. Jeffreys (1980) и
другие исследователи считают наиболее патогномоничным обнаружение признаков
шейного остеохондроза, артроза, деформирующего спондилеза у лиц старше 50, и
особенно 65 лет - до 75%. В наших же наблюдениях среди лиц, перенесших ЧМТ в
результате минно-взрывного поражения, признаки шейного остеохондроза встречаются
уже в совсем молодом возрасте не менее, чем у 25-30% обследованных. По
классификации А.И. Осна (1973), включающей четыре стадии остеохондроза, примерно
у половины больных с выявленным поражением шейного отдела позвоночника имеет
место уже 2-я стадия, сопровождающаяся нарушением фиксирующей способности
фиброзного кольца, ведущей к нестабильности шейного отдела позвоночника. Чаще
поражается нижняя половина шейного отдела позвоночника, хотя не так уж редки
признаки деформирующего артроза в атланто-аксиальном и атланто-окципитальном
соединениях, унковертебрального артроза С2 - С3 и т.д. Указанная верхнешейная
локализация поражения имеет наибольшее значение в генезе цервико-краниальных
болей, так как на протяжении от 2-го шейного позвонка до атланта позвоночная
артерия заключена между фасцией нижней косой мышцы головы и капсулой
атланто-аксиального сочленения и не отгорожена костными образованиями. Большой
затылочный нерв начинается от 2-го межпозвонкового ганглия, лежащего на
передневнутренней поверхности нижней косой мышцы головы, огибает эту мышцу и
оказывается включенным в ее фасциальное влагалище (Попелянский Я.Ю., 1981; Шток
В.Н., 1987). Толчком к возникновению цервико-краниальных болей, по мнению В.Н.
Штока (1987), является раздражение синувертебрального нерва с последующим
рефлекторным напряжением мышц или рефлекторной регионарной ангиодистонией,
ирритативно-компрессионное воздействие на корешки и сплетение позвоночной
артерии или комбинация этих факторов. Вертеброгенная головная боль мышечного
напряжения усиливается при сотрясении головы и шеи, что отличает ее от мышечной
же боли при неврозе, например. Возникает вопрос - почему у бывших участников
боевых действий уже в возрасте 25-30 лет имеют место признаки остеохондроза
шейного отдела позвоночника, и эти лица страдают, кроме всего прочего,
вертеброrенными головными болями? На наш взгляд, да и согласно данным,
представленным в военно-медицинской литературе, минно-взрывная травма является,
по сути дела, политравмой. Естественно, что и при боевой ЧМТ не может во всех
случаях сохраниться совершенно не пораженным шейный отдел позвоночника, не
возникнуть повреждения мышц головы, сосудов кранио-цервикальных отделов, самого
вещества спинного мозга.
Конечно, хотелось бы разобраться в том какую роль в происхождении именно
головных болей играет сама боевая ЧМТ, а какую – сопутствующий ХПЭС боевой
обстановки. Мы попытались в какой-то степени решить данную задачу с помощью
сравнительного анализа феномена головной боли у представителей наблюдавшихся
нами групп больных.
Больных с последствиями ЧМТ головная боль беспокоила достоверно чаще (р<0,05),
чем перенесших ХПЭС. В процессе длительного наблюдения за больными мы убедились
в том, что первично посттравматические цефалгии в отдаленном периоде ЧМТ имеют
уже смешанный механизм развития, сочетая в себе головные боли напряжения,
сосудистые цефалгии и боли, связанные с нарушением ликвородинамики.
Несмотря на проведение регулярного лечения, головная боль практически не
покидала больных; они, по их собственному выражению, «приспособились жить с
головной болью», научились самостоятельно купировать кризовые состояния.
Последние возникали у представителей всех групп, но характер кризов был
различным. У 49 (37,12%) из 132 больных 1-й группы (перенесли боевую ЧМТ) они
представлялись гипертензионными, ликвородинамическими, а у 9 (6,82%) человек – с
яркой вегетативной окраской, клинически и электроэнцефалографически связанной с
дисфункцией преимущественно лимбических структур головного мозга. При этом
головные боли были кратковременными (несколько минут), но очень выраженными,
внезапно возникали и столь же внезапно прекращались. Подобные головные боли,
сопровождавшиеся ауральными пароксизмальными проявлениями височного
эпилептического пароксизма, описаны в литературе, например, А.И. Болдыревым
(1984), В.С. Мякотных (1994), но они же в значительной степени клинически
напоминают пучковые, кластерные головные боли. У 55 (41,67%) больных с
последствиями боевой ЧМТ в течение 5-9 лет наблюдения цефалгии приобрели
клинически отчетливый сосудистый характер, не сопровождались рвотой, не
беспокоили в утренние часы. Боли, ранее локализованные в височной и лобной
областях, переместились в затылочную, теменную, появился шум и звон в голове,
ушах.
У большинства больных 2-й группы (48 из 65, т.е. 73,85%), перенесших
только ХПЭС, превалировала головная боль мышечного напряжения, однако у 6
(9,23%) человек в процессе длительного наблюдения зарегистрированы типичные
ликвородинамические кризы, что также подтверждалось развитием внутричерепной
гипертензии, данными МРТ исследования головного мозга. Мы связываем эти
изменения с вероятно имевшей место у этих больных родовой травмой, возможные
последствия которой не были учтены при призыве на службу в Армию. ХПЭС мог
вызвать декомпенсацию последствий указанной родовой травмы, которая ранее ничем
себя не проявляла. У 11 (16,92%) представителей 2-й группы головные боли к
моменту катамнестического исследования носили стойкий сосудистый характер.
У представителей группы сравнения, перенесших только бытовую ЧМТ, кризы
головных болей носили ликвородинамический характер у 11 (22%), и характер
пучковых, с выраженным вегетативным компонентом – у 6 (12%). Клиническая
трансформация посттравматических цефалгий в отчетливые сосудистые также в
течение последних 5-9 лет наблюдалась у 11 (20,75%) больных.
Таким образом, головные боли в отдаленном периоде травматической болезни
мозга приобретают смешанный характер независимо от вида травматического
воздействия, однако достоверно (р<0,05) чаще и быстрее трансформация головной
боли в сосудистую происходит у больных с боевой ЧМТ в анамнезе, нежели у больных
перенесших бытовую ЧМТ и ХПЭС. Вероятно, наличие ХПЭС в качестве фона
возникновения ЧМТ способствует ускоренному развитию сосудистой патологии
головного мозга, что подтверждают исследования В.С. Мякотных (1994), Т.А.
Боровковой (1999), В.В. Ямпольской (2007) и др.
4.1.2. Вегетативные расстройства
Те или иные варианты вегетативных нарушений наблюдаются в течение жизни у
подавляющего большинства людей. По данным эпидемиологических исследований до 80%
популяции испытывают те или иные вегетативные нарушения. Это обусловлено
ключевой ролью вегетативной нервной системы в таких основных процессах, как
поддержание гомеостаза и адаптация к меняющимся условиям среды. События и
ситуация как биологического, так и психосоциального характера могут приводить к
срыву вегетативной регуляции, что клинически проявляется в виде вегетативной
дисфункции или синдрома вегетативной дистонии. Совершенно неправильным, на наш
взгляд, является мнение о том, что с возрастом вегетативно-дистонические
проявления становятся не столь выраженными, как у молодых, а общее число
пациентов, страдающих нейроциркуляторной или вегетативно-сосудистой дистонией,
резко падает. Нам кажется, наоборот, число больных с дистоническими,
вегетативно-сосудистыми патологическими проявлениями в пожилом и старческом
возрасте нарастает, но данная патология переходит из разряда нозологии или
синдромологии в преимущественно симптоматические аспекты. На первое место в
качестве самостоятельного заболевания или синдрома выходят различные клинические
варианты атеросклероза, артериальной гипертензии, патологические процессы в
желудочно-кишечном тракте, мочевыделительной, эндокринной системах,
остеохондроз, наконец. Все эти заболевания клинически могут быть представлены
вегетативно-дистоническими расстройствами, но данные расстройства воспринимаются
уже не как синдромы, не как самостоятельные заболевания, а как один, два и более
симптома более тяжелых патологических процессов (Мякотных В.С., 1995). В связи с
этим вегетативные нарушения, наблюдаемые у ветеранов современных вооруженных
конфликтов, только на ранних этапах их возникновения и развития можно в
определенной степени связать с последствиями бывшей боевой ЧМТ, особенно при
сочетании последней с ХПЭС боевой обстановки, при развитии ПТСР. В дальнейшем,
через 5-10 и более лет, при присоединении целого комплекса соматической
патологии, что очень часто наблюдается у наблюдаемого нами контингента больных,
те или иные вегетативные расстройства не проходят, а лишь меняют свою
клиническую окраску, полисимптомность. При этом рамки клинической картины
вегетативных нарушений как бы расширяются, данные нарушения сочетаются с
расстройствами сна, с вестибулярными и постуральными симптомами, с психическими
расстройствами, и при этом очень трудно бывает отдифференцировать известные
классические варианты так называемой вегетативной, или вегетативно-сосудистой
дистонии от иных неврологических, соматических, психопатологических проявлений.
При наличии у бывших участников вооруженных конфликтов различных видов
патологии, очень тесно переплетенных между собой и патогенетически
взаимосвязанных у каждого конкретного больного, невозможно было бы игнорировать
участие вегетативного звена нервной системы в формировании сложных
патологических процессов. Как указывают А.М. Вейн с соавт. (1981), назначение
вегетативной нервной системы рассматривается в двух аспектах: первый -
поддержание постоянства внутренней среды организма (гомеостаза); второй -
обеспечение вегетативной нервной системой различных форм психической и
физической деятельности. «В период напряженной деятельности, опасности,
спортивного соревнования,- пишут авторы,- необходима существенная мобилизация
энергетических ресурсов кардиоваскулярной, дыхательной и других систем. В этих
случаях для обеспечения осуществляемой деятельности менее жесткие
гомеостатические показатели далеко отклоняются от своего уровня в состоянии
покоя. Расстройства вегетативного обеспечения (недостаточность или избыточность)
нарушают поведение человека. Таким образом, и нестойкий гомеостаз, и
недостаточность вегетативного обеспечения прежде всего отражаются на основном
проявлении жизнедеятельности человека - его адекватном, приспособительном,
целостном поведении». Приведенная цитата, на наш взгляд, полностью отражает
общие механизмы вегетативных реакций у воинов, прошедших Афганистан, Чечню или
другие «горячие точки». Причем как в период ведения ими боевых действий, так и
спустя значительное время после демобилизации. У ветеранов современных боевых
действий существует несколько основных факторов, «фундаментальных вариантов
патологии» для возникновения синдрома вегетативно-сосудистой дистонии. Основные
из них: органические поражения головного мозга; неврозы, неврозоподобные
состояния и пограничная нервно-психическая патология; патология сегментарной
вегетативной нервной системы, чаще связанная с вертеброгенными расстройствами на
фоне остеохондроза позвоночника; заболевания внутренних органов, имеющих богатую
вегетативную иннервацию; аллергии, являющиеся в определенной степени составной
частью приобретенного, скажем, в Афганистане иммунопатологического синдрома (Коломоец
Н.М. с соавт., 1992). В приведенном списке отсутствует конституциональная
природа возникновения синдрома вегетативно-сосудистой дистонии, эндокринная
перестройка организма и первичные заболевания периферических эндокринных желез.
Указанные три фактора нехарактерны для группы больных ветеранов афганской или
чеченской войн. Определенное исключение можно сделать, пожалуй, лишь в отношении
последнего фактора – заболеваний эндокринных желез. Но при этом в подавляющем
большинстве случаев поражения периферических эндокринных желез вторичны и
связаны с патологией центральной нервной системы, о чем имеются указания в
литературе (Простакова Т.И., 1978).
Как известно, вегетативные нарушения классически подразделяются на
перманентные, пароксизмальные и сочетанные перманентно-пароксизмальные
расстройства; симпатические, парасимпатические, амфотропные перманентные
нарушения; симпатико-адреналовые, вагоинсулярные и смешанные кризы;
генерализованные, системные, локальные синдромы; расстройства при патологии
сегментарных и надсегментарных вегетативных систем (Вейн А.М. с соавт., 1981).
Для каждой группы факторов, вызывающих синдром вегетативно-сосудистой дистонии,
можно выделить наиболее типичные варианты встречающихся при этом вегетативных
расстройств. При этом у лиц, участвовавших в боевых действиях на территории
Афганистана, например, они имеют свои особенности, во многом связанные как с
полифакторностью этиопатогенетических моментов вегетативно-сосудистой дистонии,
так и с характером травм, стрессовых воздействий, соматических заболеваний,
приобретенных в Афганистане и в период адаптации к мирной жизни в последующем.
То же самое можно сказать и о роли других особенностей других географических и
этнических регионов, в которых проходили боевые действия с участием наших войск.
Наиболее частой основой для возникновения синдрома вегетативно-сосудистой
дистонии у бывших «афганцев» или «чеченцев», на наш взгляд, является сочетание
органических поражений головного мозга, соматической патологии, неврозоподобных
расстройств. Отсюда - выраженный полиморфизм вегетативных нарушений. Но подобное
возможно, например, и при изолированном церебрально-органическом поражении, при
изолированно невротическом страдании, при только соматической патологии. Разные
уровни поражения головного мозга (каудальные отделы ствола, мезэнцефальные
структуры), различные варианты неврозов, патология отдельных внутренних органов
могут способствовать возникновению «своих», именно для них характерных вариантов
вегетативных нарушений. Но на практике редко встречается только одно,
изолированное, строго локальное органическое церебральное поражение, один,
мономорфный вариант невроза или поражение одного внутреннего органа, никак не
связанное с функций других органов и систем. Полиморфизм вегетативных
расстройств предопределен уже хотя бы этим. Но если мы имеем дело с
полиорганностью, полисистемностью организменной патологии, что часто наблюдается
у ветеранов Афганистана (Мякотных В.С. с соавт., 1993; Мякотных В.С., 1994), то
полиморфизм вегетативно-сосудистых расстройств должен еще более нарастать.
Подобное и отмечается у наших больных, хотя в каждом конкретном случае все же
можно выделить преобладающий клинический вариант вегетативных нарушений. Вариант
этот, правда, обычно нестоек и непостоянен, как нестойка и неврологическая
симптоматика, непостоянны и клинически нестабильны неврозоподобные и пограничные
нервно-психические расстройства, нейро- и психосоматические взаимоотношения и
т.д. Говорить о каком-то определенном варианте вегетативно-сосудистых нарушений
у таких больных можно лишь в рамках ограниченного периода времени. А период этот
может измеряться как минутами, так и, значительно реже, месяцами. Характерна как
бы суммация, но с различной выраженностью отдельных слагаемых, многочисленных
вариантов вегетативно-сосудистой патологии у каждого больного. Разнообразные
вегетативные тесты (Даньини - Ашнера, Даниелополу, Превеля и др.) могут давать
самые различные результаты в течение часов, суток при повторных исследованиях.
Преобладание парасимпатического тонуса может очень быстро и резко смениться на
преобладание симпатического, редкие пароксизмальные вегетативно-сосудистые
нарушения переходят в длительную и стойкую фазу перманентных расстройств,
особенно в рамках психовегетативного синдрома, основанного чаще всего на тесной
связи дисфункций вегетативной и эмоциональной сфер.
У ветеранов современных войн синдром вегетативно-сосудистой дисфункции, как
правило, не выступает в качестве единственного патологического синдрома при
органическом поражении головного мозга. Отмечается частое его сочетание с
другими, более или менее клинически выраженными проявлениями, касающимися
корковых, подкорковых, мозжечковых и других синдромов. Невротические,
неврозоподобные состояния, а тем более пограничные нервно-психические
расстройства отнюдь не ограничиваются симптомами вегетативно-сосудистой дистонии,
хотя последние в том или ином варианте являются практически облигатными при
данной патологии, особенно на фоне наличия выраженных астенических проявлений.
Как уже указывалось (Мякотных В.С., 1994), у бывших «афганцев» развитие
эпилептических синдромов, эпилепсии локализационно связано с поражением и
вовлечением в эпилептическую систему височных, лимбических структур. Частое
присутствие вегетативного компонента (эпигастрально-абдоминального,
кардиоваскулярного, недифференцированного общевегетативного) в эпилептических
пароксизмах в сочетании с предвестниками эпилептического пароксизма, имеющими
нередко психовегетативную окраску, может направить врачебную мысль по пути
диагностики либо неэпилептических пароксизмальных состояний, либо так называемой
диэнцефальной эпилепсии. Но последняя либо является височной эпилепсией с
вовлечением в эпилептический процесс диэнцефальных, гипоталамических
образований, либо представляет собой развернутые церебральные
вегетативно-сосудистые кризы (Вейн А. М., Карлов В. А., 1980; Карлов В. А.,
1990; Мякотных В.С., 1993, 1994). И в том, и в другом случае важно суметь
дифференцировать эпилептические от неэпилептических пароксизмов, так как от
этого будет зависеть вся дальнейшая тактика лечения, ведения больного.
Приведем пример.
Больной Б., 1969 г. рожд. Проходил срочную воинскую службу в Афганистане в
1987-1989 гг. В сентябре 1988 г. получил минно-взрывную травму, лечился два
месяца в медсанбате по поводу контузии головного мозга. В декабре 1988 г.
перенес повторную контузию в результате взрыва реактивного снаряда на расстоянии
четырех метров от пострадавшего. В течение нескольких суток находился без
сознания. Очнулся в госпитале г. Ташкента, в котором лечился около 3-х месяцев.
С этого времени отмечает почти постоянные головные боли, раздражительность,
вспыльчивость, а с 1989 г. - периодические кратковременные подъемы АД до 210/120
мм рт. ст. Тогда же появились приступы головокружения, ощущения стягивания мышц
лица, онемения рук и ног в этот период, сердцебиения, резкой потливости,
«темнеет в глазах, кажется, что вот-вот потеряю сознание». Подобного рода кризы
всегда сопровождаются повышениями АД, но его показатели бывают различными. С
1993 г. отмечаются эпизоды сноговорения, при этом будит жену, узнает ее,
понимает, где находится, но уверен, что все это происходит во сне. Кроме того,
возникают кратковременные «выпадения сознания» в дневное время, когда больной
почти не понимает обращенной к нему речи. Назвать частоту различных описанных
эпизодов затрудняется. Со слов больного, в 1994 г. после психотравмирующей
ситуации изменилась походка, стал пошатываться при ходьбе, появились трудности
при попытках следить глазами за движущимися предметами, при этом «начинает
дергаться голова».
В 1988 г., также в Афганистане, перенес болезнь Боткина. Преморбидно, до
призыва на военную службу был спокойным, общительным, занимался спортом, любил
детей.
Об-но: АД = 110/70 мм рт. ст., ЧСС = 72 в 1 мин. В легких умеренно
ослабленное везикулярное дыхание. живот при пальпации мягкий, болезненный в
точках Боаса, Макензи. Положительный симптом Алиева. Печень - у края реберной
дуги, чувствительная при пальпации.
Неврологически: положительный симптом Гуревича - Манна, болезненность верхних
точек выхода ветвей тройничного нерва при пальпации. Угнетены корнеальные
рефлексы. Опущен левый угол рта. Легко снижена мышечная сила в левых
конечностях. При ходьбе широко расставляет ноги, ходит пошатываясь. В позе
Ромберга атаксия, грубые промахивания при попытках выполнения координаторных
проб с 2-х сторон. При крайних отведениях глазных яблок нистагмоидных
подергиваний нет, но при этом 2-3 раза отчетливо дергает головой (по типу
синкинезий) в сторону поворота глаз. Чувствительных нарушений нет. Сухожильные и
периостальные pефлексы с верхних конечностей, ахилловы рефлексы живые,
симметричные; коленные отсутствуют. Выраженная вегетативная лабильность, все
вегетативные тесты - с отклонениями от нормы. Раздражителен, но сдерживает себя.
Речь громкая, говорит пренебрежительно-ироничным тоном. Внимание неустойчиво.
Память снижена на текущие события. Мышление инертное, обстоятельное.
Галлюцинаций, бреда, качественных расстройств мышления нет. Критически оценивает
свое состояние.
На глазном дне - нисходящая первичная атрофия зрительных нервов обоих глаз.
ЛОР: двусторонний кохлеарный неврит, глухота на левое ухо. На краниограммах -
признаки внутричерепной гипертензии.
ЭЭГ: диффузно-дизритмические изменения, более выраженные в передних отделах
мозга. При биполярной записи выявляется склонность к пароксизмальным состояниям
(групповые и единичные пики, острые волны) с очаговостью в правой задневисочной
области.
ЭКГ: синусовая аритмия при ЧСС = 76 за 1 мин. очаговые нарушения
внутрижелудочковой проводимости, правограмма (позиционные сдвиги).
Патологических изменений в анализах крови, мочи не выявляется.
Из приведенного примера очевидно, что у больного с повторными боевыми ЧМТ в
анамнезе, хроническим постботкинским гепатитом, хроническим холециститом
развивается синдром вегетативно-сосудистой дистонии с преобладанием
пароксизмальных расстройств по типу преимущественно симпато-адреналовых кризов.
В дальнейшем присоединяются пароксизмальные височно-эпилептические проявления,
что свидетельствует о вовлечении структур лимбико-ретикулярного комплекса в
патологический процесс. Нарастание психических расстройств приводит к
формированию психоорганического синдрома, эксплозивного варианта, с истероидной
манерой поведения, реагирования. Вегетативно-сосудистая дистония, таким образом,
превалируя клинически в начале заболевания, на сегодняшний день заявляет о себе
лишь в качестве одной из составляющих тяжелого полиорганного и полисистемного
поражения.
Наблюдение подтверждает довольно частую встречаемость вегетативных нарушений
у больных с височной эпилепсией (Вейн А.М. с соавт., 1981; Бова В.Е., 1985;
Шершевер А.С., 2005), но в то же время сочетание пароксизмальных
вегетативно-сосудистых и эпилептических проявлений, по нашим данным, довольно
редкое явление (Мякотных В.С., 1990, 1992, 1993, 1994). У бывших участников
современных войн, в особенности афганской, подобные сочетания встречаются чаще;
вероятно, в этом играет роль сочетание органической церебральной патологии и
соматических заболеваний. При сравнении клинико-анамнестических данных,
полученных при исследовании больных с первыми эпилептическими и
неэпилептическими, в частности вегетативно-сосудистыми, пароксизмами, выявлены
существенные различия (Мякотных В.С., 1990, 1994). Неэпилептические пароксизмы
обычно более продолжительны, нежели эпилептические, им чаще сопутствуют головные
боли, головокружения, колебания АД, функционально-невротические проявления. У
больных с неэпилептическими пароксизмами чаще, чем с эпилептическими, выявляется
соматическая патология, в том числе сердечно-сосудистая, и семейная
предрасположенность к обморокам, невротическим реакциям. Подавляющее большинство
неэпилептических пароксизмов, в отличие от эпилептических, возникают в ответ на
провоцирующие факторы, но характер последних существенно отличается от характера
провокаций эпилептических припадков. Для большинства больных с эпилептическими
пароксизмами характерны полная внезапность возникновения приступов, их связь с
периодом сна, яркая выраженность судорожного или психомоторного компонентов,
серии и статусы, неврологическая симптоматика, гипертензионные изменения на
краниограммах, отчетливые психические расстройства эпилептического типа. Надо
сказать, что ряд последних дифференциально-диагностических критериев, таких, как
отсутствие неврологической симптоматики, гипертензионных изменений на
краниограммах, не может быть безоговорочно применим по отношению к бывшим
«афганцам» или «чеченцам». Подобные же затруднения возникают и в отношении
частого отсутствия у больных с эпилептическими припадками соматической
патологии, в частности сердечно-сосудистой, которая, наоборот, довольно часто
встречается среди ветеранов Афганистана, реже - Чечни.
У рассматриваемого нами контингента больных не совсем обычными и привычными
являются проявления вегетативно-сосудистой дистонии на фоне неврозов. Согласно
данным А.М. Вейна с соавт. (1981), при неврозах имеется яркая перманентная и
пароксизмальная дисфункция, носящая либо полисистемный, либо преимущественно
моносистемный характер. Ведущими при этом являются симпатико-адреналовые
проявления. Возможно, при наличии невроза. так сказать, в «чистом виде» дело бы
обстояло именно так. Но здесь мы вновь возвращаемся к проблеме полипатологии,
полиорганного и полисистемного поражений, столь характерных для ветеранов
современных войн. При этом в первую очередь утрачивается моносимптомность
клинической картины вегетативно-сосудистой дисфункции. При наличии нескольких
вариантов «фоновой» патологии даже начальная, манифестная стадия каждого
вегетативно-сосудистого пароксизма у одно го и того же больного может каждый раз
протекать по разному. Иногда криз начинается с головной боли, иногда - с
неприятных эпигастрально-абдоминальных ощущений, иногда - с парестезий, ощущений
онемения дистальных отделов конечностей и т.д. Но представим при этом, что
данный невротизированный больной страдает органической церебральной патологией,
хронической патологией желудочно-кишечного тракта и так называемым синдромом
«минной стопы», включающим периферическую сосудистую и полиневритическую
симптоматику. Становится совершенно ясным механизм полисистемности как самих
вегетативно-сосудистых пароксизмов, так и возможностей их «запуска» из любой
точки, вовлеченной в патологический организменный процесс Проблематична при этом
и ведущая роль в клинической картине вегетативно-сосудистых дистоний при
неврозоподобных состояниях именно симпатико-адреналиновых проявлений. Дело в
том, что для подавляющего большинства больных - бывших «афганцев» или «чеченцев»
характерна, наоборот, брадикардия, указывающая на преобладание тонуса
вагоинсулярной системы. Именно на фоне брадикардии возникают нередко наблюдаемые
пароксизмы в проводящей системе сердца при проведении больным компьютерной
чрезпищеводной электрокардиостимуляции (ЧПЭКС). Далеко не единичны положительные
пробы Геринга, свидетельствующие о дисфункции, гиперсенситивности
сино-каротидной зоны, являющейся также представительством системы блуждающего
нерва. .Для большинства наблюдаемых нами ветеранов характерны яркий красный
дермографизм, потливость, внезапные «приливы» крови к лицу. Нередки приступы
удушья с затрудненным вдохом, что часто расценивается терапевтами как проявление
«хронического бронхита курильщика». Далеко не единичны жалобы больных на
учащенное мочеиспускание, по поводу чего они обращаются к урологу и лечатся с
диагнозом «неврогенного мочевого пузыря», а иногда и последствий якобы
перенесенного простатита. Характерна, особенно для ветеранов Афганистана,
повышенная сонливость в дневные часы. У многих больных на ЭКГ регистрируется
подъем выше изолинии сегмента S- Т, выраженное увеличение
амплитуды зубца Т, что может приводить к диагностическим ошибкам.
Таким образом, проявления вегетативно-сосудистой дистонии, в частности
перманентные, у наших больных с неврозоподобными состояниями носят по большей
части вагоинсулярный, парасимпатический характер. При возникновении же на этом
фоне вегетативно-сосудистых пароксизмов нередко на несколько минут - часов
достаточно ярко проявляются симпатико-адреналовые клинические симптомы. Но об их
ведущей роли, подавляющем преобладании на фоне перманентно существующих
парасимпатических проявлений судить трудно. Действительно, учащение сердечных
сокращений до 80-90 за 1 мин при исходном фоне ЧСС = 52-56 за 1 мин субъективно,
очень неприятно для больного, особенно астенизированного, невротизированного, с
ипохондрическими, фобическими расстройствами. Но такие учащения пульса логичней
было бы расценивать как тенденцию к установлению равновесия между
парасимпатическим и симпатическим звеньями вегетативной нервной системы, пусть
даже слегка сдвинутого в сторону последнего. То же можно сказать и о других
клинических симптомах пароксизмального звучания. В целом же создается
впечатление о том, что при наличии у больных полиорганной, полисистемной
патологии, сочетающейся нередко с неврозоподобными, пограничными
нервно-психическими расстройствами, клинические проявления
вегетативно-сосудистой дисфункции также носят полисистемный характер с
преобладанием парасимпатической, вагоинсулярной симптоматики.
Большинство синдромов, описанных при поражениях сегментарной вегетативной
нервной системы, не встречается среди бывших воинов. Совершенно нехарактерны
синдромы поражения вегетативных узлов в области лица (Сладера, Шарлена);
практически не встречались ганглиониты, трунциты, связанные с поражением
симпатической цепочки. Всего у нескольких больных нам пришлось наблюдать явления
солярита, который развивался после множественных проникающих ранений живота с
последующими неоднократными хирургическими вмешательствами. Возникавшие спаечные
процессы скорее всего и приводили к клиническим проявлениям солярита.
Клиническая картина солярита на фоне спаечной болезни органов брюшной полости
практически соответствовала описанной в многочисленных литературных источниках.
Определенные особенности представляли личностные реакции больного на пароксизмы
болей. Приступы солярита всегда сопровождаются яркими эмоциональными
проявлениями, но у ветеранов Афганистана, которые страдали ими, они выливались в
тяжелые дисфории, депрессивные состояния, в том числе и с суицидальными
тенденциями, высказываниями о никчемности и ненужности дальнейшего
существования.
Очень трудно судить о возникновении у ряда больных вегетативно-сосудистых
кризов в связи с наличием шейного остеохондроза и вовлечением в процесс
вегетативных сплетений позвоночной артерии. Речь может идти в отдельных редких
случаях, вероятно, только о пусковом механизме. Действительно, нам приходилось
наблюдать пароксизмы типа шейной мигрени, например, но это было только началом
развернутого вегетативно-сосудистого криза, в развитии которого принимали
участие и соответствующие звенья, связанные с органической церебральной
патологией, соматическими заболеваниями, неврозоподобными и пограничными
нервно-психическими расстройствами. Патология вегетативных сплетений позвоночной
артерии при этом являлась, скорее всего, лишь «спусковым крючком», триггером, а
в дальнейшем криз развивался по законам его сочетанной этиологии с
полисимптомным характером клинических проявлений.
Нередко у бывших участников боевых действий встречается синдром так
называемой «шейной стенокардии», стеноскапулии. Клинические его проявления
достаточно типичны и характеризуются болями в левой половине грудной клетки, в
области верхушки сердца, в области угла левой лопатки. Иногда боли иррадиируют в
левую руку, всю лопатку, левую половину лица, головы, в область левого
сосцевидного отростка, создавая иллюзию болей в ухе, из-за чего больные иногда
обращаются к ЛОР специалистам. Боли различны по длительности, но чаще всего
продолжаются от 30-40 минут до нескольких часов, носят колющий, реже давящий
характер, возникая обычно в утренние часы, особенно после сна в неудобной позе.
Усиление болей, возникновение типичной их локализации, иррадиации может
провоцироваться резкими движениями головой, а также пальпацией паравертебральных
точек шейного отдела позвоночника, особенно слева на уровне нижних позвонков.
Считается, что подобного рода синдром «шейной стенокардии» характерен для лиц
среднего и старшего возрастов и может сочетаться с истинной коронарной
недостаточностью. Мы не наблюдали подобного сочетания даже у бывших «афганцев»,
имеющих признаки наличия у них ишемической болезни сердца, перенесших инфаркт
миокарда. У этих лиц типичные стенокардические, ангинозные пароксизмы могли
сосуществовать с обычными корешковыми, болевыми проявлениями шейного
остеохондроза, но клинической картины «шейной стенокардии» при этом не
наблюдалось. Зато лица старших возрастных групп, ветераны Великой Отечественной
войны нередко жаловались на подобного рода пароксизмы, которые клинически как бы
дополняли имевшуюся у них стенокардию.
Согласно данным Е.Н. Лексина (1973), А.И. Арутюнова (1978) и др., ведущее
место в формировании резидуального патологического симптомокомплекса при ЧМТ
принадлежит надсегментарной вегетативной дисфункции, ядром которой выступают
регуляторные нарушения в сердечно-сосудистой системе. Существенное влияние на
характер и степень выраженности этих расстройств оказывает факт получения травмы
в условиях ХПЭС. Эти отправные пункты послужили для многих исследователей ключом
для выявления прямых связей между травматической болезнью головного мозга и
нарушениями деятельности сердечно-сосудистой системы. Проблемой занимались в
нашей стране А.Л. Мясников, Б.П. Кушелевский, Т.Г. Ренева, К.Л. Бобкова, В.В.
Громова и многие другие терапевты, кардиологи, патофизиологи. Были выделены
характерные клинические особенности так называемой постконтузионной гипертонии.
Общеизвестно положение о раннем развитии атеросклероза у больных, перенесших ЧМТ.
О значительной роли сердечно-сосудистых нарушений в структуре
посттравматического nсиховегетативного синдрома пишут А.А. Шутов, М.А. Шерман
(1992, 1994), М.А. Шерман (2003), которые обследовали ветеранов афганской войны.
Нам же кажется, что многие сердечно-сосудистые расстройства в условиях
применения современных видов вооружений, взрывчатых веществ, вызывающих не
только и не столько закрытые ЧМТ, сколько закрытое полиорганное поражение, в том
числе сердца, сосудов, связаны как с поражением головного мозга, так и с прямым
травмированием сердца, аорты и других крупных сосудов. При этом относительная
«легкость» закрытой ЧМТ может соседствовать с тяжелыми травмами сердца и
сосудов, иногда маскируя последние. В связи с этим о сердечно-сосудистых
нарушениях только в рамках психовегетативного синдрома следует говорить
осторожно, не умаляя роли возможного прямого травмирования жизненно важных
органов грудной и брюшной полостей
Лишь в единичных наблюдениях довольно редко у ветеранов современных войн
наблюдались обмороки, хотя последние и считаются одним из проявлений
психовегетативного синдрома. Даже в ходе проведения пробы Геринга, позволяющей
выявить гиперсенситивность сино-каротидной зоны, дело никогда не до ходило до
полной потери сознания, хотя проба производилась достаточно «жестко», при этом
отмечались выраженная брадикардия, падение АД. Ряд наших больных жаловался на
то, что в течение вегетативно-сосудистого пароксизма они испытывали ощущения
«наступающей потери сознания», но все же сознание оставалось сохраненным.
Возможно, отсутствие ярких синкопальных состояний у наших больных связано с тем,
что у них достаточно редко в структуре психовегетативного синдрома выявлялись
истерические стигмы, элементы астенической депрессии со склонностью к яркой
демонстративности. Не исключено, что с течением времени через несколько лет
обмороки станут достаточно частыми элементами вегетативно-сосудистой дисфункции
у бывших «афганцев» или «чеченцев», так как А.М. Вейн с соавт. (1981, 1994)
считают, что психовегетативный синдром предшествует возникновению обмороков.
Значительно чаще, по сравнению с классическими обмороками, среди наших
пациентов отмечались так называемые предобмороки, т.е. ощущения приближающегося
обморока, которому не суждено развернуться. Данные ощущения обозначаются
термином «липотимия», длятся от нескольких секунд до 2 минут, проявляются
чувством дурноты, тошноты, общего дискомфорта, холодным потом, головокружением,
неясностью зрения, мышечной слабостью, шумом в ушах и ощущением уходящего
сознания. У ряда больных при этом появляются страх, тревога, сердцебиение,
ощущение нехватки воздуха, парестезии, «ком в горле», т.е. в принципе некоторые
симптомы панической атаки, на описании которой хотелось бы остановиться
подробней.
Панические атаки - наиболее драматичное проявление синдрома вегетативной
дистонии (Вейн А.М. с соавт., 1994). Предложено множество терминов,
обозначающих, по всей видимости, идентичные состояния: диэнцефальные кризы,
церебральные вегетативные припадки, гипервентиляционные приступы, тревожные
атаки и т.д. Только с 1980 г., с появлением Американской классификации
психических болезней - DSM–III, затем DSM-IV
в международной практике для обозначения пароксизмальных состояний с
полисистемными вегетативными, эмоциональными и когнитивными расстройствами
утвердился термин «паническая атака». Данные состояния были включены в более
широкий класс «тревожных состояний». Сегодня основными критериями для выделения
панических атак являются повторяемость приступов и возникновение их вне
чрезвычайных и угрожающих жизни ситуаций. При этом панические атаки проявляются
сочетанием не менее 4 из 13 ниже перечисленных симптомов:
- диспноэ;
- «пульсация», тахикардия;
- боли или ощущения дискомфорта в левой половине грудной клетки;
- чувство удушья;
- головокружение, неустойчивость, ощущение приближающегося обморока;
- чувство дереализации, деперсонализации;
- тошнота или абдоминальный дискомфорт;
- озноб;
- парестезии в руках и ногах;
- ощущение «приливов», «волны» жара или холода;
- потливость;
- страх смерти;
- страх сойти с ума или совершить неконтролируемый поступок.
Отмечено, тем не менее, что у ряда больных в момент приступа не возникает
чувство страха, тревоги («паника без паники», «нестрашные приступы»), у части
больных эмоциональные проявления могут заключаться в чувстве тоски или
подавленности, у других это раздражение, агрессия либо просто внутреннее
напряжение. У большинства пациентов в приступе присутствуют
функционально-невротические симптомы: ком в горле, псевдопарезы, нарушения речи
и голоса, судорожные феномены и т.д. Приступы могут возникать как спонтанно, так
и ситуационно, у части больных они развиваются ночью, в период сна,
сопровождаясь нередко неприятными, тревожными сновидениями. Последние часто
предшествуют развертыванию приступа в момент просыпания, а после окончания
панической атаки полностью или частично амнезируются. При повторении пароксизмов
формируется чувство их тревожного ожидания, а затем и так называемое
избегательное поведение. Последнее в крайнем варианте выступает как
агорафобический синдром (больные становятся полностью дезадаптированными, не
могут одни оставаться дома, передвигаться без сопровождения по улице,
исключается городской транспорт и т.д.). В 30% случаев повторное возникновение
панических атак приводит к возникновению и развитию депрессивного синдрома.
Сплошь и рядом данная ситуация выливается в чувство страха сна, и больные
испытывают при этом мучительную «вынужденную« бессонницу. Нередки истерические и
ипохондрические расстройства.
Пока мы не наблюдали у ветеранов Афганистана или чеченских событий отчетливо
выраженного симптомокомплекса Рейно, относящегося к вегетативным
ангиотрофоневрозам, «вегетативной полиневропатии». У больных с так называемым
синдромом «минной стопы» клинические проявления были очень незначительными, и их
сосудистый компонент укладывался скорее в клиническую картину начинающегося
облитерирующего процесса сосудов нижних конечностей, сопровождавшегося
полиневритическими нарушениями. При этом не отмечалось типичной для синдрома
Рейно пароксизмальности болей и вегетативной симптоматики. Редко встречался так
называемый каузалгический синдром, который сопровождался болями в стопах и
голенях симпаталгического характера, потливостью ног, мраморностью окраски кожи
дистальных отделов, ломкостью ногтей. Скорее всего, подобного рода каузалгии
были связаны с вторичными сосудисто-гипоксическими и одновременно
травматическими поражениями большеберцового нерва, о чем свидетельствовали
результаты ЭНМГ и РВГ обследований нижних конечностей. Отмечено усиление болей в
ответ на психоэмоциональные нагрузки, невротизацию, алкогольные эксцессы.
Вследствие этого каузалгический синдром можно в определенной степени считать
вариантом известного психовегетативного синдрома. Это тем более очевидно, что
сами каузалгии провоцируют негативные эмоционально-невротические реакции с
выраженной вегетативной окраской, которые в качестве «следа» обострения
каузалгического синдрома могут продолжаться в течение нескольких суток.
Возникает система «порочного круга».
У ветеранов Афганистана или Чечни мы практически не наблюдали
нейро-эндокринно-обменного варианта так называемого гипоталамического синдрома,
не отмечалось ни нарушений жирового обмена по типу синдрома Иценко - Кушинга, ни
несахарного мочеизнурения, ни иных более или менее характерных для этой формы
гипоталамического синдрома сдвигов. Конечно, участие гипоталамической зоны в
возникновении и развитии вегетативно-сосудистых расстройств у бывших участников
войн не вызывает сомнений, так как имеет место сочетание и травматических, и
соматогенных, и вторично-нейроинфекционных, и невротических воздействий на этот
легко ранимый участок мозга. Широкие связи гипоталамуса с другими отделами
головного мозга, с корой височных и лобных долей предполагают его участие в
формировании психовегетативного синдрома. Но вот последний имеет свои
особенности у рассматриваемого нами контингента больных. Как уже было сказано,
это в первую очередь нашло отражение в характеристиках вегетативных нарушений
при неврозоподобных состояниях, которые отличались от классических вегетативных
сдвигов, наблюдаемых при неврозах. Даже у лиц с тревожно-депрессивными
симптомами, для которых считается характерным преобладание симпатических
вегетативных сдвигов, такового не наблюдалось. Парасимпатические, ваготонические
изменения все же оставались ведущими. Истерические синдромы, особенно их яркие
клинические варианты, довольно редко отмечались среди ветеранов Афганистана в
отдаленном от демобилизации периоде. Но при этом превалировали симпатические
пароксизмальные вегетативно-сосудистые расстройства, отчетливо связанные с
отрицательными эмоциональными стимулами. Личностные расстройства, в частности
пограничные, формирование которых зависит от множества причин, без сомнений
играют свою роль в развитии клинических проявлений психовегетативного синдрома.
Но особенности эмоциональной сферы, высшей нервной деятельности, манеры
реагирования нередко в сочетании с формированием пагубных пристрастий к
алкоголю, наркотикам, седативным средствам зачастую занимают ведущие позиции в
клинической картине неврозоподобных, пограничных нервно-психических нарушений у
ветеранов современных войн, отодвигая подчас далеко на задний план и делая
совершенно незаметными проявления вегетативно-сосудистой дисфункции. Происходит
как бы подавление гипоталамических нарушений корковыми в общем процессе
формирования психовегетативного синдрома. При этом ведущим, ярким, заметным
становится психопатологическое его звено, сопровождающееся поведенческими
расстройствами, а вегетативное отодвигается на задний план либо самостоятельно,
либо с помощью алкоголя, наркотических средств и т.д. Нередко поэтому именно при
купировании депрессивных, эксплозивных, аффективных, тревожно-ипохондрических
проявлений мы вдруг получаем от больного целый комплекс жалоб и объективных
проявлений вегетативного характера, чего ранее не отмечалось. Подобная «смена
декораций» особенно характерна для наиболее соматически отягощенных больных в
сочетании с эмоционально-волевой неустойчивостью различного происхождения. При
этом мы в состоянии проследить у пограничного больного очень быстрое развитие
типичной клинической картины так называемого гипоталамического синдрома, в
частности его вегетативно-сосудистого варианта. Патогенетически не исключается
смена так называемой детерминирующей станции отправления (Крыжановский Г.Н.,
1980) в масштабе лимбико-ретикулярного комплекса и общей интегративной
деятельности нервной системы.
Также, как в ситуации с головными болями, нам показалось интересным
определить сравнительную зависимость некоторых вегетативных расстройств,
наблюдающихся у бывших участников боевых действий в Афганистане и Чеченской
республике, от фактов получения ими боевой или бытовой ЧМТ или же переживания
исключительно ХПЭС боевой обстановки.
Оказалось, что повышенная потливость, с усиления которой нередко и
дебютировала развернутая паническая атака, одинаково часто встречалась у больных
с ЧМТ в анамнезе, независимо от условий получения травмы. Но динамики данного
симптома в отношении частоты его встречаемости в отдаленном периоде травмы не
происходило. У больных же, переживших боевой ХПЭС, но не получавших ЧМТ, частота
проявлений гипергидроза впоследствии увеличилась до аналогичной частоты больных
с ЧМТ. Возможно, это связано с хронически нарастающей дисфункцией
надсегментарного звена вегетативной нервной системы, усиления в динамике ее
симпатического тонуса.
Диссомнические расстройства являлись самой частой жалобой после головной
боли, но значительно и достоверно (р<0,05) чаще встречались среди пациентов,
перенесших боевую ЧМТ в условиях ХПЭС (таблица 3.1), чем среди лиц, либо не
имевших боевой ЧМТ в анамнезе, либо перенесших только бытовую травму. Обращает
на себя внимание тот факт, что расстройства сна в виде нарушения засыпания,
поверхностного малоэффективного сна, а также различных парасомний - сноговорений,
стереотипных кошмарных сновидений, связанных с пережитой боевой обстановкой,
даже по истечении длительного срока после психотравмирующей ситуации, имеют
место у половины бывших участников современных вооруженных конфликтов независимо
от наличия или отсутствия у них ЧМТ. К моменту повторных исследований, через 10
– 20 лет после выхода из зоны боевых действий на расстройства сна жаловались 102
(77,27%) больных 1-й группы, 34 больных (52,31%) 2-й группы и 16 (32%) человек,
перенесших бытовую ЧМТ, из группы сравнения Это свидетельствует о слабой
тенденции (р>0,05) к нарастанию диссомнических расстройств в динамике
отдаленного периода ЧМТ и ХПЭС. При этом почти все из опрошенных участников
боевых действий связывали расстройства сна не только и не столько с мыслями –
воспоминаниями из военного прошлого, которые «приходили» при повторных попытках
заснуть, но и с упоминавшимся выше определенным страхом перед этими мыслями –
воспоминаниями, которые могли спровоцировать развертывание панической атаки той
или иной степени выраженности. Другими словами, такого рода вынужденная
бессонница представляла собой описанный феномен избегания вероятного
вегетативного дискомфорта, если не страдания.
Частота встречаемости таких жалоб, как общая слабость и быстрая утомляемость
при психических и физических нагрузках была выявлена без достоверных различий (р>0,05)
у представителей всех групп. К моменту повторного осмотра подобное сходство
сохранилось: 62 (46,97%) больных 1-й группы, 31 (47,69%) больной – 2-й, 21 (42%)
– группы сравнения. Очень интересной, на наш взгляд, представляется при этом
клиническая картина упомянутой общей слабости и быстрой утомляемости, которая по
существу включала в себя почти облигатно не менее 4-х из названных выше 13
проявлений психо-вегетативного расстройства пароксизмального типа, другими
словами – панической атаки. Чаще всего это были расстройства дыхания, ощущения
сердцебиения и перебоев в работе сердца, гипергидроз и, одновременно, ощущение
сухости во рту с повышенной жаждой, липотимии, тревога, в том числе за
собственную жизнь.
Отчетливыми представляются особенности взаимоотношений тревожности и
раздражительности, даже агрессивности. Повышенная тревожность чаще, но без
достоверных различий (р>0,05) по группам, как при первом, так и при повторном
осмотрах отмечалась у 45 (34,09%) больных 1-й группы, 22 (33,85%) – 2-й, 13
(26%) – группы сравнения. При этом в динамике жалобы на повышенную тревожность у
больных с боевой ЧМТ и после перенесенного ХПЭС достоверно уменьшились (с 62% до
34,09%), в то время как у больных с последствиями бытовой ЧМТ наблюдается
обратная тенденция - увеличение тревожности с 12% до 26% (р<0,05). С другой
стороны, в отдаленном периоде боевой ЧМТ достоверно чаще (р<0,05) больные
жаловались на повышенную раздражительность, агрессивность. При обследовании в
динамике повышенная раздражительность беспокоила 98 (74,24%) больных 1-й группы,
29 (44,62%) – 2-й, 21 (42%) – группы сравнения. Эти показатели соответствуют
исходным данным. Вероятно, это связано с тем, что вышедшие из стадии
«оцепенения» и вошедшие в стадию агрессии и депрессивных проявлений, которая по
описанию американских авторов (Solomon Z.,1988;
Marciniak R.P.,1989)
длится от 2 до 8 лет, участники боевых действий столкнулись с вторичными
стрессами гражданской жизни. Статус меньшинства, относительно низкий
образовательный уровень, неудовлетворительное материальное положение, трудности,
испытываемые на семейном , бытовом и профессиональном уровнях, обусловили
определенное нежелание ветеранов входить в контакт с внешним миром. Это привело
к созданию своеобразных «анклавов» - совместное проживание, «свои» праздники,
традиции, коммерческая деятельность. Подобный вариант адаптации, вероятно,
снижает тревожные тенденции, что нами и отмечено, но на первом плане оказываются
психопатоподобные расстройства, агрессивность, нетерпимость, подозрительность,
эксплозивность. Больные же с последствиями бытовой ЧМТ вынуждены справляться со
своими проблемами «в одиночку», не чувствуя столь мощной социальной поддержки, и
поэтому частота именно тревожно-депрессивных жалоб у них повышена, а факты
раздражительности вплоть до агрессивных выпадов значительно меньше. Интересным
является также следующая особенность агрессивного поведения лиц – участников
боевых действий: как при нарастании раздражения, так и в период выхода из
ситуации раздражения и агрессии типично наличие целого комплекса вегетативных
расстройств – от тахикардии до липотимий и даже дереализационных феноменов, и
именно нарастание указанных вегетативных расстройств при нарастании же ощущений
тревоги, даже страха за собственную жизнь заставляет наших пациентов по мере
возможности прекращать конфликт, «брать себя в руки». При этом ветераны нередко
либо полностью и очень быстро, за минуты, иногда - часы забывают происшедшее,
либо помнят лишь общие моменты, как правило – только стартовую часть конфликта и
агрессии. И именно это воспринимается ими как нарушения, снижение памяти. Но с
другой стороны, снижение памяти без достоверных различий по группам отмечены у
больных с последствиями боевой и бытовой ЧМТ, но достоверно (t=10;
Р<0,001) чаще, чем у больных, перенесших только ХПЭС. При повторном
обследованиях выявлена слабая тенденция (р>0,05) к нарастанию числа больных с
мнестическими расстройствами во всех группах наблюдения: в 1-й – 75 (56,82%)
больных, во 2-й - 16 (24,62%), в группе сравнения - 28 (56%). Возможно, это
происходит вследствие нарастания корковых и внутренних атрофий головного мозга,
диффузного аксонального повреждения и стойкого нарушения таламо-кортикальных
связей, запущенных травмой головного мозга.
Головокружения очень редко наблюдались у наших пациентов в качестве одного,
не сочетаемого ни с какими другими симптома. Обычно головокружение являлось
одной из составляющих сложного симптомокомплекса вегетативных нарушений.
Возможно, именно поэтому, при отсутствии отчетливого локального морфологического
дефекта головного мозга крайне редкими были проявления системного
головокружения. А вот на головокружения несистемного характера через 4 - 15 лет
после травматического воздействия больные после перенесенной ЧМТ жаловались в 2
раза чаще, нежели перенесшие только ХПЭС (р<0,01). Число больных с жалобами на
головокружения не изменилась в динамике ни в одной из групп. Однако, частота
эпизодов головокружения наросла, что может быть связано с нарастанием
хронических расстройств кровообращения в вертебрально-базилярном сосудистом
бассейне, а данные расстройства кровообращения могли быть «запущены» травмой или
хроническим стрессом.
4.1.3. Эпилептические припадки
В подавляющем большинстве случаев эпилептические припадки, дебютировавшие
после ЧМТ, принято считать симптоматическими, а в случае дальнейшего развития
патологического процесса по известным законам эпилептогенеза сформировавшееся
вновь заболевание обозначать в качестве так называемой симптоматической,
посттравматической эпилепсии. С учетом полученных нами данных, многолетнего
наблюдения больных, страдающих посттравматическими эпилептическими припадками,
уточнения многочисленных анамнестических аспектов подобного рода утверждение
нельзя трактовать однозначно. Более того, было бы неверным считать припадки
результатом только травмы, учитывая современные представления о
полиэтиологичности эпилептического процесса (Болдырев А.И., 1984, 1990; Карлов
В. А., 1990; Мякотных В.С., 1994; Перунова Н.Ю., 2004).
В ходе проведения нашего сравнительного исследования оказалось, что
различными типами эпилептических припадков страдали 25 (18,94%) больных с
последствиями боевой ЧМТ и 6 (12%) больных - с последствиями бытовой ЧМТ, но у
всех 25 больных с последствиями боевой травмы, у которых развился эпилептический
синдром, пароксизмы исходно носили отчетливо парциальный, фокальный характер,
указывающий на преимущественное поражение височных структур головного мозга и
участие именно этих структур в формировании эпилептического очага,
эпилептической системы и эпилептического процесса в целом, что достаточно
характерно для эпилепсии травматического генеза. Это подтверждает точку зрения
большинства неврологов, нейротравматологов (Штульман Д.Р., Левин О.С. и др.,
2000), согласно которой травматическое повреждение при легкой ЧМТ особенно часто
формируется в базальных отделах лобной и передних отделах височных долей,
которые тесно соприкасаются с выступающим костным рельефом, и данный
патологический церебральный локус по существу совпадает с местом удара или
противоудара при травме.
Но, с другой стороны, полное отсутствие случаев дебюта эпилептических
припадков, в том числе «височных» у больных, не имевших ЧМТ, но подвергшихся
действию боевого ХПЭС, может свидетельствовать о том, что дизрегуляторные
мозговые процессы на уровне ретикулярной формации мозгового ствола, хотя и
связаны непосредственно с поражением лимбических структур, но в данном случае,
только в результате хронического стрессового воздействия, без отчетливых
указаний на органическое повреждение, пока не сыграли своей роли в возникновении
и клиническом развитии эпилептической патологии. Это противоречит сохраняющейся
точке зрения о возможности развития психогенных эпилептических припадков, так
называемых эпилептических реакций психогенной природы. Возможно, что такого рода
психогенные, стрессогенные эпилептические проявления и возможны, но только у лиц
с уже сформировавшимся в этиопатогенетическом отношении эпилептическим
процессом, а психогения при этом является только лишь триггером клинического
дебюта эпилептических припадков, о чем нами указывалось и ранее (Мякотных В.С.,
1991, 1993)
Дебют эпилептического синдрома у больных, перенесших боевую ЧМТ, приходился
на различные сроки после травматического воздействия: у 9 (6,82%) пациентов
припадки впервые возникли в течение первого года после получения травмы, у 9
(6,82%) - в течение от 1 года до 3 лет после травмы, у 7 (5,30%) - через 5 - 8
лет после травмы. С одной стороны, различная «удаленность» эпилептического
дебюта от факта получения боевой ЧМТ свидетельствует о пролонгированности
травматической болезни головного мозга, с другой – позволяет сомневаться в
исключительно травматическом генезе симптоматической эпилепсии, связываемой нами
с бывшей травмой. Вопрос требует, на наш взгляд, дальнейшего изучения.
Согласно классификации эпилепсий и эпилептических синдромов, принятой
Международной противоэпилептической лигой в 1989 году, а также вариантов
эпилептических припадков (Болдырев А.И., 1984, 1990) типы эпилептических
припадков в отдаленном периоде боевой ЧМТ были следующими: простые парциальные,
представленные типичными пароксизмами «височной» эпилепсии, - у 13 (9,85%)
больных, сложные парциальные, судорожные вторично-генерализованные, также
клинически с отчетливым присутствием «височного» компонента - у 12 (9,10%).
Клиническая трансформация припадков произошла почти у половины (12 из 25)
больных с первично парциальными височными пароксизмами, причем у 9 (6,82%)
пациентов - через 4 -5 лет после травмы, и у 2 (1,51%) – через 8 лет. Отчетливую
«ауру» при самом первом припадке отмечали лишь 3 (2,27%) пациента, в дальнейшем,
в отдаленном периоде ЧМТ она наблюдалась уже у всех 25 (100%) (р<0,001). Аура в
качестве субъективно ощущаемого больным компонента эпилептического пароксизма
характеризовалась нарастающими ощущениями в эпигастральной области, другими
вегетативными проявлениями, психическими симптомами типа deja
vu, ощущениями деперсонализации, ретроспективными
«вспышками» воспоминаний, страхом, раздражением. Согласно классификации
автоматизмов А. Гасто (1975), в отдаленном периоде боевой ЧМТ отмечены
алиментарные, оперкулярные автоматизмы - у 12 больных (р<0,01), у 4 больных –
мимические, и у 1 - амбулаторные. За период наблюдения у 2 больных с
оперкулярными автоматизмами отмечено учащение припадков - от 4 - 5 до 11 - 13
приступов в сутки, и у 1 больного с судорожными вторично-генерализованными
пароксизмами, дважды за период наблюдения отмечались эпилептические статусы.
Выявленная отчетливая трансформация клинической картины пароксизмального
эпилептического синдрома достаточно характерна для эпилепсии, в частности
парциальной, фокальной, в целом и свидетельствует о вовлечении в формирующуюся
эпилептическую систему все новых и новых образований головного мозга с развитием
самых разнообразных патологических связей. Но, с другой стороны, данная ситуация
может в определенной степени свидетельствовать и о продолжающемся развитии
травматической болезни головного мозга, служащей основой для продолжающегося же
развития посттравматической эпилепсии.
Приведем пример.
Больной Ф., 1963 г.рожд. Наблюдается с 1994 г. с диагнозом:
посттравматическая энцефалопатия, прогредиентное течение, астено- эксплозивный
вариант психоорганического синдрома, симптоматическая эпилепсия. В Афганистане
проходил срочную службу в 1982 – 84 гг, получил контузию головного мозга с
потерей сознания в течение 45 минут, перенес вирусный гепатит, лечился в
госпитале, имеет свидетельство о болезни. Со времени контузии беспокоят частые
головные боли, через 10 - 12 лет присоединились головокружения
несистематизированного характера. Сразу после демобилизации беспокоили частые
стереотипные кошмарные сновидения, через год появились «судороги» во
время сна, о чем больному сказала жена. С этого же времени - непроизвольные
стереотипные «жевания», иногда несколько раз в сутки. В 1993 году, через 9 лет
после демобилизации, впервые после умеренной алкоголизации развился
генерализованный судорожный припадок, затем припадки в первый год стали
возникать с частотой до 4 раз в месяц, практически сразу же отмечалась
эпигастрально-абдоминальная аура. С этого времени больному назначена
противоэпилептическая терапия (финлепсин по 200 мг 3 раза в день), но регулярно
он не лечился. В течение последних лет, вплоть до 2005 г. беспокоят ежедневные
эпизоды «уже виденного» в вечернее время. Вторично-генерализованные судорожные
эпилептические припадки с аналогичным началом наблюдаются до 5 раз в год,
однократно имел место эпилептический статус.
Неврологически: вялые зрачковые реакции, болезненность глазных яблок при их
крайних отведениях, асимметрия носогубных складок, девиация языка влево,
горизонтальный нистагм, симптом Маринеску с 2-х сторон, вялые брюшные рефлексы,
пошатывается в позе Ромберга, интенция и мимопопадание при выполнении
пальце-носовой пробы слева.
Психический статус: Сознание ясное, все виды ориентировки сохранены.
Контактен. Фон настроения снижен, описывает учащение пароксизмальных состояний.
Не пользуется общественным транспортом, не выносит очередей, так как «это его
раздражает». Внимание неустойчивое, истощаем. Отвечает на вопросы после большой
задержки. Выявляется психическая астения, увеличивается латентный период при
ответах и возрастает количество ошибок при счетных операциях. Память снижена на
текущие и прошлые события, не может назвать даты рождения своих детей, забывает
перенесенные заболевания, не всегда датирует события своей жизни. Психическая
деятельность замедлена. Вял, пассивен при беседе. Настроение депрессивное, но в
то же время считает, что всегда был пессимистом. Аффективно неустойчив,
проявляет раздражительность, но стремится сдерживаться. Галлюцинаций, бреда нет,
интеллект невысок.
При неоднократно проведенных ЭЭГ исследованиях (рис. 4.1 и 4.2) выявляется
дезорганизованный тип ЭЭГ с преобладанием альфа- тета активности (4 и 5 тип по
Е.А. Жирмунской), миграция очага эпилептической активности по височным областям
при разных исследованиях, и во всех случаях - генерализация пароксизмальной
эпилептиформной активности при нагрузках (гипервентиляции).
Рис. 4.1. ЭЭГ больного Ф., 1963 г.рожд.: дезорганизованный тип ЭЭГ с
преобладанием альфа- тета активности (4 - 5 тип по Е.А. Жирмунской),
преобладание очаговых эпилептических изменений в левой височной области
Рис. 4.2. Повторная ЭЭГ больного Ф., 1963 г.рожд.. На фоне сохраняющейся
дезорганизации основной активности очаговые эпилептические изменения преобладают
в правой височной области
МРТ головного мозга в динамике на протяжении 3- лет: признаки открытой
наружно-внутренней гидроцефалии с нарастанием ширины третьего желудочка при
повторном исследовании на 1,5 мм и нарастанием ширины сильвиевой борозды на 1,2
мм.
Люмбальная пункция: ликвор – под повышенным давлением; белок - 0,15 г/л,
цитоз - 7/3.
Неоднократно проводились курсы массивной медикаментозной терапии: диазепам
в/в капельно, сернокислая магнезия с глюкозой, амиксид, депакин–хроно,
сосудорасширяющие средства, дегидратация, витамины, биостимуляторы, курс
индивидуальной, семейной и групповой психотерапии. После лечения отмечал
улучшения состояния в виде значительного уменьшения головных болей,
раздражительности и аффективности в поведении. Реже стали простые парциальные
припадки. Рекомендован постоянный прием депакина, при нарушения режима лечения
которым не чаще двух раз в год – генерализованные судорожные эпилептические
припадки.
В приведенном наблюдении у больного с последствиями боевой ЧМТ происходит
прогредиентное развитие эпилептического процесса в течение 20 лет после травмы с
нарастанием полиморфизма, степени генерализации припадков, изменений личности.
Этому сопутствуют эпилептического типа мультифокальные изменения на ЭЭГ и
признаки нарастающей атрофии мозга по данным повторных МРТ. Лечение
малоэффективно, и больной не осознает необходимости его постоянного применения.
У 6 (12%) больных с последствиями бытовой ЧМТ припадки сразу носили
генерализованный характер и дебютировали в течение первого года после ЧМТ.
Частота припадков к моменту осмотра, в отдаленном периоде ЧМТ уменьшилась с 4 -
5 припадков за год при первичном обращении до 1 - 2 припадков в год через 12 лет
после ЧМТ, т.е в целом эпилептический процесс, обусловленный бытовой травмой,
клинически протекал более благоприятно, нежели у лиц с последствиями боевой ЧМТ,
отягощенной ХПЭС, а эпилептические пароксизмы носили менее полиморфный характер,
без ярко выраженной тенденции к клинической трансформации. Для больных же с
боевой ЧМТ характерно волнообразное течение процесса: периоды учащения припадков
(до 20 в год) сменяются периодами их урежения (до 1-2 раз в 2-3 месяца).
Необходимо отметить, что во всех случаях посттравматической эпилепсии
наследственность не отягощена.
4.1.4. Характеристика объективного неврологического статуса
Если считать последствия боевой ЧМТ исключительно органическим страданием
центральной нервной системы, а последствия боевого ХПЭС - исключительно
функциональной неврологической патологией, то в принципе не имело бы смысла
сравнивать комплекс объективных неврологических симптомов и синдромов при этих
двух вариантах рассматриваемой послевоенной патологии. Но с учетом сложившегося,
в том числе и в нашей клинике, взгляда на неврологическую патологию как на
комплекс нарушений органического и функционального происхождения, неразрывно
связанных между собой, мы все же пошли по пути данного сравнения, поставив перед
собой задачу, во-первых, определить роль наиболее тяжелого варианта стрессовых
расстройств в возможном развитии структурно-органических изменений мозга,
во-вторых, показать сходство и различия последних, вызванных как физической
травмой в сочетании с воздействием боевого ХПЭС, так и исключительно ХПЭС.
В таблице 4.3 представлены основные клинические характеристики исследования
объективного неврологического статуса у наблюдаемых групп больных на момент
первичного осмотра, через 5-8 лет после травмы или ХПЭС.
Таблица 4.3. Характеристика неврологического статуса
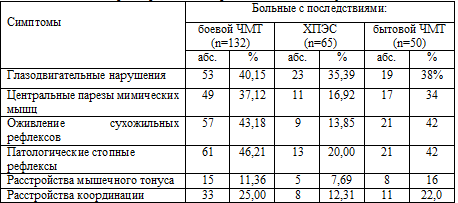
Из представленных в таблице 4.3 данных очевидно, что грубые выпадения в
двигательной, чувствительной сферах отсутствовали, и это в значительной степени
объясняется присутствием в наших наблюдениях последствий именно легкой ЧМТ.
Преобладали в разном сочетании микросимптомы органического поражения мозга,
преимущественно стволового уровня: горизонтальный мелкоразмашистый нистагм,
расстройства конвергенции глазных яблок, недоведение их до наружных углов
глазниц, снижение роговичных рефлексов, гипалгезия в зонах Зельдера на лице,
асимметрия лицевой мускулатуры, девиация языка, легкие нарушения координации,
кистевые и стопные пирамидные симптомы Бехтерева и Россолимо, рефлексы орального
автоматизма, отсутствие брюшных рефлексов, изменения чувствительности различной
локализации. Разлные сочетания органической микросимптоматики выявлялись у 100%
больных всех групп. При этом глазодвигательные расстройства недостоверно (р>0,05)
чаще встречались у больных с ЧМТ в анамнезе, что вполне объяснимо поражением
срединных структур - варолиева моста, верхних бугорков четверохолмия, непарного
нервного тяжа - ядра Панегросси, возникающих в результате коммоции мозга (Шутов
А.А., Шерман М.А., 1995, 2002). Можно предположить, что эти же образования
страдают и вследствие разбалансировки деятельности неспецифических регулирующих
структур мезодиэнцефальной области, являясь в определенной степени «мишенью»
ХПЭС у лиц, формально не перенесших ЧМТ. Страдание же пирамидной системы,
центральный парез мимической мускулатуры, расстройства координации достоверно (р<0,05)
преобладают у лиц, перенесших закрытую ЧМТ. Это свидетельствует, во-первых, о
более тяжелой степени органического повреждения центральной нервной системы
именно у травматиков по сравнению с лицами, перенесшими только ХПЭС, во-вторых,
об отсутствии полного выздоровления даже после так называемой легкой контузии
головного мозга, что позволяет судить о непрерывности посттравматического
церебрального патологического процесса. В-третьих, можно предположить, что
базальные отделы головного мозга при легкой ЧМТ страдают больше, чем
конвекситальные.
Изменения в неврологическом статусе к моменту повторного осмотра произошли
через 5 – 15 лет у 13 (9,85%) больных из группы перенесших боевую ЧМТ и
проявились в появлении симптомов орального автоматизма – у 7 (5,30%) больных,
нарастании атаксии - у 3 (2,27%), анизорефлексии - у 3 (2,27%). Указанные
изменения носят статистически недостоверный характер (p>0,05),
хотя в определенной степени указывают на возможность прогредиентности
травматической болезни мозга как таковой или в связи с появившимися ее
осложнениями (сосудистыми, например) в отдаленном от ЧМТ периоде. Улучшений
неврологического статуса в динамике отдаленного периода травматической болезни
мозга и ХПЭС не отмечено ни у одного больного из трех групп.
У всех 197 больных в отдаленном периоде ЧМТ и ХПЭС, а также у 50 больных
группы сравнения, при объективном осмотре определялись стойкие вегетативные
нарушения различной степени выраженности: тахи- и брадикардия, лабильность АД,
диффузная потливость, непереносимость душных помещений, нарушения дермографизма,
зябкость, повышенный блеск глаз, гиперсаливация или сухость во рту, боли в
животе и желудочно-кишечные дискинезии и т.д. Это в принципе подтверждало
полученные нами данные преимущественно субъективного характера, рассмотренные
выше в соответствующем разделе.
Мы смогли оценить вегетативный тонус в сроки через 4 - 15 лет после
травматического воздействия, а также через 10 - 20 лет (таблица 4.4).
В целом вегетативный тонус в отдаленном периоде легкой боевой ЧМТ (через 4 –
15 лет после ЧМТ) характеризовался преобладанием симпатикотонии у представителей
всех 3-х групп. При повторных обследованиях, также среди больных всех групп
определялась тенденция к нарастанию числа лиц с проявлениями симпатикотонии,
однако среди больных с последствиями боевой ЧМТ этот процесс происходил
достоверно быстрее (р<0,05).
Таблица 4.4. Динамика вегетативного тонуса по периодам
после ЧМТ или ХПЭС:
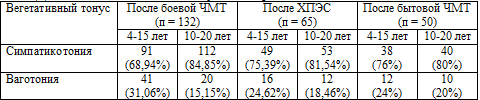
Таким образом, в отдаленном периоде боевой и бытовой ЧМТ, а также ХПЭС,
имеется тенденция к преобладанию симпатикотонии. За период наблюдения
субъективно ухудшилось самочувствие у всех больных с имевшими место
вегетативно-сосудистыми кризами. Так, у 9 (6,82%) больных, перенесших боевую ЧМТ,
вегетативно-сосудистые кризы смешанного характера стали возникать ежедневно, а у
остальных их частота увеличилась в меньшей степени – с 1- 2 раз в месяц до 2 - 4
раз в неделю. Возросла и продолжительность приступов - от 20 - 30 минут до
нескольких часов. Все больные отмечали, что стали переносить кризы тяжелее,
особенно в связи с усилением чувства тревоги.
Обычно у одного больного отмечалось несколько синдромов в клинической
картине последствий ЗЧМТ и ХПЭС. Ведущим нами считался тот синдром, клинические
проявления которого, как субъективные, так и объективные, были наиболее выражены
и послужили поводом для обращения больного к врачу. Структура выделенных нами
ведущих неврологических синдромов представлена в таблице 4.5.
Таблица 4.5. Ведущие неврологические синдромы
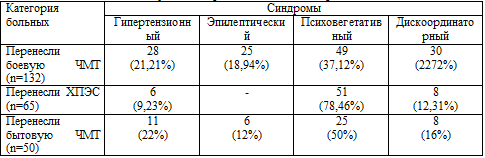
И вот здесь обнаружились отчетливые различия между пациентами, перенесшими и
не перенесшими боевую ЧМТ. Только у больных с последствиями ЧМТ, как уже сказано
выше, встречался и мог выступать в качестве преобладающего в клинической картине
заболевания эпилептический синдром, другими словами - посттравматическая
эпилепсия. Достоверно (р<0,05) чаще при наличии ЧМТ в анамнезе в качестве
ведущего диагностировался дискоординаторный синдром, а также
гипертензионно-гидроцефальный (как клинически, так и на основании МРТ
исследования). Преобладающие же в клинической картине психо-вегетативные
расстройства, наоборот, чаще встречались в качестве ведущих у лиц, не
переносивших ЧМТ, но зато тяжело переживавших ХПЭС.
Необходимо отметить, что структура выявленных ведущих неврологических
синдромов не была строго постоянной во времени и довольно отчетливо изменилась к
моменту повторного осмотра, отличаясь, тем не менее, в зависимости от
рассматриваемого варианта патологии (таблица 4.6).
Таблица 4.6. Динамика ведущих клинических синдромов по
периодам: 1 - 2, 4 - 15, 10 - 20 лет после ЧМТ или ХПЭС
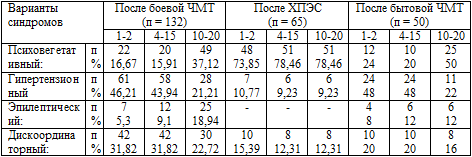
Так, в динамике боевой ЧМТ происходит нарастание частоты психовегетативного,
эпилептического синдромов и уменьшение частоты гипертензионного синдрома (р<0,05).
У пациентов с бытовой ЧМТ, в отличие от больных с последствиями ЧМТ военного
времени, частота развития эпилептических проявлений практически не нарастает.
Вероятно, ЧМТ, полученная в условиях ХПЭС, способствует развитию эпилептических
проявлений даже в отдаленном периоде ЧМТ, чего в такой же степени не отмечается
при ЧМТ, полученной в быту. Это тем более очевидно в связи с тем, что у
пациентов с боевой ЧМТ в анамнезе практически всегда диагностировался «височный»
тип эпилептических припадков, а «мишенью» сопутствующего травме ХПЭС как раз и
могут являться височные структуры головного мозга. В то же время у 6 (9,23%)
больных с ХПЭС также диагностирован в качестве ведущего гипертензионный синдром
с типичными кризами, подтвержденный данными МРТ, рентгенографии черепа, осмотром
глазного дна. Его частота в динамике практически не меняется. Это связано,
возможно, с тем, что у этих больных имела место в анамнезе родовая травма, и
ХПЭС декомпенсировал преморбидный органический фон. Динамика дискоординаторного
синдрома имеет тенденцию к урежению во всех группах, но без достоверных
различий.
4.2. Особенности психопатологической симптоматики и ее динамики в отдаленном
периоде ЧМТ и последствий ХПЭС
В предыдущих главах и разделах мы уже касались вопросов нарушений психики у
наших больных. Указывалось на особенности расстройств памяти, эмоций; некоторые
психопатологические нарушения рассматривались в качестве составляющих
психо-вегетативного синдрома и т.д. Считаем также целесообразным в отдельной
главе рассматривать нейросоматические и психосоматические расстройства. В данном
же разделе мы остановимся в основном на вопросах психоорганического синдрома и
депрессии, так как именно эти патологические состояния показалось нам особенно
интересным рассмотреть с точки зрения их зависимости как от последствий боевой
ЧМТ, полученной в условиях боевого ХПЭС, так и от исключительно последствий
боевого ХПЭС при отсутствия факта физической травмы головного мозга.
Характер психопатологических синдромов и психических отклонений прослежен
нами со времени первого обращения больных и на протяжении 10-20 лет. К моменту
начала проводимого исследования, через 4 - 15 лет после травмы или ХПЭС,
указанные расстройства выявлялись у 171 (86,80%) ветерана современных войн,
среди них у лиц, перенесших ЧМТ – в 115 (87,12%) наблюдениях, а среди
перенесших только боевой стресс - в 56 (86,15%). В группе сравнения, т.е. среди
больных, перенесших только бытовую ЧМТ, психопатологические расстройства
диагностированы у 37 (74,0%) больных.
Позднее, через 10 и более лет после травматического воздействия
психопатологические синдромы и психические расстройства выявлялись у 174
(88,32%) ветеранов современных боевых действий, среди них у лиц, перенесших
боевую ЧМТ - в 118 (89,40%) наблюдениях, а у перенесших исключительно боевой
ХПЭС - в 56 (86,15%). В группе сравнения, при наличии последствий бытовой ЧМТ
психопатологические расстройства диагностированы у 36 (72%) больных.
Таким образом, психопатологические расстройства были достаточно длительными,
существовавшими в течение многих лет после получения травмы или воздействия
боевого стресса, и общее относительное число больных, страдавших расстройствами
психики, не зависело от варианта боевого воздействия – ЧМТ в сочетании с боевым
ХПЭС или же просто ХПЭС. В то же время частота психопатологических проявлений у
больных с последствиями бытовой травмы уступала таковой, наблюдавшейся при
последствиях боевой ЧМТ.
Структура выявленных психопатологических расстройств включала ряд вариантов.
В отдаленном периоде боевой ЧМТ психоорганический синдром сформировался у 72
(54,55%) больных, его астено-эксплозивный вариант диагностирован у 22 (16,67%)
человек, астенический - у 22 (16,67%), эксплозивный - у 28 (21,21%). У 43
(32,58%) больных данной группы психоорганический синдром не сформировался и
умеренные психические расстройства представлены только астено-невротическим
синдромом - у 7 (5,30%) больных, либо только астеническим - у 39 (29,55%).
У больных с последствиями ХПЭС, не переносившими ЧМТ, также преобладал
психоорганический синдром (34 больных; 52,32%): астенический вариант - у 21
(32,1%), эксплозивный – у 8 (12,31%), астено-эксплозивный - у 5 (7,70%).
Астено-невротические расстройства диагностированы у 5 (7,70%) человек,
астенический синдром - у 10 (15,38%).
У больных с последствиями бытовой ЧМТ астенический вариант психоорганического
синдрома сформировался в 4 (8%) наблюдениях, астено- эксплозивный вариант - в 1
(2%), а эксплозивный не выявлен ни у одного пациента. Астенический синдром
выявлен у 20 (40%) больных, затянувшееся тревожно-депрессивное состояние
(ипохондрический синдром) отмечено у 11 (22%) больных.
Таким образом, формирование стойких психопатологических расстройств в форме
психоорганического синдрома достоверно чаще (р<0,05) диагностируется у лиц,
получивших боевую ЧМТ в условиях ХПЭС, либо перенесших только боевой ХПЭС по
сравнению с больными, перенесшими бытовую ЧМТ (соответственно 54,55%, 52,32% и
10%).
Эксплозивные расстройства с частыми аффективными вспышками диагностированы
только у ветеранов боевых действий, и достоверно чаще (р<0,01) преобладают у
больных, перенесших боевую ЧМТ, по сравнению с лицами, пережившими лишь боевой
стресс – соответственно в 21,21% и 12,31%. Астенические расстройства различной
степени выраженности также более характерны (р<0,05) для больных, перенесших ЧМТ,
нежели только ХПЭС.
Необходимо отметить, что только у больных с последствиями бытовой ЧМТ
обнаруживались ипохондрические и затяжные тревожно-депрессивные расстройства (в
22%), хотя жалобы на повышенную тревожность отмечались и у больных – участников
боевых действий. Возможно, это связано с тем, что для ветеранов войн более
характерен полиморфизм жалоб, и на первый план в процессе длительного наблюдения
больных у них все же выступают эксплозивные и астенические расстройства.
Интересными представляются данные о динамике развития различных вариантов
психопатологических расстройств (таблица 4.7).
Таблица 4.7. Динамика психопатологических расстройств по
периодам: 1 – 2 года, 4 – 15 лет, 10 – 20 лет после ЧМТ или ХПЭС
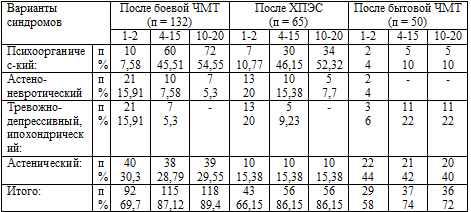
С учетом полученных нами данных можно утверждать, что формирование
психоорганического синдрома у ветеранов современных боевых действий, перенесших
ЧМТ в условиях ХПЭС связано с закономерным течением посттравматической
стрессовой реакции (ПТСР): фаза «оцепенения», фаза развертывания вторичных
симптомов ПТСР, переход в хроническую стадию (Friedman
M.J. et
al., 1994). У больных же с последствиями бытовой ЧМТ
также увеличивается в динамике отдаленного периода травмы частота присутствия в
клинической картине страдания психоорганического синдрома, но все же данный
феномен встречается значительно реже, чем у больных с последствиями боевой ЧМТ.
Полученные данные подтверждены в том числе психологическим тестированием (опросник
ПТСР И.О. Котенева, опросник Басса-Дарки, опросник Спилбергера), проводившимся в
динамике.
Астено-невротические расстройства достоверно чаще (р<0,05) выявляются в
первое время после всех видов повреждающих воздействий (боевая ЧМТ, ХПЭС,
бытовая ЧМТ). В динамике же отдаленного периода частота астено-невротических
расстройств отчетливо снижается среди представителей всех 3-х групп наблюдений.
Это связано с адаптацией, с формированием психоорганического синдрома у бывших
участников боевых действий, а у больных с последствиями бытовой ЧМТ - с
усугублением невротизации и трансформацией астено-невротических расстройств в
тревожно-депрессивные, ипохондрические, что может быть связано, кроме всего
прочего, с социальными моментами: отсутствием тесных, корпоративных, как у
ветеранов Афганистана или Чечни, связей, отсутствием социальной поддержки и
государственной программы реабилитации и т.д.
Тревожно-депрессивное состояние достоверно чаще (р<0,05) диагностировалось в
раннем отдаленном периоде ЧМТ у участников современных вооруженных конфликтов и
в позднем отдаленном периоде у больных с бытовой ЧМТ в анамнезе. Возможно, это
также связано с тем, что «афганцы» и «чеченцы» оказываются с течением времени
относительно лучше, чем больные с последствиями бытовой ЧМТ, адаптированными в
социуме. У ветеранов лучше, чем в общей популяции, поставлена система
диспансерного наблюдения. Таким образом, вероятно, необходима отчетливая
социальная и реабилитационная программа для больных и с последствиями бытовой
ЧМТ, чего, к сожалению, мы пока не видим.
Астенический синдром в первое время (1 - 2 года после ЧМТ ) достоверно чаще
выявлялся у «травматиков», независимо от условий травмы (боевая, бытовая),
нежели при последствиях боевого ХПЭС. Затем частота выявления указанного
синдрома оказывалась большей среди больных с бытовой ЧМТ в анамнезе, чем у
больных с боевой ЧМТ, т.к. у последних превалировали астенический и
астено-эксплозивный варианты психоорганического синдрома. В то же время у
больных только с последствиями боевого ХПЭС астенический синдром встречался во
все периоды наблюдения и обследования достоверно реже, чем у травматиков, хотя
относительные различия со временем сглаживалась.
Резюме
Таким образом, обобщая материалы, представленные в настоящей главе, можно
утверждать, что имеется определенное сходство клинической картины отдаленных
периодов боевой ЧМТ и боевого же ХПЭС, причем и тут, и там не отмечается полного
регресса неврологической симптоматики в динамике, а характерно ее развитие,
часто в виде трансформации клинических проявлений. В то же время, среди больных
с последствиями ЧМТ чаще встречаются более тяжелые и полиморфные синдромы,
такие, как гипертензионный, эпилептический, а у больных с последствиями ХПЭС
доминирует психовегетативный синдром, и вообще не встречается эпилепсии. При
наличии полиморфизма эпилептических припадков у всех больных с последствиями
боевой ЧМТ они клинически носят височную окраску, которая сохраняется в течение
многих лет. Это может зависеть от условий получения боевой ЧМТ – ХПЭС, который
принимает участие в «запуске» патологической активности именно височных структур
как составной части лимбико-ретикулярного комплекса. При этом как у лиц с
последствиями боевой ЧМТ, так и у пациентов, перенесших только ХПЭС боевой
обстановки, преобладают проявления симпатикотонии в вегетативном статусе, хотя
на фоне перенесенной ЧМТ развитие вегетативной недостаточности происходит
быстрее и тяжелее. Как после перенесенной боевой ЧМТ, так и в результате ХПЭС
наблюдается частое развитие психоорганического синдрома, в структуре которого
преобладают астено-эксплозивный, эксплозивный и астенический варианты. Возможно,
что длительно существующие патологические системы, запущенные ХПЭС и имеющие в
основном дисфункциональную окраску, с течением времени приводят к органическим,
микроструктурным церебральным изменениям. Клинические проявления бытовой ЧМТ и
их динамика существенно отличаются от таковых у лиц, перенесших боевую ЧМТ,
сопровождавшуюся ХПЭС. Можно считать, поэтому, травматическую болезнь головного
мозга, сформировавшуюся на основе боевой травмы, полученной в условиях ХПЭС
современного военного конфликта, совершенно особым вариантом церебральной
патологии, развивающимся по своим определенным законам, в том числе в
значительной степени по сценарию «от функционального – к органическому».

