Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
ГЛАВА 14. НАРУШЕНИЯ ОБМЕНА КАЛЬЦИЯ
Кальций – химический элемент II группы периодической системы
Менделеева Д.И. Порядковый номер 20, атомный вес 40,08. Впервые металлический
кальций получил Дэви Г. в 1807 году, хотя первая соль, до сегодняшнего дня
широко использующаяся в медицине – хлорид кальция, была получена нагреванием
нашатыря с известью в 1380 году Иссаком Голландским.
Кальций является одним из пяти (кислород, углерод, водород, азот,
кальций) наиболее распространенных элементов, встречающихся в организме
человека, а из минеральных соединений соединения кальция значительно превосходят
количество всех других.
Вероятно, впервые, значение кальция при патологии было установлено
Вейсом, работавшим в клинике Бильрота, в 1880 году (цит. по Шерешевскому Н.А.,
1936). Он показал, что оперативное удаление зоба ведет к судорогам,
сопровождающимся резким снижением кальция в крови. Затем в опытах на собаках
было показано, что после удаления паращитовидных желез и развития у них тетании,
если им ввести кальций, то судороги прекращаются, а при длительном введении
совершенно исчезают.
Хотя, как хорошо известно, заболевание, связанное с нарушением
обмена кальция – рахит, было описано еще врачами Древнего Рима – Сораном
Эфесским и Галеном (цит. по Туру А.Ф., 1966). Попутно заметим, что само название
болезни связано с фамилией врача (Ricketts), успешно лечившего рахит. Первым,
подробно описавшим клиническую картину и патологическую анатомию рахита,
является англичанин Френсис Глиссон. Случилось это в 1650 году. Именно тогда
вышел в свет главный труд Глиссона Ф. «О рахите» («De rachitide»). И хотя в
своей книге, естественно, Глиссон Ф. не указывает на роль кальция и витамина D в
патогенезе рахита, но он абсолютно правильно связывает это заболевание с
нарушениями питания и дает подробную клиническую характеристику болезни.
Большинство из симптомов, указанных им, полностью соответствуют сегодняшним
клиническим описаниям данного заболевания. Например, ранние симптомы рахита
автор описывает так:
1. «Необходимо обратить внимание на вялость, размягченность
мускулатуры, ее слабость, неподвижность и оцепенелость.
2. Обратить внимание на запястья и на концы ребер, ибо уже в
ранних стадиях на запястье появляются шишки или узлы и утолщения на концах ребер.
3. Живот заметно увеличивается в объеме, выступает вперед уже в
самом начале болезни... Живот становится непропорционально большим сравнительно с
грудью.
4. Одновременное наличие всех этих признаков дает возможность с
уверенностью поставить диагноз рахита уже в самом начале болезни».
Таким образом, достаточно давно известна важнейшая роль кальция для
организма человека. И на самом деле он является основным минералом человеческого
скелета и самым распространенным катионом организма. Примерно 90-95% кальция
находится в костной ткани, остальная часть кальция выполняет ряд важнейших
функций, не связанных со скелетом. Он принимает участие в работе многих
ферментативных систем и реакций (глюконеогенез, гликолиз), небольшое количество молекул БАВ, связываясь с рецепторами,
приводят к внутриклеточной продукции гораздо большего числа молекул второго
посредника, а они уже влияют (положительно или отрицательно) на активность еще
большего числа белковых молекул. Следовательно, происходит прогрессивное
усиление (амплификация) сигнала, исходно возникшего при взаимодействии гормона с
рецептором. Таким образом, поддержание внеклеточной концентрации кальция в узких
пределах имеет важнейшее значение функционирования большинства тканей и органов
организма. Приведем небольшой пример: в неактивированной клетке (в цитозоле)
концентрация ионов кальция всего 1/10 000 от концентрации кальция во
внеклеточной жидкости. При незначительном увеличении кальция внутриклеточно
(например, при тяжелой асфиксии новорожденных) образуется малорастворимая соль
фосфата кальция и прекращается любая продукция и утилизация АТФ. Преобладающая
часть внутриклеточного кальция содержится в органеллах – митохондриях или
цитоплазматическом ретикулуме. Повреждения клетки могут привести к увеличению
уровня внутриклеточного кальция вследствие его выхода из органелл, именно
поэтому в настоящее время пытаются синтезировать селективные блокаторы
кальциевых каналов, например, блокирующих избыточное поступление кальция только
в нейрон.
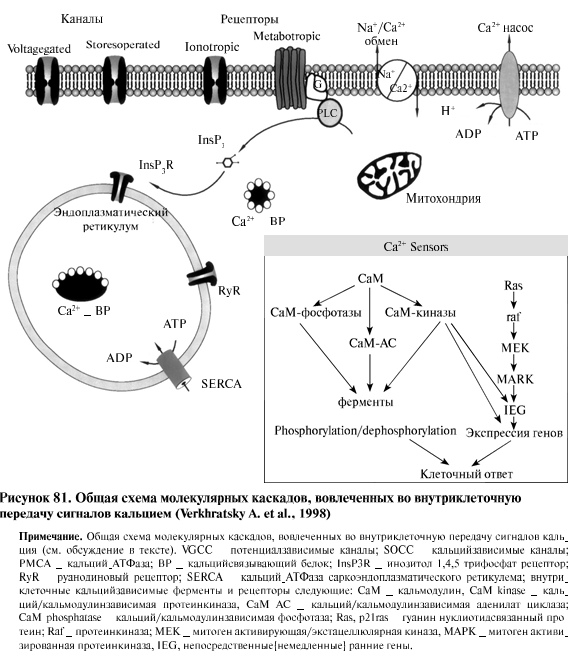
На рисунке 81 показана общая схема молекулярных каскадов,
вовлеченных во внутриклеточную передачу сигналов кальцием.
Для того, чтобы перейти к патологии обмена кальция, считаем
необходимым кратко напомнить его физиологию.
В организм человека кальций поступает с пищей, при этом основная
часть в виде фосфата кальция, поскольку именно в таком виде он содержится в
пищевых продуктах.
Всасывание ионов кальция происходит в проксимальных участках
тонкого кишечника (из общего количества усвоенного кальция 2% всасывается в
желудке, 15% в двенадцатиперстной кишке, 23% – в тощей и 60% – в подвздошной). У
взрослых всасывается примерно около половины кальция, поступающего с пищей, у
детей, а также беременных и кормящих женщин – больше. В сутки всасывается около
10 мг/кг массы тела, примерно столько же у взрослых экскретируется с мочой и
поступает обратно в просвет кишечника с продуктами его секреции, желчью и
слущенными эпителиальными клетками. Организм человека регулирует обмен кальция в
зависимости от содержания его в пищевом рационе.
Как только поступление кальция превышает потребности организма, его
всасывание уменьшается: например, 0,43 при поступлении 0,4-0,6 г/сут., 0,35 при
0,6-1,0 г/сут., 0,28 при 1,0-1,2 г/сут., 0,8 при 10 мг/сут., 0,25 при 200 мг/сут., 0,22 при
500 мг/сут. (De Grazia J.A. et al., 1965). У детей в отличие от взрослых имеется положительный баланс
кальция. Большая часть из всосавшегося в кишечнике кальция поступает в костную
ткань. Этим обуславливается то, что экскреция кальция мочой у детей любого
возраста, в том числе и новорожденных, не превышает 6 мг/кг/сут. (см. таблицу
150).
Как мы указывали, большая часть кальция находится в скелете.
Установлено, что у взрослого человека массой тела 70 кг содержится около 1000 г
ионов кальция. При этом за сутки со всеми жидкостями обменивается всего не более
0,55 г. На долю мягких тканей приходится всего 14 г, в том числе в крови 0,31 г,
легких 0,087 г, мышцах 0,87 г, печени 0,09 г, почках 0,029 г, головном мозге
0,12, коже 0,41 г (см. таблицу 151).
Таблица 150. Экскреция кальция с мочой (атомно-абсорбционная
спектрофотометрия) (Тиц Н.У., 1997)
|
Потребление кальция с пищей
|
Кальций (ммоль/сут)
|
|
возраст
|
|
1-12 мес.
|
4-7 лет
|
взрослые
|
|
У детей и младенцев |
До 0,15 ммоль/кг в сутки (6,0 мг/кг/сут)
|
|
При 800 мг/сут. (20 ммоль/сут.) |
0,5-2,5
|
0,5-3,8
|
2,5-7,5
|
|
Менее 800 мг/сут. (20 ммоль/сут.) |
–
|
–
|
1,25-1,75
|
|
При отсутствии кальция в диете |
–
|
–
|
0,13-1,00
|
Таблица 151. Содержание кальция в мг% (по отношению к весу свежего
органа) (Капланский С.Я., 1958)
|
Название органа/ткани
|
Содержание кальция
|
|
Эритроциты |
0
|
|
Цельная кровь |
5
|
|
Глазная жидкость |
5
|
|
Спинномозговая жидкость |
5±0,5
|
|
Слюна |
6
|
|
Скелетные мышцы |
7
|
|
Сердечная мышца |
9
|
|
Желчь (печеночная) |
10
|
|
Лимфа |
10
|
|
Печень |
10
|
|
Селезенка |
10
|
|
Надпочечники |
10
|
|
Сыворотка крови |
10,3±0,3
|
|
Мозг |
10,5
|
|
Кожа |
11
|
|
Кишечник |
13
|
|
Поджелудочная железа |
15
|
|
Легкие |
16
|
|
Почки |
19
|
|
Матка |
22
|
|
Молоко (женское) |
32
|
|
Щитовидная железа |
34
|
|
Хрящ |
40
|
|
Кости |
9900
|
|
Дентин |
24 500
|
|
Эмаль |
34 500
|
В биохимическом анализе крови, к сожалению, чаще всего определяют
уровень общего кальция, состоящего из трех фракций:
1) ионизированного кальция, составляющего примерно половину от
общего кальция (именно он играет роль в вышеуказанных процессах);
2) в комплексе с белком (около 40% от общего уровня),
преимущественно альбумином (до 80%);
3) недиссоциированных солей (карбоната, сульфата, цитрата,
фосфата) (около 5-10% от общего уровня).
Уровень ионизированного кальция зависит от концентрации белка и
КОС, что, на наш взгляд, необходимо учитывать в клинической практике. Известно,
что при изменении уровня альбумина в плазме на 1,0 г% уровень кальция изменяется
в том же направлении на 0,8 мг% (Тиц Н.У., 1997). При ацидозе уровень
ионизированного кальция повышается, а при алкалозе – снижается. Кроме того, в
плазме крови повышение рН также способствует связыванию кальция с белками.
Поэтому при алкалозе отношение свободного ионизированного кальция к общему
содержанию кальция понижается, и несмотря на то, что общий уровень кальция
остается в пределах нормы, могут развиться судороги. Наоборот, при ацидозе,
особенно у недоношенных детей, повышается растворимость солей костной ткани и
больше кальция, чем в норме, переходит из костей во внеклеточную жидкость и,
следовательно, в мочу. При этих условиях даже при адекватном поступлении кальция
и нормальном функционировании околощитовидных желез может развиться
остеомаляция.
Ложное повышение концентрации кальция может быть обусловлено
венозным стазом при взятии пробы и длительном хранении крови. В связи с тем, что
соли кальция осаждаются на стекле, необходимо использовать тщательно
подготовленные шприцы, контейнеры и стеклянную посуду.
Концентрация ионов кальция в плазме регулируется с высокой
точностью: изменении ее всего на 1% приводит в действие гомеостатические
механизмы, восстанавливающие равновесие. В поддержании гомеостаза кальция
принимают участие 3 основных регулятора: паратиреоидный гормон (повышающий
концентрацию свободного ионизированного кальция в плазме), кальцитонин
(оказывающий противоположное действие ПГ) и метаболиты витамина D. Кроме того,
как указывают Лисс В.Л. и соавт. (2003), в регуляции обмена кальция прямо или
косвенно принимают участие тиреоидные, половые гормоны, ИФР-I, ИФР-II, ИФРСБ,
ПТГ подобные пептиды, интерлейкины, трансформирующие факторы роста -α и -β,
тромбоцитарные факторы роста -α и -β.
Таблица 152. Уровни общего и ионизированного кальция в плазме крови (ионно-селективный электрод) (Тиц Н.У., 1997)
|
Возраст
|
Кальций (ммоль/л)
|
|
общий кальций
|
ионизированный кальций
|
|
Пуповинная кровь |
2,05-2,80
|
1,30-1,60
|
|
Недоношенные новорожденные |
1,55-2,75
|
|
|
Доношенные дети 1 ч |
2,05-2,80
|
1,21-1,46
|
|
24 ч |
1,75-3,00
|
1,10-1,36
|
|
5 дней |
2,25-2,73
|
1,22-1,48
|
|
10 дней – 2 года |
2,25-2,75
|
1,16-1,22
|
|
2-12 лет |
2,20-2,70
|
1,12-1, 23
|
|
12-18 лет |
2,10-2,55
|
1,20-1,38
|
|
Взрослые |
2,15-2,50
|
1,15-1,27
|
Примечание. Максимальные уровни общего кальция в крови
отмечены в 20 часов, минимальные – в 2-4 часа (разница около 7%). Ложная
гипокальциемия возможна вследствие венозного стаза при взятии крови, поэтому
кровь следует брать при минимальном пережатии вены, без мышечной нагрузки или
после восстановления кровообращения в течение 1-2 минут. Соли кальция
осаждаются на стекле, в связи с чем при длительном хранении образцов крови
возможна ложная гипокальциемия.
В норме уровень кальция в крови равен 2, 25-2,75 ммоль/л (1 мэкв =
20 мг; 50 мэкв = 1 г). У новорожденных гипокальциемию диагностируют при уровне
общего кальция в сыворотке крови менее 2,0 ммоль/л (8,0 мг%) (ионизированного
менее 0,87 ммоль/л (3,5 мг%)) у доношенных детей и менее 1,75 ммоль/л (7,0 мг%)
(ионизированного менее 0,75 ммоль/л (3,0 мг%)) у недоношенных детей. Конечно,
наиболее информативным является уровень ионизированного кальция, но, к
сожалению, далеко не все лаборатории имеют возможность его определения. При
невозможности его определения можно рассчитать его концентрацию по формуле Мак–Лина
и Гастинга в модификации Пейна с соавт.:
Иоан.Са = Са × (0,025 × A) ×
1,
где ион. Са – ионизированный кальций (ммоль/л); Са – общий кальций
(ммоль/л), А – концентрация альбумина (г/л).
Частота
Гипокальциемия
Наиболее часто электролитные нарушения, в том числе и нарушения
обмена кальция, встречаются в периоде новорожденности. По данным исследований
разных авторов, проводившихся в разные годы, частота гипокальциемии у
новорожденных детей очень высока. Как указывает Шабалов Н.П. (2004),
гипокальциемию в течение первых двух дней жизни можно выявить примерно у 30%
недоношенных или детей, родившихся в асфиксии (как правило, смешанной, т. е.
асфиксии, развившейся на фоне внутриутробной гипоксии) и у 50% детей – от
матерей с инсулинзависимым сахарным диабетом. Примерно такие же данные приводят
Берман Р.Е. и Клигман Р.М. По их данным, у трети детей, родившихся
в тяжелой асфиксии, в первые дни жизни можно обнаружить гипокальциемию. Согласно
данным Зилва Д.Ф. и Пэннела П.Р. (1988), гипокальциемия развивается при любом
тяжелом состояния в любом возрасте. По нашим данным (Иванов Д.О., 2002),
гипокальциемия зарегистрирована у значительного количества новорожденных с
инфекционно-септическими заболеваниями (см. таблицу 153).
Таблица 153. Частота гипокальциемии у новорожденных с
инфекционно-септическими заболеваниями (Иванов Д.О., 2002)
|
Показатель
|
Сепсис
|
Пневмония |
|
доношенные
|
масса 1500-2500 г
|
|
А (n = 31) |
Б (n = 55) |
А (n = 22) |
Б (n = 29) |
n = 62
|
|
(% детей, имеющих данный признак)
|
|
Показатели в первые 72-96 часов жизни
|
|
Гипокальциемия < 0,85 ммоль/л ионизир. Са++ |
6,41, 2
|
48,6
|
13,81,2
|
51,03
|
32,0
|
|
Показатели в разгар инфекционного процесса
|
|
Гипокальциемия < 0,85 ммоль/л ионизир. Са++ |
70,41, 2
|
43,23
|
78,21
|
51,03
|
3,2
|
Примечание. А – гипоэргический вариант сепсиса. Б –
гиперэргический вариант сепсиса. 1 – p < 0,05 – между вариантом А сепсиса и
вариантом Б сепсиса; 2 – p < 0,05 между вариантом А сепсиса и пневмонией; 3 –
p < 0,05 между вариантом Б сепсиса и пневмонией.
При этом гипокальциемия, потребовавшая коррекции, судя по уровню
ионизированного кальция, в начале заболевания в 2 раза чаще встречалась у детей
с гиперэргическим вариантом сепсиса новорожденных по сравнению с другими
группами больных (см. рисунки 82-83). Вероятно, это связано с рядом причин.
Во-первых, у детей с гиперэргическим вариантом сепсиса чаще
развивалась легочная гипертензия, для терапии которой стандартно используется
назначение гидрокарбоната натрия, приводящего к «защелачиванию» плазмы крови, а
известно, что в щелочной среде нарушается
процесс диссоциации кальция и возникает гипокальциемия, судя по
уровню ионизированного кальция, который и регистрируется современными приборами,
приводящая к нарушениям сердечного ритма.
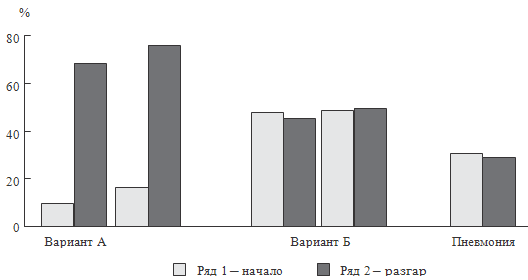
Рисунок 82. Частота гипокальциемии у доношенных (левая пара
столбцов) и недоношенных (правая пара столбцов) новорожденных с неонатальным сепсисом и
пневмонией
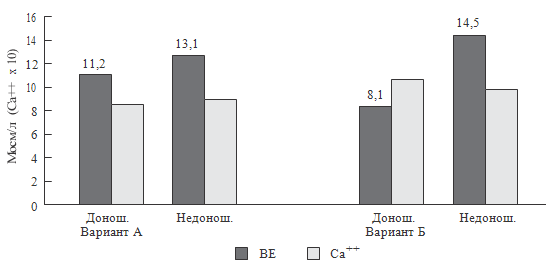
Рисунок 83. Метаболический ацидоз и уровень ионизированного кальция
в разгар септического процесса при двух вариантах сепсиса
Во-вторых, у детей с сепсисом результаты проведенных многочисленных
исследований в последние годы указывают на усиленную секрецию прокальцитонина,
предполагаемого маркера сепсиса. В связи с этим необходимо отметить, что у
большинства детей с сепсисом имелись нарушения пищеварения, имеющие, вероятно,
сложный генез, но не исключена и роль кальцитонина в этих нарушениях, как
известно, тормозящего секрецию гастрина.
В-третьих, у больных данной группы возможны множественные
гормональные дисфункции, включающие также задержку секреции паратиреоидного
гормона и недостаточную чувствительность тканей к паратгормону.
В-четвертых, возможно также нарушение всасывания кальция, связанное
с ишемией почек (снижение кальцитриола).
В-пятых, поражение печени у больных с сепсисом приводит к
понижению образования 25-гидроксихолекальциферола (25(ОН)D ).
В-шестых, как известно, ишемия кожи, особенно при септическом шоке,
приводит к снижению образования холекальциферола.
В разгар процесса произошли кардинальные изменения у детей всех
обследованных групп (см. рисунки 82-83). Так, например частота встречаемости
гипокальциемии у детей, перенесших пневмонию, снизилась в 10 раз. С другой
стороны, у доношенных с вариантом сепсиса А в 10 раз увеличилось количество
детей с зарегистрированной стойкой гипокальциемией.
Вероятно, снижение частоты гипокальциемии у детей с гиперэргическим
вариантом сепсиса в разгар процесса связано с более высоким уровнем СТГ.
Интересные результаты получила Жидкова О.Н. в 1998 году (см.
таблицу 154). Транзиторная гипокальциемия в раннем неонатальном периоде (уровень
общего кальция в сыворотке крови менее 2 ммоль/л) среди здоровых новорожденных
была выявлена у 82%. При этом выраженная гипокальциемия (общий кальций менее
1,75 ммоль/л) отмечалась у 32%. Интересно, что не было обнаружено повышения
частоты гипокальциемии у детей, перенесших асфиксию, по сравнению со здоровыми
новорожденными. В этой группе гипокальциемия встречалась у 25% новорожденных.
Таблица 154. Показатели уровня кальция в сыворотке крови
новорожденных детей в первые 48 часов жизни (Жидкова О.Н., 1998)
|
Группы детей
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
|
показатель, время определения |
M±m |
M±m |
M±m |
M±m |
M±m |
M±m
|
M±m |
|
Са ммоль/л |
при рождении |
2,21±0,05 |
2,04±0,11 |
2,35±0,17 |
2,30±0,09 |
2,17±0,15 |
2,27±0,07 |
2,24±0,09 |
|
24 часа жизни |
1,81±0,05 |
1,98±0,06 |
1,93±0,07 |
1,98±0,09 |
1,80±0,08 |
1,86±0,1 |
1,89±0,08 |
|
48 часов жизни |
1,95±0,03 |
1,97±0,04 |
1,97±0,01 |
2,06±0,07 |
1,98±0,03 |
2,0±0,06 |
2,04±0,01 |
Примечание. 1 – здоровые дети; 2 – клинически здоровые дети
от матерей с гестозом; 3 – дети, перенесшие тяжелую острую асфиксию; 4 – дети,
перенесшие острую асфиксию средней степени тяжести; 5 – дети, перенесшие
сочетанную асфиксию (острую тяжелую на фоне хронической внутриутробной); 6 –
дети, перенесшие сочетанную асфиксию (острую среднетяжелую на фоне хронической
внутриутробной); 7 – дети, перенесшие хроническую внутриутробную гипоксию.
По данным Козловой Л.В. и соавт. (2005), факторами риска развития
кальциевой недостаточности у новорожденных детей являются: возраст беременной
женщины более 30 лет, наличие хронической патологии желудочно-кишечного тракта,
курение женщин, гестоз беременных, отсутствие адекватной витаминно-минеральной
поддержки и низкий уровень сывороточного кальция к концу беременности (менее
2,25 ммоль/л). Интересно, что дети, рожденные от матерей с низким уровнем
кальция, имеют не только достоверно низкое содержание кальция в крови, но и
низкое содержание остеокальцинина, метаболитов витамина D (кальцидола). Таким
образом, дети с гипокальциемией имеют сочетанные нарушения минерального обмена,
и пониженное содержание кальция можно рассматривать как маркер изменения этого
обмена. Те же исследователи (Крутикова Н.Ю. и соавт., 2005) установили прямую корреляционную зависимость показателей
роста и массы тела у грудных детей от уровня сывороточного кальция при рождении:
у новорожденных, имеющих уровень кальция в крови менее 2,05 ммоль/л, достоверно
чаще в возрасте 6 месяцев встречаются дисфункция вегетативной нервной системы и
изменения со стороны костномышечной системы.
Классификация
У большинства больных за развитие гипокальциемии могут быть
ответственными шесть основных механизмов:
1) отсутствие паратиреоидного гормона;
2) нарушение метаболизма витамина D или снижение уровня магния,
что делает кости резистентными к воздействию паратгормона;
3) генетическое нарушение, известное под названием «псевдогипопаратиреоидизм»,
при котором органы-мишени не реагируют на действие паратиреоидного гормона;
4) уменьшение всасывания кальция из желудочно-кишечного тракта;
5) перемещение кальция между различными пространствами организма;
6) повышенная экскреция кальция с мочой.
Причины гипокальциемии (Slatopolsky E., 1987)
I. Гипокальциемия вследствие низкого уровня ПТГ в крови или его
отсутствия
а) Гипопаратиреоидизм:
– врожденный
– идиопатический
– синдром Ди Георге
– после хирургического вмешательства
– инфильтрация паращитовидных желез при злокачественных процессах
или амилоидозе
б) Транзиторный гипопаратиреоидизм:
– у новорожденных
– после аденомэктомии паращитовидной железы
в) Недостаточность магния.
II. Гипокальциемия вследствие уменьшения мобилизации кальция из
кости
а) Недостаточность витамина D:
– уменьшение поступления с пищей
– уменьшение всасывания (патология желудочно-кишечного тракта)
– частичная гастрэктомия
– анастомоз кишечника
– спру
– недостаточность поджелудочной железы
б) Недостаточность 25 (ОН)D :
– тяжелая патология печени
– билиарный цирроз
– амилоидоз
– прием противосудорожных препаратов
– нефротический синдром
в) Недостаточность 1,25 (ОН) D :
– поздняя стадия почечной недостаточности
– резко выраженная гиперфосфатемия
III. Гипопаратиреоидизм
г) Псевдогипопаратиреоидизм, типы I и II
д) Недостаточность магния
IV. Гипокальциемия вследствие уменьшенного всасывания кальция из
желудочнокишечного тракта
а) Недостаточность витамина D и его метаболитов
IV. Гипокальциемия вследствие перераспределения кальция между
различными пространствами организма
а) Гиперфосфатемия б) Введение цитратов в) Введение ЭДТА
V. Смешанные состояния
а) Панкреатит
б) Интоксикация колхицином
в) Фармакологические дозы кальцитонина г) Введение митрамицина
В настоящее время, к сожалению, не существует общепринятой
классификации неонатальных гипокальциемий. Причины, приведшие к развитию
гипокальциемий у новорожденных, могут быть разделены на 3 большие группы.
Во-первых, состояния, вызванные нарушением обмена витамина D. Чаще всего это
обусловлено уменьшением его поступления, снижением его активации или повышенными
потерями. Во-вторых, связывание ионов кальция при большом числе патологических
процессов (например, переливание цитратной крови или ее компонентов при
гемодиализе, использовании АИК, после заменных трансфузий и т.д). В-третьих, все
заболевания или состояния, сопровождающиеся дефицитом паратиреоидного гормона,
возникающие при прямом повреждении околощитовидных желез или угнетении их
функции при тяжелых заболеваниях (сепсис) или метаболических нарушениях (гипои
гипермагниемии). Аnast C.S. (1991) предлагает выделять следующие категории
неонатальных гипокальциемий:
I. Ранняя гипокальциемия новорожденных (развивающаяся в первые 48
часов жизни). Она встречается у следующих групп детей:
– недоношенных;
– больных новорожденных (перенесших асфиксию и т.д.) или
родившихся в результате патологических родов или беременности;
– от матерей, больных сахарным диабетом;
– введение беременной препаратов магния, особенно в родах.
II. Поздняя гипокальциемия новорожденных (развивающуюся к концу
первой недели жизни), которая обычно бывает у следующих групп детей:
– вскармливаемых смесями с высоким содержанием фосфатов;
– родившихся от матерей с тяжелым дефицитом витамина D во время
беременности;
– родившихся от матерей с гиперпаратиреоидизмом;
– новорожденных с гипомагниемией;
– первичном гипопаратиреоидизме.
III. Связанные с терапией (могут возникать в любое время). Обычно
это бывает при следующих терапевтических вмешательствах:
– проведении фототерапии;
– трансфузиях крови с кальцийсвязывающими (цитрат) консервантами;
– индуцированную фуросемидом;
– переливании жировых эмульсий (интралипидом);
– индуцированные переливанием соды;
– у новорожденных с заболеваниями почек (могут возникать в любое
время).
Патогенез
В патогенезе ранней гипокальциемии новорожденных отводят роль
нескольким факторам, каждый из которых играет некоторую роль у различных групп
больных, хотя выделить из них ведущий не представляется возможным.
Во-первых, отмечают (David et al., 1991) снижение секреции
паратиреоидного гормона и низкий его синтез околощитовидными железами в ответ на
гипокальциемию, особенно у недоношенных. Вероятно, у недоношенных новорожденных
имеется снижение чувствительности тканей к паратгормону.
Во-вторых, нарушенный метаболизм витамина D. Например, установлено
нарушение превращения витамина D в 25 гидроксиD в печени у новорожденных. Однако
присутствие при гипокальциемии у недоношенных новорожденных нормальных уровней
25 и 1,25 подчеркивают, что этот фактор не является единственным и/или основным
в развитии гипокальциемии у недоношенных (Glorieux et al., 1991).
В-третьих, важным этиологическим фактором при гипокальциемии
является высокая секреция кальцитонина у недоношенных детей. Обнаружена
корреляция между гестационным возрастом и уровнем сывороточного кальцитонина.
Такой же механизм развития гипокальциемии у детей, рожденных от матерей, больных
сахарным диабетом.
В-четвертых, у детей, перенесших асфиксию, выявлен высокий уровень
кортизола и катехоламинов, снижающих эффект витамина D на всасывание кальция в
кишечнике.
В-пятых, прекращение регулярного поступления кальция через плаценту
(в течение третьего триместра беременности плод получает по меньшей мере 140
мг/кг/сут. элементарного кальция через сосуды пуповины) и повышенную потребность
в нем у новорожденных, особенно у недоношенных (см. таблицу 155), как на важные
этиологические факторы гипокальциемии, указывает Шабалов Н.П. (2004).
Таблица 155. Потребности в кальции (мг/кг/сутки) (Шабалов Н.П.,
2004)
|
Возраст
|
Потребности
|
|
Взрослые |
5-8
|
|
Дети дошкольного и школьного возраста |
25-30
|
|
Дети до 1 года |
50-60
|
|
Доношенные новорожденные |
70-75
|
|
Недоношенные с массой тела менее 1000 г |
180-225
|
В патогенезе поздней неонатальной гипокальциемии важную роль
отводят дефициту витамина D, фосфатов и кальция в питании. Так, в 1 литре
женского молока содержится всего 25 МЕ витамина D, 150 мг фосфора, 300-350 мг кальция, хотя
потребности у новорожденных, особенно недоношенных, как мы указывали, гораздо
выше. Гиперфосфатемия, например при искусственном вскармливании (даже в
современных искусственных смесях (на основе коровьего молока) содержится
повышенное количество фосфора), играет достаточно важную роль в развитии поздней
неонатальной гипокальциемии. Установлена связь между высоким уровнем фосфора в
плазме и уровнем кальция. Считают (Fakhraee et al., 1980), что связано это с
уменьшением скорости клубочковой фильтрации в неонатальный период. Особенно
актуален этот механизм при почечной недостаточности, когда снижена экскреция
фосфатов.
Некоторые исследователи (Cockburn E. et al., 1980) подчеркивают
важную роль низкого уровня витамина D у беременных в происхождении поздних
неонатальных гипокальциемий.
Это приводит к нарушению образованию 1,25 (ОН) D и, как следствие,
нарушению всасывания кальция. Аналогичный механизм выявлен у недоношенных детей.
Единственное, что первичным инициирующим механизмом у них является снижение активности
α1-гидроксилазы.
У всех детей, рожденных от матерей, больных гиперпаратириозом,
выявляется гипокальциемия в первые 3 недели жизни.
Кроме того, как практически любое обменное нарушение, в том числе и
гипокальциемия, может быть обусловлена иатрогенными причинами. Например, при
лечении гидрокарбонатом натрия (содой) и развитием метаболического алкалоза. Как
мы уже указывали, доля ионизированного кальция от уровня общего кальция обратно
пропорциональна рН сыворотки крови. Поэтому у детей с алкалозом даже при уровне
общего кальция выше 1,75 ммоль/л может иметь место снижение уровня
ионизированного кальция и, как следствие, развитие гипокальциемии.
Хорошо известно, что гипокальциемия является частым осложнением
гемотрансфузий или переливания препаратов крови. Различные консерванты, например
цитрат натрия, образуют с кальцием нейтральные растворимые комплексы, в
результате чего количество ионизированного кальция может значительно снижаться,
а уровень общего при этом меняется незначительно. Интересно (Гомелла Т.Л.,
Каннигам М.Д., 1995), что через несколько часов после гемотрансфузии цитрат
превращается в бикарбонат и может приводить к алкалозу, усиливающему
гипокальциемию. Данное состояние получило название «цитратная интоксикация».
Указывают (Вейн А., 1997), что ее развитие возможно при переливании больших
объемов крови или плазмы за короткое время (более 0,25 /кг/мин). При этом
возникают нарушения гемодинамики (артериальная гипотония, тахикардия) с
выраженными изменениями ЭКГ (удлинение интервала QT, расширение комплекса QRS).
При прогрессировании интоксикации отмечается снижение сократительной функции
сердца и сердечная недостаточность. Для подтверждения диагноза необходимо
определение уровня ионизированного кальция в сыворотке крови.
Применение мочегонных средств, особенно фуросемида, приводит к
гиперкальциурии, приводящей к гипокальциемии.
Клиника
Клинические проявления гипокальциемии у больных, в том числе и
новорожденных детей, широко варьируют. Более того, как хорошо известно (Шабалов
Н.П., 2004), прямого соответствия между уровнем кальция в сыворотке крови и
клинической симптоматикой нет.
У части детей особенно ранняя гипокальциемия является лабораторной
находкой без всякой клинической симптоматики. Как правило, признаки
гипокальциемии, особенно у новорожденных, крайне неспецифичны: карпопедальный
спазм, симптом Хвостека, феномены Люста, Труссо и т.д. могут отсутствовать. К
наиболее типичным симптомам гипокальциемии относят:
– раздражительность, гиперестезия, пронзительный раздраженный
неэмоциональный высокочастотный крик;
– повышенная нервно-рефлекторная возбудимость (высокие
сухожильные рефлексы, мышечные подергивания, тремор, нарушения мышечного тонуса). В
наиболее тяжелых случаях возможно развитие судорог, как правило, тонических;
– нарушения дыхания (ларингоспазм, инспираторный стридор,
тахипноэ с втяжением межреберных промежутков). В наиболее тяжелых случаях возможны
повторяющиеся приступы апноэ;
– нарушения со стороны сердечно-сосудистой системы (тахикардия
с периодами цианоза, артериальная гипотония). В наиболее тяжелых случаях
возможно развитие сердечной недостаточности;
– нарушение со стороны ЖКТ (рвота, нарушение перистальтики
кишечника, растяжение живота, желудочно-кишечное кровотечение). В наиболее тяжелых
случаях клиника, напоминающая развитие кишечной непроходимости.
Диагностика
На рисунке 84 представлен алгоритм дифференциальной диагностики при
синдроме гипокальциемии.
При риске развития гипокальциемии измеряют уровень общего, а лучше
ионизированного кальция в крови у детей из групп риска. У больных и недоношенных
новорожденных, особенно с экстремально низкой массой тела при рождении, уровень
кальция должен быть обязательно измерен через 12, 24 и 48 часов после рождения.
Как видно из рисунка 84, при длительной гипокальциемии определяют
уровни общего белка (альбумина), фосфора, магния, натрия, калия, глюкозы,
креатинина, рН, кальцитонина в сыворотке крови и паратгормона в плазме.
Далее, при неустановленной причине гипокальциемии больные, как
правило, требуют более углубленного обследования:
– определения метаболитов витамина D в крови;
– проведения функциональных проб;
– рентгенологического исследования грудной клетки и костей.
Например, отсутствие тимуса на рентгенограмме грудной клетки – признак синдрома Ди
Джорджи. Деминерализацию костей можно достоверно установить с помощью оценки
рентгенограмм ребер и длинных трубчатых костей в динамике. Например, о рахите
свидетельствуют остеопороз и бокаловидная деформация метафизов, более
выраженные в коленных суставах и передних концах ребер;
– денситометрическое исследование костей;
– исследование функций почек и ЖКТ;
– неврологическое обследование.
Потери кальция с мочой можно определить либо проведением пробы
Сулковича или измерением его концентрации в суточной моче. Соотношение кальций:
креатинин (по данным определения их концентрации с помощью индикаторных полосок
бумаги) более 0,21-0,25 свидетельствует о гиперкальциурии. О гиперкальциурии
свидетельствует также содержание кальция в суточной моче более 4 мг/кг/сут.
Определенную помощь в диагностике гипокальциемии может сыграть ЭКГ:
удлинение интервала Q-T более 0,25 с, возникновение аритмий.
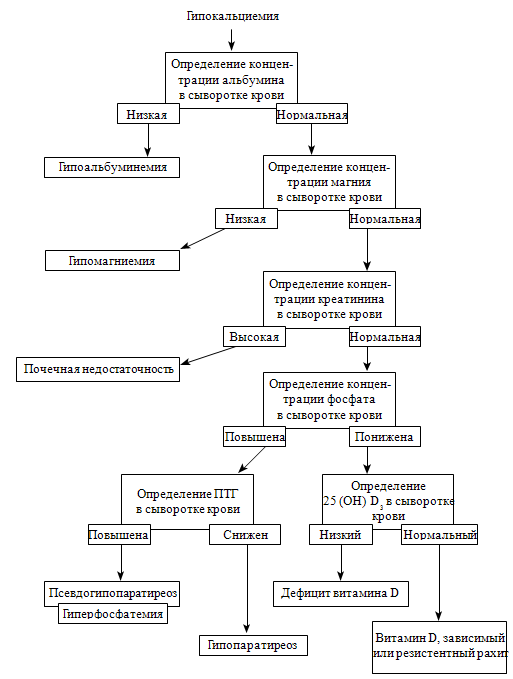
Рисунок 84. Алгоритм дифференциальной диагностики при синдроме
гипокальциемии (Лисс В.Л. и соавт., 2003)
Лечение
Бессимптомная гипокальциемия. У недоношенных детей (если нет
возможности кормить ребенка специальной смесью для недоношенных) назначают 10%
глюконат кальция
5,0-10,0 мл/кг/сут внутрь или в/в (содержание ионизированного
кальция в различных лекарственных формах (см. таблицу 156).
Таблица 156. Характеристика препаратов кальция (Лисс В.Л. и соавт.,
2003)
|
Препараты
|
Содержание кальция (мг/мл)
|
Содержание кальция
(мг/г преп.)
|
|
Растворы для внутривенного введения или приема
внутрь
|
|
Кальция хлорид 10% |
36
|
-
|
|
Кальция глюконат 10% |
9
|
|
Кальция лактат 10% |
13
|
|
Таблетированные препараты
|
|
Кальция цитрат |
-
|
210
|
|
Кальция карбонат |
400
|
|
Кальция глюконат |
90
|
|
Кальция лактат |
130
|
Ведение начинают с низкой дозы, увеличивая ее при необходимости.
Внутривенно препарат вводят в виде длительной инфузии в течении 24 часов. После
устранения причины гипокальциемии дозу кальция постепенно снижают в течение 48
часов. Как показывает клиническая практика, если гипокальциемия протекает
бессимптомно, то не требует срочной терапии. Обращаем внимание, что быстрая
коррекция бессимптомной гипокальциемии зачастую более опасна, чем сама
гипокальциемия, поэтому большинство неонатологов, если выявляется лишь
умеренное снижение уровня кальция в сыворотке крови и клиника гипокальциемии
отсутствует, предпочитают назначать препараты кальция внутрь. Связано это с тем,
что внутривенное введение препаратов кальция, особенно в дозе больше чем 20-30
мг/кг, вызывает большое количество нежелательных эффектов. Наиболее часто
возникают:
1. Струйное (микроструйное) введение кальция, особенно через
пупочную вену, может приводить к нарушениям сердечного ритма или аритмиям. Скорость
инфузии растворов кальция не должна превышать 1 мл/мин. Новорожденным детям,
получающим растворы кальция парентерально, необходим мониторинг сердечной
деятельности и гемодинамики.
2. При введении через пупочные сосуды (вену или артерию) растворы кальция
могут вызвать некрозы печени и/или сосудов печени.
3. Растворы кальция повышают частоту спазмов сосудов и, как
следствие, изменение центральной гемодинамики с резкими изменениями артериального
давления, что может приводить к развитию внутричерепных кровоизлияний,
особенно у недоношенных детей.
4. Введение растворов кальция увеличивает частоту
некротизирующего колита, особенно при внутриартериальном введении.
5. Попадание растворов кальция в окружающие ткани вызывает
тяжелый некроз.
6. Растворы кальция нельзя смешивать с бикарбонатом натрия, поскольку при
этом выпадает осадок СаСО3.
Заметим, что указанные осложнения относятся ко всем
кальцийсодержащим растворам!
Гипокальциемия с выраженными клиническими проявлениями (судороги,
нарушения сердечного ритма):
1. Болюсно внутривенно вводят 10% раствор глюконата кальция
1,0-2,0 мл/кг, т.е.10-20 мг/кг.
В европейских странах (Великобритании, Германии и т.д.) чаще
используют более низкие дозы (1,0-1,5 мл/кг). Максимальная доза – 5,0 мл для
недоношенных, 10,0 мл для доношенных новорожденных. Раствор вводят со
скоростью не более 1,0 мл/мин, мониторируя показатели центральной
гемодинамики, сердечный ритм, наблюдая ребенка на наличие признаков
экстравазации. При наличии указанных осложнений введение немедленно
прекращают. Если гипокальциемия не купирована, то можно повторить введение
препарата через
15-30 минут. Микроструйное непрерывное введение (в изотоническом
растворе хлорида натрия или 5% глюкозы) не имеет преимуществ перед
одномоментным струйным введением при лечении ранней неонатальной
гипокальциемии. Если введение глюконата кальция не сопровождается введением
фосфора, большая часть кальция выводиться с мочой (Гомелла Т.Л., Каннигам М.Д., 1995). При введении в
периферическую вену нельзя допускать попадание препарата в окружающие ткани.
2. После устранения гипокальциемии (введением насыщающей дозы) назначают
поддерживающую дозу кальция исходя из физиологической потребности
(см. таблицу 155). При этом нельзя добавлять глюконат кальция в какие-либо
растворы, содержащие бикарбонаты, сульфаты или фосфаты или вводить его
внутримышечно. Раствор глюконата кальция можно добавлять в питательную смесь,
при этом, как правило, кормление начинают с пищи с низким содержанием фосфатов
– грудного молока, смеси Similac. За рубежом обычно в первые двое суток при
пероральном назначении назначают дозу, в 4 раза превышающую внутривенную.
Например, 4,0 мл/кг сиропа Calcium-Sandoz (Neonatal formulary,
2000). Этот сироп содержит глюбионат и лактобионат кальция (22 мг
(0,54 ммоль) кальция в 1,0 мл). Необходимо помнить, что всасывание кальция в
кишечнике зависит от множества факторов (заболеваний ЖКТ, кислотности, наличия
в пище веществ, связывающих кальций, химического состава пищи и т.д.). Так,
витамин D, фосфаты, лактоза, белки обычно усиливают всасывание кальция из
желудочно-кишечного тракта, в то время как жиры снижают его. Так, несмотря на
то что карбонат кальция содержит максимальное количество элементарного кальция
по сравнению с другими препаратами, всасывается менее 5% кальция,
содержащегося в нем. Максимальное поступление кальция в кровь отмечают после
приема растворов хлорида и глюконата кальция (Лисс В.Л. и соавт., 2003).
Поэтому при лечении необходим динамический контроль уровня кальция в крови.
Более того, нельзя забывать о том, что большое количество заболеваний влияют
на всасывание кальция из ЖКТ, а следовательно, на его уровень в сыворотке
крови. Плохое всасывание кальция обнаруживается при острых и хронических
заболеваниях почек, гломерулонефрите, нефротическом синдроме, после частичной
гастрэктомии и резекции больших сегментов тонкой кишки. Наоборот, увеличенная
абсорбция его наблюдается при гипервитаминозе D, гиперфункции околощитовидных
желез, остеопетрозе, идиопатической гиперкальциурии и гиперкальциемии в раннем
возрасте (Бауман В.К., 1977; De Grazia J.A., 1971).
При отсутствии других нарушений лечение гипокальциемии даже с
выраженными клиническими проявлениями занимает не более 4-5 суток. Каждые 12-24
часа дозу препарата корректируют в зависимости от уровня кальция в сыворотке
крови.
Характеристика препаратов витамина D, использующихся в
педиатрической практике, в том числе для лечения поздней неонатальной
гипокальциемии и профилактики рахита у недоношенных, представлены в таблице 157.
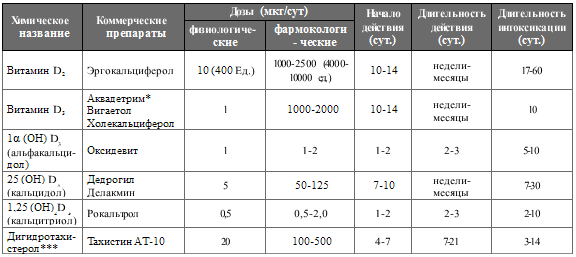
Таблица 157. Характеристика препаратов витамина D (Лисс В.Л. и
соавт., 2003)
Гиперкальциемия
Гиперкальциемия представляет собой стойкое повышение уровня
кальция в крови более 3,0 ммоль/л (у доношенных новорожденных более 2,74 ммоль/л и у
недоношенных более 2,5 ммоль/л), если показатели сывороточных белков находятся в
пределах нормы.
Существует три основных патогенетических механизма, приводящих к
развитию гиперкальциемии:
1) наиболее частый – повышенная мобилизация кальция из кости;
2) повышенное всасывание кальция из желудочно-кишечного тракта;
3) снижение экскреции кальция с мочой.
Причины гиперкальциемии
I. Гиперкальциемия на фоне повышенной мобилизации кальция из
кости:
а) Онкогенного происхождения:
– метастатическая
– неметастатическая – фактор, активирующий остеокласты (ФАО)
– простагландины (PgE2)
б) Эктопический гиперпаратиреоидизм:
1. Первичный:
– аденома
– гиперплазия
– новообразования
2. Вторичный:
– множественные эндокринные заболевания
– тип I – опухоли гипофиза и поджелудочной железы
– тип II – медуллярная карцинома щитовидной железы и
феохромоцитома
в) Иммобилизация. г) Гипертиреоидизм
д) Интоксикация витамином D
е) Почечная патология
– хроническая почечная недостаточность
– после трансплантации почки
– диуретическая фаза острой почечной недостаточностия
ж) Диуретики тиазидового ряда з) Интоксикация витамином А
II. Гиперкальциемия вследствие повышенного всасывания кальция из
желудочногокишечного тракта:
а) Саркоидоз
б) Интоксикация витамином D
в) Молочно-щелочной синдром
III. Гиперкальциемия вследствие снижения почечной экскреции
кальция:
а) Диуретики тиазидового ряда
IV. Смешанная группа:
а) Надпочечниковая недостаточность б) Туберкулез
в) Бериллиоз
г) Диспротеинемии д) Полицитемии
е) Усиленное питание
Что касается новорожденных детей, в своей монографии «Неонатология»
Шабалов Н.П. (2006) среди наиболее частых причин неонатальных гиперкальциемий
указывает следующие:
1) иатрогенные гиперкальциемии (обращаем внимание, что в эту
группу входят гиперкальциемии, вызванные не только избыточным введением кальция, но
и передозировкой диуретиков тиазидового ряда и витамином D);
2) врожденный первичный гиперпаратиреоидизм;
3) идиопатическая инфантильная гиперкальциемия;
4) синдром Уиллиамса (Williams syndrome);
5) некрозы подкожной жировой клетчатки;
6) гиперпростагландинемия, Е-синдром;
7) тяжелая инфантильная гипофосфатазия;
8) гипофосфатемический рахит недоношенных;
9) семейная доброкачественная гипокальциурическая
гиперкальциемия.
Там же он подробно описывает этиологию, патогенез, клинику этих
форм, поэтому считаем возможным на этом не останавливаться. Единственное, что
считаем необходимым отметить, что все описанные нозологические формы
укладываются в три патогенетических механизма, описанных выше, а при некоторых
клинических состояниях, при функционировании одного или нескольких этих
механизмов, развивается компенсаторная адаптация, и гиперкальциемии может не
быть, по крайней мере, выраженных клинических проявлений. Например, при
идиопатической гиперкальциурии вследствие усиленного всасывания кальция из
желудочнокишечного тракта, повышенная экскреция кальция с мочой может
препятствовать развитию гиперкальциемии. С другой стороны, при
гиперпаратиреоидизме включение всех трех механизмов (повышенная резорбция кости,
увеличенное всасывание из желудочно-кишечного тракта и сниженная почечная
экскреция кальция) приводит к развитию гиперкальциемии.
Клиника
Клиника гиперкальциемии очень полиморфна и у разных больных может
проявляться поразному. Легкая гиперкальциемия может протекать полностью
бессимптомно и обнаруживается лишь при рутинном биохимическом исследовании
крови; но гиперкальциемия может быть и настолько тяжелой, что может привести к
летаргии, коме, смерти. Более того, наиболее часто клиника зависит от скорости
развития гиперкальциемии: чаще всего манифестирует и тяжелее протекает
гиперкальциемия, развивающаяся остро.
Среди клинических проявлений гиперкальциемии можно выделить
следующие:
1. Общие: апатия, сонливость, слабость, угнетение ЦНС.
2. Сердечно-сосудистые: аритмии, гипертензия, при длительном течении,
обычно наследственных заболеваниях – кальцификация сосудов. На ЭКГ –
укорочение интервала QT. Если концентрация кальция в сыворотке крови превышает
3,75 ммоль/л (15 мг%), то возникает опасность внезапной остановки сердца.
Поэтому гиперкальциемия такой степени всегда требует неотложного лечения.
3. Почечные: полиурия, жажда, гиперкальциурия, нарушение
концентрации мочи, при длительном течении – нефрокальциноз, образование камней, почечная
недостаточность.
4. Желудочно-кишечные (кальций стимулирует секрецию гастрина, а
следовательно, образование кислоты в желудке): анорексия, тошнота, рвота,
запоры, боли в животе, возможно образование язв желудка и двенадцатиперстной
кишки.
5. Нервно-психические и мышечные (высокая концентрация
свободного ионизированного кальция угнетает нервно-мышечную возбудимость как
поперечнополосатой, так и гладкой мускулатуры): головная боль, кома, миалгии,
мышечная гипотония, артралгии. В тяжелых случаях – судороги.
При наследственных заболеваниях или длительном течении: лентовидная
кератопатия, периартикулярная кальцификация, кальцификаты внутренних органов.
Обычно при гиперкальциемии отмечаются и другие нарушения обмена:
метаболический алкалоз, гипохлоремия и гипокалиемия.
Лабораторная диагностика
1. Определение общего и ионизированного кальция.
NB. Необходимо помнить о влиянии ацидоза и гипопротеинемии, поэтому
обязательным является определение КОС, уровня белка и белковых фракций.
2. Необходимо уточнить дозы кальция, фосфора и витамина D,
которые получает больной.
3. Для выявления гиперпаратиреоидизма можно определить
содержание в крови иммунореактивного паратгормона (иПТГ).
4. Определение концентрации в крови 25 гидроксивитамина D.
5. Определение уровня кальция и фосфора в моче. Например,
поскольку при гиперпаратиреоидизме реабсорбция фосфора в канальцах снижена, то
отмечается его высокое содержание в моче, а выраженная гиперкальциурия может
быть вызвана избыточным введением кальция или недостаточным введением фосфора
при нормальной дозе кальция.
6. Рентгенография. Она может помочь установить причину
гиперкальциемии. Деминирализация костей характерна для гиперпаратиреоидизма,
остеосклероз – для гипервитаминоза D.
7. ЭКГ. Для гиперкальцигистии характерно укорочение интервала
QT.
Лечение
При лечении гиперкальциемии необходимо обратить внимание на два
обстоятельства: во-первых, степень гиперкальциемии; во-вторых, лечебные
мероприятия должны быть направлены, с одной стороны, на усиление его экскреции с
мочой и/или поступление в костную ткань, что достаточно быстро может привести к
снижению его концентрации в крови, а с другой – необходимо ограничение
потребления продуктов, содержащих кальций и прекращение лечения или профилактики
препаратами витамина D.
Считают, что если у больного нет выраженных клинических проявлений
и, что особенно важно, изменений на электрокардиограмме, характерных для
гиперкальциемии, а уровень общего кальция не превышает 3,75 ммоль/л, то
настоятельной необходимости в оказании неотложной медицинской помощи нет. Однако
сразу же при обнаружении (и подтверждении гиперкальциемии) следует приступить к
проведению лечения, учитывая опасность поражения почек.
Принимают меры по регидратации больного (инфузионная терапия
кристаллоидами в режиме форсированного диуреза). В качестве мочегонных назначают
петлевые диуретики, чаще всего фуросемид в дозе 1 мг/кг 1-4 раза в сутки. Если
имеется гипофосфатемия, то назначают препараты фосфора. Некоторые исследователи,
считают, что в данной ситуации целесообразно назначение фосфата натрия (до
1,5-2,0 ммоль/кг/сут). Он, образуя в просвете кишечника фосфат кальция,
предотвращает всасывание кальция, поступающего в желудочно-кишечный тракт, и,
следовательно, удаляет кальций из организма. Тенденцию к осмотической диарее
можно свести к минимуму, растворяя фосфат в достаточном количестве воды. При
тяжелой гиперкальциемии (если концентрация общего кальция в сыворотке крови
превышает 3,75 ммоль/л и/или имеются выраженные изменения на ЭКГ) растворы
фосфатов вводят внутривенно. Их эффект основан на выпадении в осадок
нерастворимых солей кальция. Поскольку в определенной степени это осаждение
может происходить в почках, данный способ лечения теоретически связан с риском
инициирования или усугубления почечной недостаточности.
Для нормализации экскреции кальция также вводят глюкокортикоиды,
обычно преднизолон в дозе 2 мг/кг массы тела внутривенно, внутримышечно или
внутрь. Только необходимо учитывать, что действие стероидов начинает проявляться
приблизительно через 24 часа.
При угрожающих жизни состояниях кроме фосфатов внутривенно вводят
кальцитонин 5-8 ед/кг внутривенно или внутримышечно, дозу разделяют и вводят 2
раза в сутки. Он подавляет резорбцию кальция из костной ткани.
Иногда назначают этилендиаминтетрауксусную кислоту (ЭДТА) 50 мг/кг
внутрь 3 раза в сутки. Если указанное лечение оказывается неэффективным, то
имеются указания (Лисс В.Л., 2003) на необходимость назначения дифосфонатов и трилона Б (динатриевая
соль этилендиаминтетрауксусной кислоты).
При всем этом очень строго ограничивают поступление кальция с
пищей.
Считаем необходимым обратить внимание, что быстрые изменения
концентрации кальция, как и большинства внеклеточных компонентов, могут быть
опасны, поскольку для достижения электролитного равновесия по обе стороны
клеточных мембран требуется определенное время. Целью неотложной терапии должно
быть временное снижение концентрации кальция в сыворотке крови до допустимо
безопасного уровня, с тем чтобы одновременно приступить к лечению умеренной
гиперкальциемии. Слишком быстрое снижение концентрации кальция в крови может
привести к судорогам, нарушениям ритма сердца или гипотонии, хотя уровень
кальция остается в пределах (или даже выше) нормы. Медленное понижение
концентрации кальция уменьшает также опасность кальцификации почек.

