Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
5.1. Классификация и анализ причинно-следственных связей возникновения
внутрибольничных инфекций
В рыночных условиях отечественное здравоохранение воспринимается как отрасль
народного хозяйства, производящая социальные услуги в форме собственно
медицинских услуг, со всеми вытекающими их этого экономическими, правовыми и
политическими последствиями. Специфика производства медицинских услуг определяет
конечную цель – это восстановление здоровья граждан на основе современных
достижений медицинской науки и практики. В этой связи важное значение имеет
выбор современной модели управления доступностью, качеством и безопасностью
медицинских услуг, в том числе и снижение до минимума числа ятрогенных
осложнений в виде тех или иных проявлений ВБИ.
Рутинная экспертная практика, проводимая авторами публикации в течение
нескольких десятилетий, позволяет говорить о том, что для изучения причин
возникновения и распространения ВБИ необходимо использовать систему приемов и
способов, которые были бы приемлемы и эффективны в специфических условиях
отечественных ЛПУ. Затрудняет работу в этом направлении нестабильность
управления отраслью здравоохранения в целом в течение двух десятилетий,
поскольку медицинские учреждения, как и надзорные органы, длительное время
находятся в условиях перманентного реформирования. Объектами изучения
причинно-следственных связей ВБИ являются контингенты персонала и больных,
микроорганизмы и окружающая среда. Однако течение времени, международная
практика, породили и в данном, достаточно узком вопросе, проблемы терминологии и
классификации.
Проблемы терминологии ВБИ. В терминологическом пространстве
проблематики внутрибольничных инфекций произошли определенные эволюционные
изменения, которые необходимо учитывать при профессиональном общении, в научной
литературе, в организационно-методической и правовой нормативной документации
(Покровский В.И., Акимкин В.Г., Брико Н.И. и др., 2011). Одни термины сменялись
другими, ранние термины не выходили из обращения наряду с новыми, в то же время,
стали широко использоваться термины, пришедшие в отечественную медицину из
зарубежных источников, чему способствовало более раннее обращение ряда стран к
проблеме ВБИ с точки зрения выявления, регистрации, разработки вопросов
эпидемиологического надзора и профилактики. Терминологическое многообразие в
проблематике ВБИ затрудняет взаимодействие специалистов различного профиля:
эпидемиологов, врачей клинических специальностей, организаторов здравоохранения
и др. Отсутствие единого и четкого понимания предмета обсуждения способствует
неверной трактовке ситуаций и снижает эффективность деятельности по профилактике
ВБИ.
В зарубежной эпидемиологической практике в конце прошлого десятилетия широко
применялся термин «hospital-acquired infections - HAIs» (инфекции, приобретенные
в больнице) (WHO/CDS/CSR/EPH., 2002). Однако, с точки зрения зарубежных
специалистов, этот термин необоснованно ограничивался только инфекциями,
возникающими в условиях стационаров, больниц (hospitals) и не учитывал инфекции,
которые возникают при оказании медицинской помощи на догоспитальном этапе, на
этапе реабилитации, в других медицинских учреждениях (например, в отделениях
сестринского ухода, в центрах для диализа).
Это терминологическое несоответствие привело к тому, что в зарубежной
литературе появился и получил повсеместное распространение термин «health
care-associated infections - HAIs», который является единственным термином,
используемым в официальных документах ВОЗ в настоящее время. Принятый ВОЗ
перевод термина на русский язык - «инфекции, связанные с оказанием медицинской
помощи (ИСМП)» (Horan T.C., Andrus M.A., Dudeck M., 2008). Исходное определение
на английском языке, приводится в действующих руководствах Центров по контролю и
профилактике заболеваний США (CDC). Аналогичная терминология принята и ВОЗ ((McKibben
L., Horan
T., Tokars J.I.
et al., 2005).). С точки
зрения экспертов ВОЗ, изложенной в последних руководствах, ИСМП (HAIs) включает
инфекции у пациентов, персонала, посетителей и других лиц, связанные с
медицинским учреждением (Всемирная организация здравоохранения, 2009).
Отечественное определение внутрибольничных инфекций также не включает
инфекционные заболевания, возникающие у пациентов при обращении за медицинской
помощью в амбулаторно-поликлинические учреждения, в том числе и оказание
медицинской помощи на дому, хотя отдельные нозологические формы, такие,
например, как постинъекцион- ные абсцессы, подлежат официальной регистрации, а в
российской научной литературе этим инфекциям посвящен целый ряд публикаций.
Однако единого объединяющего все эти понятия термина в отечественной теории и
практике до сих пор не существовало.
Таким образом, инфекции, связанные с оказанием медицинской помощи (ИСМП),
включают: внутрибольничные инфекции (инфекции, связанные с оказанием медицинской
помощи в стационарах); инфекции, присоединяющиеся при оказании медицинской
помощи в амбулаторно-поликлинических условиях; инфекции, возникающие при
оказании медицинской помощи на дому (вне медицинского учреждения); инфекции у
медицинского персонала, вязанные с выполнением профессиональных обязанностей.
Мнение специалистов, занимающихся изучением ВБИ (ИСМП), изложено в положении
Национальной концепции профилактики инфекций, связанных с оказанием медицинской
помощи (Покровский В.И. с соавт., 2012).
Классификация ВБИ (ИСМП). Классификация внутрибольничных инфекций
является тем краеугольным камнем, на котором базируются
организационно-методические подходы к выявлению и учету инфекционных заболеваний
(пациентов и медицинского персонала), их дифференциальная диагностика,
эпидемиологический надзор и целенаправленная профилактика. В то же время это
один из дискуссионных вопросов, отражающий различные точки зрения на
структурирование ВБИ. Кроме того, классификация - относительно консервативный
аспект проблемы ВБИ (ИСМП), ее пересмотр и обновление требуют времени и
всестороннего обсуждения (Покровский В.И., Акимкин В.Г., Брико Н.И. и др.,
2011).
Современная классификация ВБИ (ИСМП) основана на существующих теоретических
представлениях о закономерностях развития эпидемического процесса ИСМП в
учреждениях здравоохранения и сложившихся в РФ организационно-методических
подходах к их выявлению, учету, регистрации, осуществлению эпидемиологического
надзора и комплекса профилактических и противоэпидемических мероприятий (Брусина
Е.Б., Рычагов И.П., 2006; McKibben L., Horan T., Tokars J.I. et al., 2005;
Edwards J.R.,
Peterson K.D.,
Mu Y. et
al., 2009).
Общим критерием для отнесения инфекций к ВБИ (ИСМП) является то, что их
возникновение связано с оказанием медицинской помощи (лечение, диагностика,
профилактика и т.п.) (рис. 5.1). «Условия оказания медицинской помощи» - это
базовый классификационный признак, на основании которого в группу ИСМП включают
инфекции, возникшие в результате оказания медицинской помощи пациентам:
в период госпитализации (внутрибольничные инфекции) (Health
care- associated
infections in
hospitals, Hospital-acquired
infections);
в амбулаторно-поликлинических условиях (Health
care-associated
infections in
outpatient departments);
в других организациях, осуществляющих медицинскую деятельность.
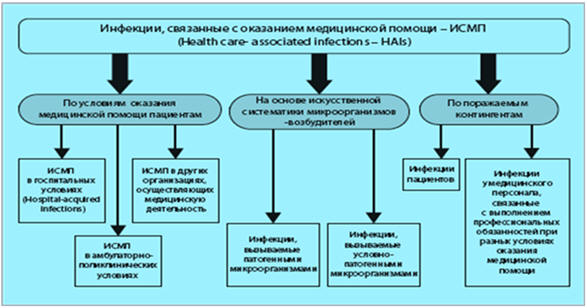
Рис. 5.1. Классификация внутрибольничных инфекций (инфекций
связанных с оказанием медицинской помощи) (Покровский В.И. с соавт., 2011)
ВБИ (ИСМП) в госпитальных условиях включают инфекции в различных типах
учреждений здравоохранения в соответствии с действующей номенклатурой. В связи с
этим признавалось важность учета эпидемиологических особенностей инфекций,
развивающихся у пациентов в условиях учреждений здравоохранения различного типа
(Шкарин В.В., Ковалишена О.В., 2009). Например, специфика медицинской помощи в
учреждениях охраны материнства и детства, определяющая клинические и
эпидемиологические особенности возникающих инфекций. Учитывая, что медицинская
помощь оказывается в различных условиях, к ИСМП относят не только случаи
инфекции, возникающие в период госпитализации, но и случаи, связанные с
оказанием медицинской помощи в амбулаторно-поликлинических условиях и при
оказании медицинской помощи на дому, в образовательных учреждениях и т.п.
Особого внимания заслуживает группа ИСМП, развивающихся в других организациях
и условиях (медико-социальных, хосписах, приютах, на улице, на этапе
транспортировки пациента в учреждение здравоохранения и т.п.)
(Санитарно-эпидемиологические правила и нормативы 2.1.3.2630 – 10., 2010).
Несомненно, что ИСМП включают и случаи инфекций у медицинских работников,
возникающие в результате их профессиональной деятельности независимо от условий.
Кроме того, не следует забывать о возможном вовлечении в эпидемический процесс
ИСМП других контингентов, в частности, ухаживающих за больными, особенно в
детских медицинских учреждениях. Лица, госпитализированные для ухода за
больными, расцениваются как пациенты. Инфекции у учащихся и сотрудников средних
и высших медицинских образовательных учреждений, занимающихся на базе
учреждения, если они связаны с профессиональной деятельностью, относятся к
группе «ИСМП у медицинского персонала».
Следует отметить, что многие вопросы построения обсуждаемой классификации
являются дискуссионными, особенно с точки зрения искусственной (ключевой)
систематики микроорганизмов ̶ возбудителей инфекции (патогенными и
условно-патогенными микроорганизмами). Хотя последняя относительна, но она
по-прежнему не устарела, имеет отражение в классификации микроорганизмов по
группам патогенности, которая изложена в современной литературе по специальности
«Микробиология» (Покровский В.И. с соавт., 2011; Минобрнауки, 2011). Выделение
групп патогенных и условно-патогенных микроорганизмов особенно значимо для ВБИ (ИСМП).
В зарубежной практике при отсутствии четкого терминологического деления ИСМП на
инфекции, вызываемые патогенными и условно-патогенными микроорганизмами, в
этиологии выделяют «сonventional pathogens» («обычные патогены»), «randitional
pathogens» («условные патогены») и «opportunistic pathogens»
(«оппортунистические патогены») (Parker
M.T., 1978).
Эпидемиологический диагноз случая ИСМП должен включать: указание
принадлежности к группе инфекций по локализации патологического процесса, с
этиологической расшифровкой, а также по условиям инфицирования, например,
«поверхностная инфекция в области хирургического вмешательства стафилококковой
этиологии (S. epidermidis), экзогенная». В зависимости от того, насколько полно
был расследован случай ИСМП, указываются источник инфекции, путь и фактор
передачи возбудителя инфекции, характер штамма (госпитальный), условия,
способствовавшие развитию ВБИ (ИСМП).
В условиях реформирования и модернизации здравоохранения происходит
увеличение объема медицинской помощи в амбулаторнополиклинических учреждениях,
развитие стационарзамещающих технологий, расширение комплекса диагностических,
лечебных и профилактических мероприятий, проводимых вне стационара.
Таким образом, при современной тенденции ВБИ (ИСМП), возникающие в условиях
амбулаторно-поликлинических учреждений, нуждаются в более углубленном изучении,
разработке и совершенствовании отличных от госпитальных
организационно-методических подходов к учету, осуществлению микробиологического
мониторинга, выявлению и оценке факторов риска, эпидемиологической диагностике,
профилактике. Требуется не просто выделение этой категории внутрибольничных
инфекций, а дальнейшая классификация с разработкой стандартов определения случая
ВБИ (ИСМП).
О риске формирования внутрибольничных инфекций. В настоящее время при
проведении экспертной работы широко используется понятие «риск», то есть речь
идет о вероятности поражения пациентов или вероятности действия чего-то в
определенных условиях. Формирование «групп риска» по ВБИ это выделение в общем
массиве пациентов той части, которая в большей мере подвержена опасности
поражения по сравнению с другими (пациенты ОРИТ, новорожденные дети и
родильницы, пациенты урологических хирургических клиник, пациенты клиник, где
широко используется полихимиотерапия и т. п.).
В качестве примера развития ВБИ у пациентов из группы риска мы приводим
вспышку гнойно-септических заболеваний, произошедшую в одном из родильных домов
г. Комсомольска-на-Амуре весной 1996 года. У пациентки, поступившей в родильный
дом для родоразрешения 27 февраля 1996 года, после операции «кесарева сечения»
развился послеоперационный эндометрит, у второй пациентки, поступившей для
родоразрешения 29 февраля 1996 года, после операции «кесарева сечения» развился
послеоперационный перитонит. Несмотря на развитие таких грозных осложнений,
родильный дом продолжал работать в прежнем режиме, анализа эпидемиологической
ситуации не проводится, и у пациенток, поступивших 1 марта, 5 марта, 6 марта, 8
марта и 12 марта 1996 года, развиваются послеродовый и послеоперационный
эндометрит и разлитой перитонит на фоне несостоятельности швов.
Только после развития тяжелых проявлений ВБИ у седьмой родильницы это
медицинское учреждение прекращает прием пациентов. Делается попытка анализа
складывающейся ситуации и выявление причин развития ВБИ. Была установлена
причина ятрогенных осложнений - применение в качестве шовного материала кетгута
в заводской упаковке со сроком годности до 1990 года, причем при
бактериологическом исследовании партии кетгута в одной из трех проб был выделен
эпидермальный стафилококк, аналогичный тому, который был изилирован из
послеоперационных ран пациенток.
Исходы лечения у всех женщин, несмотря на тяжесть проявлений ВБИ,
относительно «благоприятные». У пациенток, имевших проявления тяжелого
перитонита, проведены релапаратомии и экстирпации матки. Что касается стоимости
лечебных и других мероприятий, потребовавшихся для восстановления
функционирования родильного дома, восстановления утраченного здоровья пациенток,
то эти расходы не анализировались и были отнесены за счет общих расходов
родильного дома, который в то время финансировался из бюджета г.
Комсомольска-на-Амуре. По случаю ВБИ в родильном доме изданы «наказующие»
приказы городского отдела здравоохранения и управления здравоохранения
администрации Хабаровского края, информация о вспышке ВБИ передана в Главное
управление охраны здоровья матери и ребенка МЗ и МП РФ и во все территории
Хабаровского края. Проведены выборочные проверки сроков годности применяемого
шовного материала в ЛПУ края.
Ретроспективный анализ позволил сделать заключение, что вопросам профилактики
и распространения ВБИ в медицинских учреждениях г. Комсомольске-на-Амуре не
уделялось должного внимания. Вспышка ВБИ могла бы быть предотвращена на уровне
самоконтроля операционной медицинской сестры при анализе шовного материала
(контроль срока годности), старшей акушерки или заведующей отделением.
Распространение ВБИ после должного анализа первого случая могло ограничиться
только одним случаем ВБИ (пациентки, поступившей 27 февраля 1996 года).
Отсутствие в штате родильного дома клинического эпидемиолога еще более усугубило
сложившуюся ситуацию и привело к тяжелым последствиям для пациентов.
Структура инфекционных заболеваний находится в состоянии непрерывных
изменений. Возникают новые заболевания, получают распространение уже известные
науке заболевания, а иные, как опрометчиво считают некоторые специалисты, -
полностью искореняются. За последние несколько десятилетий мир стал свидетелем
учащения случаев заболеваний, поддававшихся ранее эффективному контролю или
встречавшихся достаточно редко, таких, как чума, туберкулез или лихорадка Эбола.
Получают более широкое распространение некоторые уже известные заболевания,
например, гепатит В. Были идентифицированы возбудители таких неизлечимых в
настоящее время заболеваний, как ВИЧ и гепатит С. Распространению указанных
заболеваний способствует ряд различных факторов: интенсивный прирост населения,
усугубление нищеты, экспансия населения в ранее недоступные районы, развитие
транспортной инфраструктуры, ведущее к ускорению распространения инфекции,
неадекватная система здравоохранения, а также отсутствие эффективных программ
профилактики инфекций. Среди инфекционной заболеваемости внутрибольничные
инфекции (ВБИ) занимают важное место (Акимкин В.Г., 2006).
Профилактика инфекций в течение длительного периода времени была направлена
на предотвращение заболеваний, возникающих в результате послеоперационного
инфицирования пациентов. В связи с появлением ВИЧ и сохраняющимися проблемами с
вирусом гепатита В, а также идентифицированными в последнее время вирусами
гепатита C и D, меры профилактики инфекций были модифицированы. В настоящее
время основное внимание уделяется сведению к минимуму риска передачи инфекции не
только пациентам, но и всем работникам медицинского учреждения , включая
технический персонал, а также жителям данной местности.
Пациенты подвергаются риску развития инфекции после проведения процедуры при
не соблюдении медицинским работником правил асептики и антисептики. Важным
является: тщательная обработка рук между процедурами, выполняемыми разным
пациентам, проведение надлежащей подготовки пациентов к процедуре, соблюдение
правил обработки медицинских инструментов и иных
предметов. Надлежащей считается обработка медицинских
инструментов и иных предметов, обеспечивающих инфекционную и иную безопасность
проведения процедур. Иногда лечащие врачи и медицинский персонал игнорируют
технологические стандарты, направленные на профилактику ВБИ. В качестве примера
приводим данные экспертизы такого случая.
Пациентка С, 79 лет, история болезни № 111, находилась на лечении в отделении
многопрофильной больницы с 19.11.2009 по 07.12.2009 с диагнозом: Полип
ректосигмального отдела толстого кишечника. Оперативное пособие 22.11.09.
Для проведения экспертизы представлена история болезни №111.
Перед экспертом поставлены следующие вопросы:
Насколько рациональной является проводимая фармакотерапия пациентке С.?
Что явилось причиной развития внутрибольничного инфицирования
послеоперационной раны?
Проведение экспертизы, осуществляется на основании выданной эксперту
государственной аккредитации №322-АКГ от 25.04.2011, Федеральной службой по
надзору в сфере здравоохранения и социального развития по направлению
«Медицинская деятельность», в части проведения экспертиз и расследований,
направленных на установление причинно-следственных связей выявленных нарушений
обязательных требований с фактами причинения вреда.
А). Проводимая фармакотерапия признана не рациональной поскольку зафиксирован
ряд отклонений от стандартных процедур:
1. Не проведена антибиотикопрофилактика внутрибольничных инфекций в рамках
исполнения Постановление Главного государственного санитарного врача РФ от 18
мая 2010 г. N 58 "Об утверждении СанПиН 2.1.3.2630-10
"Санитарно-эпидемиологические требования к организациям, осуществляющим
медицинскую деятельность" (приложение №1, раздел III,
п.п. 3.37, 3.38, 3.39, 3.40, 3.41), так как оперативное пособие было выполнено
22.11.2012. на условно-чистой раневой поверхности.
2. Итогом игнорирования рекомендаций СанПиНая стало развитие гнойно -
воспалительного процесса 25.11.2009, что зафиксировано в первичной медицинской
документации (подъем температуры до 38°С, лейкоцитоз в общем анализе крови до
10,4х 10 9 /л и назначение антибактериальной терапии двумя
препаратами).
3. Не передано экстренное извещение о случае внутрибольничной инфекции
(сокрытие факта внутрибольничного инфицирования).
4. Отсутствует протокол расследования факта ВБИ.
5. Отсутствует обоснование к назначению цефотаксима и метронидазола
25.11.2009. и назначению ципрофлоксацина 30.11.2009, а так же анальгина с
димедролом с 22.11.2009 по 04.12.2009.
Б) Проведение экспертизы было затруднено в связи с некоторыми
обстоятельствами:
1. Нарушено ведение медицинской документации (Приказ МЗ Хабаровскуого края
№63, от 03 марта 2006 г. «О совершенствовании работы врачебных
(клинико-экспертных) комиссий учреждений здравоохранения и органов управления
здравоохранением Хабаровского края» (в ред. приказов Министерства
здравоохранения Хабаровского края от 07.08.2007 N 269, от 30.07.2008 N 280)),
так в истории болезни отсутствует:
расшифровка подписей лечащего врача: 21.11.2009, 22.11.2009, 23.11. 2009,
24.11. 2009, и.т.д.
время осмотра лечащего врача 21.11.2009, 23.11.2009, 24.11.2009,
25.11.2009 и т.д.
Этапный эпикриз от 26.11.2009 не отражает динамику состояния больной и не
указана причина назначения антибактериальной терапии.
Отсутствует номер протокола оперативного вмешательства 22.11.2009.
Заключение:
- Пациентке С., 79 лет проводилась нерациональная фармакотерапия.
- Внутрибольничная инфекция развилась вследствие не выполнения обязательных
стандартных процедур – антибиотикопрофилактики и ненадлежащего ухода за
послеоперационной раной.
- Скрыт факт возникновения внутрибольничной инфекции.
- Ведение лечащим врачом медицинской документации неудовлетворительное.
Причины формирования внутрибольничных инфекций. Среди причин
возникновения и распространения ВБИ можно выделить три группы:
организационно-технические, иммунопрофилактические и дезинфектологические. В
конечном итоге, являясь комплексной проблемой современной системы производства
медицинских услуг, ВБИ являются отражением комплекса факторов, в числе которых
следующие.
Создание крупных больничных комплексов со своеобразной экологией: большой
плотностью концентрации пациентов, преимущественно ослабленных, и медицинским
персоналом, постоянно и тесно общающимся с больными; интенсивными
миграционными процессами, замкнутостью окружающей среды (палаты для больных,
кабинеты для диагностики и лечебных процедур), своеобразием микробиологической
характеристики (циркуляция ряда штаммов условно-патогенных микроорганизмов).
Формирование мощного искусственного (артифициального) механизма передачи
возбудителей инфекций, связанного с инвазивными вмешательствами, лечебными и
диагностическими процедурами, использованием медицинской аппаратуры.
Активизация естественных механизмов передачи возбудителей инфекционных
болезней, особенно воздушно-капельного и контактно-бытового, в условиях
тесного общения больных, медицинского персонала в ЛПУ.
Постоянный источник возбудителей инфекций в виде пациентов, поступающих в
стационар с нераспознанными инфекционными болезнями, лиц, у которых ВБИ
наслаивается на основное заболевание в стационаре, и медицинского персонала
(носители, больные со стертыми формами инфекции).
Широкое, подчас бесконтрольное применение антибиотиков. Не всегда
достаточно продуманная стратегия и тактика применения антибиотиков и
химиопрепаратов для лечения и профилактики заболеваний способствуют появлению
лекарственно устойчивых микроорганизмов.
Формирование внутригоспитальных штаммов большого числа микроорганизмов с
множественной лекарственной устойчивостью, обладающих селективными
преимуществами, высокой устойчивостью к неблагоприятным факторам окружающей
среды (ультрафиолетовое облучение, высушивание, действие дезинфицирующих
препаратов). Внутрибольничные штаммы сформировались у золотистого и
эпидермального стафилококков, синегнойной палочки, протея, клебсиелл,
энтеробактера, ряда сероваров сальмонелл и др.
Увеличение контингента риска - пациентов, выхаживаемых и излечиваемых
благодаря достижениям современной медицины. В прошлом эти больные считались
обреченными.
Возрастание доли пациентов, находящихся на «двух полюсах жизни», у которых
снижены защитные силы организма. Увеличение числа пожилых людей среди
пациентов отражает изменение возрастной структуры населения, увеличение
продолжительности жизни. Большое число детей раннего возраста в стационарах
связано, с одной стороны, со снижением неспецифических сил организма матерей,
а с другой - с несовершенством иммунитета у новорожденных в целом, особенно у
недоношенных детей, новорожденных с дефектами физического и психического
развития, редко выживавших в прошлом.
Снижение неспецифических защитных сил организма у населения в целом, в
силу его эволюционной неподготовленности к стремительно изменяющимся условиям
жизни в связи с бурным научно-техническим прогрессом и его теневыми сторонами
- загрязнением окружающей среды, экологическим кризисом, изменением условий
жизни населения (гиподинамия, стрессы, неблагоприятное воздействие шума,
вибрации, магнитных полей и других факторов). Тонкие механизмы защиты,
обеспечивающие поддержание постоянства внутренней среды организма и защиту от
чужеродной генетической информации, формировались на протяжении тысячелетий,
но оказались несовершенными при стремительных изменениях условий жизни за
последние 40 лет.
Все более широкое использование для диагностики и лечения сложной техники,
которая требует особых методов стерилизации. Использование приборов и
аппаратуры нередко приводит к нанесению травм слизистым оболочкам и кожному
покрову, формируя «ворота» для возбудителей инфекций.
Медленная психологическая перестройка части клиницистов, по-прежнему
рассматривающих многие ВБИ (пневмония, пиело-нефрит, воспалительные
заболевания кожи, подкожной клетчатки и др.) как неинфекционную патологию и
несвоевременно осуществляющих профилактические и противоэпидемические
мероприятия или вовсе их не проводящих.
Нарушение санитарно-гигиенического режима в ЛПУ приводит к резкому росту
заболеваемости ВБИ и возникновению вспышек, особенно это характерно для
учреждений родовспоможения, интернатных учреждений социальной защиты, где
концентрируются пациенты из групп риска.
В большинстве случаев присоединение ВБИ к основному заболеванию сводит на нет
результаты операций на жизненно важных органах, перечеркивают усилия,
затраченные на выхаживание новорожденных, увеличивают послеоперационную
летальность, влияют на уровень госпитальной летальности. Наслаиваясь на основное
заболевание, по поводу которого пациент поступает в стационар, они порождают
новые, которые в реальной ситуации следует регистрировать, как ятрогении.
Роль медицинского персонала в формировании внутрибольничных инфекций.
В настоящее время большее внимание уделяется проблеме инфицирования медицинских
работников при выполнении ими должностных обязанностей (Габриэлян Н.И., Арефиева
Л.И., Дроздова Н.Е. и др., 2007; Григорьев К.И., 2007; Государственный доклад,
2008). Уровень заболеваемости внутрибольничными инфекциями среди медработников
зависит от различных факторов: организации работы в лечебно-профилактическом
учреждении, используемых медицинских технологий и инструментов, обеспеченности
медперсонала индивидуальными средствами защиты, а также от понимания персоналом
проблемы ВБИ и риска инфицирования.
Так по данным исследования оценки санитарно-гигиенического и
противоэпидемического режима в отделениях в Краснодарского военного госпиталя,
которое включало гигиеническую оценку условий труда медицинского персонала в
2006–2011 гг. (Грушко Г.В., Линченко С.Н., Конюхов М.А., 2013) получены весьма
неоднозначные данные. В частности, опрос среднего медперсонала позволил
установить наиболее значимые факторы риска, которые могут являться причиной
развития ВБИ у медработников.
Было установлено, что 48 % медицинских работников ежемесячно отмечали
получение микротравм, связанные с нарушением целостности кожных покровов. В 95 %
случаев травмы в отделениях не учитывались, в связи с чем не проводилось
обследование рабочего места, условий труда медицинских работников, отсутствовала
экстренная превентивная противовирусная терапия. Среди причин травматизма
наиболее частыми указывались: срочность выполнения процедур (82 %),
психологическая нагрузка (61 %), нерационально оборудованное рабочее место (26
%), не использование индивидуальных средств защиты (24 %) и др.
Данные подобных исследований (Айдинов Г.Т., Швагер М.М., Митрофанова Т.В.,
1999; Григорьев К.И., 2007) показывают, что персонал медицинских учреждений и
все, кто участвует в процессе ухода, подвергаются воздействию отрицательных
факторов, поэтому в стационарных учреждениях годами нарабатываются меры контроля
и безопасности в профилактике внутрибольничных инфекций. Гораздо сложнее
предупреждать внутрибольничные инфекции в некоторых отделениях многопрофильных
клиник и медико-социальных учреждениях, основной контингент которых -
тяжелобольные пациенты старше трудоспособного возраста, входящие в высокую
группу риска инфицирования по многим причинам. Именно в таких подразделениях и
учреждениях необходима реализация алгоритмов профилактики ВБИ, поскольку
значительное влияние на распространение ВБИ оказывают факторы присущие именно
этим группам пациентов:
снижение сопротивляемости организма;
увеличение удельного веса ослабленных, пожилых пациентов;
несоблюдение правил инфекционной безопасности;
увеличение инвазивных манипуляций;
перегрузка производственных мощностей учреждений и т.д.
Резервуаром (источником) ВБИ являются руки персонала, кишечник, мочеполовая
система, кожа и слизистая оболочка, как пациента, так и персонала, а так же
пыль, вода, продукты питания, инструментарий и оборудование. Внутрибольничная
инфекция, как правило концентрируется в изделиях из резины, в приборах, где
используется вода и антисептики, аппаратах для искусственного дыхания,
инструментарии. Напомним, что такие инфекции, как золотистый стафилококк,
стрептококк А, эширехии, клебсиелла, протей, сальмонелла, синегнойная палочка,
простой герпес, гриб рода кандида, вирус гепатита А и многие другие передаются
через руки персонала. Вот почему, осуществляя уход за больным человеком в
домашних условиях или в условиях стационара, нужно в обязательном порядке
соблюдать противоэпидемический режим. Говоря об уходе за пациентами старше
трудоспособного возраста, правильно выделять четыре основных требования
противоэпидемического режима: предотвращение распространения инфекции,
соблюдение чистоты, обеспечение собственной безопасности и безопасности
пациента.
Медицинский и немедицинский персонал учреждения подвергается значительному
риску инфицирования, поскольку в своей повседневной практике они имеют дело с
потенциально инфицированным биологическим материалом. Технический персонал,
занимающийся обработкой инструментов и иных предметов, обработкой и уборкой
операционных, хирургических, инфекционных и
процедурных кабинетов, а также удалением медицинских отходов подвергаются
особому риску. Условия труда этой категории работников представляют собой
серьезную проблему там, где соответствующий персонал не обладает достаточными
знаниями и навыками, в связи с чем может не осознавать реально существующего
риска инфекции.
Справедливости ради следует отметить, что в структуре профессиональной
заболеваемости медицинского персонала по категориям заболевших первое место по
частоте заболеваний занимают средние медработники (медсестры, фельдшера) –
53,0%; врачи на втором месте – 24,5%; младший медперсонал – 10,0%; лаборанты –
3,0%. Однако, в структуре профессиональной заболеваемости медицинского персонала
по профилю медицинских учреждений, амбулаторно-поликлинические учреждения стоят
только на четвертом месте, их доля составляет менее 10,0% (Яфаев Р. X., Зуева Л.
П., 1989; Основы инфекционного контроля, 2003; Siegel J.D. et
al., 2004).
В лечебно-профилактических учреждениях распространение возбудителей ВБИ
реализуется через 5 механизмов передачи: фекально-оральный, воздушно-капельный,
трансмиссивный, контактно-бытовой (естественные) и артифициальный (Покровский
В.И., Семина Н.А., 2000). Последний (артифициальный) представляет несомненный
интерес с точки зрения формирования идеологии инфекционной безопасности
(Табл.5.1).
В настоящее время известно более 300 возбудителей, передача которых возможна
пациенту при лечебно-диагностических процедурах и медицинскому персоналу при
проведении вышеперечисленных манипуляций в условиях лечебно-профилактического
учреждения (Покровский В.И., Акимкин В.Г., Брико Н.И. и др., 2011). Инфекции в
учреждении здравоохранения на основе классификационного признака «по месту
инфицирования» подразделяются на связанныес оказанием медицинской помощи (health
care-associated
infections HAIs) и с заносом
возбудителя инфекции в учреждение здравоохранения («infections,
brought in
hospitals», «bringing
infections», «community-acquired
infections (CAIs)
of hospitalized
patients»). Указанные инфекции имеют выраженные
клинико-эпидемиологические различия, требуют выявления и учета, дифференциальной
диагностики, разных подходов к ведению эпидемиологического надзора, комплекса
профилактических и противоэпидемических мероприятий.
Имеется еще одна группа инфекций, которую следует выделять при классификации
«по месту инфицирования» ̶ внутриутробные инфекции (ВУИ) («prenatal infections,
«congenital infections»). Однако ВУИ имеют отношение только к ограниченному
контингенту - новорожденным детям, а поэтому требует отдельного обсуждения.
Таблица 5.1. Артифициальный механизм передачи возбудителей
и связанные с ним внутрибольничные инфекции (Ковалева Е.П., Семина Н.А., 1993)
| Процедуры |
Инфекции |
| I. Лечебные |
|
| 1. Трансфузии крови, сыворотки, плазмы |
Вирусные гепатиты B, C, D, ВИЧ-инфекция,
цитомегалия, сифилис, листериоз, токсоплазмоз, герпетическая инфекция,
малярия |
| 2. Инъекции подкожные, внутрикожные,
внутримышечные, внутривенные, внутрикостные |
Вирусные гепатиты B, C, D, ВИЧ-инфекция,
цитомегалия, стафилококковая, стрептококковая инфекция, инфекции,
вызываемые грамотрицательными микроорганизмами (P. Aeruginosa, протей,
энтеробактер, E. coli, клебсиеллы, серрации) |
| 3. Пересадки тканей, органов, сосудов,
костного мозга |
Те же, что и при трансфузиях и инъекциях.
Кроме того, анаэробные инфекции, кандидоз |
| 4. Операции |
Стафилококковая инфекция, инфекции,
вызываемые грамотрицательными микроорганизмами, анаэробные инфекции,
кандидоз, вирусные гепатиты B, C, D, TTV, ВИЧ-инфекция |
| 5. Катетеризация сосудов, мочевыводящих
путей |
Вирусные гепатиты B, C, D, G, TTV,
ВИЧ-инфекция, цитомегалия, сифилис, инфекции, вызываемые
грамотрицательными бактериями, стафилококками, стрептококками, анаэробные
инфекции |
| 6. Интубация |
Псевдомоноз; инфекции, вызываемые
золотистым стафилококком, стрептококком |
| II. Диагностические |
|
| 7. Взятие крови |
ВИЧ-инфекция, вирусные гепатиты B, C, D, G,
TTV |
| 8. Зондирование |
|
| 9. Скопии (эндоскопии, особенно при
эрозиях и язвах): бронхоскопия, трахеоскопия, гастроскопия, цистоскопия,
ректоскопия |
Клебсиеллезы, стафилококковая инфекция,
вирусные гепатиты B, C, D, G, TTV, кампилобактериоз, кишечные
бактериальные, вирусные инфекции, ВИЧ-инфекция |
| 10. Пункции: люмбальные, стернальные,
лимфатических узлов, органов |
Стафилококковая инфекция, инфекции,
вызываемые грамотрицательными бактериями, анаэробные инфекции, кандидоз,
вирусные гепатиты B, C, D, ВИЧ-инфекция |
| 11. Получение биоптата: тканей, органов |
Стафилококковая инфекция; инфекции,
вызываемые грамотрицательными бактериями; анаэробные инфекции, кандидоз,
вирусные гепатиты B, C, D, ВИЧ-инфекция |
| 12. Венесекции |
Стафилококковая инфекция; инфекции,
вызываемые грамотрицательными бактериями; анаэробные инфекции, кандидоз,
вирусные гепатиты B, C, D, G, TTV, ВИЧ-инфекция |
| 13. Ингаляции лечебных аэрозолей |
Легионеллезы; инфекции, вызываемые
грамотрицательными бактериями; стафилококковая, стрептококковая инфекция |
| III. Бальнеологические процедуры |
|
| 14. Лечебные души |
Легионеллезы, грибковые заболевания,
псевдомоноз, инфекции, вызываемые грамотрицательными бактериями |
| 15. Вихревые души |
|
| 16. Купание в бассейне |
|
| IV. Мануальное обследование (особенно
при эрозиях и язвах): - вагинальное - ректальное |
Трихомониаз, грибковые заболевания,
ВИЧ-инфекция, вирусные гепатиты B, C, D, G, TTV, цитомегалия |
Наряду с заносами возбудителя инфекции в учреждение здравоохранения следует
также выделить распространение возбудителя инфекции, особенно имеющего признаки
госпитального штамма, за пределы учреждения здравоохранения с образованием
территориальных эпидемических очагов (домашних, в организованных коллективах и
др.) (Санитарно-эпидемиологические правила и нормативы, 2010). Такому
распространению ВБИ способствуют манифестация инфекции после выписки пациента из
учреждения здравоохранения, этапность оказания медицинской помощи, ее
специализация и другие факторы. Дифференциальная диагностика различных видов
инфекции по месту инфицирования осуществляется в каждом конкретном случае и
применительно к данному медицинскому учреждению.
Качественное выполнение технологий инфекционной безопасности возможно при
соответствии кабинета или другого подразделения, в котором проводится
технология, санитарно-гигиеническим нормам по площади, внутренней отделке,
эффективной работе вентиляционных систем, наличии бесперебойного водоснабжения,
обеспечении стандарта оснащения кабинета, а также соответствия адекватных
дезинфектологических технологий конкретным задачам. Стандарт оснащения кабинета,
помимо медицинского оборудования, мебели, предполагает наличие дезинфекционной,
стерилизационной аппаратуры, дезинфекционных средств и кожных антисептиков,
средств барьерной защиты, прочего оснащения (емкости для дезинфекции, уборочный
инвентарь, средства для сбора и обеззараживания медицинских отходов класса "В",
средства экспресс-контроля и др.).
На пути снижения уровня резистентности микроорганизмов. Несмотря на
значительные успехи клинической микробиологии в отечественной медицине,
этиотропная, целенаправленная терапия инфекционной патологии,
по крайней мере, на начальном этапе всё равно остается эмпирической и, вероятно,
будет таковой в обозримом будущем. Основой режимов эмпирической
антибактериальной терапии являются данные о природной
чувствительности к антимикробным препаратам (АМП) наиболее
вероятных возбудителей. Однако проблема значительно осложняется
распространением, как во внебольничных, так и особенно в госпитальных условиях,
приобретенной резистентности. Естественный процесс
селекции под воздействием АМП среди микроорганизмов,
циркулирующих в человеческой популяции, устойчивых штаммов, их последующего
широкого распространения проходит в несколько этапов.
На первом этапе начинается выделения отдельными группами микробиологов
единичных устойчивых к конкретному АБП микроорганизмов.
На такие сообщения обращают внимание лишь немногочисленные профессионалы. Они
начинают целенаправленно искать подобные штаммы и изучать биохимические, а также
генетические механизмы их устойчивости. Как правило, на этом этапе к процессу
изучения этих штаммов подключается фармацевтические фирмы, которые начинают
поиск новых ЛС, способных преодолевать сформировавшуюся устойчивость.
На втором этапе, когда выделение устойчивых микроорганизмов
перестает быть редким явлением, появляются публикации о частоте
распространения резистентности. Однако широкую аудиторию
врачей-клиницистов эти публикации, как правило, не интересуют. Они живут старыми
представлениями о высокой эффективности применяемых АМП. На неудачи реализации
устаревших схем лечения они обращают внимание в тех случаях, когда уровень
летальных исходов или тяжелых осложнений преодолевает все разумные пределы. Но в
большинстве случаев в этом периоде АМП применяют при легких и среднетяжелых
инфекциях, когда хороший исход без лечения является скорее правилом, чем
исключением, то зафиксировать снижение эффективности гораздо сложнее, даже при
проведении специальных исследований. Длительность второго этапа предсказать
сложно, поскольку приходится подвергать анализу значительное число факторов.
По мере роста частоты распространения резистентности и
достижения некоего критического уровня, для многих лечащих врачей «вдруг
становится очевидным», что «модный» и эффективный еще вчера АМП стал
неэффективным. Тогда и возникает необходимость в пересмотре применяемых годами
схем лечения. В большинстве наших наблюдений антибиотикорезистентность сначала
проявлялась в госпитальных условиях, а затем распространялась на
микроорганизмы, циркулирующие у пациентов
амбулаторно-поликлинических учреждений.
Антибиотики — это тот инструмент, которым пользуются врачи практически всех
без исключения специальностей, инструмент эффективный, но в то же время
требующий осторожного обращения. При их назначении врачу необходимо ответить не
только на вопрос: «Что? Кому? Когда?», но и на вопрос: «В какой дозе? Как часто?
Насколько долго?». Исследование данной проблемы, проводимые в течение последнего
десятилетия, формируют стандартизованные подходы применения АБП при отдельных
инфекционных заболеваниях, таких как инфекционный эндокардит, пневмонии и
бронхиты, перинатальные инфекции, инфекций мочевыводящих путей и др.
Некогда триумфальный успех применения пенициллина в значительной степени был
обусловлен впечатляющим снижением летальности при пневмониях. Сегодня в
современной медицине используется широкий арсенал антибактериальных средств, что
теоретически обеспечивает подавление любых микроорганизмов. Тем не менее,
реальная клиническая практика свидетельствует о том, что назначение АМП не
является абсолютной гарантией успешного исхода.
Безуспешность антибактериальной терапии может объясняться как объективными,
так и субъективными причинами. Объективной реальностью является возрастание
эпидемиологической значимости ранее малоизвестных возбудителей пневмонии, таких
как легионелла, микоплазма, хламидия, пневмоцисты, различные микобактерии со
своеобразным спектром чувствительности к антибиотикам. Наконец, к реалиям
современной жизни следует отнести увеличение численности «иммуноскомпрометированных»
лиц. Это люди пожилого и старческого возраста, страдающие серьезными
хроническими заболеваниями; больные новообразованиями, диабетом, заболеваниями
почек и печени, алкоголики и наркоманы; лица, получающие кортикостероиды и
иммунодепрессанты. К субъективным причинам нерациональной антибактериальной
терапии и все увеличивающегося числа неблагоприятных исходов можно отнести
ошибки в диагностике инфекционных заболеваний и в тактике антибактериальной
терапии.
Резистентность микроорганизмов и рост ВБИ (ИСМП).
Современные внутрибольничные инфекции в хирургических клиниках
вызываются различными микроорганизмами и проявляются в основном синдромами
нагноений и септических поражений. Наиболее часто возбудителями внутрибольничных
инфекций являются резистентные к антибиотикам штаммы кишечной палочки,
золотистого стафилококка, синегнойной палочки, протея, кишечной палочки,
клебсиелл, грибов кандида и др.
Существующая в настоящее время сложная эпидемиологическая ситуация
обосновывает повышенное внимание к профилактике инфекционных заболеваний и рост
требований к качеству дезинфекционных мероприятий, направленных на выявление
факторов передачи и уничтожение возбудителей инфекций в лечебно-профилактических
учреждениях. В этой связи следует отметить, что внутрибольничные инфекции ─
понятие собирательное, включающее различные нозологические формы заболеваний.
Как о том свидетельствует история медицины, ВБИ являются ровесником больниц.
После введения в хирургию асептики и антисептики внутрибольничные инфекции почти
полностью исчезли, на протяжении десятилетий большинство операционных ран
заживало без каких-либо осложнений. Казалось, что использование сульфаниламидов,
а позднее — антибиотиков позволит устранить и оставшиеся немногие случаи
инфекций. Этого, однако, не произошло. Никто не предполагал, что патогенные
агенты смогут выработать резистентность к лекарствам. Но случилось именно так, и
теперь мы вновь встречаемся со старой проблемой инфекции, хотя и в новой форме.
В эпидемиологии внутрибольничных инфекций важную роль играет восприимчивость
организма. В некоторых случаях снижена не резистентная способность организма в
целом, а только местная резистентность (locus minoris resistentiae),
способствующая возникновению локальной инфекции. Подобным местным (локальным)
восприятием инфекции является и каждая рана, в которой имеется серома, гематома,
ишемическая или некротическая ткань, инородное тело (нитка, протез). Хорошо
известно, насколько велика роль местных условий (поражение тканей, ишемия,
присутствие инородного тела и т.п.) при заражении различными бактериями. Наряду
с местным поражением тканей важную роль играет иммунобиологическое состояние
всего организма. Если вне медицинского учреждения инфицируется почти всегда
здоровый организм, то большинство внутрибольничных инфекций развивается на
иммунобиологически неполноценном, больном организме как вторичная болезнь.
Некоторые лекарства также повышают подверженность организма инфекциям. Подобным
действием обладают, например, антибиотики широкого спектра действия и стероидные
препараты.
По мнению большинства экспертов, которые занимаются оценкой ущерба здоровью
пациентов полученного в результате оказания медицинской помощи, к
внутрибольничной инфекции можно отнести следующие случаи:
если пациент повторно поступает в стационар с установленной инфекцией
явившейся следствием предыдущей госпитализации;
если инфекция развилась через 48 ч и более, после поступления в лечебное
учреждение.
Общепризнанным является положение о том, что в первую очередь должны
существовать клинические признаки наличия инфекции, которые выявляются или путем
непосредственного («прямого») наблюдения за пациентом, или при анализе первичной
документации пациента. Дополнением к клиническим признакам инфекции являются
результаты параклинических методов исследования (например, рентгенологического
исследования при внутрибольничной пневмонии), а также данные лабораторных
исследований (микробиологические, серологические и экспресс-методы диагностики).
При комплексном анализе этих данных необходимо принимать во внимание, что
некоторые внебольничные инфекции имеют инкубационный период более 48 часов,
например, брюшной тиф.
Если состояние пациента требует систематического наблюдения, применения
сложных диагностических и лечебных процедур, специализированной медицинской
помощи, его направляют в лечебное учреждение стационарного типа. Стационар (лат.
stationarius – стоящий, неподвижный) –
структурное подразделение медицинского учреждения (больницы, медсанчасти,
диспансеры), предназначенное для обследования и лечения больных в условиях
круглосуточного (за исключением дневного стационара) их пребывания в данном
учреждении под наблюдением медицинского персонала. С точки зрения значимости
экспертного контроля над распространением ВБИ, специалистов в большей мере
интересуют хирургические стационары, хотя внутрибольничное инфицирование
возможно и в стационарах терапевтического профиля, а так же родильных,
инфекционных и других медицинских учреждениях, начиная с поликлиник, кончая
станциями скорой медицинской помощи.
Современные подходы к организации работы медицинских учреждений, управлению
персоналом и ресурсами предполагают следующие базовые индикаторы: максимально
полное обследование больных и постановка клинического диагноза, которые должны
осуществляться в первые двое суток пребывания больного в стационаре. Во многих
случаях удается добиться снижения уровня госпитальной летальности за счет
организации эффективной антибактериальной терапии, уменьшения вероятности
формирования антибиотикорезистентности и ошибок при назначении АМП.
В реальных условиях при назначении антибактериальной терапии каждый хирург
обязан строго соблюдать рекомендации, позволяющие эффективно лечить пациентов:
Использовать антибиотики, обладающие высокой активностью в отношении
выделенного возбудителя инфекции (по возможности следует использовать
антибиотики узкого спектра).
Ограничивать применение антибиотиков, к которым наблюдается рост
резистентности микроорганизмов или наблюдается высокий уровень ее
распространенности.
Системные антибиотики не должны применяться местно.
Антибиотики следует назначать в адекватных дозах с соблюдением
оптимального пути введения и режима дозирования.
Знать возможные нежелательные лекарственные реакции и проводить их
мониторинг.
Не использовать новые, дорогостоящие антибиотики в тех ситуациях, когда
более дешевые традиционные препараты обладают сходной эффективностью.
В то же время применение АМП сопровождается побочными эффектами, которые
отрицательно сказываются на состоянии пациентов и конечных результатах лечения.
В 2004 г. Международная организация по экономическому сотрудничеству и
развитию (OECD) предложила перечень индикаторов,
которые рекомендовано использовать во всех странах для оценки безопасности
пациентов в процессе оказания медицинской помощи. Именно в этом перечне первое
место занимают внутрибольничные инфекции, как наиболее значимые индикаторы
безопасности. Следует отметить, что ведущее место среди этих
индикаторов занимают ВБИ и связанные с ними состояния. Предполагается, что
унифицированный подход позволит стандартизировать данные о частоте и структуре
побочных эффектов, объективно выявлять проблемы и, соответственно, предлагать
пути их решения. Особое внимание международные эксперты обращают на
необходимость контроля за наиболее тяжелыми и опасными осложнениями, связанными
с лечением. Такие осложнения входят в группу «случаев, подлежащие особому
контролю» (sentinel events).
Американская объединенная комиссия по аккредитации учреждений здравоохранения
(JCAHO) дает им следующее определение: «Случаи,
подлежащие особому контролю, - это непредвиденные случаи смерти или причинения
серьезного вреда физическому или психическому здоровью пациента во время
оказания медицинской помощи, а также зафиксированный риск возникновения такого
случая». Риск возникновения случая, подлежащего особому контролю, - это
выявленное отклонение в лечебно-диагностическом процессе, при повторении
которого существует значительная вероятность развития тяжелого осложнения,
связанного с оказанием медицинской помощи. Выделение такого специального класса
побочных эффектов связано с необходимостью проведения немедленного расследования
обстоятельств и причин их возникновения, а также организации мероприятий,
направленных на их устранение и профилактику. Именно к этой категории случаев,
подлежащих особому контролю и относятся все эпизоды ВБИ (ИСМП).
Причины госпитальной летальности и ВБИ. Внутрибольничные инфекции
являются одной из главных причин развития тяжелых осложнений в процессе оказания
медицинской помощи. Распространенность ВБИ остается исключительно высокой. Так,
в Великобритании в 2003 г. ВБИ наблюдались приблизительно у 1 из 10
госпитализированных больных, стоимость лечения подобных осложнений обходится
здравоохранению Великобритании в 1 миллиард фунтов стерлингов в год.
Уровень госпитальной летальности в отечественных стационарах в последние годы
в определенной мере стал связываться с уровнем распространения внутрибольничных
инфекций. В экономически развитых странах летальность от ВБИ выше смертности в
результате дорожно-транспортных происшествий. При этом в отечественных
медицинских учреждениях ВБИ регистрируются крайне редко, а значит, не
разрабатываются мероприятия по снижению летальности от них.
Вообще же оценка уровня госпитальной летальности должна осуществляться во
взаимосвязи с оценкой тяжести состояния пациента на момент госпитализации. Один
из основных индикаторов работы стационара - это доля пациентов, сразу
поступивших или переведенных в отделения реанимации и интенсивной терапии, от
общего числа поступивших в больницу. Уровень летальности напрямую зависит от
числа больных, поступивших или переведенных в отделения реанимации и интенсивной
терапии: чем выше доля пациентов, прошедших через отделения реанимации, тем ниже
летальность.
В этой связи следует отметить, что в ЛПУ интенсивного лечения, куда
изначально поступают преимущественно тяжелые пациенты, летальность, как это ни
прискорбно была, есть и будет всегда.
В особой мере это
относится к ЛПУ, где есть отделения нейротравмы, отделения реанимации
новорожденных, отделения экстренной травматологии и т.п. Но и в этом направлении
необходимо и возможно работать более эффективно, чем сегодня. При реализации
современных медицинских технологий, в том числе и высокотехнологичной
медицинской помощи, больной может погибнуть в течение короткого временного
промежутка. Это происходит в тех случаях, когда тяжесть патологии несовместима с
жизнью. В остальных случаях витальные функции пациента должны быть
восстановлены.
Системный анализ функционирования различных ЛПУ показал наличие достаточно
устойчивой связи между уровнем внутрибольничных инфекций и показателем
летальности. Утверждения некоторых специалистов о том, что при высоком
уровне медицинских технологий сама вероятность внутрибольничного инфицирования
выглядит парадоксальной, не имеют под собой реальных оснований. Сегодня
абсолютно исключить вероятность появления внутрибольничных инфекций в стационаре
не представляется возможным, хотя, безусловно, можно до минимума снизить такую
опасность для пациента. И один из путей профилактики внутрибольничного
инфицирования больных ─ сокращение сроков его пребывания в стационаре до
разумных пределов именно за счет повышения интенсивности, качества и
безопасности лечения.
Как не трудно сегодня говорить о реальном функционировании многих медицинских
учреждений, но следует признать неприятный факт того, что работа клинических
отделений крупных больниц в значительной мере сводится к оказанию гостиничных, а
не медицинских услуг. Тем более, что более четверти пациентов в праздничные и
выходные дни покидают стационары под разными предлогами. Это резко снижает
эффективность функционирования ЛПУ за счет необъяснимо длительных сроков лечения
в стационаре и противоречит самой сути той миссии, которая возложена на
клинические отделения. И, тем не менее, в большинстве многопрофильных ЛПУ, даже
в тех, где в структуре коечного фонда превалируют хирургические койки,
продолжается реализация идеологии необоснованной госпитализации в стационар
«амбулаторных» больных и стремление к удлинению сроков лечения, что так или
иначе связано с внутрибольничным инфицированием.
В плену у иллюзий и заблуждений. В условиях большинства медицинских
учреждений значительная часть врачей-клиницистов, а так же администраторов не
отдает себе отчета в том, что большая часть случаев летальности в хирургических
и других стационарах является следствием нарушения принципов инфекционного
контроля, отсутствия системы управления качеством производства медицинских
услуг. Они искренне убеждены в том, что основная часть гнойно-септических
осложнений является следствием ошибок отдельных врачей или медицинских сестер.
Выпускаемые Международным обществом по инфекционным болезням (ISID)
руководства по инфекционному контролю до сих пор остаются не востребованными,
хотя адресованы широкому кругу госпитальных эпидемиологов, врачам различных
специальностей, бактериологам, организаторам здравоохранения и преподавателям
медицинских ВУЗов. В то же время распространению внутрибольничных инфекций не
уделяется должного внимания, а случаи ВБИ в медицинских учреждениях, которые
сопровождаются тяжелыми последствиями или летальными исходами, предаются
забвению без квалифицированного анализа причинно-следственных связей. Анализ
отчетных данных нескольких десятков отделений многопрофильных ЛПУ ДФО,
проведенных нами в течение последнего десятилетия указывает на то, что в
большинстве из них отсутствует даже упоминание о ВБИ, хотя длительные
фактические сроки послеоперационного лечения отдельных пациентов и высокий
уровень послеоперационной летальности свидетельствуют об обратном.
При проведении экспертизы условно можно выделить три вида ВБИ:
у пациентов, инфицированных в стационарах;
у пациентов, инфицированных при получении поликлинической помощи;
у медицинских работников, заразившихся при оказании медицинской помощи
больным в стационарах и поликлиниках.
Объединяет все три вида ВБИ место инфицирования ─ медицинское учреждение.
Гнойно-септические инфекции. Анализ имеющихся данных показывает, что
в структуре ВБИ, выявляемых в крупных многопрофильных ЛПУ, гнойно-септические
инфекции (ГСИ) занимают ведущее место, составляя до 75-80% от их общего
количества. Наиболее часто ГСИ регистрируются у больных хирургического профиля,
в особенности в отделениях неотложной и абдоминальной хирургии, травматологии и
урологии. Основными факторами риска возникновения ГСИ являются: увеличение числа
носителей штаммов резидентного типа среди сотрудников, формирование госпитальных
штаммов, увеличение обсеменности воздуха, окружающих предметов и рук персонала,
диагностические и лечебные манипуляции, несоблюдение правил размещения больных и
ухода за ними и т.д.
Кишечные инфекции. Другая большая группа ВБИ - кишечные инфекции. Они
составляют в ряде случаев до 7-12% от их общего количества. Среди кишечных
инфекций преобладают сальмонеллезы. Регистрируются сальмонеллезы в основном (до
80%) у ослабленных больных хирургических и реанимационных отделений, перенесших
обширные полостные операции или имеющих тяжелую соматическую патологию.
Выделяемые от больных и с объектов внешней среды штаммы сальмонелл отличаются
высокой антибиотикорезистентностью и устойчивостью к внешним воздействиям.
Ведущими путями передачи возбудителя в условиях ЛПУ являются контактно-бытовой и
воздушно-пылевой.
Гемоконтактные вирусные гепатиты. Значимую роль во внутрибольничной
патологии играют гемоконтактные вирусные гепатиты В, С, D, составляющие 6-7% в
ее общей структуре. Более всего риску заболевания подвержены больные, которым
проводятся обширные хирургические вмешательства с последующей
кровезаместительной терапией, программный гемодиализ, инфузионная терапия.
Обследования, проводимые стационарным больным с различной патологией, выявляют
до 7-24% лиц, в крови которых обнаруживаются маркеры этих инфекций. Особую
категорию риска представляет медицинский персонал госпиталей, чьи обязанности
предусматривают выполнение хирургических манипуляций или работу с кровью
(хирургические, гематологические, лабораторные, гемодиализные отделения). При
обследованиях выявляется, что носителями маркеров гемоконтактных вирусных
гепатитов являются до 15-62% персонала, работающего в этих отделениях. Эти
категории лиц в ЛПУ составляют и поддерживают мощные резервуары хронических
вирусных гепатитов.
Прочие инфекции. На долю других инфекций, регистрируемых в ЛПУ,
приходится до 5-6% от общей заболеваемости. К таким инфекциям относятся грипп и
другие острые респираторные инфекции, дифтерия, туберкулез и др., которыми
довольно часто болеют не столько пациенты, сколько медицинский персонал.
В этой связи следует избавиться от иллюзий о том, что ВБИ − это проблема
пациентов. Ведь еще до недавнего времени считалось, что заражение
медицинского персонала происходит, главным образом, в результате повреждения
кожных покровов или слизистых иглой или инструментом. Однако даже при тщательном
соблюдении мер предосторожности кровь, сыворотки или биологическая жидкость,
попадая на одежду медработника, поглощается ею и проникают далее вглубь, а если
на теле имеются порезы или мелкие травмы, наличие которые может вообще не
фиксироваться, или имеются поражение кожи в виде банального дерматита, то риск
заражения резко возрастает. Кроме того, небезопасен и процесс дальнейшей
обработки белья и одежды, на которую попала кровь, ее компоненты, либо иные
выделения. Ни один медицинский работник, занимаясь
профессиональной деятельность, не может быть уверен в том, что он не
подвергнется заражению ВБИ сегодня или завтра.
В этой связи, хотелось бы избавить коллег от сложившихся под влиянием
представителей управляющих структур заблуждений по данному вопросу −
нозокомиальные (внутрибольничные) инфекции представляют собой серьезную проблему
современной медицины. Вообще же, не стоит думать о том, что ВБИ - беда только
отечественных ЛПУ. По сообщению национального центра контроля и предотвращения
заболеваний США, как минимум 90 тысяч американцев погибают ежегодно из-за ВБИ.
Немцы регистрируют 450 - 650 тысяч случаев госпитальных инфекций каждый год и
оценивают ущерб от них в 3 миллиарда немецких марок. Французы конкретизируют
ситуацию, заявляя, что на совести медперсонала, который недостаточно тщательно
моет руки, в 2001 году уже 4 миллиона лишних койко-дней. Мы склонны поддержать
мнение авторов определенных документов, в которых указывается на то, что высокий
уровень ВБИ весьма характерная особенность отечественных стационаров, требующая
своевременных оценок, профилактических и других мероприятий по борьбе с ней.
Следует уточнить, что к ВБИ также относятся случаи суперинфицирования в ЛПУ;
носительство возбудителей традиционных инфекций также учитывается как внутри
больничное заражение, если доказано, что его не было у пациента до поступления в
стационар. В конечном итоге, каждый случай ВБИ имеет свое «микробиологическое
лицо», характерное именно для данного стационара.
Нозокомиальная (госпитальная) пневмония. Нозокомиальная пневмония (НП)
— это пневмония, развившаяся через 48 часов и позднее после госпитализации (при
исключении инфекционных заболеваний с поражением легких в инкубационный период
на момент госпитализации больного). Рост резистентности нозокомиальной флоры
опережает разработку новых препаратов для эффективного лечения инфекций. В этих
условиях необходимы взвешенные меры по повышению эффективности применения
антибактериальных препаратов и ограничению роста резистентности нозокомиальной
флоры. К сожалению, в здравоохранения ДФО системной проработкой таких мер пока
никто не занимается, а отрывочные, единичные НИОКР по данной проблеме, как
правило, проводятся под патронажем фармацевтических фирм, которые заняты
реализацией «своих» антибактериальных препаратов, поэтому результаты многих
подобных НИОКР заранее предсказуемы. В сложившихся условиях антибактериальная
резистентность и нерациональная антибактериальная терапия являются двумя
сторонами одной медали, что, так или иначе, оказывает влияние на распространение
ВБИ, в том числе и нозокомиальной пневмонии.
В любом стационаре существует вероятность развития нозокомиальной пневмонии.
Риск развития НП составляет от 0,3 % до 20 % и более, что зависит от профиля
отделения (в ОРИТ — максимальный риск развития), эпидемиологической обстановки в
ЛПУ, клинических и индивидуальных особенностей находящихся на лечении пациентов
и т. д. Летальность от НП составляет 10-80 % и существенно зависит как от
особенностей возбудителя НП, так и от правильно назначенного лечения. Не
вызывает сомнения, что эффективность лечения существенно возрастает при
правильном определении возбудителя заболевания.
Проблема качественной диагностики возбудителя в региональных ЛПУ сопряжена с
рядом сложностей. Основными, на наш взгляд, являются следующие:
нехватка сертифицированных лабораторий;
отсутствие оборудования, необходимого для экспресс-диагностики;
отсутствие единых стандартов диагностики в микробиологических
лабораториях;
частое несоблюдение методик взятия и условий доставки биоматериалов в
лабораторию, а также — методик их исследования;
недостаточная кооперация в работе врача-клинициста и микробиолога.
Первые три пункта этого перечня в значительной мере связаны с уровнем
общеэкономического благосостояния региона, так как требуют значительных
финансовых вложений. Хотя, безусловно, сертификация лабораторий и стандартизация
их работы полезна на любом, даже городском, уровне, так как обеспечивает
относительно унифицированный подход к процессу диагностики. Используются сходные
методики, сопоставимые среды и т. д., что позволяет проводить перекрестное
сравнение полученных результатов, с получением преемственной информации, важной,
в первую очередь, для врачей-клиницистов. В идеале же необходимо наличие единого
стандарта микробиологической диагностики в масштабах страны.
Основным и наиболее часто изучаемым биоматериалом в пульмонологической
практике является мокрота. Требования к забору и качеству мокроты следующие:
первую пробу мокроты желательно получить до начала курса
антибиотикотерапии;
мокроту оптимально собирать утром, до приема пищи, после тщательного
туалета полости рта (полоскание кипяченой водой);
больным нужно доступно объяснить, что требуется получить именно содержимое
нижних отделов дыхательных путей, а не ротоглотки, и, по возможности,
проконтролировать их действия;
забор материала проводить в стерильные интактные контейнеры;
продолжительность хранения мокроты в контейнерах не должна превышать 2 ч
(в летнее время желательно не более 1 ч);
в условиях лаборатории качество мокроты оценивается после окрашивания
мазка по Граму (при наличии в мазке менее 25 лейкоцитов и более 10
эпителиальных клеток, при просмотре не менее 8-10 полей зрения при малом
увеличении, мокрота признается некачественной, дальнейшее ее исследование
нецелесообразно, так как, скорее всего, материал получен из ротовой полости);
высокая диагностическая ценность исследования признается при выделении
возбудителя в концентрации х 106 КОЕ/мл.
Диагностическая ценность бронхоальвеолярного лаважа и метода защищенных щеток
существенно выше (104 и 103 КОЕ/мл соответственно),
поэтому для больных, находящихся на ИВЛ, они более предпочтительны.
При наличии плеврального выпота и при проведении диагностической или лечебной
пункции полученная жидкость также подлежит микробиологическому исследованию.
Следует учитывать, что если пациенту уже установлены дренажные трубки, из
которых затем взята жидкость для исследования, то высока вероятность выделения
сапрофитной флоры из трубок. Тогда, скорее всего, патогенная флора (за счет
гораздо более низкой концентрации) не будет выделена, либо лабораторией будут
даны ложноположительные результаты (сапрофитная флора).
У длительно температурящих больных, у пациентов с тяжелым течением
заболевания (подозрение на септический процесс) рекомендуется на высоте
температуры брать анализ крови на стерильность. Исследуется венозная кровь,
взятая из разных вен с интервалом более 10 мин. Посев необходим как на аэробные,
так и на анаэробные (или комбинированные) среды. Чувствительность этого метода
не очень высока, однако чрезвычайно высока достоверность полученных результатов,
при условии выделения возбудителя.
Как эпидемиологические и ретроспективные методы диагностики могут применяться
серологические исследования, полимеразно-цепная реакция. Лучше всего эти
методики разработаны по отношению к "атипичным" возбудителям: микоплазма,
хламидия, легионелла.
В условиях лаборатории обязательно должен проводиться такой простой, однако
достаточно информативный метод, как микроскопия мазков, окрашенных по Граму.
Экспресс-проведение такого исследования позволяет сделать предварительные выводы
относительно патогена (Гр+, Гр-, палочки, кокки) уже через несколько часов после
взятия анализа мокроты. Основываясь на таких данных, эмпирическая терапия
является гораздо более эффективной. Кроме того, в условиях существующей эпидемии
туберкулеза биоматериал всех пациентов должен прицельно исследоваться на предмет
вероятного наличия бактерий Коха. В случае исследования мокроты рекомендуется
проводить ее микроскопию после окраски по Циль-Нильсену.
Пневмония может развиваться как у хирургических больных, нуждающихся в
интубации трахеи и искусственной вентиляции легких (ИВЛ), так и у пациентов не
нуждающихся в ИВЛ из-за снижения объема дыхания и развития ателектазов. Обычно
различают «раннюю» и «позднюю» нозокомиальную пневмонию. Это условное деление
связано с существенными различиями в этиологии, а стало быть, и выборе
антибактериальных препаратов для лечения. В этиологии «ранней» пневмонии
важнейшее значение имеют возбудители, которые пациенты привносят с собой из
внебольничных условий, и обычно эти микробы являются возбудителями внебольничной
пневмонии (пневмококк, гемофильная палочка). Поздними считаются пневмонии,
которые развиваются после 5 суток пребывания пациента в стационаре,
возбудителями которых обычно являются грамотрицательные (Pseudomonas
aeruginosa, Enterobacter spp., Klebsiella pneumoniae и др.) и
грамположительные (S. aureus и др.) бактерии.
Большинство нозокомиальных пневмоний вызваны резистентной флорой, так как
развиваются на фоне антибактериальной терапии, которая применяется по поводу
первичной хирургической инфекции. Выбор антибиотиков для лечения нозокомиальной
пневмонии существенно затруднен именно из-за отсутствия информации о
резистентности флоры. Особенности резистентности флоры у конкретного пациента
могут быть выявлены только после корректного микробиологического исследования
содержимого трахеобронхиального дерева с помощью бронхоскопии. Эмпирический
выбор антибактериального препарата основывается на данных мониторинга
нозокомиальной флоры конкретного отделения, стационара или региона, при этом
необходимо учитывать и глобальные тенденции резистентности нозокомиальной флоры.
По современным представлениям, в тех случаях, когда именно нозокомиальная
пневмония является фактором риска неблагоприятного исхода пациента,
предпочтительно применение принципа деэскалационной антибактериальной терапии.
Этот принцип заключается в выборе на эмпирическом этапе лечения (до получения
микробиологических данных) препаратов, обладающих спектром, достаточным для
эффективного подавления наиболее вероятных возбудителей нозокомиальной инфекции,
в том числе резистентных. Необходимо отметить важную роль стартовой терапии
нозокомиальной пневмонии, так как выбор адекватного антимикробного препарата или
комбинации препаратов способен снизить летальность в два раза по сравнению с
неадекватными препаратами.
Организация деэскалационной терапии ВБИ. Многими экспертами в области
антибактериальной терапии поддерживается концепция деэскалационной терапии и
необходимости применения адекватной антимикробной терапии для стартовой терапии
тяжелых инфекций. Учитывая то, что концепция деэскалационной терапии выдвинута
сравнительно недавно, крупных систематических исследований по оценке ее
клинической эффективности в России пока проведено недостаточно. Однако аргументы
и логика применения этого подхода, имеющиеся клинические данные вписываются в
объективную необходимость совершенствования глобальной стратегии
антибактериальной терапии и заслуживают самого внимательного изучения и
применения в региональной клинической практике.
В течение последних десятилетий для борьбы с тяжелыми проявлениями
инфекционных поражений органов и тканей, особенно с нозокомиальными инфекциями
разработана стратегия деэскалационной терапии в виде четырех основных принципов:
безотлагательный старт антибактериальной терапии,
выбор АМП с учетом его способности проникать в ткани,
высокие и индивидуально подобранные дозы АБП,
начало терапии АБП широкого спектра действия.
Деэскалация предполагает сначала назначение стартового антибиотика (или
комбинации антибиотиков) широкого спектра действия для охвата наиболее вероятных
возбудителей, а затем переход на терапию АМП основанной на результатах
микробиологического исследования. Несмотря на то, что пациенты с тяжелыми
нозокомиальными инфекциями требуют комплексного лечения, именно неадекватная
антимикробная терапия инфекции является неблагоприятным прогностическим фактором
и достоверно увеличивает вероятность неблагоприятного исхода инфекции.
Концепция деэскалационной терапии содержит доказательства необходимости
применения у пациентов с тяжелыми нозокомиальными инфекциями наиболее
эффективных антимикробных препаратов в режиме стартовой терапии и объясняет
причины недостаточной эффективности эскалационного принципа лечения, который
предполагает применение в режиме стартовой терапии препаратов, которые обычно
обладают высокой эффективностью в отношении внебольничных инфекций. Основным
различием возбудителей вне- и внутрибольничных инфекций является их
резистентность к антимикробным препаратам и, следовательно, выбор антимикробных
препаратов является ключевым моментом, способным оказывать влияния на исход
лечение больных тяжелыми нозокомиальными инфекциями.
Именно на уровне выбора АМП и совершается значительное число ошибок, которые
и приводят к осложнениям, а в более позднем временном промежутке и к печальным
последствиям для пациента. В этой связи следует отметить, что проблема
осложнений терапии АМП становится все более актуальной во всем мире. Это
связано, прежде всего, с внедрением в медицинскую практику большого числа ЛС,
обладающих высокой биологической активностью, сенсибилизацией населения к
биологическим и химическим веществам, нерациональным использованием лекарств,
ошибками врачей и применением не качественных и фальсифицированных препаратов.
Результаты проведенных за последние годы фармакоэпидемиологических исследований
позволяют говорить о том, что недооценка и запоздалое решение этой проблемы
чреваты развитием самых серьезных последствий.
Сегодня медицинским работникам нужны сведения о ВБИ, которые могут убедить их
в нескольких вещах. Во-первых, что проблема ВБИ актуальна не только для «чужих»
клиник, но и для своего ЛПУ. Во-вторых, для ее решения необходимы изменения, и
что эти изменения принесут пользу не только пациентам, но самим работникам.
Такая информация должна носить приоритетный характер, быть достоверной,
воспроизводимой, неопровержимой, четко сформулированной, составленной с учетом
степени риска и распространенности различных видов патологии, а также удобной
для пользования. Но в реальной клинической практике, кроме наличия достоверной
информации, необходимы и действенные пути предупреждения и снижения уровня ВБИ.
Источниками внутрибольничной инфекции в отечественных ЛПУ продолжают
оставаться больные острыми и хроническими формами гнойносептических заболеваний
и бессимптомные носители патогенных микроорганизмов среди больных и персонала. В
зависимости от локализации возбудителя его выделение из организма больного или
носителя происходит через различные органы и ткани - дыхательные пути,
желудочно-кишечный тракт, мочеполовой тракт. Распространение возбудителей
внутрибольничной инфекции происходит двумя путями: воздушно-капельным и
контактным. Основными факторами передачи являются воздух, руки, многочисленные
объекты внешней среды (белье, перевязочный материал, инструментарий, аппаратура
и т. д.). Именно на внедрении технологий, которые позволяют снизить
распространение ВБИ и строится идеология инфекционного контроля.

