Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
2.1. Электроды сравнения
Потенциал измерительного электрода определить очень сложно. Поэтому
измеряют разность потенциалов между измерительным электродом и электродом
сравнения, потенциал которого постоянен. Обычно в качестве электродов сравнения
выбирают электроды, потенциалы которых стабильны во времени, хорошо
воспроизводимы, несложны в изготовлении, а протекающие на них электрохимические
процессы высокообратимы. Большая часть электродов сравнения относится к
электродам второго рода. Электроды второго рода представляют собой полуэлементы
из металла, покрытого слоем его малорастворимого соединения (хлорида, оксида или
гидрооксида), погруженного в раствор хорошо растворимой соли другого металла,
содержащей тот же анион, что и у малорастворимого соединения электродного
металла [Скорчеллети В.В., 1974г., Ротинян А.Л., с авторами, 1981г.].
Такие электроды обратимы не только к катионам металла (Ag+,
Hg+ и т.д.), но и к
общему аниону (например, Cl-)
солей.
Важнейшими из электродов второго рода являются хлорсеребряный,
ртутнокаломельный, оксиднортутный, ртутносульфатный. Только каломельный и
хлорсеребряный электроды сравнения нашли применение в конструкциях рН-датчиков
для измерения внутрижелудочной кислотности.
Ртутнокаломельный электрод сравнения
Ртутнокаломельный электрод сравнения представляет собой ртутный
электрод, находящийся в контакте с раствором, содержащим ртутистые катионы и
ионы хлора, например, с раствором хлорида калия, насыщенным каломелью. Каломель,
то есть хлорид ртути (Hg2Cl2),
имеет относительно малую растворимость в воде: при 20°С – 0,0002 г в 100 граммах
воды; при 43°С ~ 0,001 г. Поэтому в конструкциях ртутно-каломельных электродов
сравнения использовали насыщенный каломелью раствор хлористого калия в
присутствии избытка твердой каломели.
Для ртутнокаломельных электродов сравнения, применяемых в
рН-датчиках для измерения внутрижелудочной кислотности, обычно применяли
насыщенный раствор хлористого калия в присутствии избытка твердого хлорида
калия. Преимуществом насыщенного раствора является то, что, с одной стороны, он
обеспечивает постоянство концентрации ионов хлора, а следовательно, и ионов
ртути при избытке твердой соли, а с другой стороны, диффузионный потенциал на
границе насыщенный раствор хлорида калия – исследуемый раствор меньше, чем при
использовании растворов хлорида калия меньшей концентрации (табл.4).
Таблица 4. Диффузионные потенциалы на границе раствора хлористого калия с раствором соляной кислоты при 25°С [Бейтс Р., 1972 г.]
|
Раствор хлористого калия |
Раствор соляной кислоты |
Диффузионный потенциал, мВ |
|
KCl (насыщенный)
KCl (0,1 М)
|
HCl (0,1 М)
HCl (0,1 М) |
4,6
26,9 |
|
KCl (насыщенный)
КCl (0,1 М)
|
HCl (0,01 М)
HCl (0,01 М) |
3,0
9,1 |
Электродная реакция сводится к восстановлению каломели до
металлической ртути и аниона хлора.
Hg2Cl2
+ 2 e → 2
Hg + 2 Cl¯
Стандартный потенциал ртутнокаломельного электрода равен 0,26804 и
0,26390 В соответственно при температуре 26 и 37°С (Бейтс Р., 1972г.).
Потенциал ртутнокаломельного электрода зависит от активности ионов
хлора (аCl
-) и определяется по формуле:
φ = φ0
- 2,3 RT/F lg аCl-
,
где 2,3·RT/F
– коэффициент Нерста, равный 0,05916 и 0,06134 соответственно при 25 и 37°С.
Обычно при расчетах за коэффициент активности ионов хлора принимают
средний коэффициент активности (γ) хлористого калия. Для насыщенного раствора
KCl (4,80
m при 25°С) активность ионов хлора:
аCl- =
m γ = 4,8 · 0,583 = 2,7984,
где m – молярная
весовая концентрация
Поэтому потенциал насыщенного ртутнокаломельного электрода будет
равен при 37°С:
φ=0,2639-0,06134·lg
2,7984=0,2365 В.
Обычно сам электрод сравнения выполнен в виде трубки из диэлектрика
(стекла, керамики, пластмассы), в дне которой герметично закреплен кусочек
платиновой проволоки. В трубку наливали чистую ртуть, чтобы покрыть кончик
платиновой проволоки. Затем слой ртути покрывали слоем пасты, приготовленной из
каломели, тщательно растертой со ртутью и хлористым калием. Затем на слой этой
пасты помещали несколько кристаллов хлористого калия и оставшуюся полость трубки
заполняли кусочками асбеста или бумаги [Линар Е.Ю., 1968г.], пропитанных
насыщенным раствором хлорида калия.
Трубку, внутри которой находился ртутнокаломельный электрод,
изготовливали из стекла или керамики, и закрепляли ее внутри пластмассового
(рис. 5а) или керамического (рис. 5б) корпуса диаметром около 7 мм. В
керамическом корпусе имелась полость, в которой находились кристаллы хлористого
калия, а в процессе измерения рН – насыщенный раствор хлористого калия. В дне
такого корпуса было сквозное отверстие (рис. 5б), обеспечивающее
электролитический контакт ртутно-каломельного электрода с исследуемой в желудке
средой [Новоселец С.А., 1999г.].
Схемы конструкций ртутнокаломельного электрода сравнения во
внутрижелудочных датчиках кислотности показаны на рис.8.
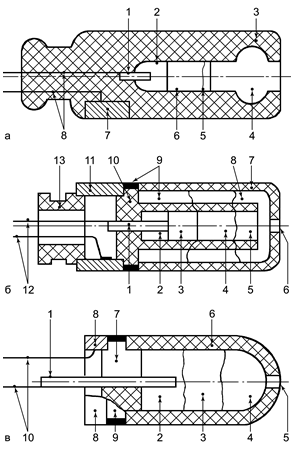
Рис. 8 Конструкции ртутнокаломельных электродов сравнения:
а) 1 – вывод из платины; 2 – ртуть; 3 – корпус из полистирола; 4 –
асбест, пропитанный насыщенным раствором КСl;
5 – кристаллы КСl; 6 – паста из
каломели, ртути и КСl; 7 –
сурьма; 8 – проводники;
б) 1 – вывод из платины; 2 – ртуть; 3- паста из каломели, ртути и
КСl; 4 – кристаллы КСl;
5 – асбест; 6 – отверстие; 7 – корпус из керамики; 8 – раствор КСl;
9 – клей; 10 – основание корпуса; 11 – сурьмяное кольцо; 12 – проводники; 13 –
втулка керамическая;
в) 1 – вывод; 2 – ртуть; 3- паста из каломели, ртути и КСl;
4 – раствор КСl; 5 – отверстие;
6 – корпус из керамики; 7 – основание корпуса; 8 – кольцо из сурьмы; 9 – клей;
10 – проводники.
В 1994г. Новоселец С.А. с соавторами разработали для обследования
детей конструкцию рН-зонда с ртутнокаломельным электродом сравнения (рис.8в),
размещенным непосредственно внутри керамической капсулы (корпуса) с наружным
диаметром около 4 мм. То есть ртуть и каломель с кристаллами хлористого калия
находились в полости этой капсулы, в дне которой выполнено сквозное отверстие.
Такой корпус данного ртутнокаломельного электрода не был герметичным.
В ХХ веке указанный ртутнокаломельный внутриполостной электрод
сравнения широко использовался в нашей стране в конструкциях внутрижелудочных
рН-зондов. Практически все разработчики конструкций таких рН-зондов обосновывали
свой выбор ртутнокаломельного электрода сравнения ссылкой на работу Кертиса Г.,
опубликованную в 1956г. Так они отмечали, что ртутнокаломельный электрод лучше
хлорсеребряного потому, что он обладает постоянным и воспроизводимым
потенциалом, если только при изготовлении ртутнокаломельного электрода соблюдены
все необходимые меры предосторожности. Вот и все обоснование.
Хотя из самых общих соображений у ртутнокаломельного электрода
сравнения были и очень серьезные недостатки, на которые им необходимо было
обратить внимание при оценке возможности его использования в конструкциях
внутрижелудочных рН-зондов для обследования человека.
Из общедоступных справочников известно, что главным недостатком
ртутнокаломельного электрода, является то, что его основные компоненты: ртуть и
каломель относятся к очень ядовитым веществам. Они отличаются высокой
токсичностью для любых форм жизни. Основной мерой предосторожности при работе с
изделиями, содержащими ртуть и ее соединения, является исключение попадания
ртути в организм человека через дыхательные пути и поверхность слизистой рта,
желудочно-кишечного тракта (ЖКТ) или кожи.
Появление паров ртути возможно в помещениях, в которых хранилисься
ртутьсодержащие рН-датчики (рН-зонды и т.д.) и проводились исследования
внутрижелудочной кислотности. Известно, что максимально возможная концентрация
паров ртути в воздухе при 20°С может достигать 15,2 мГ/м3 при ПДК
(предельно допустимой концентрации) ртути в воздухе 0,0003 мГ/м3.
Даже при концентрации паров ртути 0,005 мГ/м3 уже через 3 месяца
снижается мышечная работоспособность и наблюдается патология в печени, почках и
т.д.
Особенно чувствительны к ртутному яду дети. В конструкциях
каломельных электродов, применявшихся для детских внутрижелудочных рН-зондов,
ртуть находится в непосредственной близости к отверстию в дне корпуса
ртутнокаломельного электрода сравнения (рис. 5).
Известно, что недостатком ртутнокаломельного электрода сравнения [Линар
Е.Ю. 1968г., Панцырев Ю.М. со авторами 1972г. и др.] является соскальзывание
ртути с кончика платиновой проволоки и смешивание ее с наполнителем
ртутнокаломельного электрода. Очевидно, что при изучении кислотности в верхних
отделах ЖКТ человека, который при обследовании в основном сидит,
ртутнокаломельный электрод рН-зонда направлен своим торцем с отверстием вниз.
Следовательно, полость с кристаллами хлористого калия находилась ниже слоев
ртути и каломели, поэтому частицы ртути и каломели, имеющих значительно большую
плотность (соответственно 13,55 и 7,15 г/м3), чем плотность
насыщенного раствора хлорида калия, могли опускаться на дно корпуса электрода.
Нами был проведен визуальный осмотр содержимого, находящегося в
полости ртутнокаломельного электрода сравнения диаметром 7 мм (рис. 5б)
рН-зондов базовой конструкции [Новоселец С.А., 1999г.], находившихся в
эксплуатации в течение нескольких месяцев и после эксплуатации в течение года.
После снятия керамического колпака с отверстием диаметром 0,1 мм с
керамического корпуса ртутнокаломельного электрода на дне полости колпака была
обнаружена порошкообразная смесь каломели со ртутью. В этой смеси было много
шариков ртути диаметром 0,2÷0,5 мм и менее. Следовательно, при
эксплуатации паста каломели со ртутью и ртуть выпали из внутреннего отверстия
основания корпуса электрода (рис. 5б) и попали на дно колпака. Причиной этого
могли быть также: резкие движения концом зонда, удары, циклы «размачивания»
электрода сравнения с последующим высыханием между обследованиями.
Очевидно, что данные Линаром Е.Ю. в 1968 году и Панцыревым Ю.М. с
соавторами в 1972г рекомендации о необходимости хранения рН-зонда
ртутнокаломельным электродом вниз или вверх при температуре 10-25°C и
относительной влажности не ниже 80% реально не могли исправить основные
недостатки этих зондов даже, если бы в указанных рекомендациях были следующие
пункты: рН-зонды с ртутнокаломельным электродом в негерметичном корпусе должны
храниться в вытяжных шкафах и эксплуатироваться при температуре не выше 18°C;
они также подлежат утилизации и уничтожению после эксплуатации.
При хранении таких рН-зондов после высыхания полости каломельного
электрода происходило проникновение паров ртути в помещение через отверстие в
корпусе этого электрода.
Попадание ртути в организм человека могло происходить и в случае,
если каломельный электрод находится в ЖКТ. Отверстие диаметром около 0,1 мм в
корпусе ртутнокаломельного электрода может препятствовать попаданию в ЖКТ частиц
металлической ртути или каломели размером более 0,1 мм, но легко пропускает ионы
ртути. Растворимость ртути в воде составляет около 0,06 мГ/л при ПДК ртути в
воде 0,0005 мГ/л. ПДК каломели (в пересчете на ртуть) составляет 0,0005 мГ/л, а
реальная концентрация каломели в воде на порядки выше (несколько мГ на литр).
Учитывая то, что ртутнокаломельный электрод содержал достаточно
большое количество жидкой ртути и твердой каломели, попадание ионов ртути из
насыщенного каломелью раствора хлорида калия в желудок человека могло
происходить на протяжении всего срока эксплуатации каломельного электрода
сравнения в составе рН-датчика. Это обусловлено, в частности, тем, что диффузия
ионов через жидкостную границу между исследуемым раствором в ЖКТ человека и
соединительным раствором в ртутнокаломельном электроде протекает в обоих
направлениях.
Только из-за приведенных выше факторов опасности для человека
ртутнокаломельный электрод сравнения нельзя было применять, по-нашему мнению, в
конструкциях внутрижелудочных рН-зондов. Согласно «Санитарных правил…»,
утвержденных 6 марта 1969г., проведение работ, связанных с применением приборов
с ртутным заполнением, допускалось с разрешения органов санитарного надзора лишь
в тех случаях, когда технологически не представляется еще возможным замена их не
содержащими ртуть приборами.
А такая возможность у разработчиков рН-зондов с внутрижелудочным
ртутнокаломельным электродом была. Это применение хлорсеребряных электродов
сравнения.
В настоящее время ртутнокаломельные электроды сравнения в
конструкциях отечественных рН-зондов не используются.
Хлорсеребряный электрод сравнения
Хлорсеребряный электрод сравнения состоит из серебряного электрода,
хлористого серебра и раствора, содержащего анионы хлора, например, водного
раствора хлористого калия. Он функционирует согласно реакции:
AgCl + е → Ag
+ Cl¯
Неизменность этой реакции доказана в растворах, рН которых лежат в
пределах от 0 до 13 [Бейтс Р., 1972г.]. Хлорсеребряный электрод имеет потенциал,
зависящий от концентрации ионов хлора в растворе, в который электрод погружен,
так как она определяет растворимость хлористого серебра и, следовательно,
концентрацию катионов серебра. Величины стандартного потенциала хлорсеребряного
электрода приведены в таблице 5.
Таблица 5. Стандартный потенциал (φ0) хлорсеребряного электрода
|
Температура, °С |
20 |
25 |
35 |
40 |
|
φ0, В |
0,2256 |
0,2223 |
0,2156 |
0,2121 |
Потенциал хлорсеребряного электрода в насыщенном растворе
KCl при 37°С равен:
φ=0,215-0,061·lgаCl-=0,215-0,061·
lg(4,8·0,583)=0,188 В.
Потенциал хлорсеребряного электрода в нормальном (1н.) растворе
KCl будет составлять при 37°С:
φ=0,215-0,061·lg
(1,154·0,6)=0,225 В.
Величина потенциала насыщенного хлорсеребряного электрода в
децинормальном растворе HCl
составляет около 0,199 В (Бейтс Р.,1972г.). В эту величину входит и диффузионный
потенциал соединения между насыщенным KCl
и раствором соляной кислоты (0,1М). То есть реальный потенциал хлорсеребряного
электрода в сильнокислой среде может отличаться от потенциала последнего в
растворе KCl на величину
диффузионного потенциала между электродом и исследуемой средой.
Хлорсеребряный электрод характеризуется постоянным устойчивым и
воспроизводимым потенциалом в интервале температур 0 - 95°С, полностью безопасен
и довольно прост в изготовлении (Бейтс Р., 1972г.).
Наиболее простым по конструкции и технологии изготовления является
хлорсеребряный электрод, состоящий из серебра, находящегося в контакте с пастой
на основе хлористого серебра и хлорида калия (или хлорида натрия). Так, Белоусов
А.С. и Ястреб Н.И. в 1972г описали конструкцию такого хлорсеребряного электрода,
использованного в рН-датчике внутрижелудочной радиокапсулы. Хлорсеребряный
электрод представлял собой стаканчик из листового серебра, заполненный пастой из
равных частей хлористого серебра и хлористого натрия.
Более сложными в технологическом плане являются электролитический и
термический способы изготовления. Конструкция и технология изготовления таких
электродов достаточно подробно описаны различными авторами [Бейтс, 1972г., и
другие]. Электролитический способ изготовления хлорсеребряного электрода
заключается в создании на рабочей части серебряных элементов, изготовленных,
например, из проволоки диаметром 0,5 мм, слоя хлористого серебра путем анодного
электролиза в 1 М растворе соляной кислоты в течение 30 - 45 минут.
В процессе электролиза серебряные элементы являются анодом, а
катодом служит платиновая спираль. Слой хлористого серебра должен быть
достаточно толстым, а в противном случае равновесие на электроде будет
устанавливаться медленно. Для обеспечения достаточно прочного сцепления
сплошного слоя хлорида серебра с рабочей поверхность серебряного элемента
необходимо создать на ней неровности (царапины, выступы и т.д.).
Указанную технологию изготовления хлорсеребряных электродов
элктролизом мы применяли при изготовлении электродов сравнения в корпусах с
наружным диаметром не более 3÷4 мм (рис. 9).
Такие хлорсеребряные электроды сравнения для рн-зондов были впервые
созданы в нашей стране в 1990-91г.г. группой сотрудников ГНПП «Исток» (г.
Фрязино, Московская область) в составе Матафоновой Л.Ф., Цыкина А.В., Яковлева
Г.А., собранной по инициативе Калюжного В.Н., и успешно применены в конструкциях
первых в Российской Федерации и полностью безопасных для человека рН-зондов в
качестве внутриполостного электрода сравнения, закрепленного на рабочем конце
рН-зонда. Конструкция этих внутрижелудочных хлорсеребряных электродов сравнения
защищена патентом РФ № 2008035 с приоритетом от 12.02.91г.
Как видно из рисунка 9 а, корпус этих электродов был составной –
пластикокерамический. Хлорсеребряный элемент (Ag/AgCl)
закрепляется в пластиковом основании (втулке), с которым герметично был соединен
полимерным клеем керамический колпак с отверстием. Полость керамического колпака
заполняется мелкозернистым порошком хлористого калия. Перед измерением
внутрижелудочной кислотности керамический колпак погружали в насыщенный раствор
хлористого калия, который проникал через капиллярное отверстие внутрь колпака,
образовывая при этом насыщенный раствор хлористого калия с избытком его твердых
кристаллов.
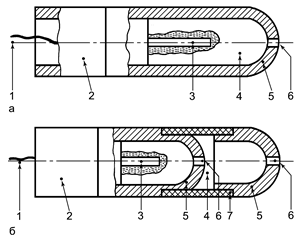
Рис. 9 Конструкции внутриполостных хлорсеребряных электродов
сравнения с одним (а) и двумя электролитическими ключами (б)
а) 1 – проводник; 2 – основание корпуса; 3 –
Ag/AgСl
электрод; 4 – кристаллы КСl; 5
– керамический колпак с отверстием 6;
б) 1 – проводник; 2 – основание корпуса; 3 –
Ag/AgСl
электрод; 4 – кристаллы КСl; 5
– керамический колпак с отверстием 6; 7 – полимерная трубка.
Понятно, что при длительной (до года и более) многократной
эксплуатации такого электрода, особенно в случаях длительных (до 24ч) циклов
измерения кислотности и циклов обработки (длительностью до 6 часов) в жидких
дезинфицирующих средствах на основе воды, концентрация хлористого калия в водном
насыщенном растворе электрода сравнения может уменьшаться, в частности, за счет
вымывания (вытяжки) хлористого калия из керамического корпуса электрода. Это
будет приводить к росту потенциала электрода сравнения (см. табл. 4), а,
следовательно, к изменению (увеличению) электродвижущей силы (ЭДС) рН-датчика.
С целью предотвращении этого явления нами была разработана
конструкция электрода сравнения с двумя последовательно соединенными отрезком
полимерной трубки керамическими колпаками (рис.9 б). В полости первого колпака
размещен хлорсеребряный элемент вместе с кристаллами хлористого калия, а вторая
полость, образованная вторым колпаком и отрезком полимерной трубки, заполнена
кристаллами хлористого калия и защищает первую основную рабочую полость
хлорсеребряного электрода от «вымывания» хлористого калия. Второй колпак может
быть съемным, а при эксплуатации в него по мере необходимости может добавляться
хлористый калий. Эти конструкции внутрижелудочных электродов сравнения защищены
патентами РФ [Яковлев Г.А. рН-зонд. Патенты РФ №2115444; РФ №2063250].
Одна из разновидностей термического типа хлорсеребряных электродов
представляет собой смесь серебра и хлорида серебра, образованную, например,
термической диссоциацией пасты, нанесенной на платину (Бейтс Р., 1972г.). Паста
может, например, состоять из смеси окисла серебра (Ag2О)
и хлората серебра (AgClО3)
или смеси окисла серебра и хлорида серебра (AgCl).
В первом случае нагрева до 400°С и выше из окиси серебра образуется серебро, а
из хлората серебра, уже начиная с температуры 270°С, образуется хлорид серебра.
Нами были разработаны конструкции хлорсеребряных электродов
термического типа для многократного применения и технология их изготовления.
Конструкции этих электродов защищены патентами Российской Федерации [Яковлев
Г.А. Электрод для снятия биопотенциала. Патент РФ №2093067; Яковлев Г.А.
Хлорсеребряный электрод для снятия биопотенциала. Патент РФ № 2177714]. Рабочий
конец серебряного элемента электрода размещен на дне полости керамического
корпуса, плотно заполненной материалом на основе хлорида серебра (рис. 10).
Хлорсеребряный электрод в керамическом корпусе имеет наружный
пластмассовый корпус тарелкообразной формы с плоским фланцем, обеспечивающий
контакт с кожей человека. То есть эти хлорсеребряные электроды, изготовленные в
автономном пластикокерамическом корпусе, крепятся при обследовании к коже,
например, запястья человека, с помощью ремня с липкой лентой или с помощью
пластыря.
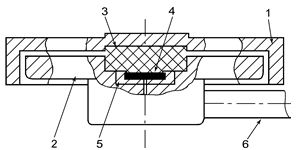
Рис. 10 Конструкция накожного хлорсеребряного электрода
1 – съемная крышка; 2 – пластмассовый корпус; 3 – электродная
паста; 4 - Ag/AgСl
электрод; 5 – керамический корпус; 6 – проводник
Нами был также предложен и разработан способ надежного
«герметичного» крепления накожного электрода сравнения к коже обследуемого,
например, в подключичной области с помощью двух пластырей: двухстороннего
пластыря в виде кольца и одностороннего пластыря в виде квадрата с отверстием.
Сначала фланец накожного электрода сравнения приклеивают к коже с
помощью двухстороннего кольцевого пластыря, а затем окончательно закрепляют
накожный электрод сравнения с частью электродного провода на коже посредством
прямоугольного, одностороннего пластыря с отверстием.
Испытания такого способа крепления накожного электрода сравнения
рН-зонда проведенные на кафедре детских болезней №2 РГМУ и в других клиниках
показали надежность фиксации электрода сравнения в течение всего периода
суточного мониторирования рН, отсутствие реакций со стороны кожи в месте
крепления и, следовательно, безопасность его для пациента.
Для обеспечения надежного и длительного (до 24ч и более)
электрического контакта накожного хлорсеребряного электрода с кожей человека
нами была усовершенствована электродная паста, содержащая воду, хлористый калий,
глицерин и другие компоненты.
Состав этой пасты защищен патентом РФ [Яковлев Г.А. Электродная
паста для накожного хлорсеребряного электрода сравнения рН-зонда. Патент РФ №
2204994]. Содержание в пасте 5,5÷8,5 мас.%
хлористого калия обеспечивает качественную и достаточно быструю подготовку
накожного электрода к работе, необходимую электропроводность контактной
прослойки между электродом и кожей человека и относительно невысокое
сопротивление (не более 20-30 кОм) хлорсеребряного электрода.
Электродная паста находится в полости хлорсеребряного электрода.
Для предотвращения быстрого высыхания электродной пасты электрод имеет крышку,
изготовленную из непрозрачной пластмассы. Крышка защищает также хлорсеребряный
электрод от действия прямых солнечных лучей.
При эксплуатации рН-зонда электродную пасту в полости накожного
электрода необходимо заменять на свежую ежедневно в зависимости от режима
работы.
Были проведены медицинские испытания электродной пасты на кафедре
гастроэнтерологии ФУВ РГМУ (зав. кафедрой гастроэнтерологии д.м.н., профессор
Яковенко Э.П.), в МОНИКИ, на базе отделения гастроэнтерологии РНЦХ РАМН и ряде
других клиник. Установлено, что паста обеспечивает надежный контакт накожного
хлорсеребряного электрода с кожей пациента, не оказывает раздражающей
аллергической реакции на кожу пациента, не высыхает в процессе суточного
обследования в случае герметичного крепления накожного электрода к коже
посредством двух пластырей и легко удаляется с кожи с помощью воды.
Токсиколого-гигиенические испытания накожного хлорсеребряного
электрода и пасты показали, что они нетоксичны и полностью отвечают требованиям,
предъявляемым к медицинским изделиям, длительно контактирующим с неповрежденной
кожей.

