 |
|  |
| Медицинская библиотека / Раздел "Книги и руководства" |
|
|
|
| 3.2. Особенности нарушений липидного обмена у лиц с посттравматическим стрессовым расстройством |
|
Медицинская библиотека / Раздел "Книги и руководства" / Стресс и возраст / 3.2. Особенности нарушений липидного обмена у лиц с посттравматическим стрессовым расстройством
Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Cлов в этом тексте - 8178; прочтений - 1269
Размер шрифта:
12px |
16px |
20px
3.2. Особенности нарушений липидного обмена у лиц с
посттравматическим стрессовым расстройством
Нарушения липидного обмена считаются одним из основных факторов,
приводящих к атеросклеротическим изменениям сосудов. Не затрагивая
патогенетических механизмов развития атеросклеротической бляшки, необходимо
отметить, что большое значение в развитии атеросклероза имеет не абсолютное
содержание липопротеинов в крови, а сохранение баланса атерогенных липопротеинов,
т.е. липопротеинов низкой и очень низкой плотности - соответственно ЛПНП и ЛПОНП,
и антиатерогенных липопротеинов, т.е. липопротеинов высокой плотности - ЛПВП
(Никитин Ю.П., 2006). В связи с этим мы в своих исследованиях также стремились
максимально детализировать липидный спектр.
Средние показатели липидного спектра крови наблюдавшихся нами
пациентов представлены на рис. 10 и в табл. 35.
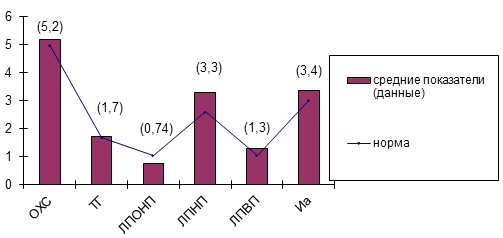
Рис. 10. Средние показатели липидов крови (ммоль/л)
Таблица 35. Средние показатели липидного спектра
в сравнении с рекомендуемыми ВНОК нормами (ммоль/л)
|
Показатели липидного спектра |
Средние данные
M±m |
ДИ±95% |
Показатели, рекомендованные ВНОК |
|
Общий холестерин |
5,24±0,09 |
5,1-5,4 |
<5,0 |
|
Триглицериды |
1,69±0,08 |
1,6-1,9 |
<1,7 |
|
ЛПОНП |
0,75±0,03 |
0,68-0,82 |
<1,04 |
|
ЛПНП |
3,29±0,09 |
3,1-3,5 |
<3,0 |
|
ЛПВП |
1,30±0,03 |
1,2-1,4 |
>1,0 |
|
Индекс атерогенности |
3,37±0,14 |
3,1-3,7 |
<3,0 |
Мы сравнили показатели липидного обмена у ветеранов боевых действий
со средними показателями в соответствующих возрастных группах мужчин,
проживающих в г.Новосибирске (Шальнова С.А., Никитин Ю.П., Симонова Г.И., 2010).
Полученные различия касались прежде всего триглицеридов и ЛПВП. Если у мужского
населения г. Новосибирска повышенное содержание триглицеридов (>1,7 ммоль/л)
отмечено в 18%, то среди участников боевых действий - в 36,2% (p<0,05), низкое
содержание ЛПВП (<1,0 ммоль/л) – соответственно в 16% и 24,6%. Встречаемость
повышенных значений ЛПНП не различались - у 53% и 50,3% пациентов.
Показатели общего холестерина к ветеранов боевых действий
коррелировали с их возрастом (r=0,24; р=0,021) и индексом массы тела - ИМТ (r=0,17;
р=0,034). Кроме того, корреляционная связь ИМТ была выявлена с уровнем
триглицеридов (r=0,37; р=0,0001), ЛПОНП (r=0,39; р=0,0001), ЛПНП (r=0,2; р=0,033)
и индексом атерогенности (r=0,36; р=0,0001). Показатели же ЛПВП обнаружили
обратную корреляционную зависимость от ИМТ (r=-0,33; р=0,0001).
По типу дислипидемий (рис. 11), согласно классификации ВОЗ, у
ветеранов боевых действий преобладал 2а тип (32,3%). 2в тип определялся у 16,8%
ветеранов, и 4 тип - у 8,7%. У 71 (44,1%) участника боевых действий уровень
липидов находился в пределах нормальных показателей. Выявленные типы
дислипидемий были связаны с возрастом (F=3,2;р=0,024) и ИМТ (F=6,6;р=0,0003).
Нормальные показатели липидного обмена и 4 тип дислипидемии преобладали в более
молодом возрасте, что вполне объяснимо с позиций ассоциативности атеросклероза с
процессом старения.
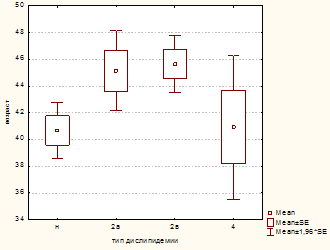
Рис. 11. Тип дислипидемии и возраст участников
боевых действий Примечание: n-
рекомендованные нормальные показатели
У ветеранов афганской войны чаще, чем у ветеранов боевых действий
на Северном Кавказе, определялся 2в тип дислипидемии (р=0,016), регистрировались
более высокие показатели общего холестерина (р=0,006), ЛПНП (р=0,02), индекс
атерогенности (р=0,027). И наоборот, у бывших участников боевых действий на
Северном Кавказе чаще, чем у ветеранов войны в Афганистане, диагностировались 4
тип дислипидемии и нормальные показатели липидного обмена (р=0,018). При этом
нормальные показатели липидов ассоциировались не только с более молодым
возрастом. Например, среди ветеранов войны на Северном Кавказе нормальные
показатели преобладали в возрастных категориях 24-34 и 55-69 лет, а среди
ветеранов войны в Афганистане – в возрасте 35-54 лет. У бывших участников обоих
вооруженных конфликтов 4 тип дислипидемии определялся чаще в возрасте до 44 лет,
а среди ветеранов войны в Афганистане во всех возрастных категориях чаще
выявлялся 2в тип дислипидемии, а 2а тип – после 55 лет (табл. 36).
Таблица 36. Зависимость типов дислипидемий от
возраста и зоны боевых действий
|
Возраст (лет) |
Зона боевых действий |
Типы дислипидемий |
Норма
n (%±m) |
|
2а тип
n (%±m) |
2в тип
n (%±m) |
4 тип
n (%±m) |
|
24-34 |
Сев. Кавказ (n=40) |
10
(25,0±0,1) |
2
(5,0±0,1) |
5
(12,5±0,2) |
23
(57,5±0,1) |
|
35–44 |
Афганистан
(n=30) |
7
(23,3±0,1) |
6
(20,0±0,1) |
3
(10,0±0,3) |
14
(46,7±0,1) |
|
Сев. Кавказ (n=18) |
7
(38,9±0,1) |
1
(5,6±0,1) |
1
(5,6±0,3) |
9
(50,0±0,1) |
|
45–54 |
Афганистан (n=46) |
13
(28,3±0,1) |
14
(30,4±0,1) |
1
(2,2± 0,5) |
18
(39,1±0,1) |
|
Сев. Кавказ (n=20) |
5
(25,0±0,1) |
4
(20,0±0,1) |
1
(5,0±0,5) |
10
(50,0±0,1) |
|
55–69 |
Афганистан (n=10) |
8
(80,0±0,1) |
- |
1
(10,0±0,5) |
1
(10,0±0,2) |
|
Сев. Кавказ (n=7) |
2
(28,6±0,2) |
- |
1
(14,3±0,5) |
4
(57,1±0,2) |
Выявленные значения липопротеидов при всех заболеваниях
сердечно-сосудистой системы у ветеранов боевых действий оказались выше
рекомендованных ВНОК. Кроме того, изменения индекса атерогенности, особенно при
нейроциркуляторной дистонии, свидетельствовали о выраженном изменении
соотношения фракций липидов – уменьшение ЛПВП и увеличение ЛПНП Статистический
анализ изменений липидного обмена при заболеваниях сердечно-сосудистой системы
показал, что артериальная гипертония сопровождалась повышением уровня общего
холестерина (р=0,001), триглицеридов (р=0,0029), ЛПОНП (р=0,0025) и индекса
атерогенности (р=0,017). При ишемической болезни сердца определялись еще более
высокие показатели общего холестерина (р=0,029), ЛПНП (р=0,037) и индекса
атерогенности (р=0,05). Цереброваскулярные заболевания, особенно в сочетании с
артериальной гипертонией, и нейроциркуляторная дистония сопровождались
повышением индекса атерогенности. Кроме того при нейроциркуляторной дистонии
были повышены ЛПОНП (р=0,001), а при отчетливой цереброваскулярной патологии
триглицеридемия была выше 2,0 ммоль/л.
Патология сердечно-сосудистой системы у бывших участников боевых
действий, за исключением нейроциркуляторной дистонии, в основном дебютировала
после 35 лет. Вполне естественно, поэтому, что зависимость дислипидемии от
возраста была особенно заметной для лиц, страдающих артериальной гипертонией (р=0,0002),
ишемической болезнью сердца (р=0,002), цереброваскулярными заболеваниями (р=0,0001).
В эксперименте (Панин Л.Е., 2006) было показано различное действие
фракций липопротеидов на скорость коронарного кровотока и частоту сердечных
сокращений. Так, повышенное содержание ЛПОНП и ЛПНП способствовало снижению
коронарного кровотока и увеличению частоты сердечных сокращений, создавая
предпосылки к гипоксии миокарда. В нашем исследовании мы также сопоставили
результаты ЭКГ и показатели липидного обмена (табл. 37).
Таблица 37. Показатели липидного обмена и
изменения ЭКГ (M±m)
|
ЭКГ-синдромы |
Общий холестерин (ммоль/л) |
Триглицериды (ммоль/л) |
ЛПОНП (ммоль/л) |
ЛПНП (ммоль/л) |
ЛПВП (ммоль/л) |
Индекс атерогенности |
|
Норма |
5,4±0,5 |
1,5±0,2 |
0,6±0,1 |
2,6±0,3 |
1,4±0,3 |
2,8±0,7 |
|
Ми |
5,3±0,3 |
1,8±0,3 |
0,8±0,1 |
3,1±0,3 |
1,6±0,1 |
2,8±0,4 |
|
Нпв |
5,3±0,5 |
1,6±0,1 |
0,72±0,04 |
3,3±0,1 |
1,3±0,06 |
3,3±0,2 |
|
Глж |
5,8±0,3 |
2,07±0,3 |
0,9±0,1 |
3,5±0,3 |
1,3±0,1 |
3,9±0,5 |
|
Сррж |
5,2±0,3 |
1,5±0,3 |
0,55±0,06 |
3,1±0,3 |
1,4±0,1 |
3,1±0,5 |
|
Н. ритма |
5,8±0,9 |
2,4±0,1 |
1,1±0,01 |
3,9±0,9 |
0,8±0,05 |
6,2±1,1 |
Примечания: Ми – метаболические изменения, Нпв - нарушения
проведения возбуждения, Глж- гипертрофия левого желудочка сердца, Сррж- синдром
ранней реполяризации желудочков, Н. ритма- нарушение сердечного ритма
Индекс атерогенности оказался в пределах нормы при нормальных же
результатах ЭКГ исследования, а также при выявленных метаболических изменениях
миокарда; повышенные значения этого индекса определялись при нарушениях
сердечного ритма, гипертрофии левого желудочка сердца, нарушении проведения
возбуждения в миокарде.
Ранее проведенное исследование липидного обмена у ветеранов боевых
действий (Karlovic
D., Martinac
М., Buljan
D., Zoric
Z., 2004) показало, что боевое
ПТСР сопровождалось более высоким уровнем общего холестерина (р=0,001), ЛПНП (р=0,002),
триглицеридов (р=0,001) и снижением ЛПВП (р<0,001), чем у военнослужащих без
ПТСР. R.
Von Känel,
B.
Kraemer, H.
Saner
et al.
(2010) выявили снижение ЛПВП при ПТСР. Наши исследования подтвердили эти данные.
Более того, имеется тенденция к обратной зависимости показателей общего
холестерина, ЛПНП и выраженности симптоматики ПТСР у ветеранов боевых действий.
Так, сравнивая показатели холестерина крови у пациентов с выраженным ПТСР (более
70 баллов) и у лиц без ПТСР, мы убедились в том, что более высокие значения
уровня холестерина имели место у ветеранов без ПТСР (табл. 38). Кроме того,
статистически достоверными оказались результаты определения ЛПНП у ветеранов с
выраженным ПТСР и при его незначительных проявлениях (t=2,1;
р=0,042).
Таблица 38. Показатели липидного обмена при
различной выраженности ПТСР (M±m)
|
Выраженность ПТСР |
Общий холестерин (ммоль/л) |
Триглицериды (моль/л) |
ЛПОНП (ммоль/л) |
ЛПНП (ммоль/л) |
ЛПВП (ммоль/л) |
Индекс атерогенности |
|
Без ПТСР |
5,7±0,6 |
1,6±0,2 |
0,7±0,07 |
3,55±0,08 |
1,38±0,13 |
3,5±0,6 |
|
Незначительное |
5,4±0,2 |
1,78±0,2 |
0,7±0,07 |
3,48±0,16 |
1,25±0,1 |
3,7±0,3 |
|
Умеренное |
5,2±0,2 |
1,75±0,1 |
0,73±0,06 |
3,2±0,17 |
1,34±0,06 |
3,2±0,2 |
|
Выраженное |
5,0±0,1 |
1,66±0,1 |
0,79±0,07 |
3,1±0,14 |
1,33±0,07 |
3,3±0,2 |
|
F |
1,46 |
0,13 |
0,41 |
1,21 |
0,38 |
0,87 |
Примечание: F- критерий Фишера
В табл. 39 показана частота выделенных типов дислипидемий у
пациентов с различной выраженностью ПТСР. Нормальные показатели липидного обмена
чаще выявлялись у ветеранов с выраженными (53,5%) и умеренными (44,7%) ПТСР.
Меньшая выраженность ПТСР (61 балл) была у пациентов с 2а типом дислипидемии (р=0,026).
При 2в и 4 типе дислипидемий не определено достоверной связи с выраженностью
ПТСР.
Таблица 39. Наличие и выраженность ПТСР при
различных типах дислипидемий
|
Тип дислипидемии |
Нет ПТСР (n=14) абс.-% |
Незначительное ПТСР
(n=42)
абс. - % |
Умеренное ПТСР (n=47)
абс. - % |
Выраженное ПТСР (n=58)
абс. - % |
ПТСР (баллы) M±m |
|
Нормальные показатели |
6-42,6 |
14-33,3 |
21-44,7 |
32-55,2 |
67,7±1,5* |
|
2а тип |
4-28,6 |
20-47,6 |
14-29,8 |
12-20,7 |
61,9±1,5 |
|
2в тип |
3-21,4 |
6-14,3 |
7-14,9 |
9-15,5 |
65,6±2,5 |
|
4 тип |
1-7,1 |
2-4,8 |
5-10,6 |
5-8,6 |
66,6±2,9 |
Примечание:*- р=0,026 достоверная разность нормальных показателей
липидного обмена и 2а типом дислипидемии
Нами показана обратная корреляционная зависимость выраженности ПТСР
и значений общего холестерина (r=-0,16; р=0,038). Показатели общего холестерина
(р=0,018), ЛПНП (р=0,022) коррелировали со снижением памяти, ЛПОНП – с
злоупотреблением алкоголем (р=0,001), нарушением сна (р=0,018) и тревожностью (р=0,041).
Перенесенные стрессы мирной жизни коррелировали с уровнем ЛПНП (r=0,23;
р=0,023). Интенсивность болевого синдрома по ВАШ коррелировала со значениями
ЛПВП (r=0,21; р=0,019). Связи
депрессии с изменениями липидного спектра, на первый взгляд, не выявлялось, но
при сопоставлении с выявленными типами дислипидемий получены несколько иные
результаты (табл. 40).
Таблица 40. Выраженность психопатологических
состояний (баллы) при различных типах дислипидемии (M±m)
|
Психопатологические состояния |
Типы дислипидемий и выраженность психопатологических
состояний в баллах |
|
Норма |
2а тип |
2в тип |
4 тип |
|
ПТСР |
68,1±1,5 (р=0,003) |
61,5±1,5 |
66,5±2,5 |
65,2±2,8 |
|
Депрессия |
13,9±0,9 (р=0,022) |
10,1±1,0 |
12,3±1,3 |
9,6±1,5 |
|
Тревожность |
26,8±1,9 |
22,7±2,1 |
30,3±2,7 |
22,6±3,0 |
Примечание: статистическая достоверность - между группами контроля
(нормальные показатели) и 2а типом дислипидемии; депрессия оценивалась по тесту
А. Бека, реактивная тревожность – по анкете Спилбергера-Ханина.
Оказалось, что нормальные показатели липидного обмена связаны с
более выраженными проявлениями ПТСР, депрессии. При 2в типе гиперлипопротеинемии
выраженность ПТСР, депрессии и тревожности были наиболее высокими.
Выявленные изменения липидного обмена у ветеранов боевых действий,
страдающих ПТСР, представляется возможным объяснить следующим образом (Мякотных
В.С., Торгашов М.Н., 2015).
Под действием эндогенных глюкокортикоидов и катехоламинов при
стрессе усиливается липолиз, повышается уровень триглицеридов. Глюкокортикоиды
действуют на липидный метаболизм в печени по-иному, чем в периферической жировой
ткани. Длительный избыток глюкокортикоидов в печени активирует
1-α-фосфотидатфосфогидролазу. При этом происходит стимуляция этерификации
неэтерифицированных жирных кислот и увеличивается синтез, продукция и накопление
триглицеридов и ЛПОНП, а увеличение в крови ЛПНП является вторичным (Михайлов
В.В., 2001; Пшенникова М.Г., 2001). Поэтому стресс, особенно, длительный и
хронический, может приводить к гиперлипопротеидемии. Часто ПТСР неверно
связывают с понятием хронический стресс, хотя на самом деле ПТСР является
заболеванием, связанным со стрессовым событием экстраординарной важности, и при
этом стресс может быть как острым, так и хроническим. Морфологические изменения,
наблюдаемые при ПТСР, связаны с дизрегуляцией отделов ЦНС, участвующих в
стресс-реакции, и в конечном счете, приводят к нарушениям в
гипоталамо-гипофизарно-надпочечниковой системе. Как показано во многих
исследованиях, при ПТСР наблюдается пониженное содержание кортизола в крови,
изменение его циркадного ритма (Mason
J.W.,
Giller
E.L.,
Kosten
T.R.,
et al.,
1988; Yehuda
R., Halligan
S.L.,
Grossman
R. et
al., 2002). Стрессовая реакция
характеризуется увеличением выделения кортизола, катехоламинов; при ПТСР эта
реакция приобретает более интенсивный характер вследствие изменения функций
стресс-лимитирующей системы. Нарушения адаптации организма на повторные стрессы
заключаются в длительной гормональной нагрузке и неспособности «выключить»
стресс-ответ. Если при непродолжительном стрессовом воздействии кортизол и
катехоламины проявляют свои защитные и адаптивные функции, то при хронических
стрессах или дизрегуляции гормонального ответа на стресс включается их
патогенетическое действие (McEvan B.S., 1998). Являясь результатом недостаточной
адаптации на повторные стрессы, у ветеранов, перенесших стрессы мирной жизни,
чаще выявлялась гиперлипопротеинемия 2а типа (р=0,037), а также более высокие
показатели ЛПНП (р=0,023).
Надо сказать, что несмотря на некоторые статистически недостоверные
различия по представленным группам, в целом интенсивность ПТСР в наших
наблюдениях не зависела от возраста (табл. 41). Средний возраст лиц с выраженным
ПТСР составил 43,1±1,2 лет, умеренным - 42,4±1,4 лет, незначительным - 43,5±1,5
лет; отсутствие признаков ПТСР отмечено у лиц в среднем возрасте 41,2±2,8 лет. В
то же время имеются различия в связи с той или иной зоной боевых действий;
определяется отчетливое преобладание лиц с выраженным ПТСР среди ветеранов
боевых действий на Северном Кавказе (р<0,001), а с умеренно и незначительно
выраженным ПТСР, наоборот, среди бывших участников войны в Афганистане. Наиболее
высокая доля лиц с выраженным ПТСР была среди участников обоих вооруженных
конфликтов, о чем говорилось выше.
Таблица 41. Интенсивность ПТСР в зависимости от
возраста
|
Интенсивность ПТСР |
Число больных с разной интенсивностью ПТСР:
n (%±m) |
|
24-34 лет (n=40) |
35-44 лет (n=46) |
45-54 лет (n=59) |
55-69 лет (n=16) |
|
Нет ПТСР (n=14) |
3 (7,5±0,6) |
5 (10,9±1,4) |
5 (8,5±0,5) |
1 (6,3) |
|
Незначительное (n=42) |
10 (25,0±1,0) |
10 (21,7±1,0) |
18 (30,5±0,6) |
4 (25,0±1,2) |
|
Умеренное (n=47) |
14 (35,0±0,6) |
12 (26,1±0,8) |
17 (28,8±0,5) |
4 (25,0±1,3) |
|
Выраженное (n=58) |
13 (32,5±0,8) |
19 (41,3±0,5) |
19 (32,2±0,4) |
7 (43,8±1,3) |
Учитывая разный период времени, прошедший с момента окончания
участия в боевых действиях, можно предположить, что степень выраженности ПТСР
может постепенно снижаться по мере увеличения продолжительности послевоенного
периода - аналогично тому, что было отмечено у бывших участников Великой
Отечественной войны (Мякотных В.С., Боровкова Т.А., 2009). При этом запущенный
боевым стрессом и следующим за ним ПТСР ускоренный процесс формирования и
развития сердечно-сосудистой патологии, в том числе на основе атеросклероза, и
связанной с ним гиперлипидемии переходит в новую, возрастзависимую стадию и
становится неразрывно связанным уже более с процессом старения организма в
целом, чем с воздействием ПТСР.
При сравнительном анализе некоторых биохимических показателей и
показателей уровня липидов определена корреляционная связь значений сахара крови
с уровнем триглицеридов (r=0,26;
р=0,008), ЛПОНП (r=0,25; р=0,005),
ЛПНП (r=0,18; р=0,046) и
индексом атерогенности (r=0,2;
р=0,027). Показатели уровня мочевой кислоты коррелировали с показателями
триглицеридов (r=0,79; р=0,000)
и ЛПОНП (r=0,78; р=0,000), что
согласуется с данными некоторых исследований о патогенетической роли мочевой
кислоты в развитии сердечно-сосудистых заболеваний (Кобалава Ж.Д., Толкачева
В.В., 2011). Показатели тимоловой пробы коррелировали со значениями
триглицеридов (r=0,45; р=0,000),
ЛПОНП (r=0,38; р=0,005) и
индексом атерогенности (r=0,34;
р=0,009), и это может указывать на то, что изменение метаболизма жира в
гепатоцитах является следствием нарушения обмена свободных жирных кислот, а это
сопровождается снижением синтеза и секреции ЛПОНП, что приводит к стеатозу (Буеверов
А.О., Драпкина О.М., Ивашкин В.Т., 2008). Количество факторов, участвующих в
формировании стеатогепатита обширно, но основная роль (около 75%) в этом
процессе принадлежит алкоголю. Усиление синтеза триглицеридов обусловлено
повышением глицеро-3-фосфата в результате окисления этанола в печени и снижением
β-окисления свободных жирных кислот в митохондриях гепатоцитов (Буеверов А.О.,
Драпкина О.М., Ивашкин В.Т., 2008; Вовк Е.И., 2011). Вероятно поэтому показатели
триглицеридов (r=0,2; p=0,023)
и ЛПОНП (r=0,29;
p=0,001) были отчетливо повышены у
лиц, злоупотребляющих алкоголем. Важным фактором в развитии стеатоза печени
являются инфекционные заболевания, которые, как известно, были широко
распространены среди военнослужащих на территории Афганистана (Мякотных В.С.,
2009; Альтман Д.Ш., Давыдова Е.В., Кочеткова Н.Г., Светлакова В.А., 2012).
Последствия вирусного гепатита А, брюшного тифа и других инфекционных
заболеваний на фоне нередкого злоупотребления алкоголем приводили к изменениям
метаболизма свободных жирных кислот. Отсюда более высокие показатели общего
холестерина (р=0,006), ЛПНП (р=0,02) именно у ветеранов Афганистана, в том числе
и при патологии печени, выявленной методами УЗИ.
Результаты исследования (табл. 42) убедительно показывают, что
жировые изменения печени, особенно сопровождающиеся гепатомегалией, изменяют
липидный обмен. Стеатоз печени приводит к так называемому «липидному квартету»,
характерному для гиперлипопротеинемии 2в, а именно к повышению уровней общего
холестерина, триглицеридов, ЛПОНП и ЛПНП и, как следствие, к увеличению
коэффициента атерогенности (Вовк Е.И., 2011). Среди наблюдавшихся нами бывших
участников боевых действий данный тип дислипидемии диагностирован чаще у
ветеранов войны в Афганистане.
Таблица 42. Показатели липидного спектра и
патология печени (M±m)
|
Состояние печени |
Общий холестерин (ммоль/л) |
Триглицериды (ммоль/л) |
ЛПОНП (ммоль/л) |
ЛПНП (ммоль/л) |
ЛПВП (ммоль/л) |
Индекс атерогенности |
|
Норма (n=27) |
5,0±0,2 |
1,54±0,2 |
0,67±0,1 |
2,89±0,2 |
1,3±0,1 |
2,8±0,2 |
|
Жировой гепатоз (n=13) |
5,2±0,5 |
1,87±0,3 |
0,84±0,2 |
3,59±0,5 |
1,07±0,1 |
4,3±0,8 р=0,017 |
|
Гепатомегалия (n=11) |
4,8±0,2 |
1,65±0,2 |
0,76±0,1 |
2,9±0,1 |
1,25±0,1 |
3,2±0,4 |
|
Сочетание жирового гепатоза и гепатомегалии (n=4) |
6,2±0,5 р=0,04 |
2,99±1,4 р=0,04 |
1,36±0,6 р=0,034 |
4,3±0,3 р=0,026 |
1,3±0,5 |
5,3±0,9 р=0,017 |
Примечание: статистическая достоверность рассчитывалась по критерию
Стьюдента с нормальными показателями
При подведении итогов представленных исследований возникает четкое
ощущение того факта, что ПТСР, хронические болевые синдромы и целый ряд
соматических патологических процессов являются звеньями одной цепи, которая и
создает ситуацию формирования и развития так называемой стресс-индуцированной
патологии в целом. В наибольшей степени при этом, конечно же, страдают нервная и
сердечно-сосудистая системы. Но если в диагностике патологических процессов в
нервной системе, в частности травматической болезни головного мозга,
значительную, если не первостепенную роль играет доказанный факт получения
физической травмы, то в диагностике же патологии сердечно-сосудистой системы и
построении ее патофизиологической схемы нередко требуется доказательство бывшего
стрессового расстройства, в нашем случае боевого, и ПТСР. При этом несомненно
доказано, что преобладающим вариантом патологии сердечно-сосудистой системы у
ветеранов боевых действий является артериальная гипертония, и нейроэндокринные
изменения, возникшие вследствие перенесенного боевого стресса, явились важным
фактором как ее патогенеза, так и в целом сердечно-сосудистой патологии на
раннем этапе. В дальнейшем формирование и развитие сердечно-сосудистой патологии
у бывших участников боевых действий уже в значительной степени оказывается
зависимым от возраста пострадавших и от продолжительности периода, прошедшего
после окончания участия в военных кампаниях. Последний фактор является особенно
значимым для развития цереброваскулярной патологии. Изменения центральной
регуляции нервной системы при ПТСР со временем, при отсутствии адекватной
терапии приводят к несомненной трансформации так называемой нейроциркуляторной
дистонии в артериальную гипертонию, и с этих позиций указанную
нейроциркуляторную дистонию можно с уверенностью рассматривать в качестве ранней
стадии артериальной гипертонии. Негативные последствия боевого стресса в
дальнейшем могут усиливаться неблагоприятными социальными и
финансово-экономическими факторами мирного, послевоенного времени, связанными в
основном с трудовой деятельностью. При этом нарастающие процессы дезадаптации
формируют уже целый ряд патологических единиц, неразрывно связанных между собой.
Это и «палитра» хронических болевых синдромов, и заболевания желудочно-кишечного
тракта, опорно-двигательного аппарата, и наконец, развитие дислипидемий,
способствующих формированию атеросклеротических изменений сосудов в достаточно
молодом возрасте. В итоге выраженное ПТСР оказывается коморбидно сочетанию
артериальной гипертонии с патологией желудка, что убедительно указывает на
дезадаптационный характер той и другой патологии, а показатели липидного спектра
ветеранов боевых действий отчетливо выше не только рекомендованных значений ВНОК,
но и показателей, зарегистрированных среди лиц, не принимавших участия в боевых
действиях и не страдавших ПТСР. Более того, в отличие от гражданского населения,
у бывших участников боевых действий значительно чаще выявляются
гипертриглицеридемия и снижение значений ЛПВП, а также тенденция к обратной
зависимости выраженности ПТСР и значений общего холестерина и ЛПНП. Все это
определяет высокий индекс атерогенности при всех заболеваниях
сердечно-сосудистой системы у ветеранов боевых действий. Но с другой стороны, не
только боевой стресс и следующее за ним ПТСР способствуют развитию нарушений
липидного обмена. Например, ПТСР, развивающееся уже непосредственно в
постстрессовом периоде, не способствует развитию гиперлипидемии, а
следовательно, и атеросклероза. Более того, выраженность ПТСР снижается по мере
удаления от момента воздействия боевого стресса, а наблюдаемая у ветеранов
современных боевых действий гиперлипидемия не находится в прямой зависимости от
выраженности ПТСР, а оказывается более связанной с увеличением возраста
пациентов. Возможно, именно поэтому нами выявлены различия в характере изменений
липидного спектра у ветеранов войны в Афганистане и на Северном Кавказе, хотя
определенное влияние на этот процесс, вероятно, привнесли патологические
изменения метаболизма печени, связанные с перенесенными тяжелыми инфекциями, а
также нередко имевшая место алкогольная зависимость.
Определенное своеобразие имеют хронические болевые синдромы,
развивающиеся на фоне последствий боевого стресса и ПТСР, а само ПТСР имеет ряд
особенностей именно у лиц, страдающих хроническими болями. В частности, в
симптоматике ПТСР у пациентов с хронической болью в груди преобладали симптомы
вторжения и гиперактивации. Вероятно, в результате нейроэндокринных изменений
при ПТСР и хронической боли происходит интенсификация адренергических влияний и
формируется дисбаланс в гипоталамо-гипофизарно-надпочечниковой и
симпатоадреналовой системах. Адренергические влияния на миокард приводят не
только к изменениям в проводящей системе, что фиксировалось на ЭКГ, но и к
нарушениям в системе перекисного окисления липидов (ПОЛ), к повреждениям
мембранного аппарата и к усилению кальциевой альтерации миокарда, к изменению
энергозависимых процессов, что в конечном итоге приводит к его гипоксии.
Формируется и развивается определенного рода взаимоподдерживающая система
гипоксии миокарда при ПТСР, схематично представленная на рис. 12.
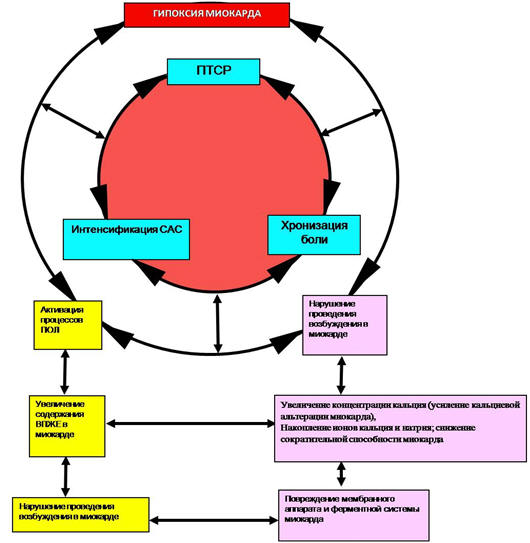
Рис. 12. Схема формирования гипоксии миокарда при
ПТСР
В целом патология сердечно-сосудистой системы и хронические боли в
груди у ветеранов, перенесших боевой стресс, имеют полифакторный характер.
Показатели общего холестерина возрастают в прямой зависимости от увеличения
возраста, а показатели ЛПОНП, ЛПНП, ЛПВП и тригдицеридов, кроме того, зависят от
индекса массы тела. Преобладающим является 2а тип дислипидемий, выявляемый в
возрасте старше 55 лет и тесно связанный с развитием атеросклероза коронарных и
церебральных артерий, а 4, менее агрессивный тип дислипидемий, оказывается более
характерным для молодого возраста. Но через 15-25 лет после окончания участия в
боевых действиях выраженность ПТСР, как нами показано, может снижаться, а
сердечно-сосудистая патология, связанная с атеросклерозом и нарастающими
параллельно снижению интенсивности ПТСР расстройствами обмена липидов, наоборот,
приобретать более выраженное клиническое «звучание». Возможно даже, что речь
идет о некоей трансформации биохимизма образования липидов и связанного с этим
процессом ускоренного развития атеросклероза на фоне часто встречающейся
артериальной гипертонии ветеранов боевых действий при уменьшении выраженности
ПТСР, что неизбежно происходит через 15-25 лет после выхода из зоны боевых
действий. Механизм развития дислипидемии в таких случаях, запущенный ранее при
непосредственном участии боевого стресса и ПТСР, приводит к ускоренному развитию
атеросклероза и ассоциированной с атеросклерозом сердечно-сосудистой патологии.
Затем, при постепенном снижении влияний ПТСР данный атеросклероз развивается уже
по своим законам - происходит трансформация атеросклеротических бляшек по
известным стадиям, усиливается тромбогенная и эмбологенная составляющая
развитого атеросклеротического процесса. Другими словами, развитие атеросклероза
становится в значительной степени более зависимым не столько от ПТСР, сколько от
процесса старения, который, как известно, формируется у ветеранов боевых
действий ускоренными темпами.
В отличие от сердечно-сосудистой, патология желудочно-кишечного
тракта у ветеранов боевых действий достаточно редко, только в 6,2%,
сопровождается хронической болью. С другой стороны, заболевания
желудочно-кишечного тракта, проявляя себя не столько хронической болью, сколько
иными вариантами симптоматики, в значительной степени являются следствием
нарушения процессов адаптации на боевой стресс, т.к. нарушение интегративного
контроля ЦНС приводит к формированию нейросоматической патологии. В результате
складывается патологическая система с первичным звеном в ЦНС и периферическим -
в органах желудочно-кишечного тракта (Гусев Е.И., Крыжановский Г.Н., 2009;
Мякотных В.С., Торгашов М.Н., 2015).
Несомненно, что важная роль в развитии патологической системы, как
результата боевого стресса, принадлежит дизрегуляционным изменениям в
гипоталамо-гипофизарно-надпочечниковой и симпатоадреналовой системах, иммунной
системе и последующим нейропластическим и нейротрансмиттерным нарушениям в ЦНС.
Хроническая боль и ПТСР в данной патогенетической цепи могут являться так
называемым взаимоподдерживающим состоянием (системой), в котором хроническая
боль возвращает ветерана к травмирующим боевым событиям, а ПТСР приводит к
усилению центральной сенситизации боли. Весь этот цикл можно представить в виде
схемы (рис. 13).
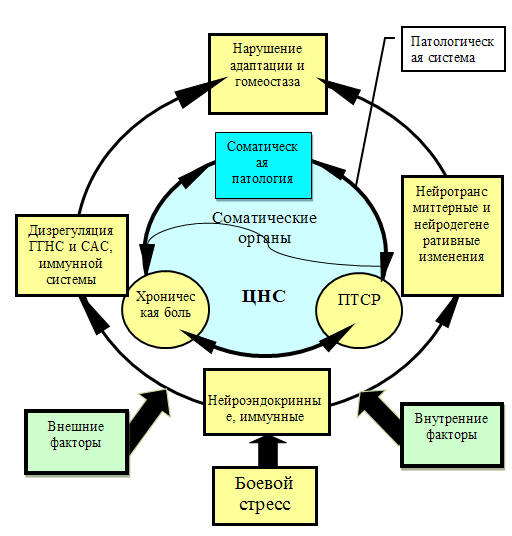
Рис. 13. Взаимоподдерживающая патологическая
система
Примечание: ГГНС – гипоталамо-гипофизарно-надпочечниковая система;
САС – симпатоадреналовая система
Первичными, центральными звеньями представленной на схеме
патологической системы являются боевой стресс и следующее за ним ПТСР, которые
определяют дизрегуляцию в ЦНС, нейроэндокринной системе, нарушения адаптации и
гомеостаза в целом. Соматическая патология по существу является вторичным,
периферическим звеном патологической системы, а хронические болевые синдромы –
следствием. Но при этом, с одной стороны, дизрегуляция ЦНС является фактором
хронизации боли, с другой стороны, соматическая патология, в особенности на
начальном этапе своего формирования - источником ноцицептивного потока в ЦНС, и
чем он интенсивней, тем труднее его сдерживать «антисистемам», и быстрее
формируется хроническая боль. Патологическое состояние отчетливо принимает форму
«порочного круга».
Нашими исследованиями убедительно показан полиорганный характер
стресс-индуцированных заболеваний (Мякотных В.С., Торгашов М.Н., 2015), а
широкое распространение хронических болевых синдромов у лиц, перенесших
неоднократное воздействие тяжелых стресс-факторов, связано, прежде всего, с
дизрегуляцией в ЦНС. Комплексные патогенетические связи развития
стресс-индуцированных заболеваний на фоне ПТСР (Торгашов М.Н., Мякотных В.С.,
2016) представлены на рис. 14.
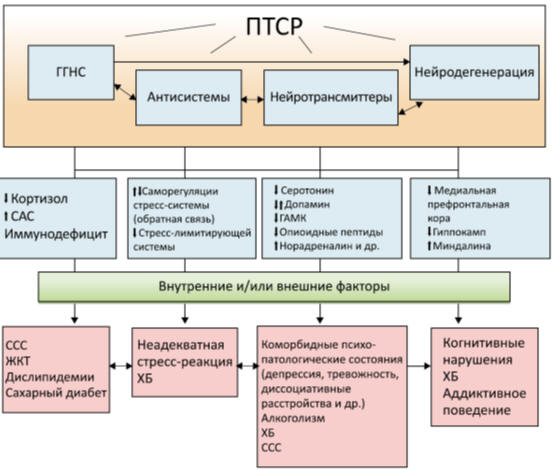
Рис. 14. Патогенетические связи развития
стресс-индуцированных заболеваний на фоне ПТСР.
Примечание: ГГНС - гипоталамо-гипофизарно-надпочечниковая система,
ССС -сердечнососудистая система, ЖКТ – желудочно-кишечный тракт, ХБ –
хроническая боль
Хотелось бы также сказать о том, что в процессе развития ПТСР
сначала имеют место «первичные» клинические проблемы, включающие отрицательные
психологические, социальные и иные проявления и зависящие от воздействия
стресс-факторов. Постепенно они утрачивают своё значение, но появляются новые,
«вторичные» проблемы, так или иначе связанные уже не столько со
стресс-факторами, сколько с клиническими проявлениями самого ПТСР. Это
физические, психологические, эмоциональные страдания, агрессивность, аддиктивное
поведение, алкогольная и наркотическая зависимости. И только потом, в качестве
третьей ступени клинико-патогенетического комплекса в полной мере формируется
клинически развернутая стресс-индуцированная патология соматического круга – АГ,
ранние атеросклеротические поражения различной локализации, патологические
процессы в желудочно-кишечном тракте, хронические боли. Именно эти проблемы,
т.е. уже отчетливо клинически обозначившие себя соматические страдания, можно
рассматривать в качестве «третичных» по отношению к имевшему место стрессу.
Описанная последовательность, разумеется, создает сложности диагностики ПТСР, а
именно выявления его начальных проявлений в латентной стадии. Часто в этот
период пациенты не обращают или не акцентируют своё внимание на своём же
психопатологическом состоянии, и все жалобы концентрируются вокруг соматических
проявлений - болевом синдроме при заболеваниях опорно-двигательного аппарата,
повышенном АД, патологических проявлениях со стороны желудочно-кишечного тракта,
головных болях, снижении памяти (51,6%), нарушениях сна (53,4%),
раздражительности.
Таким образом, основным пусковым механизмом многих заболеваний
являются последствия тяжелого, в нашем случае боевого стресса в виде ПТСР,
которые в последующем, с возрастом ослабевают, и в патогенезе патологических
процессов более значимую роль начинают играть возрастные изменения организма.
Это согласуется с тем, что после 60 лет распространенность ПТСР составляет всего
0,9% (Charles
E., Gafand
L.,
Ducrocq F.,
Clement
J.P.,
2005). Частые злоупотребления алкоголем, курение усиливают морфологические
органные изменения. Неудовлетворительные социальные и материальные условия
являются дополнительным дестабилизирующим фактором. В целом можно сказать, что
стресс-индуцированные заболевания у лиц с ПТСР формируются в двух основных
направлениях. Первое - это заболевания, развивающиеся в результате дизрегуляции
ЦНС с образованием многоуровневой патологической системы с первичным звеном в
ЦНС и вторичным - в органах-мишенях. Именно при этом варианте развития
формируются хронические болевые синдромы. Второе направление – развитие
патологии, которая связанна с возрастными изменениями организма, но проявляется
в более раннем возрасте, чем это описано для популяционных стандартов (Мякотных
В. С., 2009; Fulco С.,
Liverman C.T.,
Sox H.C.
et al.,
2008). Сюда относятся дегенеративные изменения ОДА с хронической болью,
патология сердечно-сосудистой системы, нарушения липидного обмена, язвенная
болезнь желудка и 12-перстной кишки, хеликобактерная инфекция, а также
заболевания и так называемые вредные привычки, которые связанны в том числе и с
образом жизни, нарушением иммунитета, аддиктивными наклонностями. Эти факторы
наряду с другими также, в свою очередь, провоцируют патологию
желудочно-кишечного тракта, артериальную гипертонию и иные варианты патологии.
Выявленные особенности патогенеза, формирования и развития множественной
стресс-индуцированной патологии, конечно же, необходимо учитывать при разработке
конкретных схем патогенетического лечения.
[ Оглавление книги | Главная страница раздела ] |
|
| Поиск по медицинской библиотеке |
|
|
|
|  |
| 
|

