
Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Энтероколитический синдром, индуцированный пищевыми белками,
в практике детского аллерголога
Г. А. Новик, доктор медицинских наук, профессор
Е. Г. Халева
ГБОУ ВПО СПбГПМУ МФ, Санкт-Петербург
Существует целый спектр аллергических заболеваний пищеварительного тракта.
Непосредственно к атопическим, т. е. IgE-опосредованным, относятся лишь
немедленная гастроинтестинальная гиперчувствительность и оральный аллергический
синдром. В отдельную группу выделяют эозинофильные заболевания пищеварительного
тракта. В их патогенезе участвуют как IgE-зависимые, так и клеточные механизмы,
где ключевое значение имеют эозинофилы. Морфологическими особенностями,
характерными для этой группы заболеваний, являются преобладание в воспалительном
инфильтрате эозинофилов, их группировка (эозинофильные микроабсцессы), внедрение
в эпителий и дегрануляция. Не-IgE-зависимая, клеточно-опосредованная пищевая
аллергия включает в себя индуцированный пищевыми белками синдром энтероколита (Food
Protein Induced Enterocolitis Syndrome, FPIES), индуцированный пищевыми белками
аллергический проктоколит, индуцированную пищевыми белками энтеропатию, синдром
Хейнера (легочный гемосидероз), целиакию и индуцированную белками коровьего
молока железодефицитную анемию [1, 2]. Клеточно-опосредованные аллергические
реакции на белки коровьего молока (КМ) встречаются часто и составляют примерно
40% аллергии на белки КМ у новорожденных и детей младшего возраста (рис. 1).
Цель этого обзора — обобщить клинический опыт и знания об этиологии, клинической
картине, иммунологических механизмах, диагностике и лечении FPIES для разработки
новых подходов к терапии и профилактике.

Эпидемиология FPIES
К сожалению, на сегодняшний день отсутствуют точные данные о
распространенности FPIES в Российской Федерации. Согласно результатам
национального популяционного когортного исследования в Израиле, частота FPIES на
КМ составляет 0,34%, тогда как IgE-зависимая пищевая аллергия диагностирована в
0,5% случаев у детей до 12 месяцев [3]. Семейный анамнез по атопии был отягощен
у 40–80% пациентов, в 20% по пищевой аллергии и в 6% случаев по FPIES [4, 5]. До
40% детей с FPIES имеют повышенный уровень IgE на другие продукты [5, 6].
Примерно 30% детей с FPIES сформировали аллергические заболевания, такие как
экзема (35%), астма или ринит (20%), или позже лекарственную
гиперчувствительность, что отражает ситуацию в популяции в целом.
Иммунологические механизмы FPIES
Патогенез иммунологических реакций и клиническая картина при IgE-зависимой
пищевой аллергии хорошо описаны и изучены (рис. 2) [7, 8]. В отличие от этого
механизма, при патогенезе FPIES нет четкого обоснования, какие иммунологические
процессы сопровождают гастроинтестинальные и системные реакции в виде рвоты,
гипотензии и диареи. Активация Т-клеток на пищевые аллергены может
способствовать местному воспалению кишечника через выброс провоспалительных
цитокинов, например, ФНО-α и ИФН-γ, что приводит к увеличению проницаемости
кишечного барьера и выходу жидкости [2]. Местное воспаление может быть
опосредовано через активацию периферических мононуклеарных клеток, увеличение
ФНО-α и снижение уровня экспрессии ФНО-ß рецепторов в слизистой оболочке
кишечника [9]. FPIES часто сопровождается лейкоцитозом и тромбоцитозом.
Рвота связана со стимуляцией хемо- или механорецепторов верхних отделов
желудочно-кишечного тракта (ЖКТ). В качестве возможного пути ее индуцирования
рассматривается роль энтерохромаффинных клеток ЖКТ, продуцирующих серотонин,
который в свою очередь может активировать блуждающий нерв и вызвать рвоту. На
сегодняшний день обсуждаются вопросы об участии энтерохромаффинных клеток в
распознавании специфических антигенов в кишечнике, а также о возможном
нейроэндокринно-иммунном пути взаимодействия, который ведет к острым проявлениям
FPIES. К сожалению, в настоящее время отсутствует экспериментальная модель с
участием лабораторных животных для воспроизведения FPIES. Поэтому необходимо
более тщательно наблюдать больных с FPIES, чтобы ответить на эти фундаментальные
вопросы.

Клиническая картина FPIES
FPIES у младенцев обычно проявляется в виде профузной повторяющейся рвоты
(начало в течение 1–3 часов после приема пищи) и диареи (начало в течение 5–10
часов) (рис. 3) [10]. Дыхательные и кожные проявления отсутствуют [11]. FPIES
наиболее часто вызывают КМ и соя [3, 5, 6, 12, 13]. Обычно симптомы начинают
проявляться в периоде новорожденности или в течение первого года жизни [14, 15].
Позднее начало обычно связывают с задержкой введения КМ, сои или других
прикормов детям на грудном вскармливании [5]. КМ и/или соя в качестве триггера
FPIES у младенцев, находящихся на исключительно грудном вскармливании,
встречается очень редко, что указывает на важную защитную роль грудного
вскармливания [16, 17]. Тем не менее, в когорте 30 японских младенцев с
диагностированным FPIES, вызванным КМ, 10% детей сформировали симптомы, находясь
на грудном вскармливании, что предполагает существование различных фенотипов
FPIES согласно этническим группам [18, 19]. По данным K. M. Jarvinen, A.
Nowak-Wegrzyn (2013) причиной развития FPIES может быть рис, овес, мясо, рыба и
яйцо [10]. FPIES на рыбу или морепродукты, как правило, проявляется у детей
более старшего возраста и взрослых [5, 20].
Хронический FPIES у младенцев
В самых тяжелых случаях симптомы начинаются в течение первых дней жизни у
младенцев, вскармливаемых смесью на основе КМ или сои, с периодической рвотой и
хронической диареей (может быть кровавой), без связи с приемом пищи [18, 21,
22]. Хронический FPIES проявляется вздутием живота, потерей веса,
обезвоживанием, метаболическим ацидозом, анемией, повышением уровня лейкоцитов с
эозинофилией и гипоальбуминемией. У 1/3 детей раннего возраста с тяжелой
степенью FPIES и ацидемией наблюдалась транзиторная метгемоглобинемия [23].
Часто на обзорной рентгенограмме брюшной полости можно увидеть интрамуральное
скопление газа, что необходимо дифференцировать с некротическим энтероколитом
[4, 13]. В целом 75% младенцев заболевают остро, из которых только у 15% FPIES
сопровождается гипотензивным синдромом и требует госпитализации [12].
Острый FPIES
Острый FPIES вызывается белками КМ, сои и других продуктов у младенцев и
маленьких детей. Младенцы с хроническим FPIES при введении жидкости внутривенно
(в/в) или переводе на высокогидролизную смесь улучшают свое состояние в течение
3–10 дней [21]. Повторное введение причинно-значимого продукта после периода
элиминации вызывает появление острых симптомов, обычно проявляющихся в виде
повторяющейся рвоты (до 10–20 раз) в течение 1–3 часов после приема пищи. Диарея
обычно начинается в течение 2–10 часов (в среднем 5 часов) с кровью, слизью и
повышенным содержанием лейкоцитов, эозинофилов и углеводов [21]. У некоторых
детей острый FPIES может осложниться гипотензией и гиповолемическим шоком [20,
24]. В периферической крови повышено количество нейтрофилов, с пиком через 6
часов и нормализацией уровня в течение 18–24 часов [21]. В редких случаях
тяжелое вздутие живота может вызвать подозрение на непроходимость кишечника и
приводит к диагностической лапаротомии [25].
Причинно-значимые продукты
Большинство (60%) пациентов реагируют только на один продукт [5,6]. Наиболее
распространенные это КМ или соя, но до 40% детей могут реагировать на оба
продукта. FPIES может также быть вызван и другими продуктами, такими как рис,
овес, ячмень, курица, индейка, яичный белок, зеленый горошек и арахис [26].
Среди младенцев с FPIES на прикормы у 65% был ранее диагностирован FPIES на КМ
и/или сою, получавших казеиновый гидролизат или аминокислотную смесь, и лишь 35%
были на грудном вскармливании [4].
Диагностика FPIES
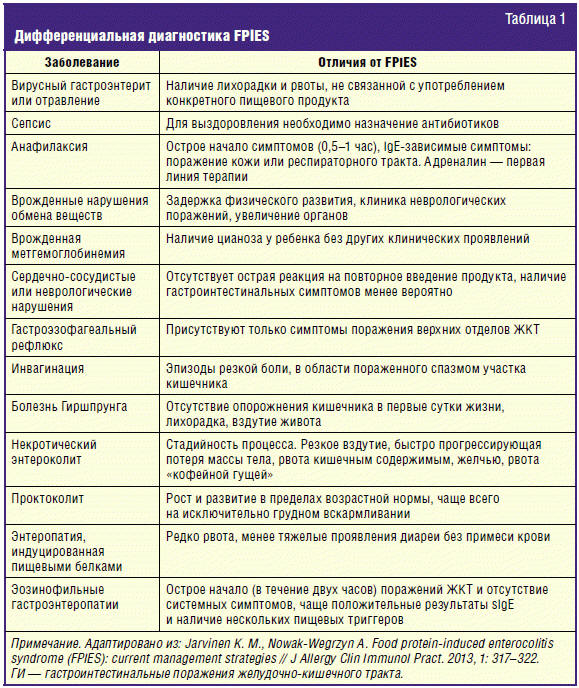
Диагностика FPIES основывается на анамнезе, клинической картине, исключении
других заболеваний со сходной клинической картиной и проведении провокационного
теста (табл. 1) [11]. Часто присутствует поздняя диагностика, что возможно
связано с отсутствием типичных кожных и респираторных аллергических симптомов.
Кроме того, рис, овес и овощи редко вызывают IgE-зависимую аллергию и считаются
гипоаллергенными, поэтому их редко подозревают в качестве виновных продуктов в
тяжелых аллергических реакциях. Отсутствие четких диагностических алгоритмов
также способствует поздней диагностике. В отличие от большинства пациентов из
США, Европы, Австралии и Израиля, 47% японских детей раннего возраста с FPIES на
КМ имеют повышенный уровень специфического IgE в сыворотке крови [18].
Исследователи из Японии предполагают, что расы или национальности могут влиять
на фенотип FPIES [19]. На основе предполагаемых Т-клеточных реакций в развитии
данного заболевания, были оценены аппликационные накожные тесты (патч-тесты) в
качестве диагностики сенсибилизации при FPIES. Результаты оказались
противоречивы. В настоящее время патч-тесты не рекомендуются для диагностики
сенсибилизации при FPIES [6, 27, 28].
Оральный провокационный тест (ОПТ) является золотым стандартом для
диагностики FPIES. К сожалению, провокационные пробы с пищевыми аллергенами в РФ
не сертифицированы. Соответственно, при FPIES основное диагностическое значение
приобретает диагностическая элиминационная диета с последующим повторным
введением продукта. Для большинства грудных детей нет необходимости в
подтверждении FPIES через ОПТ, особенно если они имеют классический анамнез
тяжелых, повторных реакций и после элиминации подозреваемого продукта происходит
нормализация клинической картины [1].
Гипоальбуминемия и прибавка в весе менее 10 г/сут были определены как
независимые предикторы FPIES на КМ у маленьких детей с хроническими
гастроинтестинальными симптомами [15]. Оценка копрограммы у новорожденных с
хроническим FPIES и диареей неспецифична и только говорит о наличии скрытой
крови, интактных полиморфно-ядерных нейтрофилах, эозинофилах и кристаллах Шарко–Лейдена.
Проведение эндоскопии до установления диагноза у новорожденных с FPIES на КМ
и/или сою показала наличие ректальных язв и кровотечение из рыхлой слизистой
оболочки [22].
На рентгенограмме детей с хронической диареей, ректальным кровотечением и/или
отставанием в физическом развитии были описаны уровни жидкости, неспецифическое
сужение и наличие «отпечатков больших пальцев» в прямой и сигмовидной кишке,
утолщение циркулярных складок двенадцатиперстной и тощей кишки с избытком
полостной жидкости [29]. При подозрении на непроходимость кишечника была
выполнена лапаротомия и диагностировано вздутие тонкой кишки и утолщение стенки
тощей кишки дистальнее связки Трейца с диффузным субсерозным кровотечением [25].
У детей, находящихся на строгой диете, на повторной рентгенограмме наблюдалась
ее нормализация.
Определение IgE при FPIES
FPIES классифицируется как не-IgE-зависимая пищевая аллергия [1, 4, 30, 31].
По данным исследований 4–25% детей с диагнозом FPIES изначально имели повышенный
уровень специфических IgE (sIgE) АТ [3, 5, 6]. У детей с FPIES на КМ и высоким
уровнем sIgE наблюдалось более позднее улучшение клинической картины, по
сравнению с детьми, у которых уровень sIgE был в норме [5, 12, 32]. У
большинства детей с высоким уровнем sIgE сохраняется FPIES-фенотип, но, тем не
менее, механизм пищевой аллергии может измениться на немедленную
IgE-опосредованную. В исследовании под руководством J. C. Caubet (2014), у 35%
детей с FPIES, индуцированным КМ и sIgE к КМ, диагностированы немедленные
аллергические проявления аллергии на белки КМ [5]. Целесообразно включать
прик-тест и/или измерение сывороточного sIgE для первоначальной и последующей
оценки пациента.
Элиминационная диета
Принципы построения диеты при FPIES аналогичны IgE-зависимой пищевой
аллергии. Большинство существующих международных рекомендаций предполагают
использование в качестве диетотерапии FPIES смесей на основе
высокогидролизованного белка [33–35]. В литературе прошлых лет описаны случаи
непереносимости детьми с FPIES смесей на основе высокогидролизованного белка,
причем независимо от вида белка, входившего в состав смеси [36, 37]. К
настоящему времени состав смесей претерпел значительное улучшение, тем не менее,
отсутствие ожидаемого эффекта от применения смесей на основе
высокогидролизованного белка встречается в клинической практике. В таких случаях
диетотерапию необходимо проводить с использованием аминокислотных смесей,
использование которых в лечении FPIES поддерживается и рекомендациями ESPGHAN
[38].
В настоящее время на российском потребительском рынке для больных с пищевой
аллергией представлены 4 продукта, созданных на основе смеси свободных
аминокислот, — Неокейт LCP, Нутрилон Аминокислоты, Неокейт Эдванс и Алфаре Амино
(табл. 2). Все аминокислотные смеси имеют сбалансированный жировой и углеводный
состав, обогащены необходимыми для детей витаминами и микроэлементами.
Алфаре Амино — это новая смесь на основе аминокислот и свободная от молочного
белка и лактозы, использование которой позволяет полностью избежать молочных и
пищевых аллергенов. Алфаре Амино позволяет значительно улучшить лечение и
нутритивную поддержку детей, у которых применение высокогидролизованной смеси не
приносит положительных результатов. Смесь Алфаре Амино предназначена для
длительного применения в диетотерапии детей, страдающих тяжелой и осложненной
пищевой аллергией на белок коровьего молока и пищевой непереносимостью (табл.
3).

Лечение острого FPIES
В качестве первой линии терапии применяют быструю в/в регидратацию (20 мл/кг
физиологического раствора струйно) при тяжелых острых реакциях или при ОПТ.
Основываясь на предполагаемом Т-клеточном воспалении кишечника, часто
назначаются внутривенные кортикостероиды при тяжелых реакциях. Адреналин также
должен быть доступен при потенциальных тяжелых сердечно-сосудистых реакциях, в
виде гипотензии и шока. Однако назначение адреналина не улучшает симптомы рвоты,
которые быстро устраняются при интенсивном в/в введения жидкости [20]. Несколько
исследователей описали эффективное в/в назначение ондансетрона для остановки
рвоты, индуцированной во время проведения ОПТ при FPIES [39]. Пять детей старше
трех лет с рвотой, индуцированной в течение проведения ОПТ при FPIES, лечили
ондансетроном в дозе 0,2 мг/кг вместе с в/в введением физиологического раствора
струйно. Трое из четырех детей получили в/в ондансетрон и добились результата в
течение 10–15 минут, в то время как одному ребенку требовалась дополнительное
введение ондансетрона. Другой ребенок получал ондансетрон перорально, но
требовалось дополнительное в/в введение ондансетрона для уменьшения сильной боли
в животе. Еще одно исследование, проведенное в Италии, подтвердило эффективность
внутримышечного введения ондансетрона для лечения острого FPIES у детей раннего
возраста при ОПТ [40]. Ондансетрон высокоселективно блокирует центральные
(хеморецепторы триггерной зоны, рвотный центр) и периферические серотониновые
5-HT3-рецепторы. Подавляет рвотный рефлекс, устраняет и предупреждает тошноту и
рвоту, опосредованную высвобождением серотонина, и часто используется после
химиотерапии, а также при вирусных гастроэнтеритах. При назначении ондансетрона
необходимо обратить особое внимание на детей с сопутствующей патологией сердца,
из-за возможного удлинения интервала QT. Ондансетрон не зарегистрирован в РФ для
лечения FPIES.
Определение оптимального времени для повторного введения продукта
На данный момент нет конкретных рекомендаций о сроках проведения ОПТ. По
опыту США диагностический ОПТ обычно пытаются провести в течение 12–18 месяцев
после последней реакции [32, 10]. Однако в проспективном исследовании из Кореи
рассматривались более ранние попытки проведения ОПТ [14]. В это исследование
были включены 23 новорожденных с FPIES на КМ или сою (диагностирован в среднем в
36 дней, диапазон 13–58 дней) с двухлетним наблюдением. В результате к 6 месяцам
27% развили толерантность к КМ и 75% к сое, соответственно 42% и 91% к 8 месяцам
и 64% и 92% к 10 месяцам. Все дети полностью поправились к 2 годам при FPIES на
КМ и к 14 месяцам при FPIES на сою. В проспективном когортном исследовании из
Израиля все дети к 6 месяцам были с диагнозом FPIES, индуцированным белками КМ,
и у 50% исчезли клинические проявления заболевания в течение первого года жизни,
у 89% к возрасту двух лет, и у 90% к возрасту трех лет [3]. С другой стороны,
ретроспективные исследования, проведенные в США, описали низкие темпы разрешения
FPIES на КМ или сою: 35% к возрасту 2 лет, 70% к возрасту 3 лет, и 85% к
возрасту 5 лет [5, 6]. Эти различия могут отражать различия в дизайне
исследования и/или выборки в сторону более тяжелых фенотипов. Таким образом,
согласно последним данным ОПТ с КМ может быть выполнен после 12 месяцев, в то
время как с соей может быть рассмотрен после шести месяцев [5, 14, 41]. У детей
с FPIES на рис или овес нормализация клинической картины происходит позже,
обычно к возрасту 4–5 лет [5, 6, 42]. Нет данных о разрешении FPIES на
морепродукты у детей старшего возраста. Рекомендуется периодическая оценка
состояния в этой группе пациентов.
Заключение
FPIES — распространенное проявление не-IgE-зависимой пищевой аллергии в
раннем возрасте и в большинстве случаев проходит в первые годы жизни. Постановка
правильного диагноза зачастую осложняется отсутствием неинвазивных
подтверждающих тестов и маркеров. Лечение таких больных основывается на
элиминации пищевых аллергенов и периодических попытках их введения.
Литература
- Boyce J. A., Assaad A., Burks A. W. Guidelines for the diagnosis
and management of food allergy in the United States: summary of the
NIAID-Sponsored Expert Panel Report // J Allergy Clin Immunol. 2010, 126:
1105–1118.
- Caubet J. C., Nowak-Wegrzyn A. Current understanding of the
immune mechanisms of food protein-induced enterocolitis syndrome // Expert Rev
Clin Immunol. 2011, 7: 317–327.
- Katz Y., Goldberg M. R., Rajuan N. The prevalence and natural
course of food protein-induced enterocolitis syndrome to CM: a large-scale,
prospective population-based study // J Allergy Clin Immunol. 2011, 127: 647–
653. e1–3.
- Nowak-Wegrzyn A., Sampson H. A., Wood R. A., Sicherer S. H. Food
protein-induced enterocolitis syndrome caused by solid food proteins //
Pediatrics. 2003, 111: 829–835.
- Caubet J. C., Ford L. S., Sickles L. Clinical features and
resolution of food protein-induced enterocolitis syndrome: 10-year experience
// J Allergy Clin Immunol. 2014, 134: 382–389.
- Ruffner M. A., Ruymann K., Barni S. Food protein-induced
enterocolitis syndrome: insights from review of a large referral population //
J Allergy Clin Immunol Pract. 2013, 1: 343–349.
- Новик Г. А. Пищевая аллергия у детей раннего возраста // Лечащий
Врач. 2011; 4: 54–61.
- Новик Г. А., Ткаченко М. А. Гастроинтестинальные проявления
пищевой аллергии у детей // Лечащий Врач. 2012, № 1, с. 16–25.
- Chung H. L., Hwang J. B. Expression of transforming growth factor
ß1, transforming growth factor type I and II receptors, and TNF-а in the
mucosa of the small intestine in infants with food protein-induced
enterocolitis syndrome // J Allergy Clin Immunol. 2002, 109: 150–154.
- Jarvinen K. M., Nowak-Wegrzyn A. Food protein-induced
enterocolitis syndrome (FPIES): current management strategies // J Allergy
Clin Immunol Pract. 2013, 1: 317–322.
- Feuille E., Nowak-Wegrzyn A. Definition, etiology, and diagnosis
of food protein-induced enterocolitis syndrome // Opin Allergy Clin Immunol.
2014, 14: 222–228.
- Sicherer S. H., Eigenmann P. A., Sampson H. A. Clinical features
of food protein-induced enterocolitis syndrome // J Pediatr. 1998, 133:
214–219.
- Mehr S., Kakakios A., Frith K., Kemp A. S. Food proteininduced
enterocolitis syndrome: 16-year experience // Pediatrics. 2009, 123:
e459–e464.
- Hwang J. B., Sohn S. M., Kim A. S. Prospective follow-up oral
food challenge in food protein-induced enterocolitis syndrome // Arch Dis
Child. 2009, 94: 425–428.
- Hwang J. B., Lee S. H., Kang Y. N. Indexes of suspicion of
typical cow’s milk protein-induced enterocolitis // J Korean Med Sci. 2007,
22: 993–997.
- Monti G., Castagno E., Liguori S. A. Food protein-induced
enterocolitis syndrome by cow’s milk proteins passed through breast milk // J
Allergy Clin Immunol. 2011, 127: 679–80.
- Tan J., Campbell D. Food protein-induced enterocolitis syndrome
in an exclusively breast-fed infant-an uncommon entity // J Allergy Clin
Immunol. 2012, 129: 873, author reply 873–874.
- Nomura I., Morita H., Hosokawa S. Four distinct subtypes of
non-IgE-mediated gastrointestinal food allergies in neonates and infants,
distinguished by their initial symptoms // J Allergy Clin Immunol. 2011, 127:
685–688. e1–8.
- Nomura I., Morita H., Ohya Y. Non-IgE-mediated gastrointestinal
food allergies: distinct differences in clinical phenotype between Western
countries and Japan // Curr Allergy Asthma Rep. 2012, 12: 297–303.
- Fernandes B. N., Boyle R. J., Gore C. Food protein-induced
enterocolitis syndrome can occur in adults // J Allergy Clin Immunol. 2012,
130: 1199–1200.
- Powell G. K. Milk- and soy-induced enterocolitis of infancy.
Clinical features and standardization of challenge // J Pediatr. 1978, 93:
553–560.
- Gryboski J. D. Gastrointestinal milk allergy in infants //
Pediatrics. 1967, 40: 354–362.
- Murray K. F., Christie D. L. Dietary protein intolerance in
infants with transient methemoglobinemia and diarrhea // J Pediatr. 1993, 122:
90–92.
- Coates R. W., Weaver K. R., Lloyd R. Food protein-induced
enterocolitis syndrome as a cause for infant hypotension // West J Emerg Med.
2011, 12: 512–514.
- Jayasooriya S., Fox A. T., Murch S. H. Do not laparotomize
food-protein-induced enterocolitis syndrome // Pediatr Emerg Care. 2007, 23:
173–175.
- Borchers S. D., Li B. U., Friedman R. A., McClung H. J.
Riceinduced anaphylactoid reaction // J Pediatr Gastroenterol Nutr. 1992, 15:
321–324.
- Fogg M. I., Brown-Whitehorn T. A., Pawlowski N. A. Atopy patch
test for the diagnosis of food protein-induced enterocolitis syndrome //
Pediatr Allergy Immunol. 2006, 17: 351–355.
- Jarvinen K. M., Caubet J. C., Sickles L. Poor utility of atopy
patch test in predicting tolerance development in food proteininduced
enterocolitis syndrome // Ann Allergy Asthma Immunol. 2012, 109: 221–222.
- Richards D. G., Somers S., Issenman R. M., Stevenson G. W. Cow’s
milk protein/soy protein allergy: gastrointestinal imaging // Radiology. 1988,
167: 721–723.
- Sampson H. A., Anderson J. A. Summary and recommendations:
classification of gastrointestinal manifestations due to immunologic reactions
to foods in infants and young children // J Pediatr Gastroenterol Nutr. 2000,
30 (Suppl.): S87–S94.
- Sicherer S. H., Burks A. W. and Sampson H. A. Clinical features
of acute allergic reactions to peanut and tree nuts in children // Pediatrics.
1998, 102: e6.
- Sicherer S. H. Food protein-induced enterocolitis syndrome: case
presentations and management lessons // J Allergy Clin Immunol. 2005, 115:
149–156.
- Boyce J. A., Assa’ad A., Burks A. W. et al. Guidelines for the
diagnosis and management of food allergy in the United States: report of the
NIAID-sponsored expert panel. J Allergy Clin Immunol 2010; 69:11–24
- Kemp A. S., Hill D. J., Allen K. J. et al. Guidelines for the use
of infant formulas to treat cows milk protein allergy: an Australian consensus
panel opinion. Med J Aust 2008; 188:109–112
- Fiocchi A., Brozek J., Schunemann H. et al. World Allergy
Organization (WAO) Diagnosis and Rationale for Action against Cowas Milk
Allergy (DRACMA) guidelines. World Allergy Organ J 2010; 3:57–161.
- Vanderhoof J. A., Murray N. D., Kaufman S. S. et al. Intolerance
to protein hydrolysate infant formulas: an underrecognised cause of
gastrointestinal symptoms in infants. J Pediatr 1997; 131:741–744
- Kelso J. M., Sampson H.A. Food protein-induced enterocolitis to
casein hydrolysate formulas. J Allergy Clin Immunol 1993; 92:909–910.
- Koletzko S., Niggermann B., Arato A. et al. Diagnostic approach
and management of cow’s milk protein allergy in infants and children: ESPGHAN
GI Committee practical guidelines. J Pediatr Gastroenterol Nutr 2012;
55:221–229.
- Holbrook T., Keet C. A., Frischmeyer-Guerrerio P. A., Wood R. A.
Use of ondansetron for food protein-induced enterocolitis syndrome // J
Allergy Clin Immunol. 2013, 132: 1219–1220.
- Sopo S. M., Greco M., Monaco S. Ondansetron for food protein–induced
enterocolitis syndrome // Arch Allergy Immunol. 2014, 164: 137–139.
- Sopo S. M, Iacono I. D., Greco M., Monti G. Clinical management
of food protein-induced enterocolitis syndrome // Opin Allergy Clin Immunol.
2014, 14: 240–245.
- Katz Y., Goldberg M. R. Natural history of food proteininduced
enterocolitis syndrome // Opin Allergy Clin Immunol. 2014, 14: 229–239.
- Баранов А. А., Намазова-Баранова Л. С, Боровик Т. Э, Макарова С. Г.
Диагностика и лечение аллергии к белкам коровьего молока у детей грудного и
раннего возраста: практические рекомендации / Союз педиатров России. Москва:
ПедиатрЪ, 2014. 48 с.
Статья опубликована в журнале
Лечащий Врач
Если вы заметили орфографическую, стилистическую или другую ошибку на этой странице, просто выделите ошибку мышью и нажмите Ctrl+Enter. Выделенный текст будет немедленно отослан редактору
|
|
|
|

