Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Эффективное лечение симптоматической диабетической
полиневропатии при помощи высокочастотной внешней электростимуляции мышц
аппаратом HiTop 191
L. Reichstein . S. Labrenz
. D. Ziegler . S. Martin
Отрывок Цели/гипотеза: Диабетическая периферическая симметрическая сенсорная полиневропатия (DSP) возникает у 20–30%
пациентов-диабетиков. В качестве физиотерапии предлагались чрезкожная
электростимуляция нервов (TENS) и электростимуляция
спинного мозга. Мы провели контролируемое, рандомизированное экспериментальное
исследование с целью сравнить эффективность воздействия высокочастотной внешней
электростимуляции мышц (HF) и чрезкожной
электростимуляции нервов на пациентов, страдающих симптоматической
DSP.
Методы: Пациенты с диабетом типа 2 и DSP (n=41)
были рандомизированы для получения лечения при помощи TENS
или HF с учетом уровней для пациентов с безболезненными (n=20)
и болезненными сенсорными симптомами (n=21).
Обе нижние конечности подвергались лечению в течение трех последовательных дней
по 30 минут в день. Уровень выраженности симптомов болезни и болевых ощущений пациентов
определялся ежедневно по шкале от 1 до 10 перед началом, во время и в течение
двух дней по окончании лечения. Реакции определялись облегчением одного или
более симптомов по крайней мере на три пункта.
Результаты: Две группы пациентов были сходными в том, что касается основных
характеристик, таких как возраст, длительность заболевания диабетом, баллы по
неврологическим симптомам и баллы по неврологической нетрудоспособности. Доля
положительных откликов была значительно больше (p<0.05)
в группе HF (80%, 16 из 20), чем в группе
TENS (33%, 7 из 21). Анализ подгрупп показал, что
HF более эффективно, чем
TENS облегчает симптомы безболезненной невропатии (HF:
100%, 7 из 7; TENS: 44%, 4 из 9;
p<0.05) и болезненной невропатии (HF:
69%, 9 из 13; TENS: 25%, 3 из 12;
p<0.05). Отклики не различались в
том, что касается уменьшения средней интенсивности симптомов во время
исследования.
Выводы/истолкование: Это экспериментальное исследование впервые показало, что HF может облегчить дискомфорт и болевые ощущения,
связанные с DSP, и привело к предположению, что
HF более эффективна, чем TENS.
Внешняя электростимуляция мышц представляет собой новый вариант лечения
DSP.
Ключевые слова: Сахарный диабет. Периферическая симметрическая сенсорная полиневропатия. Высокочастотная внешняя электростимуляция мышц. Чрезкожная
электростимуляция нервов.
Аббревиатуры.
DSP: периферическая симметрическая сенсорная
полиневропатия. HF: высокочастотная внешняя
электростимуляция мышц. TENS: чрезкожная
электростимуляция нервов. TSS: множество всех симптомов
Введение
Диабетическая периферическая симметрическая сенсорная полиневропатия (DSP)
возникает примерно у 20–30% пациентов с диабетом типа 2, лежащих в больнице, и
20% пациентов, переносящих болезнь на дому [1, 2]. Невропатические симптомы
могут быть разделены на положительные и отрицательные, основанные соответственно
на самопроизвольных сенсорных симптомах или пониженной способности к
реагированию на стимулы [3]. Существует целое множество положительных сенсорных
симптомов, и было предложено разделить их на болезненную и безболезненную
категории [3]. Так как этиология DSP у человека не вполне
понятна, лечение симптомов при помощи анальгетиков, трициклических
антидепрессантов и противосудорожных препаратов часто является единственным
способом облегчить дискомфорт и болевые ощущения, на которые жалуются эти
пациенты [2]. Опубликованный недавно метаанализ предоставил доказательства, что
внутривенное введение α-липоевой кислоты облегчает положительные невропатические
симптомы и невропатическую недостаточность при DSP [4].
Чрезкожная электростимуляция нервов (TENS) [5, 6],
подкожная электростимуляция нервов [7], стимуляция спинного мозга [8], другие
физиотерапевтические процедуры [11, 12] и иглотерапия [13] также успешно
использовались в качестве нефармакологического лечения, в то время как
электростимуляция при помощи чулочных электродов была неэффективна [14].
Ранее мы заметили облегчение невропатических симптомов у пациентов,
проходивших лечение при помощи высокочастотной внешней электростимуляции мышц (HF).
На основе этого открытия целью данного рандомизированного экспериментального
исследования стало сравнение эффекта от применения
HF-терапии с эффектом, производимым
традиционной TENS-терапией,
у пациентов с DSP.
Субъекты и методы
Субъекты Пациенты, страдающие диабетом типа 1 или 2 и невропатией, в возрасте
от 18 до 80 лет с уровнем HbA1c
< 11% были вовлечены в настоящее исследование. Пациенты, принимавшие лекарства,
которые могли воздействовать на невропатические симптомы (такие как α-липоевая
кислота, антидепрессанты или противосудорожные препараты), а также пациенты с
язвами, ампутациями, вызванными ишемией или раковыми заболеваниями, были
исключены. Сорок один взрослый пациент-диабетик были включены в данное
исследование; все участники дали на это свое письменное согласие. Протокол
исследования был одобрен Советом по этическим вопросам Университета Хайнриха
Хайне (Дюссельдорф).
Для установления пригодности испытуемых было проведено детальное исследование
истории протекания диабета, а также неврологическое обследование нижних
конечностей (таблица 1). Классические симптомы и неврологическая недостаточность
определяли DSP. Баллы за неврологические симптомы или
неврологическую недостаточность использовались для оценки тяжести заболевания
DSP [15]. Участники были наугад приписаны к группам
TENS или HF с использованием
уровней для пациентов с безболезненными (парестезия, онемение) и болезненными
невропатическими симптомами (в добавление к безболезненным симптомам; жжение,
колющая боль, внезапная острая боль электрической природы).
Процедура лечения Каждый пациент получал лечение по 30 минут в течение трех
последовательных дней. В группе TENS электроды
располагались на нижних конечностях, как описано ранее [4] (Рис. 1a).
Таблица 1 Исходные характеристики 41 взрослого пациента с
диабетом, которые участвовали в исследовании
| Характеристика |
Группа TENS (n=21) |
Группа HF (n=20) |
| Возраст (лет) |
57.8±12.5 |
64.2±12.7 |
| Продолжительность заболевания диабетом
(лет) |
13.0±9.6 |
13.7±11.5 |
| Тип диабета (тип
1/тип 2) |
3/18 |
4/16 |
| Пол (женский/мужской) |
11/10 |
8/12 |
| Способ лечения диабета (инсулин/оральные
гипогликемические препараты) |
18/3 |
17/3 |
| Индекс массы тела (кг/м2) |
28.1±5.8 |
29.5±5.9 |
| Баллы по неврологическим симптомам |
6.6±1.3 |
7.1±1.3 |
| Баллы по
всем симптомам |
6.6±3.2 |
7.0±3.6 |
| Баллы по неврологической недостаточности |
5.5±3.2 |
7.4±1.6 |
| HbA1c (%) |
9.3±1.6 |
9.3±2.4 |
| Триглицериды (ммоль/л) |
3.0±4.3 |
1.9±1.3 |
| Холестерин (ммоль/л) |
6.0±2.0 |
5.6±1.0 |
| Липопротеины высокой плотности (ммоль/л) |
1.1±0.4 |
1.3±0.4 |
| Липопротеины низкой плотности (ммоль/л) |
3.7±1.2 |
3.7±0.9 |
| Глумат-оксалацетат-трансаминаза (ед./л) |
24.5±13.0 |
25.7±13.1 |
| Аланинаминотрансфераза (ед./л) |
27.8±15.4 |
25.7±13.4 |
| Креатинин (ммоль/л) |
65.5±13.3 |
71.6±22.1 |
| Мочевина (ммоль/л) |
6.0±1.9 |
6.8±2.0 |
Данные приведены в
виде средних значений±стандартное
отклонение
Чрескожная электротерапия проводилась при помощи аппарата, создающего волны
типа Н (Dumo 2.4; CEFAR
Medical, Лунд, Швеция), портативного, перезаряжаемого
устройства, которое генерирует двухфазную экспоненциально угасающую форму волны
с длительностью импульса 4 мсек, ≤35 мА, ≤35 В и 180 Гц. Интенсивность
регулировалась соответственно пациенту и варьировалась от 20 до 30 мА.
При проведении высокочастотной терапии электроды размещались на мышцах бедер
(Рис. 1б). Внешняя электростимуляция мышц проводилась при помощи непереносного
аппарата – источника питания на 230 В (HiTop 181-H;
gbo Medizintechnik, Римбах,
Германия), который генерирует импульсы длительностью ≤350 мА, ≤70 В. Мы
использовали начальную частоту в 4,096 Гц, которая повышалась до 32,768 Гц в
течение трех секунд; максимальная частота применялась в течение трех секунд, а
затем понижалась с 32,768 до 4,096 Гц. Для каждого пациента интенсивность
электростимуляции регулировалась до приятного уровня так, чтобы она не вызывала
никаких болевых ощущений или дискомфорта из-за парестезии.
Градуирование симптомов.
Пациентов попросили записать показатели исходного уровня основных симптомов –
боли, онемения, онемения в болезненных зонах, жжения, парестезии и дизестезии в
нижних конечностях – при помощи отдельных наглядных линейных 10-бальных шкал,
где 1=отсутствие симптома, а 10=худшее из когда-либо ощущавшихся проявлений
[16]. Опросные листы заполнялись участниками за 1 день до первого сеанса
лечения, через 1-2 часа после окончания терапии в каждый из трех дней лечения и
через 2 дня после окончания терапии. Облегчение симптомов определялось как
улучшение показателей на 3 балла (или больше) по крайней мере одного из
симптомов. Данные также анализировались при помощи балла за множество всех
симптомов [17].
Статистический анализ.
Все данные были выражены в виде среднего
значения±стандартное отклонение или в виде процентного соотношения. Анализ
данных по реакции пациентов проводился при помощи проверки по критерию
хи-квадрат. Изменение балла за множество всех симптомов подсчитывалось при
помощи проверки по парному критерию Стьюдента (на основе двойной выборки).
Значение p менее чем 0.05 считалось статистически важным.
Статистический анализ проводился при помощи программы
GraphPadPrism, Версия 3.0 (GraphPad
Software, Сан Диего, Калифорния, США).
Рис. 1. Расположение электродов во
время процедуры TENS (a) и
HF (б)
a
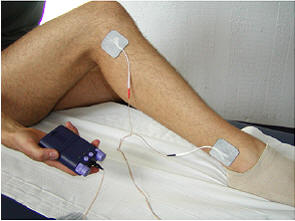
б

Результаты
Пациенты были рандомизированы для получения процедур TENS
(n=21) или
HF (n=20).
Исходные демографические данные, результаты лабораторных исследований и
неврологические симптомы и уровень недостаточности были сходными для обеих
лечебных групп (Таблица 1). Обе формы электротерапии хорошо переносились, без
каких-либо локальных или соматических побочных эффектов. Только один пациент
сообщил о некотором мышечном дискомфорте в ногах после первого сеанса
HF, который исчез
через несколько часов. Все пациенты (41
человек) заполнили протокол
исследования.
Семь из 21 пациента (33%) в группе TENS и 16 из 20
пациентов (80%) в группе HF сообщили об облегчении
симптомов (p<0.05)
(Рис. 2). Лечение в группе HF было более эффективным, чем
в группе TENS,
для пациентов с безболезненной DNP (HF:
100%, семь из семи; TENS: 44%, четыре из девяти;
p<0.05) и для
пациентов с болезненной DNP (HF:
69%, 9 из 13; TENS: 25%, три из 12;
p<0.05) (Рис. 2).
Оба метода лечения привели к снижению балла за множество всех симптомов со
значительной разницей между исходным и конечным значениями за период наблюдения,
хотя это снижение было более выраженным в группе HF (с
7.0±3.6 до 4.6±3.4, p<0.005),
чем в группе TENS (с 6.6±3.2 до 5.4± 3.8,
p<0.05).
Отклики членов обеих групп анализировались по отдельности, чтобы была
возможность сравнить периоды облегчения симптомов после лечения (Рис. 3).
Средние баллы по симптомам в откликах снижались с 7.3±0.6 до 3.6±0.6 в группе
HF и с 5.4±0.6 до 1.9±0.4 в группе TENS.
Облегчение симптомов отмечалось сразу после окончания первого сеанса лечения с
дальнейшим снижением баллов в течение последующих дней. Облегчение симптомов
документировалось в период до двух дней после окончания лечения. Тем не менее,
пациенты сообщали о повторном проявлении симптомов несколько дней спустя,
ситуация улучшалась при дальнейшем использовании электротерапии (данные не
указаны).
Рис. 2 Результаты
лечения методом TENS против
HF для целых групп
и отдельных пациентов,
разбитые не безболезненную
и болезненную группы.
Пациенты с диабетической периферической
невропатией (n=41)

Положительные отклики определялись как отклики пациентов, у которых произошло
облегчение на три пункта и больше хотя бы одного симптома по линейной
10-балльной шкале. Статистическая разница подсчитывалась при помощи проверки по
критерию хи-квадрат. + Облегчение
хотя бы на
три пункта по
шкале симптомов
Рис. 3 Шкала средних значений для симптомов (+стандартное
отклонение) у пациентов из групп TENS (черные
треугольники, пунктирная линия; n=7) и HF
(черные квадраты, сплошная линия; n=16)

Обсуждение
В этом перспективном рандомизированном клиническом экспериментальном
исследовании мы впервые показали, что HF может уменьшить
болевые ощущения и дискомфорт, вызываемые DSP. Эта
нефармакологическая форма лечения хорошо переносилась и может предлагаться как
альтернативный вариант для облегчения симптомов.
Наше открытие, что внешняя электростимуляция мышц уменьшает проявление
невропатических симптомов, соответствует клиническим наблюдениям, согласно
которым невропатические симптомы появляются, когда люди не используют свои мышцы
во время сна, и исчезают, когда они встают или ходят [18]. Ранее было показано,
что лечение при помощи TENS эффективно облегчает боль и
дискомфорт, связанные с DSP [5, 6]. Во время этих
исследований контрольная группа получала имитацию лечения при помощи
плацебо-стимуляторы; тем не менее, применение этой процедуры не исключает
эффекта плацебо. В нашем исследовании мы избежали этой проблемы.
Для внешнего сокращения мышц использовалась специальная система стимуляции (HiTop
181-H). Мы односекундно применяли частоты от 4,096 до
32,768 Гц, вводя в мышцы ток до 5,000 мВт. Высокочастотная электростимуляция
спинного мозга при помощи вживляемых электродов ранее показала свою
эффективность в облегчении невропатических болей при хроническом диабете [8] и
некоторых других хронических болезненных состояниях, включающих боли в спине,
фантомные боли в конечностях, болезнь периферических сосудов и тяжелую
стенокардию [19, 20].
Тогда как эта процедура не лишена риска и может привести к
появлению опасной для жизни инфекции [21], лечение при помощи HF,
использовавшееся во время нашего исследования, безопасно и потенциально может
применяться при других хронических болях. Механизмы, лежащие в основе
положительных результатов, связанных с лечебным воздействием HF,
не ясны. Было высказано предположение, что электростимуляция активирует
позвоночные столбы, которые задерживают С-образные волокна, прерывая/стробируя
таким образом болевые импульсы [22]. Более того, кратковременная высокочастотная
электростимуляция нервов уменьшает возбудимость коры двигательного нерва [23].
Эксперименты показали, что за электростимуляцией следует уменьшение концентрации
возбуждающих аминокислот глутамата и аспартата в спинном роге и что посредником
этого эффекта является ГАМК-эргический механизм [24].
Капиллярные изменения, уменьшенный кровоток, давление кислорода в нервах [25,
26] и другие сосудистые факторы [27] вносят свой вклад в патогенез диабетической
невропатии. Интересно, что электростимуляция, как сообщается в отчетах, улучшает
капиллярный кровоток при тяжелой форме ишемии конечностей [28], оказывает
положительное воздействие на заживление ран (показывает улучшение циркуляции в
тканях) [29, 30] и повышает резистентность к инсулину [31–34]. Одним из
ограничений, связанных с нашим экспериментальным исследованием, является его
короткая продолжительность, чем, возможно, объясняется слабая эффективность
лечения методом TENS. Для того чтобы выяснить, каков
общий эффект от применения HF
у диабетиков, необходимы длительные исследования. Было обнаружено, что болевые
ощущения и дискомфорт вновь появляются у пациентов через несколько дней после
окончания терапии, что наводит на мысль, что непрерывное лечение было бы более
благотворным. Последовавший за этим ограниченный опыт применения данного метода
у пациентов нашей клиники позволяет предположить, что получаемое еженедельно
лечение может облегчить продолжительные невропатические боли.
В заключение наше исследование говорит о том, что HF
является полезным, неинвазивным, нефармакологическим видом терапии для лечения
периферической полиневропатии у пациентов-диабетиков.
Ссылки
1. Harris M, Eastman R, Cowie C (1993) Symptoms of sensory neuropathy in
adults with NIDDM in the U.S. population. Diabetes Care 16:1446–1452
2. Boulton AJ, Malik RA, Arezzo JC, Sosenko JM (2004) Diabetic somatic
neuropathies. Diabetes Care 27:1458–1486
3. Apfel SC, Asbury AK, Bril V et al (2001) Positive neuropathic sensory
symptoms as endpoints in diabetic neuropathy trials. J Neurol Sci 189:3–5
4. Ziegler D, Nowak H, Kempler P, Vargha P, Low PA (2004) Treatment of
symptomatic diabetic polyneuropathy with the antioxidant alpha-lipoic acid: a
meta-analysis. Diabet Med 21:114–121
5. Kumar D, Marshall HJ (1997) Diabetic peripheral neuropathy: amelioration
of pain with transcutaneous electrostimulation. Diabetes Care 20:1702–1705
6. Kumar D, Alvaro MS, Julka IS, Marshall HJ (1998) Diabetic peripheral
neuropathy. Effectiveness of electrotherapy and amitriptyline for symptomatic
relief. Diabetes Care 21:1322–1325
7. Hamza MA, White PF, Craig WF et al (2000) Percutaneous electrical nerve
stimulation: a novel analgesic therapy for diabetic neuropathic pain. Diabetes
Care 23:365–370
8. Tesfaye S, Watt J, Benbow SJ et al (1996) Electrical spinal-cord
stimulation for painful diabetic peripheral neuropathy. Lancet 348:1698–1701
9. Weintraub MI, Wolfe GI, Barohn RA et al (2003) Static magnetic field
therapy for symptomatic diabetic neuropathy: a randomized, double-blind,
placebo-controlled trial. Arch Phys Med Rehabil 84:736–746
10. Khaodhiar L, Niemi JB, Earnest R et al (2003) Enhancing sensation in
diabetic neuropathic foot with mechanical noise. Diabetes Care 26:3280–3283
11. Leonard DR, Farooqi MH, Myers S (2004) Restoration of sensation, reduced
pain, and improved balance in subjects with diabetic peripheral neuropathy: a
double-blind, randomized, placebo-controlled study with monochromatic
near-infrared treatment. Diabetes Care 27:168–172
12. Zinman LH, Ngo M, Ng ET et al (2004) Low-intensity laser therapy for
painful symptoms of diabetic sensorimotor polyneuropathy: a controlled trial.
Diabetes Care 27:921–924
13. Ewins DL, Vileikyte L, Borg-Costanzi J, Carrington A, Boulton AJ (1995) A
novel treatment for painful neuropathy. In: Hotta N, Greene DA, Ward JD (eds)
Diabetic neuropathy, new concepts and insights. Excerpta Medica, Amsterdam, pp
405–408
14. Oyibo SO, Breislin K, Boulton AJ (2004) Electrical stimulation therapy
through stocking electrodes for painful diabetic neuropathy: a double blind,
controlled crossover study. Diabet Med 21:940–944
15. Young MJ, Boulton AJ, MacLeod AF, Williams DR, Sonksen PH (1993) A
multicentre study of the prevalence of diabetic peripheral neuropathy in the
United Kingdom hospital clinic population. Diabetologia 36:150–154
16. Galer BS, Jensen MP (1997) Development and preliminary validation of a
pain measure specific to neuropathic pain: the neuropathic pain scale. Neurology
48:332–338
17. Ziegler D, Hanefeld M, Ruhnau KJ et al (1995) Treatment of symptomatic
diabetic peripheral neuropathy with the anti-oxidant alpha-lipoic acid: a 3-week
multicentre randomized controlled trial (ALADIN study). Diabetologia
38:1425–1433
18. Watkins PJ (1984) Pain and diabetic neuropathy. Br Med J (Clin Res Ed)
288:168–169
19. North RB, Kidd DH, Zahurak M, James CS, Long DM (1993) Spinal cord
stimulation for chronic, intractable pain: experience over two decades.
Neurosurgery 32:384–394
20. TenVaarwerk IA, Jessurun GA, DeJongste MJ et al (1999) Clinical outcome
of patients treated with spinal cord stimulation for therapeutically refractory
angina pectoris. The Working Group on Neurocardiology. Heart 82:82–88
21. Torrens JK, Stanley PJ, Ragunathan PL, Bush DJ (1997) Risk of infection
with electrical spinal-cord stimulation. Lancet 349:729
22. Watkins ES, Koeze TH (1993) Spinal cord stimulation and pain relief. BMJ
307:462
23. Mima T, Oga T, Rothwell J et al (2004) Short-term highfrequency
transcutaneous electrical nerve stimulation decreases human motor cortex
excitability. Neurosci Lett 355:85–88
24. Lundeberg T, Kjartansson J, Samuelsson U (1988) Effect of electrical
nerve stimulation on healing of ischaemic skin flaps. Lancet 2:712–714
25. Tesfaye S, Harris ND, Wilson RM, Ward JD (1992) Exerciseinduced
conduction velocity increment: a marker of impaired peripheral nerve blood flow
in diabetic neuropathy. Diabetologia 35:155–159
26. Tesfaye S, Harris N, Jakubowski JJ et al (1993) Impaired blood flow and
arterio–venous shunting in human diabetic neuropathy: a novel technique of nerve
photography and fluorescein angiography. Diabetologia 36:1266–1274
27. Stevens MJ, Feldman EL, Greene DA (1995) The aetiology of diabetic
neuropathy: the combined roles of metabolic and vascular defects.
Diabet Med 12:566–579
28. Jacobs MJ, Jorning PJ, Joshi SR et al (1988) Epidural spinal cord
electrical stimulation improves microvascular blood flow in severe limb
ischemia. Ann Surg 207:179–183
29. Baker LL, Chambers R, DeMuth SK, Villar F (1997) Effects of electrical
stimulation on wound healing in patients with diabetic ulcers. Diabetes Care
20:405–412
30. Lundberg TCM, Ericksson SV, Malm M (1992) Electrical nerve stimulation
improves healing of diabetic ulcers. Ann Plast Surg 29:328–331
31. Goodyear LJ, King PA, Hirshman MF et al (1990) Contractile activity
increases plasma membrane glucose transporters in absence of insulin. Am J
Physiol 258:E667–E672
32. Lund S, Holman GD, Schmitz O, Pedersen O (1995) Contraction stimulates
translocation of glucose transporter GLUT4 in skeletal muscle through a
mechanism distinct from that of insulin. Proc Natl Acad Sci U S A 92:5817–5821
33. Chilibeck PD, Bell G, Jeon J et al (1999) Functional electrical
stimulation exercise increases GLUT-1 and GLUT-4 in paralyzed skeletal muscle.
Metabolism 48:1409–1413
34. Hamada T, Hayashi T, Kimura T, Nakao K, Moritani T (2004) Electrical
stimulation of human lower extremities enhances energy consumption, carbohydrate
oxidation, and whole body glucose uptake. J Appl Physiol 96:911–916

