Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Эффективность энерготропной терапии при вегетативной дистонии
с кардиальными изменениями у детей и подростков
Н.А. Коровина, Т.М. Творогова, И.Н. Захарова, А.А. Тарасова, К.М. Хрунова
Российская медицинская академия последипломного образования, Москва
Проведено изучение эффективности энерготропных препаратов
L-карнитина (Карнитон), коэнзима Q10
(Кудесан) и их комбинации у 72 детей и подростков с вегетативной дистонией,
имеющих неспецифические невоспалительные кардиальные изменения. При обследовании
выявлены различные причинные факторы кардиальных изменений. Последние выражались
электрокардиографическими нарушениями (по данным стандартной ЭКГ и Холтеровского
мониторирования), изменением морфометрических и гемодинамических показателей (по
результатам ЭХО КГ), а также низкой толерантностью к физической нагрузке. После
курса лечения энерготропными препаратами получена позитивная динамика
исследуемых параметров, наиболее выраженная на фоне комбинированной терапии. При
низкой толерантности к физической нагрузке комбинированная терапия оказалась
также предпочтительней. Результаты работы позволяют проводить адекватную терапию
кардиальных изменений при вегетативной дистонии у детей и подростков.
Ключевые слова: энерготропные препараты, L-Карнитин,
Коэнзим Q10.
В настоящее время в структуре сердечно-сосудистых заболеваний у детей и
подростков значительно возросло количество неспецифических, невоспалительных
изменений миокарда [1, 2, 3]. Достижения современных научных исследований
свидетельствуют о том, что в генезе неспецифичес-кой кардиальной патологии
наряду со структурными изменениями в ЦНС, нейроэндокринной и вегетативной
дисрегуляцией существенную, иногда первостепенную роль играют нарушения
клеточного энергообмена мио-карда [3–8].
Установлено, что даже минимальные нарушения функции миокарда обусловлены
изменением субклеточных структур клетки – энергообразу-ющих органелл-митохондрий
[1, 8, 9]. К наиболее значимым причинным факторам изменения энергетики в
миокарде относятся хронические очаги инфекции, высокая частота заболеваемости
вирусными и микробными инфекциями, физическое перенапряжение, интра- и
перинатальная ги- поксия с нарушением координаторно-интегральной функции
гипоталами-ческих структур и развитием вегетативной дисрегуляции.
Вегетативный дисбаланс с повышением тонуса симпатоадреналовой системы
сопровождается повышенными энергетическими потребностями
миокарда с неэкономным использованием кислорода, что приводит к де-фициту
макроэргических соединений (АТФ, креатинфосфата) и развитию гипоксии. При этом
возникающие: внутриклеточный ацидоз, изменения электролитного баланса,
накопление неокисленных жирных кислот, усиле-ние процессов перекисного окисления
липидов нарушают энергообразу-ющую функцию митохондрий и, соответственно,
усугубляют энергетиче-ский дефицит в организме, особенно в таком
энергопотребляющем органе, как сердце. Более того, избыток катехоламинов сам
непосредственно нару-шает ионный клеточный баланс, что способствует нарушению
процесса ре-поляризации, ослаблению инотропного и изменениям хронотропного
эф-фектов миокарда. Аналогичное действие оказывает и гиперпродукция
аце-тилхолина при усилении парасимпатических влияний[1, 6, 9, 10].
Известно, что биохимические процессы тканевого дыхания в миокарде
многообразны и важнейшими из них являются транспорт жирных кислот и их окисление
в митохондриях с образованием АТФ, а также перенос электронов в дыхательной цепи
митохондрий, необходимый для активации кислорода [11]. При этом значительная
роль отводится отдельным незаменимым компонентам клеток – L-карнитину
и коэнзиму Q10 (убихинону).
L-карнитин выполняет функцию основного трансмембранного переносчика
жирных кислот в митохондрии, где осуществляется их окисление до ацетилкоэнзима А
с последующим синтезом АТФ [11].
Коэнзим Q10, являясь коферментом и
обязательным компонентом дыхательной цепи, осуществляет активный перенос
электронов в полиферментной системе митохондрий, а также участвует в обеспечении
взаимосвязи между электронным транспортом и процессом окисления жирных кислот.
Не менее важной является его антиоксидантная функция. Принципиальным отличием
коэнзима Q10 от других антиоксидантов является
его способность к восстановлению своей антиоксидантной активности после
окисления [11].
В настоящее время отмечена целесообразность применения L-карнитина
в качестве корректора обменных нарушений; коэнзима Q10,
как наиболее эффективного антиоксиданта, при соматических и психоневрологических
заболеваниях [11, 12, 13]. Доказана эффективность применения монотерапии
энерготропными препаратами (L-карнитином, коэнзимом
Q10 и др.) при кардиальной патологии [14, 15,
16].
В то же время далеко не всегда удается выявить конкретные нарушения в
митохондриях и точно подобрать лекарственный препарат. В связи с этим в
медицинской практике применяются различные комплексы энерготропных препаратов,
воздействующие одновременно на различные звенья энергообмена в клетке [1, 12].
Однако сведений об эффективности и возможности применения комбинированной
энерготропной терапии в педиатрической практике недостаточно. Имеются лишь
данные о позитивных результатах лечения комплексом энерготропных лекарственных
средств первичной генетически детерминированной митохондриальной патологии у
детей [1, 8, 12, 17]. Комбинированная терапия энерготропами оказалась
эффективной у детей с эпилепсией [13].
В настоящей работе проведена оценка эффективности комбинированной
энерготропной терапии, включавшей коэнзим Q10
(Кудесан) и L-карнитин (Карнитон) при невоспалительных,
неспецифических кардиальных изменениях у детей и подростков с вегетативной
дистонией (ВД).
Материалы и методы исследования
В исследование было включено 72 человека с ВД, из них 49 детей в возрасте от
8 до 13 лет и 23 подростка в возрасте от 14 до 16 лет. ВД протекала по
симпатикотоническому варианту у 25, по ваготоническому – у 20, по смешанному – у
27 пациентов. Критериями отбора детей и подростков являлись сохраняющееся в
процессе обследования нарушение процесса реполяризации в миокарде либо его
сочетание с другими электрокардиографическими изменениями по данным стандартной
ЭКГ.
Характер и количественная характеристика кардиальных изменений приведены в
таблице 1.
Обследование включало:
физикальный осмотр; анализ генеалогического анамнеза, клинико-анамнестических
данных; общеклинические и биохимические исследования; оценку состояния
вегетативной системы (тонус, реактивность, вегетативное обеспечение);
стандартную ЭКГ лежа, стоя и после физической нагрузки (10–15 приседаний в
зависимости от возраста); суточное мониторирование АД; Холтеровское
мониторирование ЭКГ (ХМ ЭКГ); ультразвуковое исследование (ЭхоКГ) по стандартной
методике с применением секторных датчиков с частотами сканирования от 3,5 до 5
МГц с определением морфометрических показателей, параметров систолической и
диастолической функций левого желудочка. Анализ результатов осуществлялся в
соответствии с нормативными показателями, применяемыми в педиатрии [19–21].
Таблица 1. Кардиальные изменения у обследуемых детей и подростков с ВД по данным
стандартной электрокардиографии (в %)

Исследование проводилось по программе, включавшей скрининговую фазу (3–8
недель), период лечения, катамнестическое наблюдение (1–2 месяца).
Для оценки эффективности проводимой терапии, обследуемые дети и подростки
были рандомизированы на три равные группы, сопоставимые по возрасту, полу,
характеру кардиальных изменений и варианту ВД.
I-я группа получала комбинированную терапию Карнитоном и Кудесаном
[ЗАО «Аквион», Россия ]; II-я группа – Кудесан; III-я группа – Карнитон.
Лечебные дозы препаратов составляли:
- для Кудесана – детям до 10 лет – 30 мг/сутки (11 кап. х 2
раза); старше 10 лет – 45 мг/сутки (11 кап. х 3 раза);
- для Карнитона – 25 мг/кг/сутки независимо от возраста (в 1 табл. 500 мг).
Продолжительность курса лечения – 4 недели.
В период лечения другие кардиотрофические препараты не назнача-лись. С целью
коррекции вегетативной дисрегуляции применялись различные варианты
немедикаментозного лечения (ЛФК, массаж, групповой или индивидуальный
аутотренинг, водные процедуры и т. д.) в сочетании с витаминотерапией.
Исследование проводилось на клинической базе кафедры педиатрии РМАПО в
Тушинской детской городской больнице г. Москвы.
Статистический анализ результатов осуществляли стандартными методами. Для
малочисленных групп, в которых количество больных было менее 10, использован
метод статистического анализа Стентона Гланса [22]. Степень достоверности
количественных показателей оценивали по t-критерию
Стьюдента. Статистически значимыми считали различия при величине р<0,05.
Результаты и их обсуждение
В процессе обследования выявлено, что ВД развивалась при наличии отягощенного
акушерского анамнеза (у 63% матерей) и последствий анте- и интранатальной
патологии ЦНС (у 45% обследуемых); в генеалогическом анамнезе отмечались
сердечно-сосудистые заболевания – у 72%, эндокринная патология (семейная
низкорослость, заболевания щитовидной железы, сахарный диабет) – у 5%
обследуемых. Хронические очаги инфекции в носоглотке (хронический тонзиллит,
гипертрофия носоглоточной миндалины, синусит с частыми обострениями) имели место
более чем у половины больных (57%). Интенсивная физическая нагрузка наблюдалась
у 13 детей и подростков (18%), гиподинамия – у 22 (30%). Избыточную массу тела
или ожирение имели 14 человек (19,3%).
У подростков на фоне ВД по симпатикотоническому и смешанному вариантам
выявлена артериальная гипертензия (АГ) I степени (у 15
чел.) и лабильная АГ (у 8 чел.).
Характер жалоб в основном носил неспецифический характер, при этом наиболее
часто отмечались утомляемость, раздражительность, тре-вожность, снижение
умственной работоспособности, головная боль, трудности засыпания. Лишь у 9
человек (12,5%) наблюдались кратковременные кардиалгии, сердцебиения, ощущения
усиленных сокращений сердца, появляющиеся в момент физической нагрузки и при
волнении, реже в покое.
Анализ клинико-анамнестических данных и результатов дополнительных методов
исследования позволили исключить органическую патологию сердца и
симптоматическую АГ. Отмечено, что кардиальные изменения в группах наблюдения
имели вторичный характер и обусловлены нейровегетативной дисрегуляцией либо ее
сочетанием с хроническими очагами инфекции в носоглотке (интоксикацией),
нарушением жирового обмена, физическим перенапряжением у большинства обследуемых
пациентов.
Эффективность энерготропной терапии нашла отражение в положи-тельной динамике
ЭКГ в 3-х группах наблюдения. Анализ конечной части желудочкового комплекса (ST-T
нарушений), по данным стандартной ЭКГ, показал, что положительный эффект в
виде нормализации процесса реполяризации наблюдался в первой группе у
58% (терапия Карнитоном и Кудесаном), во второй группе – у 37,5% (терапия
Кудесаном), в третьей группе – у 33,3% (терапия Карнитоном) обследуемых.
Отчетливое улучшение процесса реполяризации отмечено в
I-й группе (Карнитон и Кудесан) – у 25%, во II-й группе (Кудесан)
– у 37,5%, в III-й группе (Карнитон) – у 29% обследуемых.
Незначительное улучшение (отсутствие эффекта) определялось в
I-й группе – у 16,6%, во II-й
группе – у 20,8%, в III-й группе – у 33% обследуемых.
Исходя из полученных данных, следует, что наиболее значимая положительная
динамика в виде нормализации ST-T
нарушений наблюдалась в I-й группе больных (терапия
Карнитоном и Кудесаном), в то время как во II-й (Кудесан)
и III-й (Карнитон) группах преобладал позитивный эффект в
виде улучшения показателей ЭКГ. Усугубления ST-T
нарушений не выявлено ни у одного пациента. Динамика детальных изменений
ST-T нарушений после курса моно- и
комбинированной энерготропной терапии приведена в таблице 2.
Таблица 2. Динамика ST-T нарушений, по
данным стандартной ЭКГ, после курса лечения энерготропными препаратами у трех
групп детей с ВД (в %)

Помимо положительной динамики изменений конечной части желудочкового
комплекса, в целом снизилась частота регистрации синоатриальной блокады (СА)
II степени у 50% больных, нивелировались эпизоды миграции
водителя ритма у 44% больных. Это привело к снижению процента выявления
брадикардии с 22% до 9,5%. Частота сердечных сокращений при синусовой тахикардии
достоверно не изменялась.
Холтеровское мониторирование ЭКГ (ХМ ЭКГ) позволило выявить у пациентов
больший процент изменений, чем на стандартной ЭКГ, в частности, миграция
водителя ритма на фоне синусовой брадикардии составила 21%; СА–блокада
II степени с сопутствующей вставочной одиночной
суправентрикулярной экстрасистолией – 18%. Непостоянная АВ-блокада
I степени обнаружена у 4% обследуемых. Динамика отдельных
показателей ХМ ЭКГ в зависимости от эффективности энерготропной терапии
приведена в таблице 3.
Таблица 3. Отдельные показатели ХМ ЭКГ на фоне энерготропной терапии у детей и подростков с ВД
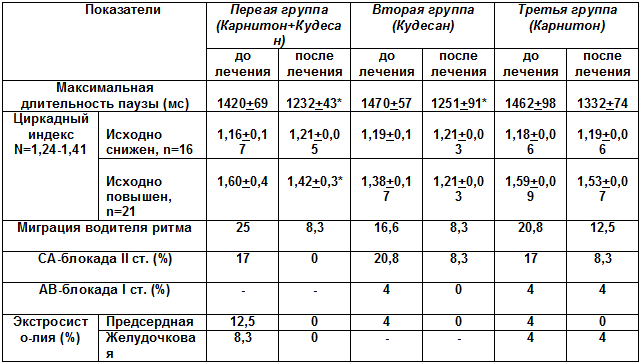
*р < 0,05 при сравнении до и после лечения
Из результатов ХМ ЭКГ следует, что после лечения в I-й
группе об-следуемых (терапия Карнитоном и Кудесаном) отмечалась достоверная
динамика циркадного индекса за счет увеличения средненочной ЧСС с уменьшением
максимальной длительности пауз ритма (р<0,05). Исходно повышенный циркадный
индекс, как проявление симпатикотонии, имел тенденцию к снижению.
Во II-й группе (терапия Кудесаном) наблюдалось
достоверное уменьшение длительности асистолии, в III-й
группе (терапия Карнитоном) определялась тенденция к ее уменьшению без
существенной динамики средненочной ЧСС и соответственно циркадного индекса.
Кроме того, на фоне энерготропной терапии в трех группах наблюда-емых детей и
подростков отмечалось заметное увеличение представленности синусового ритма в
общем объеме кардиоциклов за счет уменьшения эпизодов миграции водителя ритма,
СА-блокады и экстрасистолии. Из данных, приведенных в Таблице 3, следует, что по
окончании курсового лечения наибольшее снижение процента указанных изменений
наблюдалось в первой группе больных (Карнитон +Кудесан). Во II-й
(Кудесан) и III-й (Карнитон) группах отмечалась аналогичная динамика, однако
менее выраженная. Из анализа результатов следует, что энерготропная монотерапия
в большинстве случаев эффективна не только при нарушении процесса реполяризации,
но и при изменениях автоматизма, проводимости и возбудимости сердца. Однако при
назначении комбинации препаратов позитивные результаты лечения наиболее
выражены.
ЭХО КГ выявила изменения отдельных морфометрических и гемоди-намических
показателей сердца во всех трех группах наблюдения среди подростков с
симпатикотоническим и смешанным вариантами вегетативной дистонии, протекавшей с
АГ I степени и лабильной АГ.
Средние величины отдельных показателей приведены в таблице 4.
Таблица 4. Морфометрические и гемодинамические показатели сердца на фоне энерготропной
терапии у подростков с ВД, протекавшей с АГ
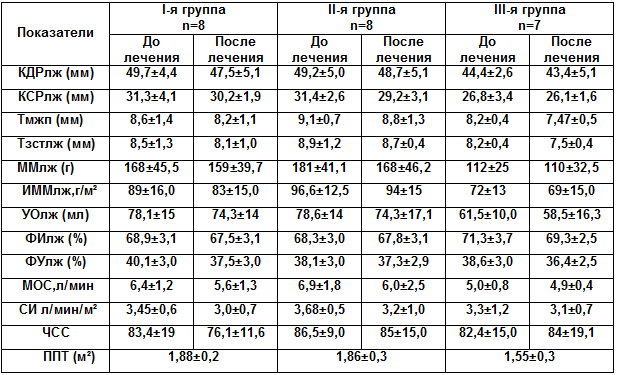
Условные обозначения:
КДРлж – конечный диастолический размер левого желудочка; КСРлж – конечный
систолический размер левого желудочка; Тмжп – толщина межжелудочковой
пе-регородки; Тзслж – толщина задней стенки левого желудочка; ММлж – масса
миокарда левого желудочка; ИММ – индекс массы миокарда; УОлж – ударный объем
левого желудочка; ФИлж – фракция изгнания; ФУ – фракция укорочения левого
желудочка; МОС – минутный объем сердца; СИ – сердечный индекс; ЧСС – частота
сердечных сокращений; ППТ – площадь поверхности тела.
Анализ полученных результатов показал, что КДРлж и КСРлж у пациентов трех
групп не превышал нормативных значений, однако отмечалась тенденция к увеличению
этих показателей у пациентов с избыточной массой тела и ожирением (КДРлж = 50,8
+ 4,1 мм; КСРлж = 32,3 +3,4 мм), у них же имелась тенденция к
преобладанию Тмжп и Тзслж.
При оценке систолической функции сердца в трех группах наблюдения выявлена
тенденция к увеличению средних значений УОлж, МОС, СИ, наиболее выраженная в
первой и второй группах по сравнению с возрастной нормой. В ходе исследования
гемодинамики у наблюдаемых пациентов было установлено, что эукинетический тип
наблюдался у 46%, гипокинетический тип – у 42%, гиперкинетический тип – у 12%
подростков.
При оценке диастолической функции левого желудка отмечено, по средним данным,
увеличение фракции предсердного наполнения, которая составляла в первой, второй
и третьей группах соответственно 39,7+8,8%, 41,1+6,9%, 40,5+3,9%.
Анализ индивидуальных результатов позволил более отчетливо выявить нарушения
диастолической функции с преобладанием трансмитрального кровотока у 11 пациентов
среди всех трех групп наблюдения. Это выражалось в уменьшении максимальной
скорости раннего диастолического наполнения (0,54+0,1м/с) в увеличении
максимальной скорости кровотока в предсердную систолу (0,85+0,2 с/с), в
увеличении времени замедления раннего диастолического наполнения (262+39,6
м/с) и изоволюметрического расслабления (39,7+11,5 м/с).
После курса терапии энерготропными препаратами в трех группах пациентов
наблюдалась тенденция к уменьшению ММ и ИММ, что свиде-тельствовало о влиянии
Карнитона и Кудесана на процессы ремоделирования миокарда.
Позитивная динамика систолической функции характеризовалась уменьшением МОС
за счет снижения УО в условиях нормализации АД, что более отчетливо наблюдалось
в первых двух группах пациентов. Частота эукинетического типа гемодинамики
увеличилась до 54% за счет подростков, имевших ранее гиперкинетический и
гипокинетический типы. Однако частота гипокинетического типа оставалась
достаточно высокой (38%).
Нарушение диастолической функции левого желудочка с преобладанием
предсердного наполнения имело обратное развитие в трех группах наблюдения,
составляя соответственно 33,5+2,8% (Карнитон+Кудесан), 36,2+5,4% (Кудесан),
35+2,8% (Карнитон). При этом достоверное уменьшение наблюдалось в первой
(терапия Карнитоном+Кудесаном) и третьей группах (терапия Карнитоном) (р<0,05).
Среди изменений трансмитрального кровотока (у 11 пациентов) отмечалась
нормализация максимальных скоростей раннего диастолического наполнения и
кровотока в предсердную систолу, а также времени раннего диастолического
наполнения, что свидетельствовало об улучшении диастолического наполнения левого
желудочка после проведенного курса лечения.
Полученные результаты согласуются с литературными данными об эффективности
энерготропных препаратов при нарушениях функциональной способности сердца и
гипертрофии миокарда [15, 18].
Таким образом, полученные данные ЭхоКГ-исследования свидетельствуют о том,
что применение Карнитона и Кудесана как в комбинации, так и в виде монотерапии
эффективны для коррекции систолической и диастолической дисфункций, а также при
формировании патологического ремоделирования миокарда.
Анализ результатов ЭКГ после проведения физической нагрузки выявил как
усиление имевшихся ЭКГ-изменений (у 68% пациентов), так и по-явление новых вне
связи с ЭКГ-отклонениями в состоянии покоя (у 77%). Это касалось нарушения
процесса реполяризации и проводимости (АВ- или СА-блокада), удлинения интервала
QT и синусовой тахикардии (более 125 ударов в минуту).
Сказанное иллюстрирует рис. 1.


Рис. 1. Количественная характеристика ЭКГ изменений до и после
физической нагрузки у обследованных больных (в %)
I - снижение, инверсия зубца Т до физической нагрузки;
Iа - снижение, инверсия зубца Т после физической нагрузки;
II – депрессия интервала ST до физической
нагрузки;
IIa – депрессия интервала ST после физической
нагрузки;
III – синусовая тахикардия до физической нагрузки;
IIIa – синусовая тахикардия после физической нагрузки;
IY – удлинение интервала QT до физической
нагрузки;
IYa – удлинение интервала QT после физической
нагрузки;
Y – АВ + СА блокада до физической нагрузки;
Ya – АВ + СА блокада после физической нагрузки.
После курса энерготропной терапии повторное проведение пробы не обнаружило
отрицательной динамики ни у одного пациента. Более того, была отмечена
положительная динамика ЭКГ-изменений во всех исследуемых группах. Так, в первой
группе пациентов (Карнитон+Кудесан) полностью исчезли появившиеся на нагрузку
ST-T нарушения, АВ-блокада
I степени и СА-блокада II степени,
не определялось удлинения интервала QT, синусовая
тахикардия (свыше 125 ударов в минуту) сохранялась у 45% пациентов. Усиление
исходных ЭКГ-изменений на нагрузку нивелировалось полностью.
Во II-й (Кудесан) и III-й (Карнитон) группах
положительная динамика также выражалась в значительном уменьшении ЭКГ-изменений.
Анализ полученных данных свидетельствует о перспективности применения
энерготропных препаратов Карнитон и Кудесан для повышения толерантности к
физической нагрузке у детей и подростков при ВД. Следует отметить, что влияние
энерготропной терапии на частоту сердечных сокращений менее выражено, чем на
проводимость, нарушение и продолжительность реполяризации в миокарде. Комбинация
препаратов Карнитон и Кудесан оказывает более отчетливое позитивное действие уже
через месяц терапии. Возможно, что увеличение лечебной дозы и продолжительности
курса монотерапии может привести к аналогичным результатам.
У пациентов, получавших Карнитон, Кудесан либо Карнитон и Кудесан совместно,
положительная динамика кардиальных изменений сочеталась с выраженным уменьшением
клинических проявлений ВД в виде нормализации сна, адекватности реакций,
устойчивости к ин-теллектуальным нагрузкам, отсутствия выраженной утомляемости,
жалоб на головную боль, кардиалгии, сердцебиения.
Заключение
Многообразие возможных биохимических сдвигов в клеточной био-энергетике в
сочетании с трудностями их конкретного выявления делают оправданным применение
комбинации энерготропных препаратов (Карнитон+Кудесан), воздействующих на
субклеточном уровне на различные звенья энергообмена в миокарде. Эффективность
комбинированной терапии при кардиальных изменениях у детей и подростков с ВД,
развившейся на фоне резидуальных изменений ЦНС и протекавшей с хроническими
очагами инфекции, АГ, ожирением, гипо- и гипердинамией, выше, чем при
монотерапии Карнитоном или Кудесаном. Это выражается в достаточно быстром
достижении позитивного лечебного эффекта с нормализацией или значительным
улучшением процессов реполяризации и проводимости, с уменьшением
продолжительности асистолии в ночные часы и количества эпизодов миграции
водителя сердечного ритма. Как комбинированная терапия Карнитоном и Кудесаном,
так и монотерапия этими препаратами может быть рекомендована для коррекции
диастолической и систолической дисфункции, а также в начальной стадии
формирования гипертрофии миокарда левого желудочка.
Целесообразно назначение как комбинации Карнитона и Кудесана, так и
монотерапии одним из препаратов детям и подросткам с вегетативной дистонией,
имеющим снижение толерантности к физической нагрузке с появлением или ухудшением
электрокардиографических изменений.
Литература
- Леонтьева И.В. Лекции по кардиологии детского возраста. – М., 2005:
76–126.
- Беленков Ю.И., Серегин К.Е. Проблемы сердечно-сосудистой патологии у
подростков. / Кардиология. – 1987; 9:115–118.
- Дембо А.Г., Земцовский Э.В. Спортивная кардиология. – Л., 1989: 262–368.
- Земцовский Э.В. Дистрофия миокарда у спортсменов. / Кардиология. – 1994;
9: 66–74.
- Саркисов Д.С., Втюрин Б.В. Дистрофия миокарда, ее обратимость и пути
профилактики в ультраструктурном изображении. Дистрофия миокарда. – Л.,
1971: 69–78.
- Сумароков А.В., Моисеев В.С. Клиническая кардиология. – М., 1995:
185–189.
- Маколкин В.И. Нейроциркуляторная дистония. Терапевтический архив. – 1995;
67; 6: 66–70.
- Сухоруков В.С., Николаева Е.А. Нарушения клеточного энергообмена у детей.
–М., 2004: 7–79.
- Кушаковский М.С. Метаболические болезни сердца. – СПб., 2000: 5–128.
- Вельтищев Ю.Е. цит. Леонтьевой И.В. (1).
- Практические рекомендации по энерготропной терапии. – М., 2007: 4–21.
- Сухоруков В.С. К разработке рациональных основ энерготропной терапии.
Рациональная фармакотерапия. – 2007; 2: 40–47.
- Ключников С.О. Перспективы применения L-карнитина
в педиатрии. Consilium medicum.
– 2007; приложение 2: 116–119.
- Школьникова М.А., Березницкая В.В. Отчет о научно-исследовательской
работе по теме: «Исследование действия «Кудесана» при тахиаритмиях». Сб.:
Антиоксидантный препарат Кудесан, применение в кардиологии. – М., 2006:
83–90.
- Балыкова Л.Н., Абдулкави А.М. Отчет о применении препарата «Кудесан» у
детей с нарушением сердечного ритма и проводимости. Сб. Антиоксидантный
препарат Кудесан, применение в кардиологии. – М., 2006: 90–97.
- Аронов Д.М. Применение Коэнзима Q10 в
кардиологической практике. / РМЖ. – 2004; 12(15): 905–909.
- Казанцева Л.З.,Юрьева Э.А. Основные методы лечения детей, страдающих
митохондриальными заболеваниями. Методические указания. – М., 2001: 2–14.
- Маркелова И.А., Балыкова Л.А. с соавт. Применение метаболической терапии
для оптимизации толерантности юных спортсменов к физическим нагрузкам. /
Педиатрия. – 2008: 4: 51–55.
- Детская ультразвуковая диагностика. Под ред. М.И.Пыкова, К.В.Ватолина. –
М., 2001: 104–150.
- Доскин В.А., Келлер Х., Мураенко Н.М. и др. Морфофункциональные константы
детского организма. Справочник. – М.: Медицина, 1997.
- Фейгенбаум Х. Эхокардиография. 5-е изд. Пер. с англ. Под ред.
В.В.Митькова. – М., 1999.
- Гланс С. Медико-биологическая статистика. – М.: Практика, 1999.

